MATERIAL TEKNIK 2 SKS Ruang B 2 2

MATERIAL TEKNIK 2 SKS Ruang B 2. 2 Jam 8. 40 -11. 10 Dedi Nurcipto, MT dedinurcipto@dsn. dinus. ac. id

Struktur Atom • Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta elektron bermuatan negatif yang mengelilinginya • Inti atom mengandung campuran proton (bermuatan positif) dan neutron (bermuatan netral). • Elektron-elektron pada suatu atom terikat pada inti atom oleh gaya elektromagnetik.

Struktur Atom • Sekumpulan atom dapat berikatan satu dengan yang lainnya membentuk sebuah molekul. • Atom dikelompokkan pada jumlah proton dan neutron pada inti atom tersebut. • Jumlah proton dan neutron menentukan berat atom yang bersangkutan. • Gerakan elektron dari atom ke atom dikatakan sebagai arus listrik.

Struktur Atom Model-model Atom 1 Model Atom John Dalton - atom adalah bagian terkecil suatu unsur - atom tidak dapat diciptakan, dimusnahkan, terbagilagi, diubah menjadi zat lain - atom-atom suatu unsur adalah sama dalam segala hal, tetapi berbeda dengan atom-atom unsur lain

Struktur Atom 2 Model Atom JJ Thomson - atom merupakan suatu bola bermuatan positif dan didalamnya tersebar elektron - Elektron seperti kismis - jumlah muatan positif sama dengan muatan negatif, sehingga atom bersifat netral

Struktur Atom 3 Model Atom Rutherford - atom terdiri dari inti atom yang sangat kecil dengan muatan positif yang massanya merupakan massa atom tersebut - elektron-elektron dalam atom bergerak mengelilingi inti tersebut - banyaknya elektron dalam atom sama dengan banyaknya proton dalam inti dan ini sesuai dengan nomor atomnya

Struktur Atom 4 Model Atom Niels Bohr - elektron-elektron dalam mengelilingi inti berada pada tingkat - tingkatenergi(kulit)tertentu tanpa menyerap atau memancarkan energi - elektron dapat berpindah dari kulit luar ke kulit yanglebih dalam dengan memancarkan energi, atau sebaliknya

Struktur Atom 5 Model Atom Mekanika Gelombang - elektron tidak mengorbit pada lintasan tertentu - elektron-elektron berada pada orbital-orbital dengan tingkat energi tertentu - orbital merupakan daerah dengan kemungkinan terbesar untuk menemukan elektron disekitar inti atom

Kulit Atom
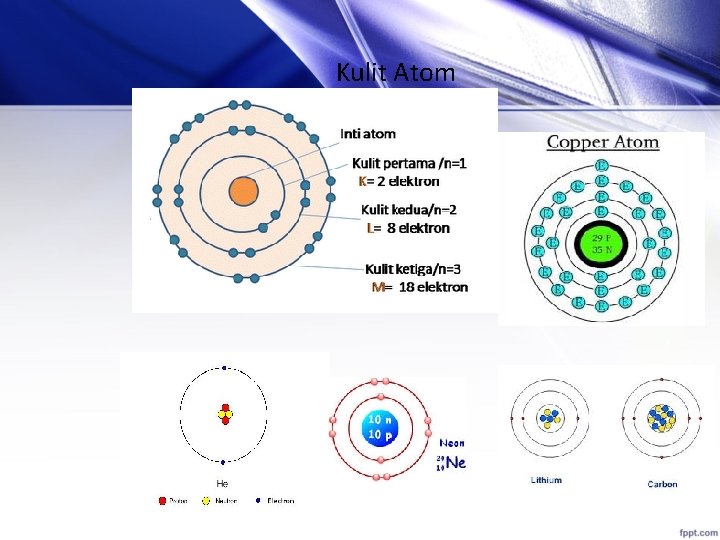
Kulit Atom

Berat Atom

Nomer Atom • Dalam tabel priodik nomer atom merupakan jumlah proton dalam atom. • Jumlah elektron dalam sebuah atom neutral adalah sama dengan jumlah proton dalam inti. Muatan Atom • Muatan atom ditentukan oleh muatan proton dan elektron, bila kedua muatan mempunyai jumlah sama maka dikatakan atom tersebut tidak bermuatan. • Muatan positif bila atom kehilangan elektron. • Muatan negatif bila atom kelebihan elektron

Elektron Bebas • Merupakan elektron yang tidak menempel pada sebuah atom disebut free electron. • Dibutuhkan energi dari luar untuk melepaskan elektron dari orbitnya, bisa berupa panas, tegangan, medan magnet dll. • Elektron yang lepas dari orbit akan menabrak lektron lainya dari atom tetangga. Arus Listrik • Arus listrik merupakan elektron bebas yang mempunyai kemampuan menggeser elektron lain dari orbitnya • Arus listrik adalah aliran dari partikel bermuatan negatif.
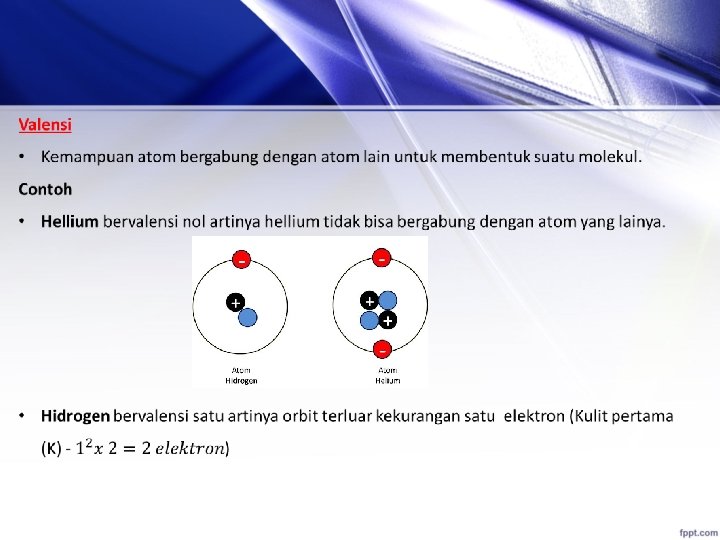
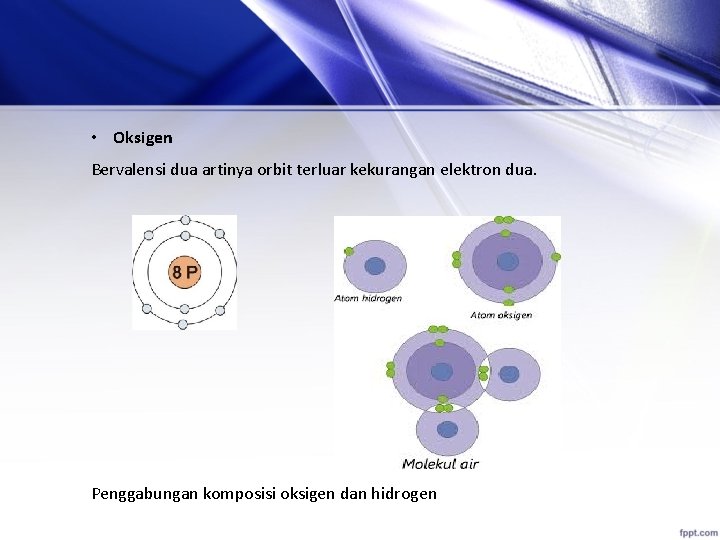
• Oksigen Bervalensi dua artinya orbit terluar kekurangan elektron dua. Penggabungan komposisi oksigen dan hidrogen

Pita Energi Elektron dalam sebuah atom tunggal hanya boleh menempati tingkat-tingkat energi tertentu. Jika banyak atom saling berdekatan maka elektron-elektron dari kulit terluar (elektron valensi) saling berinteraksi sehingga tingkat energinya saling bertumpukan dianggap membentuk pita energi Pita Energi 1. Pita valensi 2. Pita konduksi 3. Pita larangan


Struktur Atom Pita Energi Elektron dalam sebuah atom tunggal hanya boleh menempati tingkat-tingkat energi tertentu. Jika banyak atom saling berdekatan maka elektron-elektron dari kulit terluar (elektron valensi) saling berinteraksi sehingga tingkat-tingkat energinya saling bertumpukan dianggap membentuk pita energi

Struktur Atom

Struktur Atom Perbedaan jenis bahan berdasarkan pita energinya : 1. Isolator 2. Semikonduktor 3. Konduktor

Struktur Atom 1. Isolator Bahan-bahan isolator mempunyai pita larangan yang cukup lebar . Untuk memindahkan elektron dari pita valensi ke pita konduksi diperlukan energi yang lebih besar. Karena elektron-elektron ini sukar bergerak maka bahan isolator sukar menghantarkan arus listrik. 2. Konduktor Bahan-bahan konduktor tidak mempunyai pita larangan. Antara pita valensi dan pita konduksinya bisa saling bertumpuk. Elektron-elektron dapat bergerak bebas pada bahan konduktor.

Struktur Atom 3. Semikonduktor Bahan-bahan semikonduktor mempunyai pita larangan yang lebih sempit. Untuk pita larangan yang lebih sempit. Untuk memindahkan elektron dari pita valensi ke pita konduksi diperlukan energi yang lebih kecil. Elektron-elektron dapat bergerak pada bahan semikonduktor dengan energi yang kecil.

Bahan Listrik Pentingnya pengetahuan bahan listrik ? 1. Mengetahui jenis bahan 2. Mengetahui sifat baha

Agar dapat : 1. Memperlakukan/memanfaatkan bahan dengan sebaik-baiknya 2. Mengetahui batasan aman/bahaya suatu bahan

Pita Energi Perbedaan jenis bahan berdasarkan pita energinya : 1. Isolator 2. Semikonduktor 3. Konduktor Pita energi adalah kumpulan garis pada tingkat energi yangsama akan saling berimpit dan membentuk pita Pada orbit bagian luar terdapat elktron yang sangat banyak dengan tingkat- tingkat energi yang berimpit satu sama lain

SEMIKONDUKTOR Disebut semi atau setengah konduktor, karena bahan ini memang bukan konduktor murni. Bahan - bahan logam seperti tembaga, besi, timah disebut sebagai konduktor yang baik sebab logam memiliki susunan atom yang sedemikian rupa, sehingga elektronnya dapat bergerak bebas.

Susunan Atom Semikonduktor Bahan semikonduktor yang banyak dikenal contohnya adalah Silicon (Si), Germanium (Ge) dan Galium Arsenida (Ga. As). Germanium dahulu adalah bahan satu-satunya yang dikenal untuk membuat komponen semikonduktor. Namun belakangan, silikon menjadi popular setelah ditemukan cara mengekstrak bahan ini dari alam. Silikon merupakan bahan terbanyak ke dua yang ada dibumi setelah oksigen (O 2).

DOPING Pemberian doping dimaksudkan untuk mendapatkan elektron valensi bebas dalam jumlah lebih banyak dan permanen, yang diharapkan akan dapat mengahantarkan listrik

Tipe-N Bahan silikon diberi doping phosphorus atau arsenic yang pentavalen yaitu bahan kristal dengan inti atom memiliki 5 elektron valensi. Dengan doping, Silikon yang tidak lagi murni ini (impurity semiconductor) akan memiliki kelebihan elektron. Kelebihan elektron membentuk semikonduktor tipe-n. Semikonduktor tipe-n disebut juga donor yang siap melepaskan elektron.
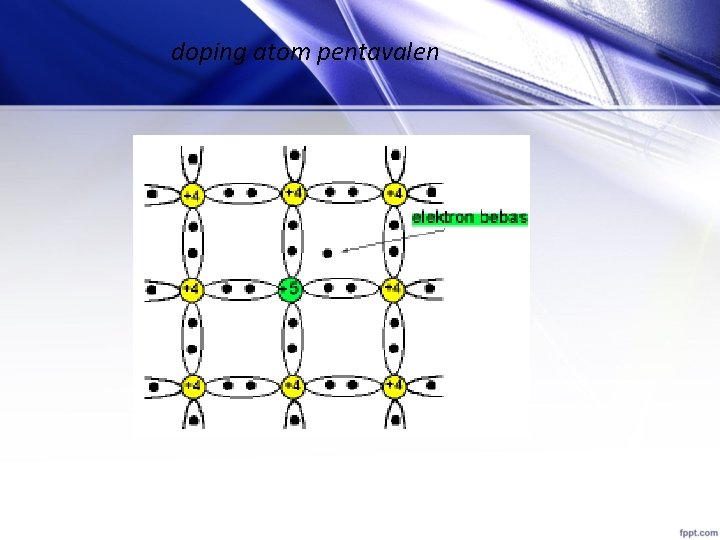
doping atom pentavalen

Tipe-P Kalau silikon diberi doping Boron, Gallium atau Indium, maka akan didapat semikonduktor tipe-p. Untuk mendapatkan silikon tipe-p, bahan dopingnya adalah bahan trivalen yaitu unsur dengan ion yang memiliki 3 elektron pada pita valensi. Karena ion silikon memiliki 4 elektron, dengan demikian ada ikatan kovalen yang lubang (hole). Hole ini digambarkan sebagai akseptor yang siap menerima elektron. Dengan demikian, kekurangan elektron menyebabkan semikonduktor ini menjadi tipe-p.
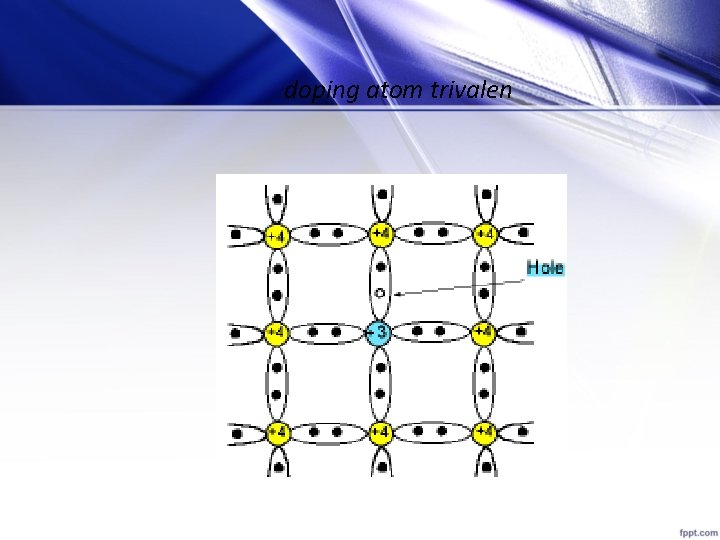
doping atom trivalen

Arus Hole • Bila ikatan kovalen pada kristal silikon terputus, maka akan terjadi kekosongan atau lubang (Hole) yang mempunyai kelebihan muatan positif. • Hole juga dapat bergerak dan menghasilkan arus, dengan kata lain didalam semikonduktor ada dua macam arus yang berbeda, yaitu arus pita konduksi dan arus hole.
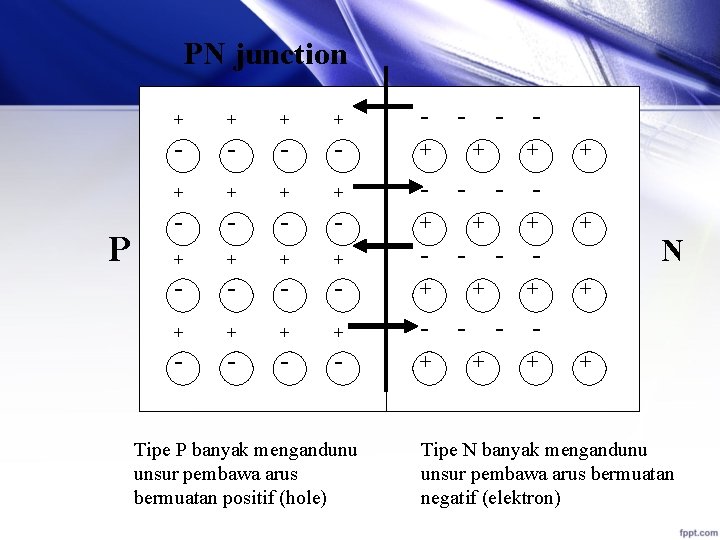
PN junction P + + + + - - - - - - - - + Tipe P banyak mengandunu unsur pembawa arus bermuatan positif (hole) + + + + + N + + Tipe N banyak mengandunu unsur pembawa arus bermuatan negatif (elektron)
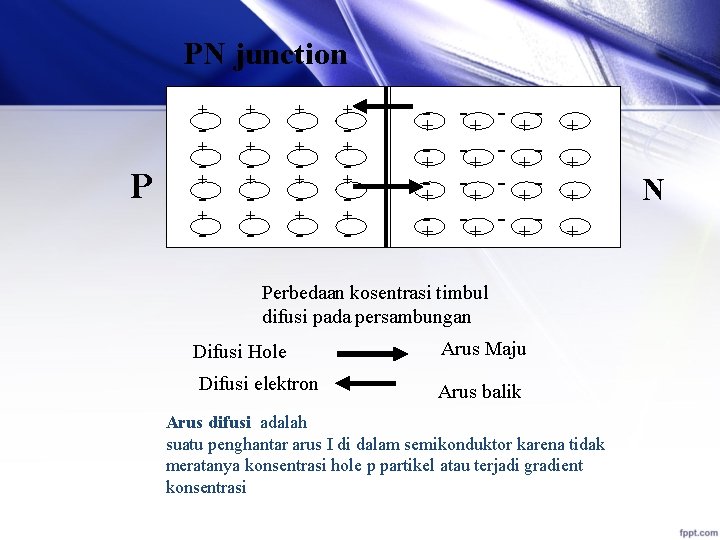
PN junction + P + -+ + - + -+ + - - - + + + - - + + + + + Perbedaan kosentrasi timbul difusi pada persambungan Difusi Hole Difusi elektron Arus Maju Arus balik Arus difusi adalah suatu penghantar arus I di dalam semikonduktor karena tidak meratanya konsentrasi hole p partikel atau terjadi gradient konsentrasi N
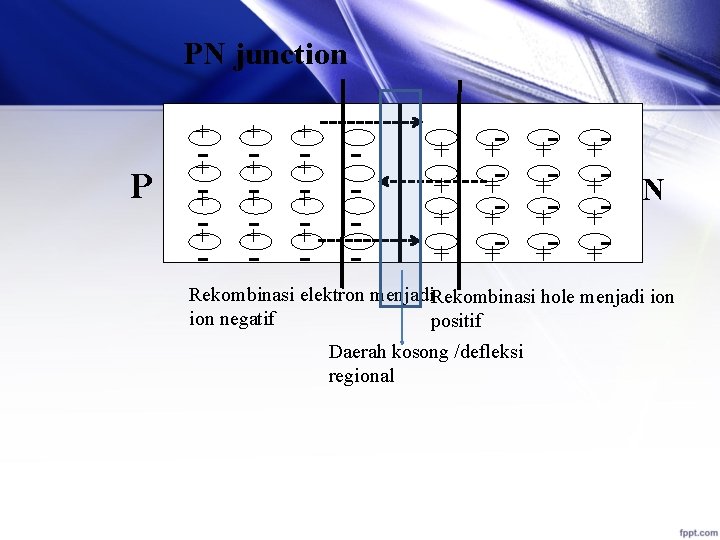
PN junction P + + + + - - - + + + + - - - + + N Rekombinasi elektron menjadi Rekombinasi hole menjadi ion negatif positif Daerah kosong /defleksi regional
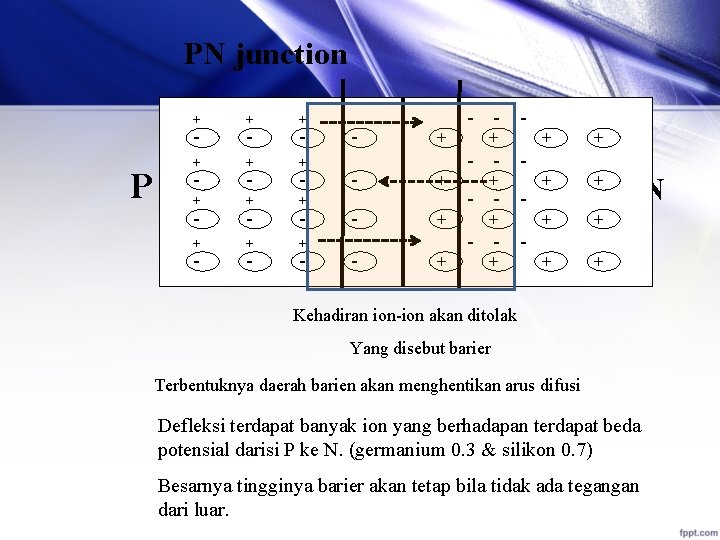
PN junction + P + + - - - + + + - - - + + - - + + + - - N - - - + + Kehadiran ion-ion akan ditolak Yang disebut barier Terbentuknya daerah barien akan menghentikan arus difusi Defleksi terdapat banyak ion yang berhadapan terdapat beda potensial darisi P ke N. (germanium 0. 3 & silikon 0. 7) Besarnya tingginya barier akan tetap bila tidak ada tegangan dari luar.
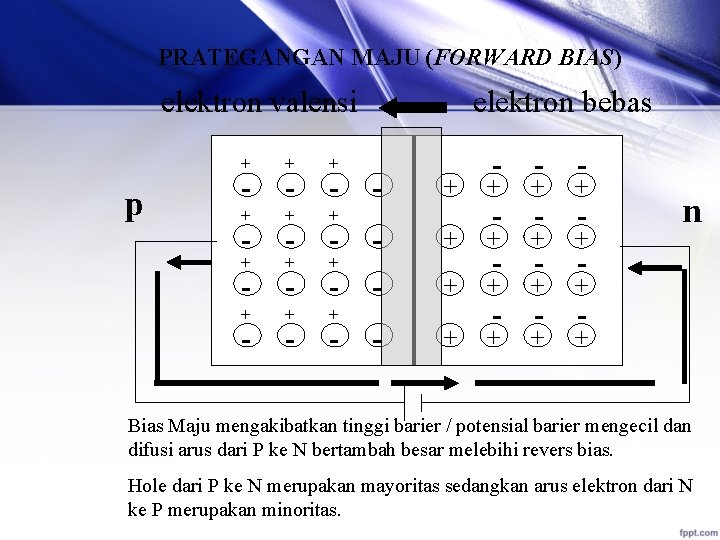
PRATEGANGAN MAJU (FORWARD BIAS) elektron valensi p + + + - - + + - elektron bebas - - + + + - - - + + - - - n - - - Bias Maju mengakibatkan tinggi barier / potensial barier mengecil dan difusi arus dari P ke N bertambah besar melebihi revers bias. Hole dari P ke N merupakan mayoritas sedangkan arus elektron dari N ke P merupakan minoritas.
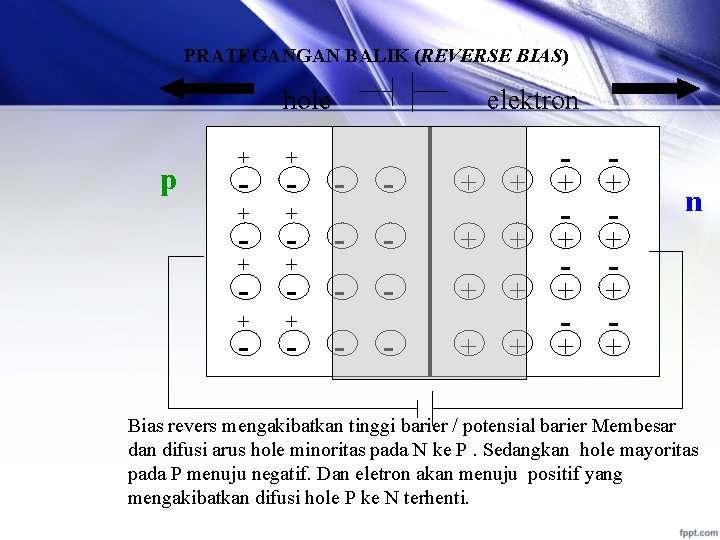
PRATEGANGAN BALIK (REVERSE BIAS) hole p + + + - elektron - - - + - - + + + - - + + - - n - - Bias revers mengakibatkan tinggi barier / potensial barier Membesar dan difusi arus hole minoritas pada N ke P. Sedangkan hole mayoritas pada P menuju negatif. Dan eletron akan menuju positif yang mengakibatkan difusi hole P ke N terhenti.

Perbedaan struktur logam dan non logam Perbedaan yang sangat mendasar antara bahan logamdibanding dengan bahan bukan logam adalah mengenai struktur atomnya. Selain itu juga terdapat perbedaan mengenai daya hantar listrik maupun daya hantar panasnya.
Bahan- bahan Logam Sifat- sifat Struktur Kristal Bahan Logam Ikatan Atom Sifat campuran dari bahan Logam

Sifat- Sifat Logam • Logam bersifat konduktor ( dapat menghantarkan panas & aliran listrik ). • Logam tidak mudah leleh, namun logam pun bisa leleh juga dalam temperatur yang tinggi. • Logam dapat ditempa ( malleable ) dan dapat diregangkan ( ductile ). • Mengkilap jika digosok. • Berwujud padat, kecuali raksa (cair). • Logam terdiri dari atom-atom yang sangat rapat satu sama lainnya dan mempunyai berat jenis yang sangat tinggi.
Jenis-jenis Ikatan Kristal Ion Kristal Kovalen Jenis-jenis Kristal Krista Molekuler Kristal Logam

Kristal Ion Ikatannya timbul karena gaya tarik diantara ionion yang bermuatan listrik. Struk natrium Klorida dan klor merupakan contoh dari kristal

Kristal Kovalen Pada Kristal kovalen, atom yang satu dengan atom yang lainnya terikat oleh adanya elektron kulit terluar yang dimiliki bersama. Struktur kristal intan dan sejumlah silikat tertentu terjadi karena jenis ikatan seperti ini.

Kristal Molekuler terbentuk oleh molekul yang jenuh secara kimia, yang terikat oleh satu sama lainnya oleh adanya gaya-gaya Van Der Wals. Struktur Kristal dari gas-gas inert yang beku dan sejumlah banyak bahan organik yang termasuk dalam golongan ini.

Lanjutan. . . Karena orbital atom bertumpangtindih berulang-ulang, elektron-elektron di kulit terluar setiap atom akan dipengaruhi oleh banyak atom lain. Elektron semacam ini tidak harus dimiliki oleh atom tertentu, tetapi akan bergerak bebas dalam kisi yang dibentuk oleh atom-atom ini. Jadi, elektron-elektron ini disebut dengan elektron bebas.

Sifat Alloy merupakan paduan logam yang memiliki sifat yang berbeda dari komponen-komponen pembentuknya. Pengaruh dari unsur pemadu tergantung pada bagaimana unsur itu terdapat dalam alloy. Dengan cara paduan sifat-sifat mekanis seperti kekuatan, derajat kekerasan dapat ditinggalkan.

SIFAT LISTRIK Sifat listrik : 1. Jika elektron bergerak bebas, mudah terjadi arus listrik, maka dapat disebut sebagai penghantar listrik (logam). 2. Jika bahan mudah membentuk kutub positif dan negatif, memiliki sifat dielektrik, dapat disebut sebagai konduktor ion positif/negatif [keramik].

3. Jika elektron terikat pada atom, tidak mudah terjadi arus listrik, dapat disebut sebagai isolator atau nonkonduktor 4. Jika bahan dielektrik diberi medan listrik cukup kuat yang melebihi “kekuatan dielektrik”nya, isolator dapat menjadi konduktor.

SIFAT LISTRIK 1. Tahanan kemampuan menahan arus listrik 2. Konduktivitas kemampuan menghantarkan arus listrik 3. Kekuatan dielektrik kemampuan menahan tembus tegangan (batas kemampuan isolasi bahan bila diberi tegangan tertentu sampai isolasinya bocor, arus mengalir)
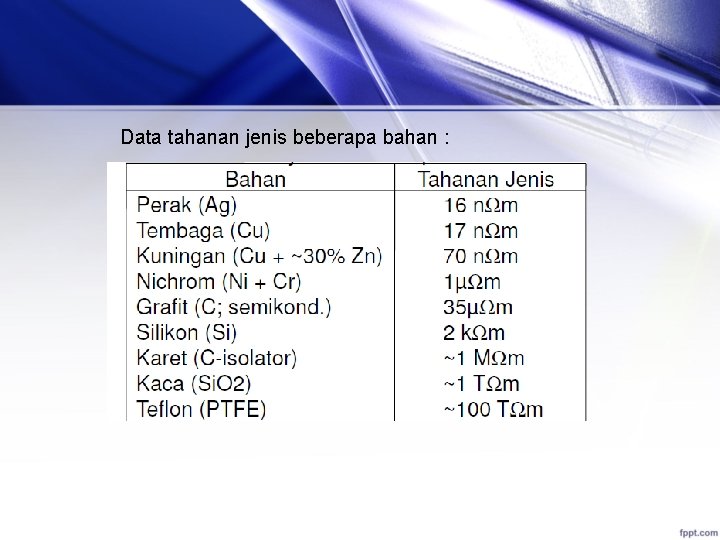
Data tahanan jenis beberapa bahan :

Data kekuatan dielektrik beberapa bahan : Jika tubuh manusia menjadi konduktor, dan dialiri > 1 m. A, jantungnya dapat kacau denyutnya, di samping terjadi konversi energi listrik menjadi energi termal.
- Slides: 53