Materi 4 Bioenergetik Energi anabolisme katabolisme BIOENERGETIKA OKSIDASI

Materi 4 Bioenergetik Energi, anabolisme, katabolisme

BIOENERGETIKA , OKSIDASI BIOLOGI DAN RANTAI RESPIRASI Bioenergetika dan ATP Bioenergetika atau termodinamika biokimia adalah ilmu pengetahuan mengenai perubahan energi yang menyertai reaksi biokimia. Sistem nonbiologik dapat menggunakan energi panas untuk melangsungkan kerjanya. Sedangkan sistem biologik bersifat isotermik dan menggunakan energi kimia untuk memberikan tenaga bagi proses kehidupan.

Kaidah Termodinamika • Kaidah termodinamika dalam sistem biologik • Kaidah pertama termodinamika: • Kaidah pertama ini merupakan hukum penyimpanan energi, yang berbunyi: energi total sebuah sistem, termasuk energi sekitarnya adalah konstan. Ini berarti bahwa saat terjadi perubahan di dalam sistem tidak ada energi yang hilang atau diperoleh. Namun energi dapat dialihkan antar bagian sistem atau dapat diubah menjadi energi bentuk lain. Contohnya energi kimia dapat diubah menjadi energi listrik, panas, mekanik dan sebagainya

lanjutan • Kaidah kedua termodinamika: • Kaidah kedua berbunyi: entropi total sebuah sistem harus meningkat bila proses ingin berlangsung spontan. Entropi adalah derajat ketidakteraturan atau keteracakan sistem. Entropi akan mencapai taraf maksimal di dalam sistem seiring sistem mendekati keadaan seimbang yang sejati. Dalam kondisi suhu dan tekanan konstan, hubungan antara perubahan energi bebas (ΔG) pada sebuah sistem yang bereaksi, dengan perubahan entropi (ΔS), diungkapkan dalam persamaan: • ΔG = ΔH – TΔS • Keterangan: ΔH adalah perubahan entalpi (panas) dan T adalah suhu absolut.

lanjutan • Di dalam kondisi reaksi biokimia, mengingat ΔH kurang lebih sama dengan ΔE, perubahan total energi internal di dalam reaksi, hubungan di atas dapat diungkapkan dengan persamaan: • ΔG = ΔE – TΔS • Jika ΔG bertanda negatif, reaksi berlangsung spontan dengan kehilangan energi bebas (reaksi eksergonik). Jika ΔG sangat besar, reaksi benar-benar berlangsung sampai selesai dan tidak bisa membalik (irreversibel). • Jika ΔG bertanda positif, reaksi berlangsung hanya jika memperoleh energi bebas (reaksi endergonik). Bila ΔG sangat besar, sistem akan stabil tanpa kecenderungan untuk terjadi reaksi.

lanjutan • Peran senyawa fosfat berenergi tinggi dalam penangkapan dan pengalihan energi • Untuk mempertahankan kehidupan, semua organisme harus mendapatkan pasokan energi bebas dari lingkungannya. Organisme autotrofik melakukan metabolisme dengan proses eksergonik sederhana, misalnya tumbuhan hijau menggunakan energi cahaya matahari, bakteri tertentu menggunakan reaksi Fe 2+ Fe 3+. Sebaliknya organisme heterotrofik, memperoleh energi bebasnya dengan melakukan metabolisme yaitu pemecahan molekul organik kompleks.

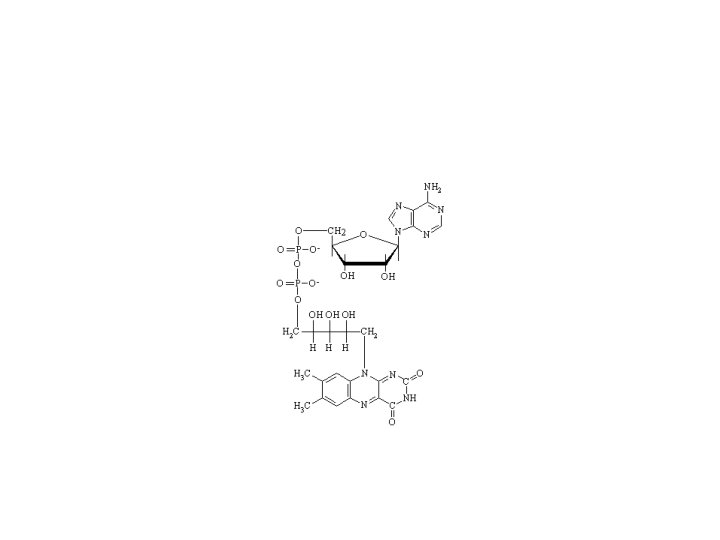
lanjutan • Mg 2+ • Adenosin trifosfat (ATP) berperan sentral dalam pemindahan energi bebas dari proses eksergonik ke proses endergonik. ATP adalah nukleotida trifosfat yang mengandung adenin, ribosa dan 3 gugus fosfat (lihat Gambar 3. 1). Dalam reaksinya di dalam sel, ATP berfungsi sebagai kompleks Mg 2+ • Gambar 3. 1 ATP diperlihatkan sebagai kompleks magnesium
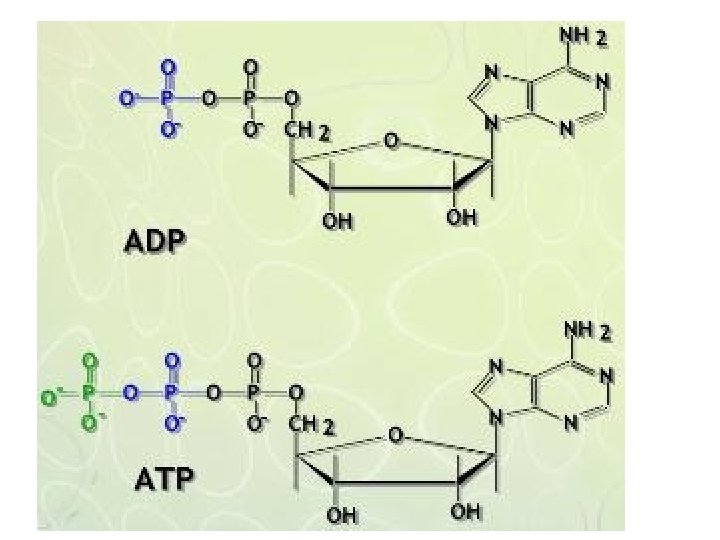

lanjutan • Energi bebas baku hasil hidrolisis senyawa-senyawa fosfat penting dalam biokimia tertera pada Tabel 3. 1. Terlihat bahwa nilai hidrolisis gugus terminal fosfat pada ATP terbagi menjadi 2 kelompok. Pertama, fosfat berenergi rendah yang memiliki ΔG lebih rendah dari pada ΔG 0 pada ATP. Kedua, fosfat berenergi tinggi yang memiliki nilai ΔG lebih tinggi daripada ΔG 0 pada ATP, termasuk di dalamnya, ATP dan ADP, kreatin fosfat, fosfoenol piruvat dan sebagainya.

lanjutan • Senyawa biologik penting lain yang berenergi tinggi adalah tiol ester yang mencakup koenzim A (misal asetil-Ko. A), protein pembawa asil, senyawa-senyawa ester asam amino yang terlibat dalam sintesis protein, Sadenosilmetionin (metionin aktif), uridin difosfat glukosa dan 5 -fosforibosil-1 -pirofosfat.

lanjutan • Tabel 3. 1 Energi bebas baku hasil hidrolisis beberapa senyawa • organofosfat yang memiliki peran penting dalam biokimia • Gugus fosfat berenergi tinggi oleh Lipmann dilambangkan dengan ~℗. Simbol ini menunjukkan bahwa gugus yang melekat pada ikatan, pada saat peralihan pada suatu akseptor yang tepat, akan mengakibatkan pemindahan kuantitas energi bebas yang lebih besar. Oleh karena itulah sebagian ahli biokimia lebih menyukai istilah potensial pemindahan gugus daripada ikatan berenergi tinggi.

lanjutan • Berdasarkan posisi ATP pada Tabel 3. 1, maka ATP merupakan donor fosfat berenergi tinggi (donor energi bebas) bagi senyawa-senyawa di bawahnya. Di sisi lain, ADP dapat menerima fosfat berenergi tinggi untuk membentuk ATP dari senyawa yang berada di atas ATP dalam tabel. Akibatnya siklus ATP/ADP menghubungkan proses-proses yang menghasilkan ~℗ dan proses-proses yang menggunakan ~℗. Dengan demikian ATP terus dikonsumsi dan terus diproduksi. Proses terjadi dengan kecepatan sangat tinggi, karena depot ATP/ADP sangat kecil dan hanya cukup untuk mempertahankan jaringan aktif dalam beberapa detik saja.

lanjutan • Ada 3 sumber utama ~℗ yang berperan dalam konservasi atau penangkapan energi. 1. Fosforilasi oksidatif • Fosforilasi oksidatif adalah sumber ~℗ terbesar dalam organisme aerobik. Energi bebas untuk menggerakkan proses ini berasal dari oksidasi rantai respirasi di dalam mitokondria dengan menggunakan oksigen. 2. Glikolisis • Dalam glikolisis terjadi pembentukan netto dua ~℗ yang terjadi akibat pembentukan laktat 3. Siklus asam sitrat/Siklus Krebs/Siklus Asam Tri Karboksilat • Dalam siklus asam sitrat satu ~℗ dihasilkan langsung pada tahap suksinil tiokinase.

lanjutan 4. Oksidasi biologi • Oksidasi adalah pengeluaran elektron dan reduksi adalah pemerolehan elektron. Sebagai contoh adalah oksidasi ion fero menjadi feri yang dilukiskan pada Gambar 3. 3. Dengan demikian oksidasi akan selalu disertai reduksi akseptor elektron. e- (elektron) • Fe 2+ Fe 3+ • Gambar 3. 3 Oksidasi ion fero menjadi feri

lanjutan • Enzim-enzim penting dalam oksidasi biologi • Enzim-enzim yang terlibat dalam reaksi reduksi dan oksidasi dinamakan enzim oksidoreduktase. Terdapat 4 kelompok enzim oksidoreduktase yaitu: oksidase, dehidrogenase, hidroperoksidase dan oksigenase.

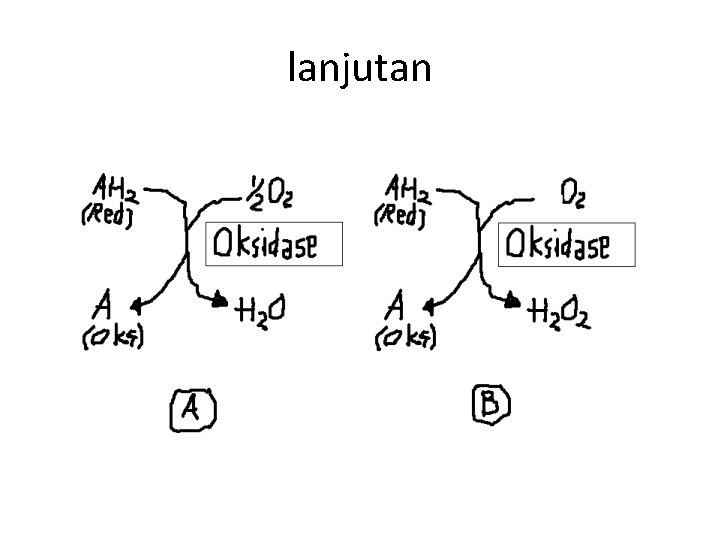
lanjutan • • Oksidase Enzim oksidase mengkatalisis pengeluaran hidrogen dari substrat dengan menggunakan oksigen sebagai akseptor hidrogen. Enzimenzim tersebut membentuk air atau hidrogen peroksida. Contoh peran enzim tersebut dilukiskan pada Gambar 3. 4
lanjutan

lanjutan • Gambar 3. 4 Oksidasi metabolit yang dikatalisis oleh enzim oksidase • Termasuk sebagai oksidase antara lain sitokrom oksidase, oksidase asam L-amino, xantin oksidase, glukosa oksidase.

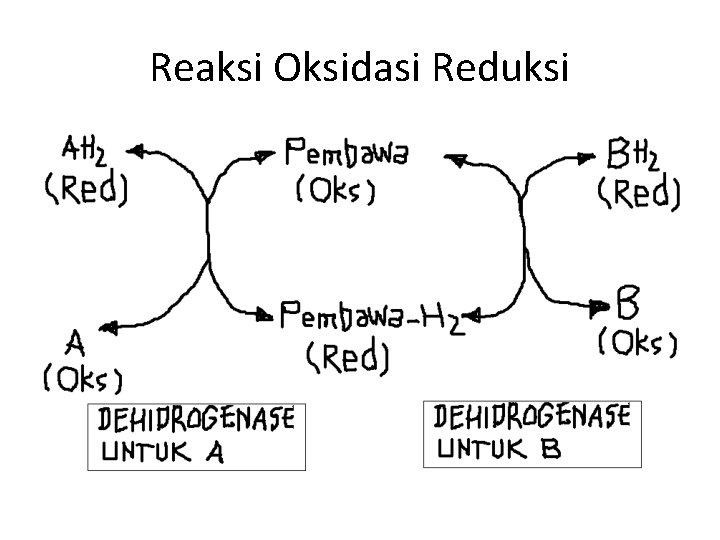
lanjutan • • Dehidrogenase tidak dapat menggunakan oksigen sebagai akseptor hidrogen. Enzim-enzim ini memiliki 2 fungsi utama yaitu: Pertama, berperan dalam pemindahan hidrogen dari substrat yang satu ke substrat yang lain dalam reaksi reduksi-oksidasi berpasangan. Kedua, sebagai komponen dalam rantai respirasi pengangkutan elektron dari substrat ke oksigen.
Reaksi Oksidasi Reduksi

lanjutan • Gambar 3. 5 Oksidasi suatu metabolit yang dikatalisis oleh enzim-enzim dehidrogenase • Contoh dari enzim dehidrogenase adalah suksinat dehidrogenase, asil-Ko. A dehidrogenase, gliserol-3 -fosfat dehidrogenase, semua sitokrom kecuali sitokrom oksidase.

lanjutan • • Hidroperoksidase Enzim hidroperoksidase menggunakan hidrogen peroksida atau peroksida organik sebagai substrat. Ada 2 tipe enzim yang masuk ke dalam kategori ini yaitu peroksidase dan katalase. Enzim hidroperoksidase melindungi tubuh terhadap senyawa-senyawa peroksida yang berbahaya. Penumpukan peroksida menghasilkan radikal bebas yang dapat merusak membran sel dan menimbulkan kanker serta aterosklerosis.

lanjutan • • Hidroperoksidase Enzim hidroperoksidase menggunakan hidrogen peroksida atau peroksida organik sebagai substrat. Ada 2 tipe enzim yang masuk ke dalam kategori ini yaitu peroksidase dan katalase. Enzim hidroperoksidase melindungi tubuh terhadap senyawa-senyawa peroksida yang berbahaya. Penumpukan peroksida menghasilkan radikal bebas yang dapat merusak membran sel dan menimbulkan kanker serta aterosklerosis.

lanjutan • • Oksigenase mengkatalisis pemindahan langsung dan inkorporasi oksigen ke dalam molekul substrat. Enzim ini dikelompokkan menjadi 2 yaitu monooksigenase dan dioksigenase.

Rantai Respirasi • Rantai respirasi dan fosforilasi oksidatif • Rantai respirasi terjadi di dalam mitokondria sebagai pusat tenaga. Di dalam mitokondria inilah sebagian besar peristiwa penangkapan energi yang berasal dari oksidasi respiratorik berlangsung. Sistem respirasi dengan proses pembentukan intermediat berenergi tinggi (ATP) ini dinamakan fosforilasi oksidatif. Fosforilasi oksidatif memungkinkan organisme aerob menangkap energi bebas dari substrat respiratorik dalam proporsi jauh lebih besar daripada organisme anaerob.

Fosforilasi Oksidatif • Proses fosforilasi oksidatif • Organisme kemotrop memperoleh energi bebas dari oksidasi molekul bahan bakar, misalnya glukosa dan asam lemak. Pada organisme aerob, akseptor elektron terakhir adalah oksigen. Namun elektron tidak langsung ditransfer langsung ke oksigen, melainkan dipindah ke pengemban-pengemban khusus antara lain nikotinamida adenin dinukleotida (

Fosforilasi oksidatif di Mitokhondria • NAD+) dan flavin adenin dinukleotida (FAD). • Pengemban tereduksi ini selanjutnya memindahkan elektron ke oksigen melalui rantai transport elektron yang terdapat pada sisi dalam membran mitokondria (Gambar 3. 7). Gradien proton yang terbentuk sebagai hasil aliran elektron ini kemudian mendorong sintesis ATP dari ADP dan Pi dengan bantuan enzim ATP sintase. Proses tersebut dinamakan fosforilasi oksidatif. Dalam hal ini energi dipindahkan dari rantai transport elektron ke ATP sintase oleh perpindahan proton melintasi membran. Proses ini dinamakan kemiosmosis.
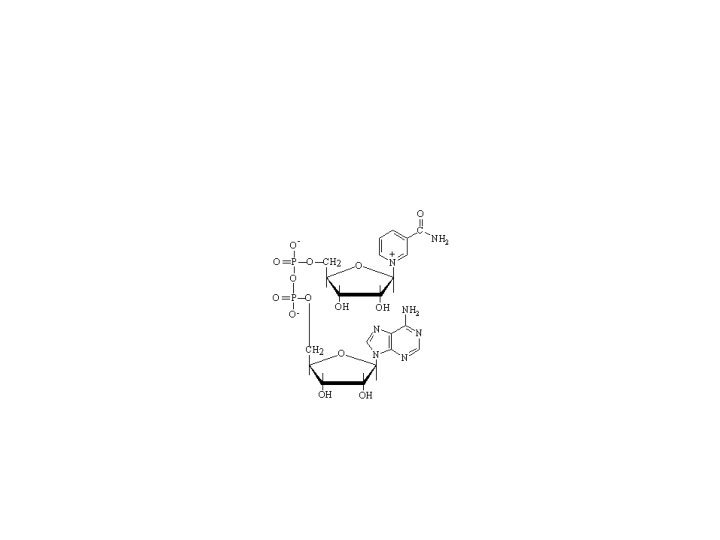
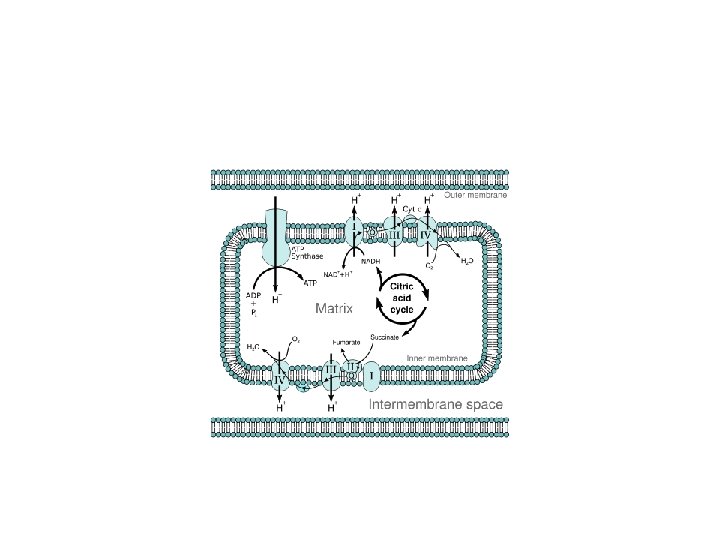

• Gambar 3. 7 Ringkasan proses fosforilasi oksidatif di dalam mitokondria. Rantai transport elektron membawa proton dan elektron, memindahkan elektron dari donor ke akseptor dan mengangkut proton melalui membran. • Kompleks INADH + H+FMNFe 2+SCo. QNAD+FMNH 2 Fe 3+SCo. QH 2 Kompleks IISuccinate. FADFe 2+SCo. QFumarate. FADH 2 Fe 3+SCo. QH 2 Kompleks IIICo. QH 2 cyt b ox. Fe 2+Scyt c 1 oxcyt c red. Co. Qcyt b red. Fe 3+Scyt c 1 redcyt c ox. Kompleks IVcyt c redcyt a oxcyt a 3 red. O 2 cyt c oxcyt a redcyt a 3 ox 2 H 2 OGambar 3. 8 Tahap-tahap proses fosforilasi oksidatif. Secara ringkas fosforilasi oksidatif, terdiri atas 5 proses dengan dikatalisis oleh kompleks enzim, masing-masing kompleks I, kompleks III, kompleks IV dan kompleks V (Tabel 3. 2). • Tabel 3. 2 Informasi tentang enzim yang berperan dalam fosforilasi oksidatif

• Nama. Penyusun k. Da Polypeptides. Kompleks INADH dehydrogenase (or) NADH-coenzyme Q reductase 80025 Kompleks IISuccinate dehydrogenase (or) Succinate-coenzyme Q reductase 1404 Kompleks IIICytochrome C - coenzyme Q oxidoreductase 250910 Kompleks IVCytochrome oxidase 17013 Kompleks VATP synthase 38012 -14 • Pada Gambar 3. 8, kotak biru (gelap) di bawah menunjukkan reaksi oksidasi-reduksi yang terjadi pada masing-masing kompleks enzim. Singkatan-singkatan diuraikan sebagai berikut: FMN: flavin mononukleotida, Fe 2+S: besi tereduksisulfur, Fe 3+S: besi teroksidasi-sulfur, cyt: sitokrom, Co. Q: koenzim Q.

lanjutan • • Kompleks I Pada tahap ini, masing-masing molekul NADH memindahkan 2 elektron berenergi tinggi ke FMN, kemudian ke protein besisulfur dan terakhir ke koenzim Q (ubiquinon) •

lanjutan • • Kompleks II FADH 2 dihasilkan oleh suksinat dehidrogenase dalam siklus asam sitrat, memindahkan elektron ke Co. Q melalui kompleks II. FADH 2 dihasilkan oleh asil Ko. A dehidrogenase dalam oksidasi beta asam lemak, memindahkan elektron ke Co. Q melalui kompleks yang sama.
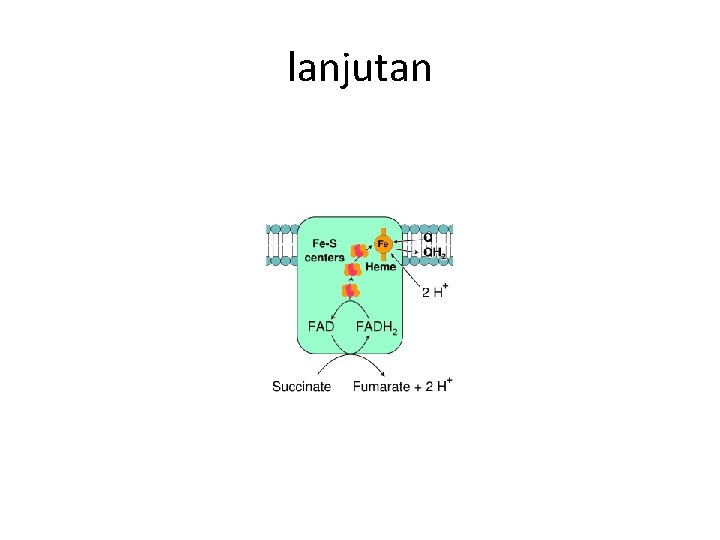
lanjutan

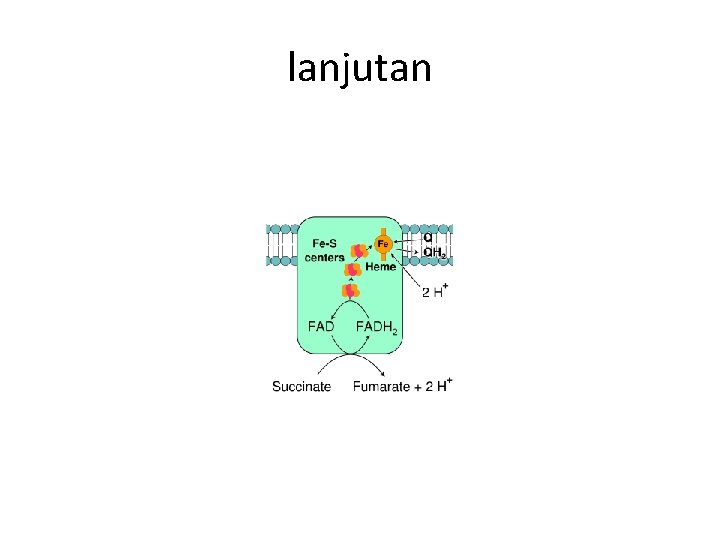
lanjutan • • Kompleks III Co. Q memindahkan elektron ke serangkaian sitokrom dan protein besi-sulfur. Sitokrom terdiri atas kelompok heme seperti hemoglobin dan besi dengan heme menerima elektron.
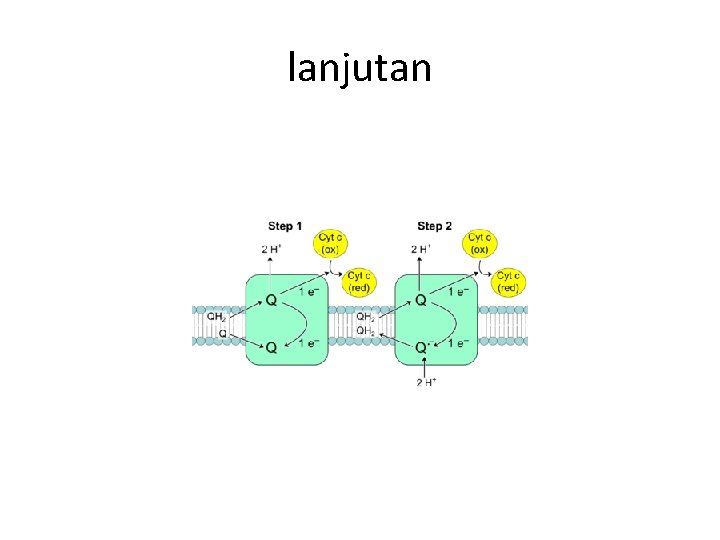
lanjutan
lanjutan

lanjutan • • Kompleks III Co. Q memindahkan elektron ke serangkaian sitokrom dan protein besi-sulfur. Sitokrom terdiri atas kelompok heme seperti hemoglobin dan besi dengan heme menerima elektron.

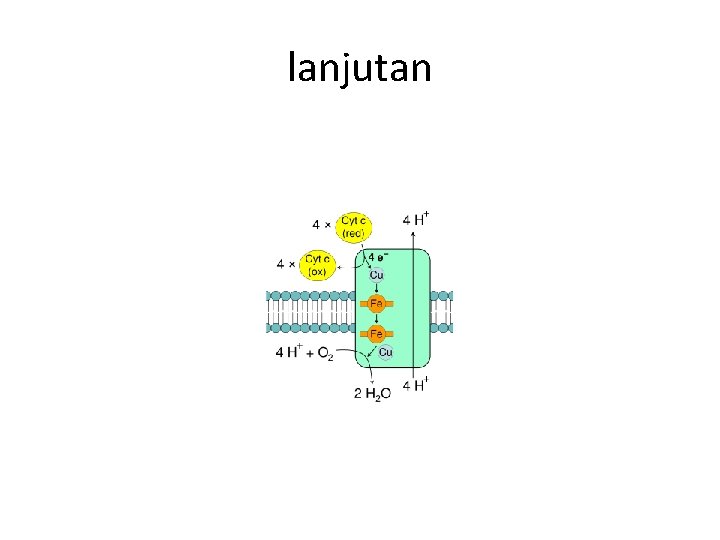
lanjutan • • Kompleks IV Penerima terakhir dari rantai transport elektron adalah kompleks besar terdiri atas 2 heme dan 2 atom tembaga.
lanjutan

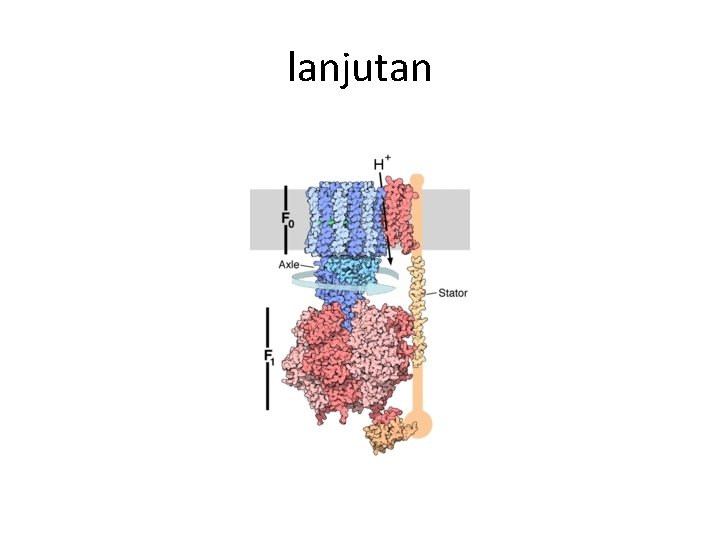
lanjutan • • Kompleks V Pada tahap ini, protein kompleks yang mengkatalisis konversi ADP menjadi ATP, diisikan oleh gradien kemiosmotik. Proton mengalir kembali ke matriks mitokondria melalui kompleks ATP sintase dan energi berasal dari penurunan gradien p. H digunakan untuk membentuk ATP.
lanjutan

lanjutan • Pada fosforilasi oksidatif, pelibatan NADH menghasilkan pembentukan 3 molekul ATP, sedangkan pelibatan FADH 2 menghasilkan pembentukan 2 molekul ATP.

Metabolisme

Metabolisme – semua proses kimia dan reaksi kimia yang terjadi dalam sel • 1. Katabolisme ( Katabolik ) – Pemecahan molekul organik kompleks menjadi senyawa sederhana – Melepaskan ENERGI • 2. Anabolisme ( Anabolik) – Pembentukan / Pembangunan molekul organik kompleks dari senyawa sederhana – Membutuhkan ENERGI

Enzymes - adalah katalis yang mempercepat dan langsung terlibat mempercepat reaksi kimia, enzym sendiri tidak ikut dalam reaksi • A. Enzym yg kerjanya spesifik – Lipase – Sukrase – Urease – Protease – Dnase Lemak / Lipida Sukrose Urea Protein DNA
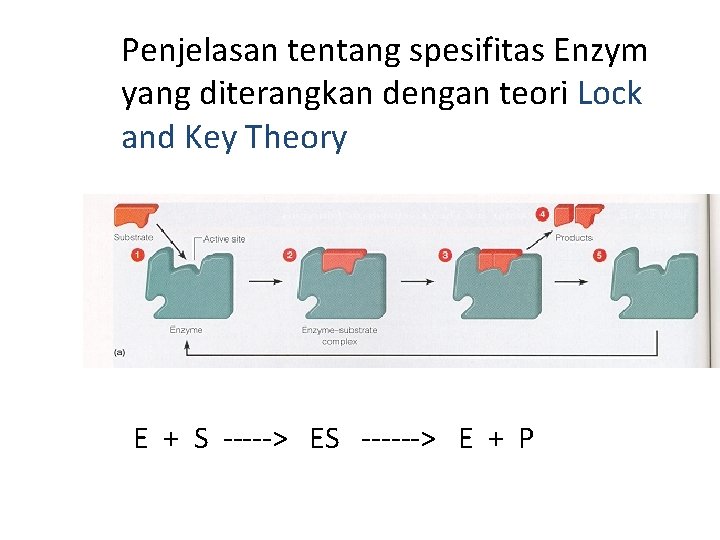
Penjelasan tentang spesifitas Enzym yang diterangkan dengan teori Lock and Key Theory E + S -----> ES ------> E + P

Pemberian Nama Enzym – adalah memberikan tambahan “ase” pada substrat • • • Sukrosa Lemak DNA Protein Pemindahan Hydrogen Pemindahan fofat Sukrase Lipase DNase Protease Dehydrogenase Phosphotase

Penggolongan Enzym berdasarkan aktivitasnya • Juga berdasarkan proses yang dikatalisa • 1. Oxidoreductase oxidation & reduction • 2. Hydrolase hydrolysis • 3. Ligase synthesis
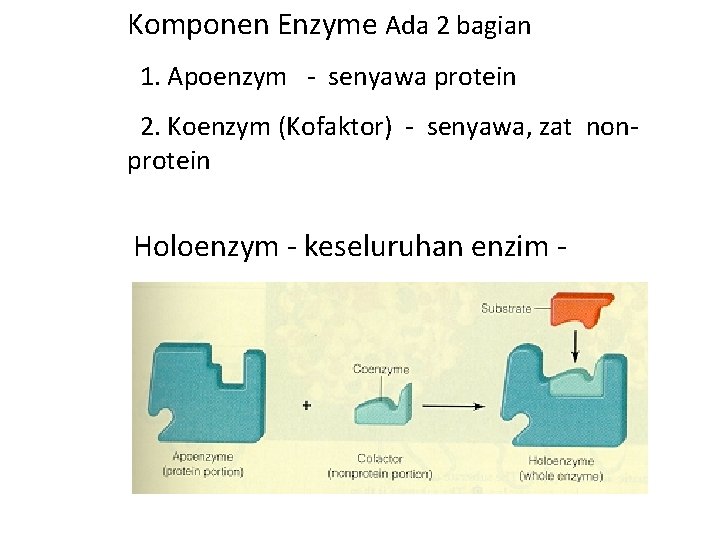
Komponen Enzyme Ada 2 bagian 1. Apoenzym - senyawa protein 2. Koenzym (Kofaktor) - senyawa, zat nonprotein Holoenzym - keseluruhan enzim -

Koenzym • Babarapa diperoleh dari vitamin • 1. Niasin – NAD (Nikotinamid adenin dinukleotida) • 2. Riboflavin – FAD (Flavin adenin dinucleotida) • 3. Asam Pantantotenat (Pantothenic Acid) – Co. Enzyme A
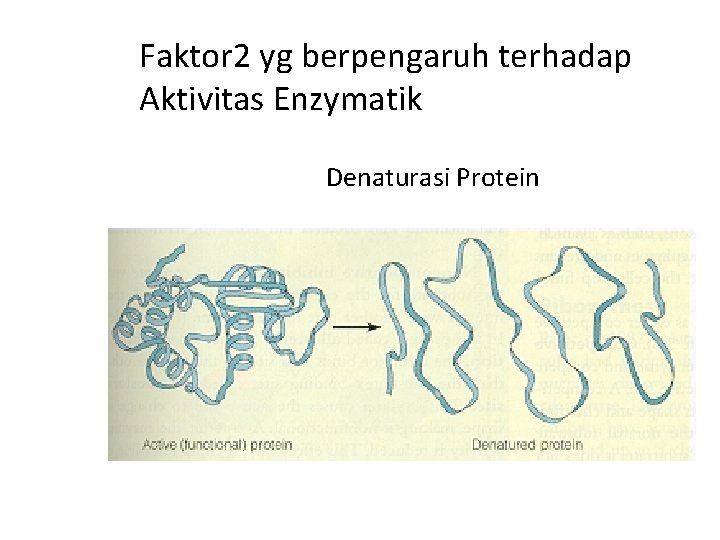
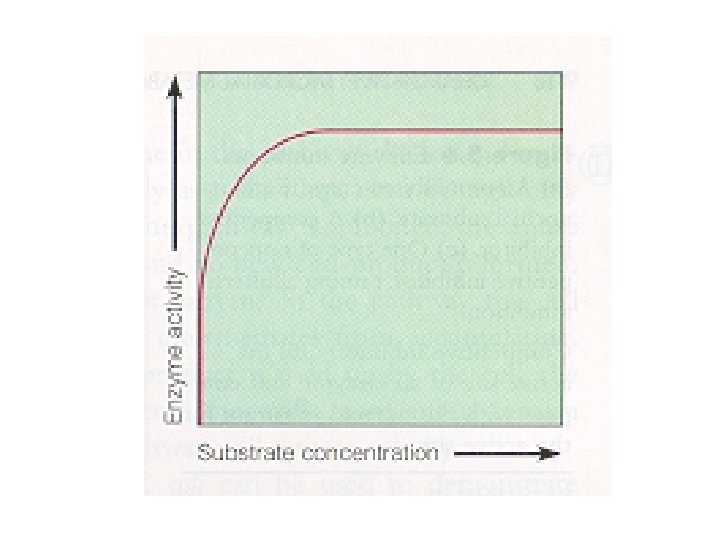
Faktor 2 yg berpengaruh terhadap Aktivitas Enzymatik Denaturasi Protein
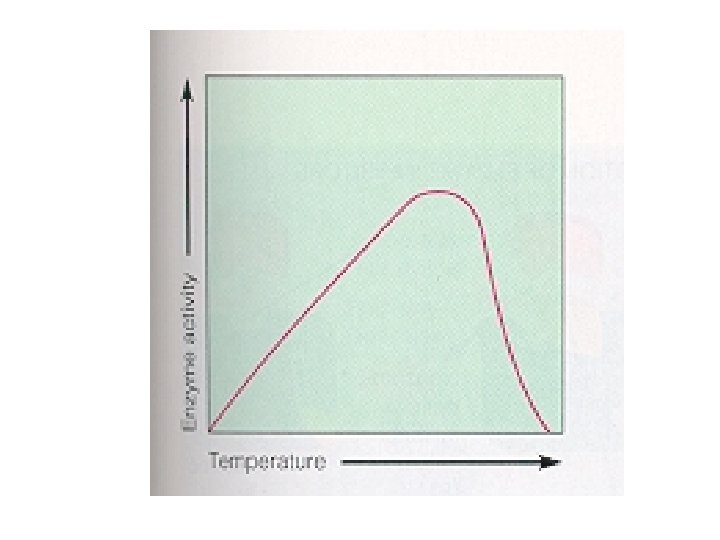
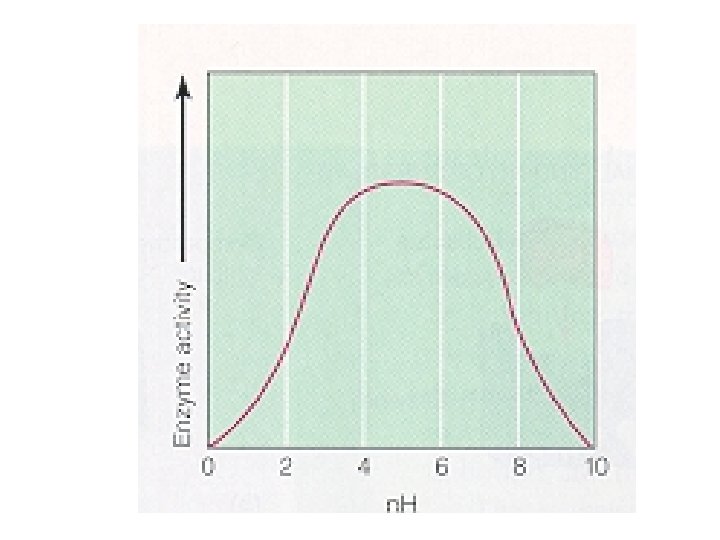
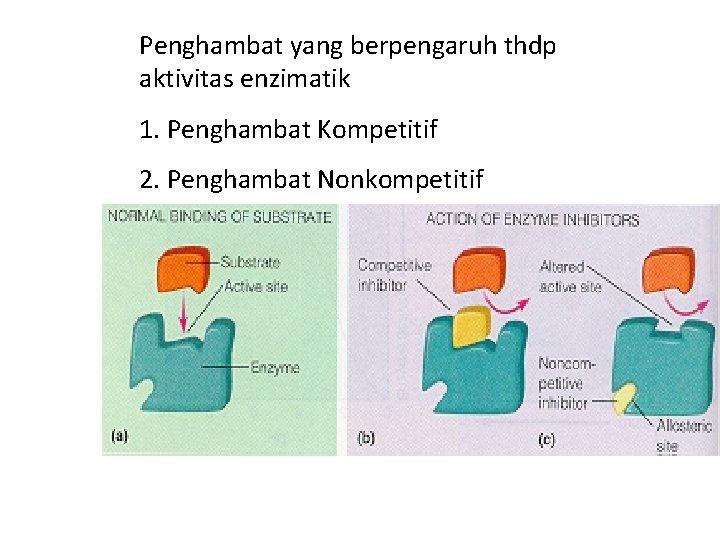
Penghambat yang berpengaruh thdp aktivitas enzimatik 1. Penghambat Kompetitif 2. Penghambat Nonkompetitif

Penghambat Kompetitif – memblok sisi aktif • 1. Penisilin – Memblok sisi aktif enzim sehingga terjadi penghambatan karena adanya jembatan silang pentaglisin • 2. Sulfanilamid ( Obat 2 Sulfa ) – memblok sisi aktif pada enzym yg mengkorvensi PABA menjadi Asam Folat • Folic Acid - required for the synthesis of DNA and RNA Selective Toxicity
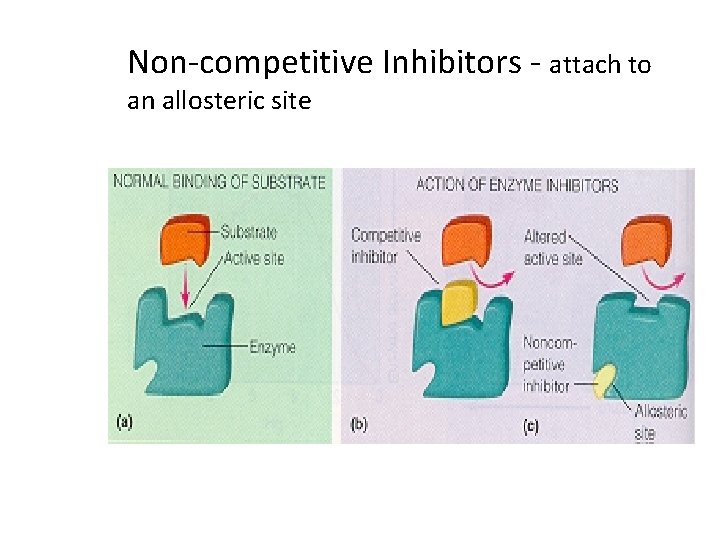
Non-competitive Inhibitors - attach to an allosteric site
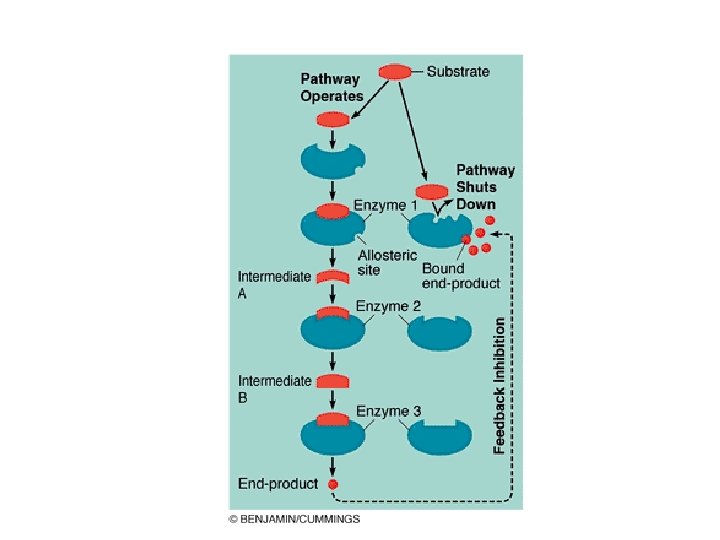

Produksi Energi • 1. Oksidasi – Menunjuk pada lepasnya / hilangnya Hidrogen dan atau elektron • 2. Reduksi – Penangkapan/Penggabungan Hidrogen dan/atau elektron NAD Cycle

Katabolisme Karbohidrat • Mikroorganisme mengoksidasi karbohidrat sebagai sumber energi primer • Glukosa – secara umum dapat menjadi sumber energi • Energi dapat dihasilkan dari Glucosa dengan cara : – Respirasi – Fermentasi

Respirasi Selular secara Aerobik • Elektron dilepaskan dari oksidasi melalui cara Sistem Transport Elektron ( Electron Transport System ) dengan oksigen sebagai penerima elektron (Final Electron Acceptor) • Persamaan Umum : • Glukosa + oksigen----> Karbon dioksida + air • • ATP

Persamaan Kimia • C 6 H 12 O 6 + 6 O 2 -------> 6 CO 2 + 6 H 2 O • • 38 ADP + 38 P 38 ATP

Respirasi Seluler Aerobik • 4 subpathway • • 1. Glikolisis 2. Reaksi Transisi 3. Siklus Kreb 4. Sistem Transport Elektron (Electron Transport System)

1. Glikolisis (pemecahan gula ) • Oksidasi Glukosa menjadi 2 molekul Asam Piruvat • Siklus Embden-Meyerhof • Hasil akhir Glycolisis: – 2 Asam Piruvat – 2 NADH 2 – 2 ATP

2. Reaksi Transisi • Menghubungkan Glikolisis ke Siklus Kreb • Hasil akhir : – 2 Asetyl Ko. Enzym A – 2 CO 2 – 2 NADH 2

3. Silus Krebs (Siklus Asam Sitrat ) • Urutan reaksi kimia awal dan akhirnya asam sitrat • Hasil akhir: – 2 – 6 – 2 – 4 ATP NADH 2 FADH 2 CO 2

4. Sistem Transport Elektron (Electron Transport System) • Terjadi dalam membran sel bakteri • Model Khemiosomosa Mitchell – 34 ATP

Bagaimana penjelasan 34 ATP dari E. T. S. ? 3 ATP for each NADH 2 2 ATP for each FADH 2 • • Glicolisis • R. Tansisi • Siklus Kreb • Total NADH 2 2 2 6 10 • 10 x 3 = 30 ATP • FADH 2 • Glicolisis • R. Transisi • Siklus Kreb • Total • 2 x 2 = 4 ATP 0 0 2 2
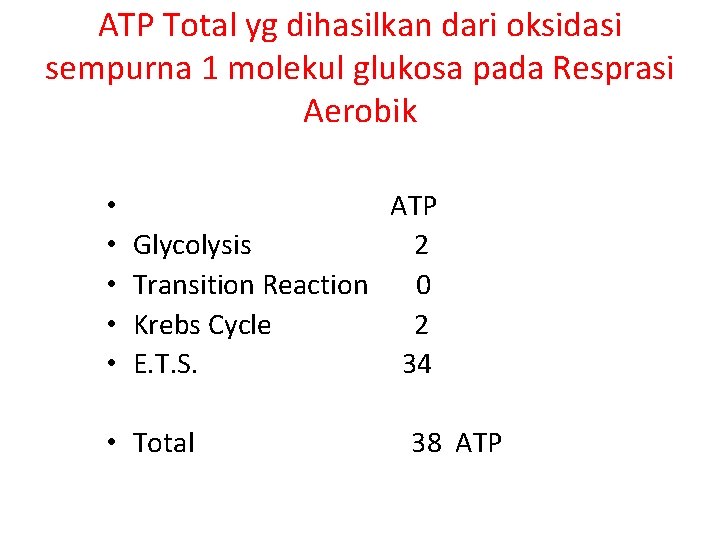
ATP Total yg dihasilkan dari oksidasi sempurna 1 molekul glukosa pada Resprasi Aerobik • • • ATP Glycolysis 2 Transition Reaction 0 Krebs Cycle 2 E. T. S. 34 • Total 38 ATP

Respirasi Anaerob • Elektron yg dihasilkan melalui oksidasi melalui E. T. S. , tetapi oksygen tidak sebagai elektron aseptor terakhir • Nitrat (NO 3 -) ----> Nitrit (NO 2 -) • Sulfat (SO 24 -) ----> Hidrogen Diulfida (H 2 S) • Karbonat (CO 24 -) -----> Metan (CH 4)

Fermentasi • Proses Anaerob yg tidak memlaui E. T. S. Umumnya melibatkan oksidasi yang tidak sempurna dari karbohidrat sehingga dapat menjadikan oksigen sebagai aseptor elektron terakhir. • Glicolisis – ditambah tahapan tambahan

Fermentasi dapat menghasilkan sejumlah hasil akhir 1. Jenis mikroorganisme 2. Substrat Original 3. Kandungan Enzym yg sedang ada dan aktif

1. Fermentasi Asam Laktat • • Hanya 2 ATP Hasil akhir - Asam Laktat Makanan Busuk Produksi Makanan – Yogurt - Susu/Milk – “Pickles” - timun/Cucumbers – “Sauerkraut” - Kubis • 2 Genera: – Streptococcus – Lactobacillus

2. Fermentasi Alcohol • Hanya 2 ATP • Hasil akhir : • • – alcohol – CO 2 Minuman Beralkohol Roti yang sudah beralkohol Buah 2 an sudah beralkohol Saccharomyces cerevisiae (Yeast)

3. Fermentasi Asam Campuran • Hanya 2 ATP • Hasil akhir - “Tidak Jelas” • Escherichia coli dan beberapa mikroorganisme enteric

Fermentasi Asam Propionat • Hanya 2 ATP • Hasil akhir : – Asam Propionat – CO 2 • Propionibacterium sp.
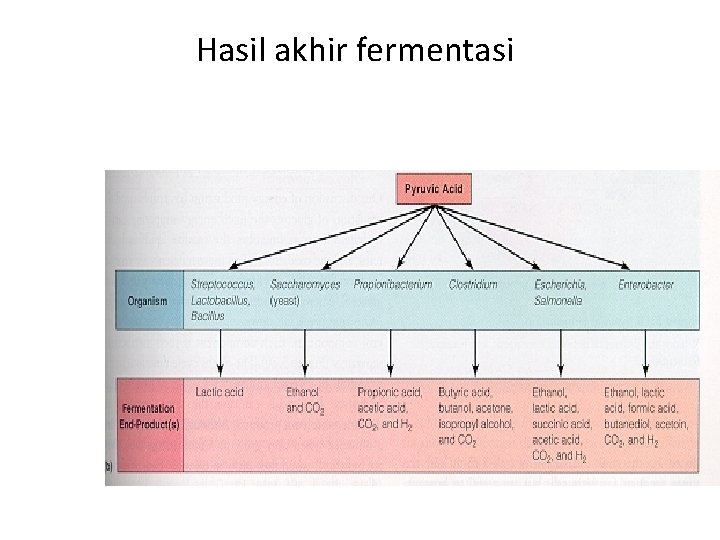
Hasil akhir fermentasi
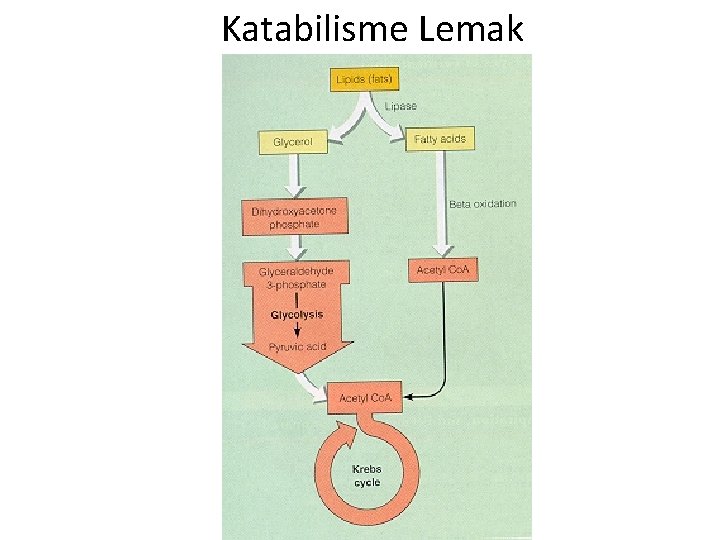
Katabilisme Lemak
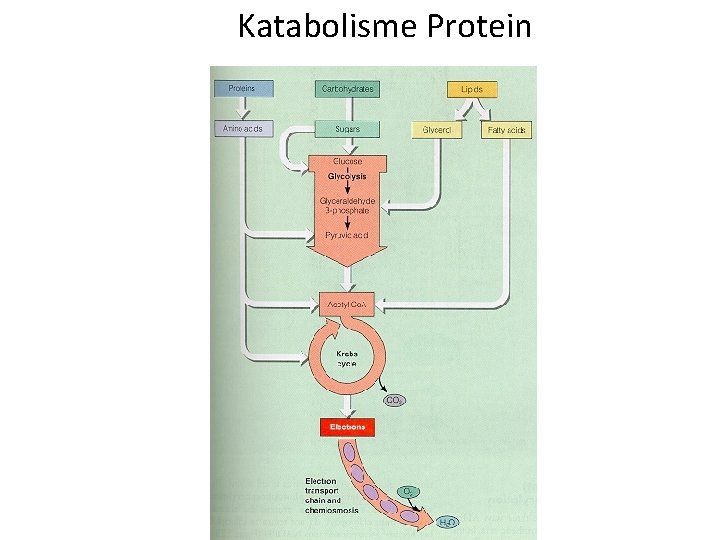
Katabolisme Protein

Fotosintesis - Konversi of energi dari sinar matahari menjadi energi kimia • Energi kimia digunakan untuk mereduksi CO 2 menjadi gula (CH 2 O) • Fiksasi Karbon – siklus karbon di lingkungan (Kehidupan sangat tergantung dari hal tersebut ) • Photosynthesis – Tanaman Hijau – Algae/Ganggang – Bakteri fotosintesis (Cyanobacteria)

Persamaan Reaksi • 6 CO 2 + 6 H 2 O + sinar matahari -----> C 6 H 12 O 6 + 6 O 2 • 2 Bagian : – 1. Reaksi Terang – 2. Reaksi Gelap

Reaksi Terang • Fotofofosforilasi Non-Siklis – O 2 – ATP – NADPH 2 • Reaksi Terang (disederhanakan )

2. Reaksi Gelap

Power. Point to accompany Foundations in Microbiology Fifth Edition Talaro Chapter 8 Copyright The Mc. Graw-Hill Companies, Inc. Permission required for reproduction or display.

Microbial Metabolism: The Chemical Crossroads of Life Chapter 8

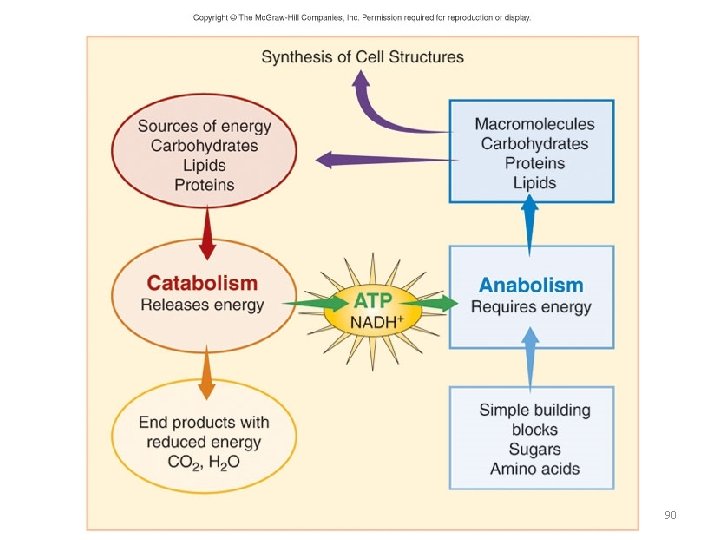
Metabolism The sum total of all chemical reactions & physical workings occurring in a cell

2 types of metabolism • Anabolism - biosynthesis – building complex molecules from simple ones – requires energy (ATP) • Catabolism - degradation – breaking down complex molecules into simple ones – generates energy (ATP) 89
90

91
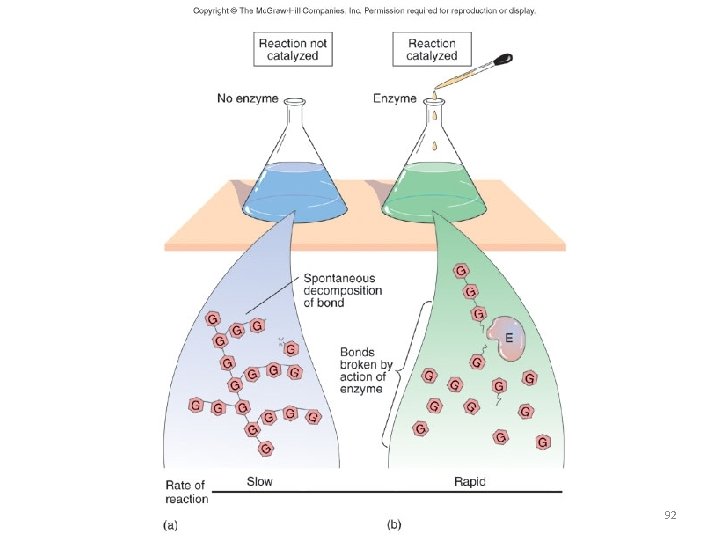
92

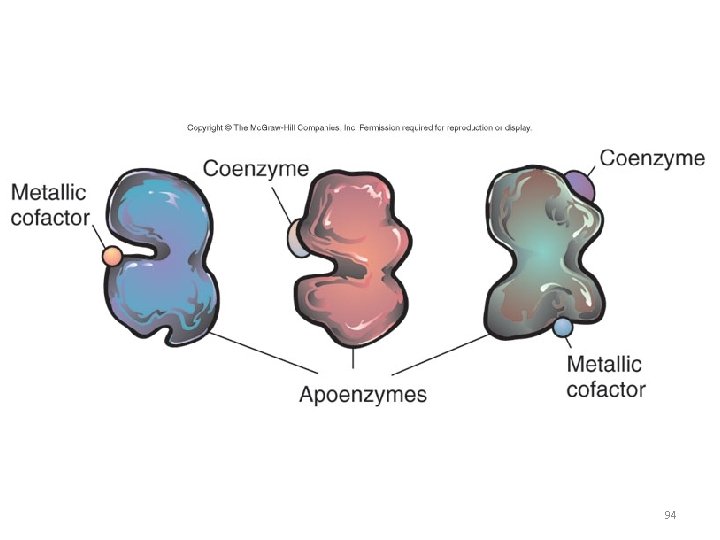
Enzyme structure • Simple enzymes – consist of protein alone • Conjugated enzymes or holoenzymes – contain protein and nonprotein molecules – apoenzyme –protein portion – cofactors – nonprotein portion • metallic cofactors – iron, copper, magnesium • coenzymes -organic molecules - vitamins 93
94
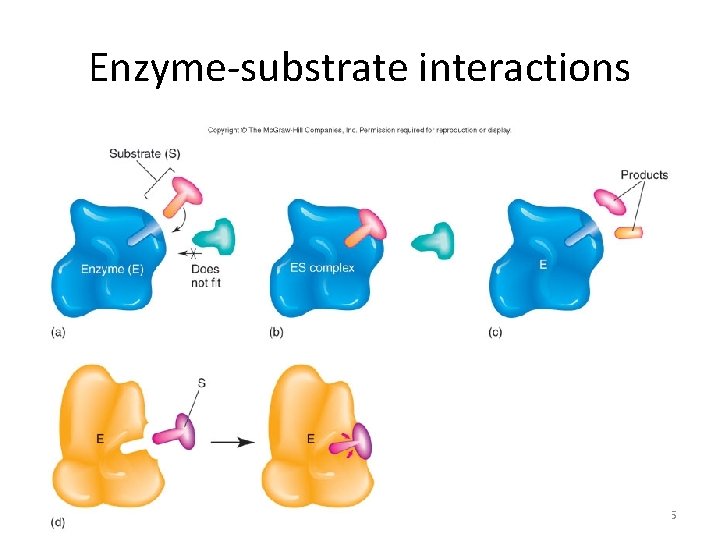
Enzyme-substrate interactions 95

• Exoenzymes – transported extracellularly, where they break down large food molecules or harmful chemicals; cellulase, amylase, penicillinase • Endoenzymes – retained intracellularly & function there 96
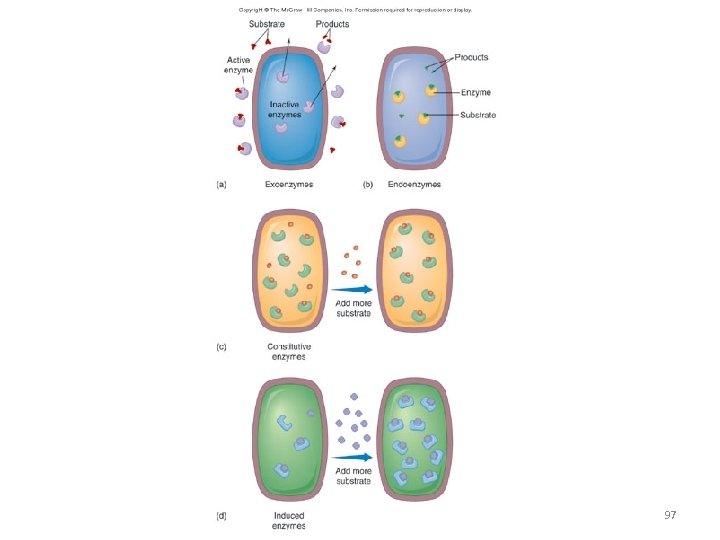
97

• Constitutive enzymes – always present, always produced in equal amounts or at equal rates, regardless of amount of substrate; enzymes involved in glucose metabolism • Induced enzymes – not constantly present, produced only when substrate is present, prevents cell from wasting resources 98
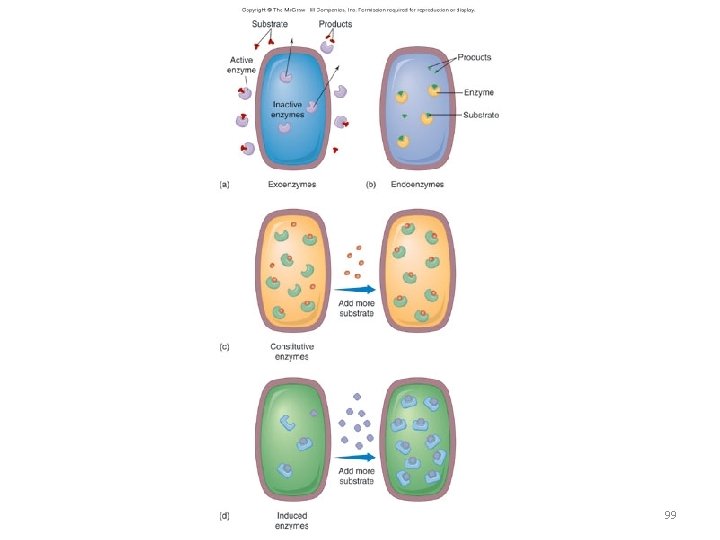
99

• Synthesis or condensation reactions – anabolic reactions to form covalent bonds between smaller substrate molecules, require ATP, release one molecule of water for each bond • Hydrolysis reactions– catabolic reactions that break down substrates into small molecules, requires the input of water 100
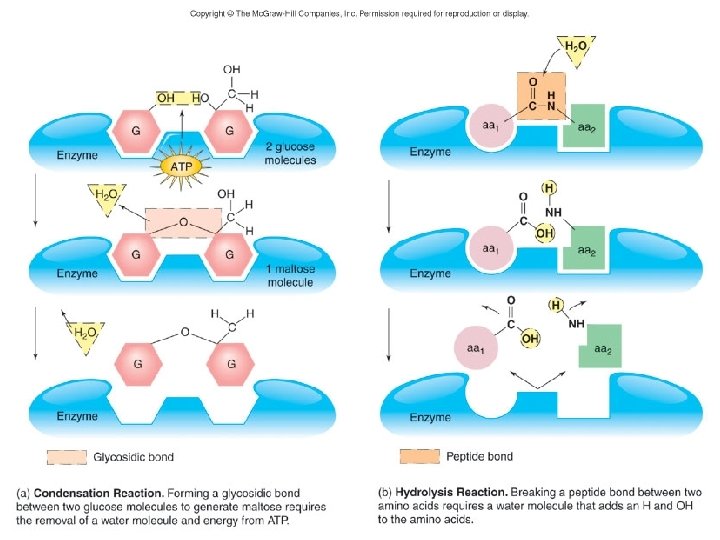
101

Transfer reactions by enzymes 1. Oxidation-reduction reactions – transfer of electrons 2. Aminotransferases – convert one type of amino acid to another by transferring an amino group 3. Phosphotransferases – transfer phosphate groups, involved in energy transfer 4. Methyltransferases – move methyl groups from one molecule to another 5. Decarboxylases – remove carbon dioxide from organic acids 102
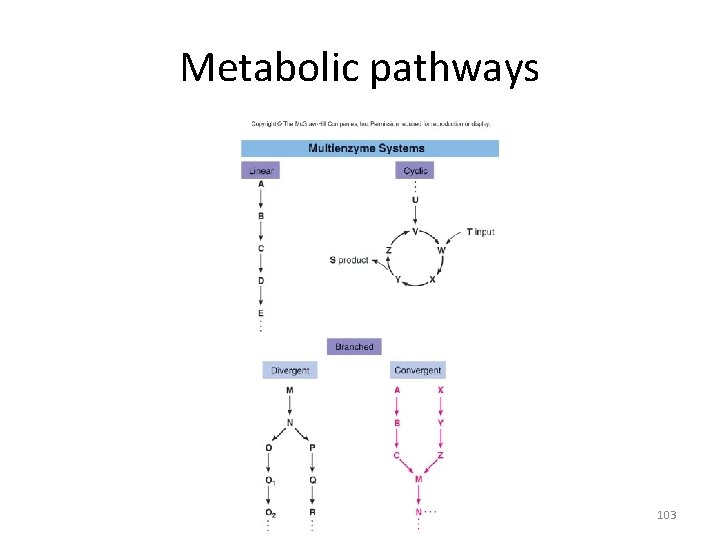
Metabolic pathways 103

Control of enzyme activity 1. Competitive inhibition – substance that resembles normal substrate competes with substrate for active site 2. Feedback inhibition – concentration of product at the end of a pathway blocks the action of a key enzyme 3. Feedback repression – inhibits at the genetic level by controlling synthesis of key enzymes 4. Enzyme induction – enzymes are made only when suitable substrates are present 104
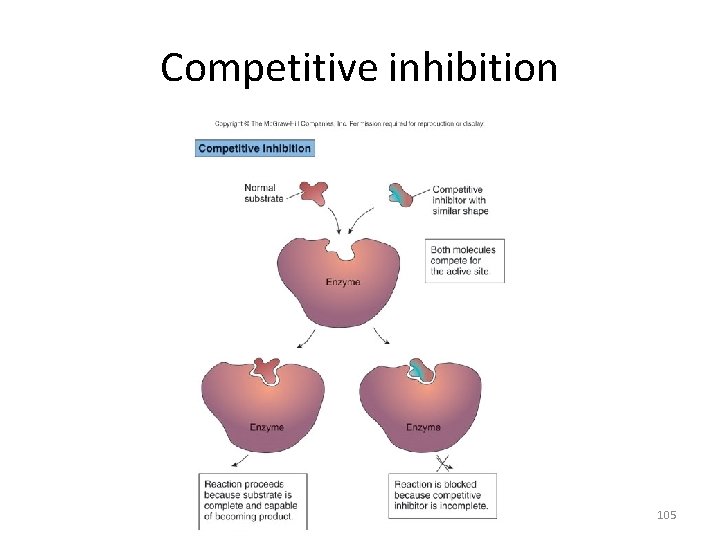
Competitive inhibition 105

Energy –capacity to do work or cause change • Endergonic reactions – consume energy • Exergonic reactions – release energy 106

Redox reactions • always occur in pairs • There is an electron donor and electron acceptor which constitute a redox pair • The process salvages electrons & their energy. • released energy can be captured to phosphorylate ADP or another compound 107

Electron carriers • resemble shuttles that are loaded and unloaded with electrons and hydrogen • most carriers are coenzymes, NAD, FAD, NADP, coenzyme A & compounds of the respiratory chain 108
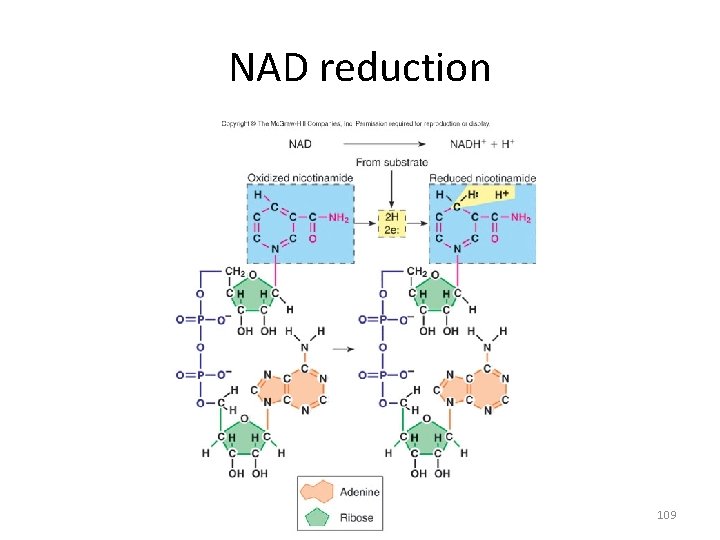
NAD reduction 109
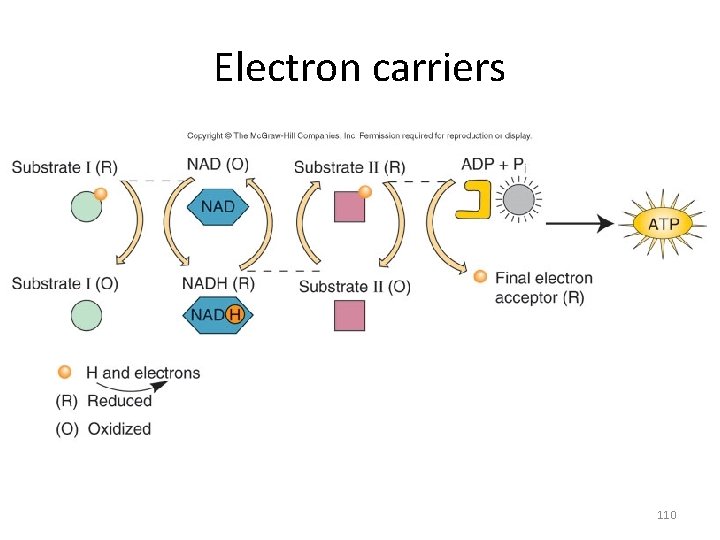
Electron carriers 110

ATP • 3 part molecule consisting of – adenine – a nitrogenous base – ribose – a 5 -carbon sugar – 3 phosphate groups • Removal of the terminal phosphate releases energy 111
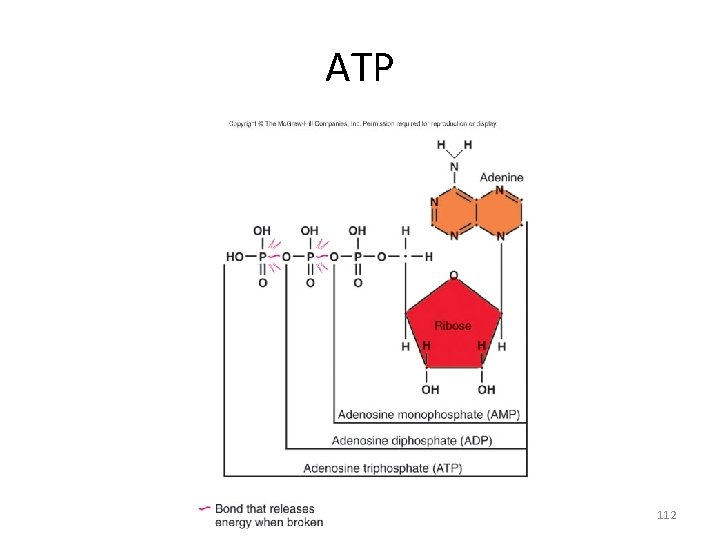
ATP 112
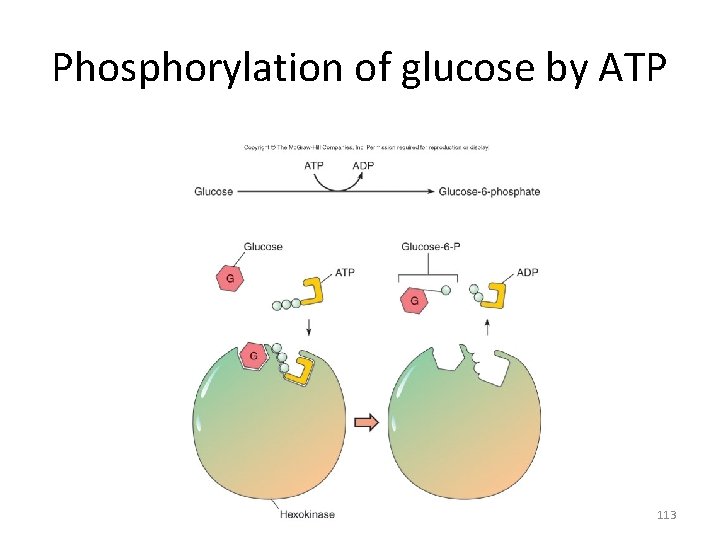
Phosphorylation of glucose by ATP 113

Formation of ATP 1. substrate-level phosphorylation 2. oxidative phosphorylation 3. photophosphorylation 114
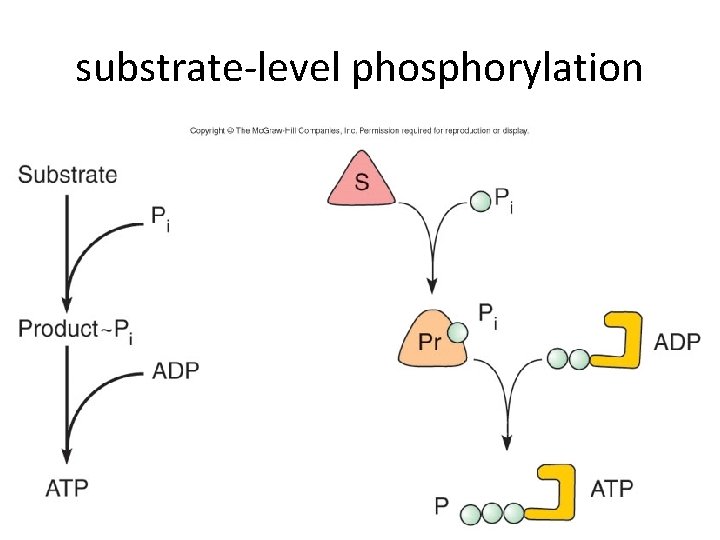
substrate-level phosphorylation 115

Catabolism of glucose 1. Glycolysis 2. Tricarboxylic acid cycle, Kreb’s cycle 3. Respiratory chain, electron transport 116

Metabolic strategies Aerobic respiration Pathways Final eacceptor involved Glycolysis, O 2 TCA, ET Anaerobic respiration Glycolysis, NO 3 -, So 4 -2, TCA, ET CO 3 -3 Fermentation Glycolysis Organic molecules ATP yield 38 variable 2 117
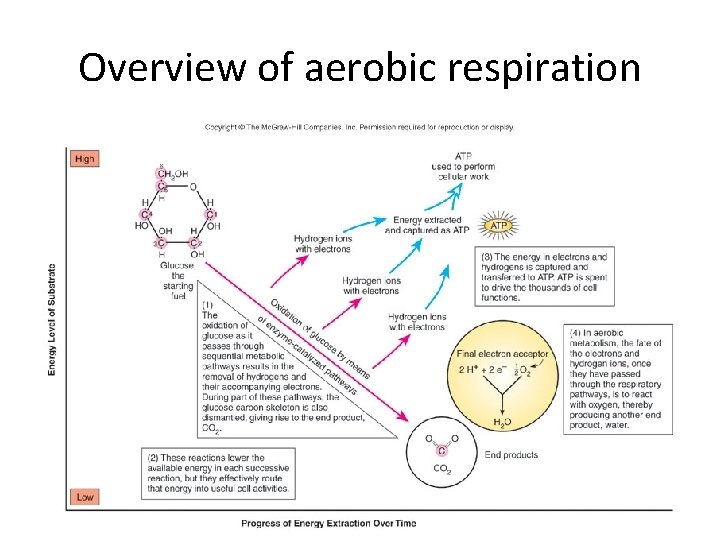
Overview of aerobic respiration 118

Overview of aerobic respiration • Glycolysis – glucose (6 C) is oxidized and split into 2 molecules of pyruvic acid (3 C) • TCA – processes pyruvic acid and generates 3 CO 2 molecules • Electron transport chain – accepts electrons NADH & FADH, generates energy through sequential redox reactions called oxidative phosphorylation 119
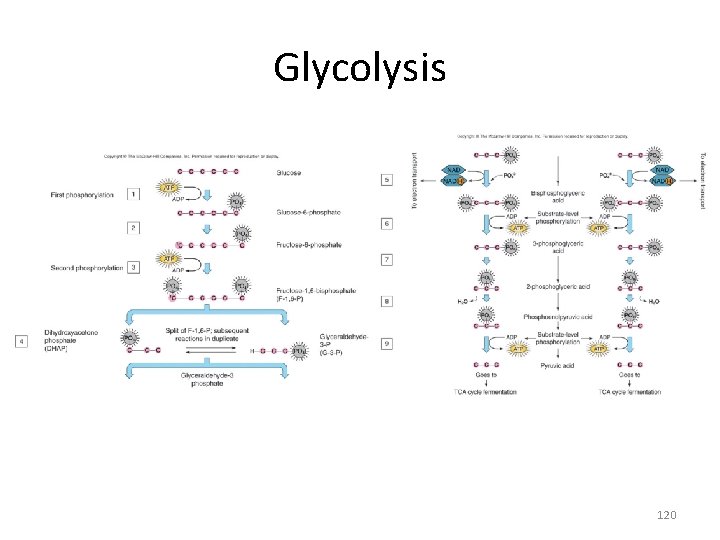
Glycolysis 120
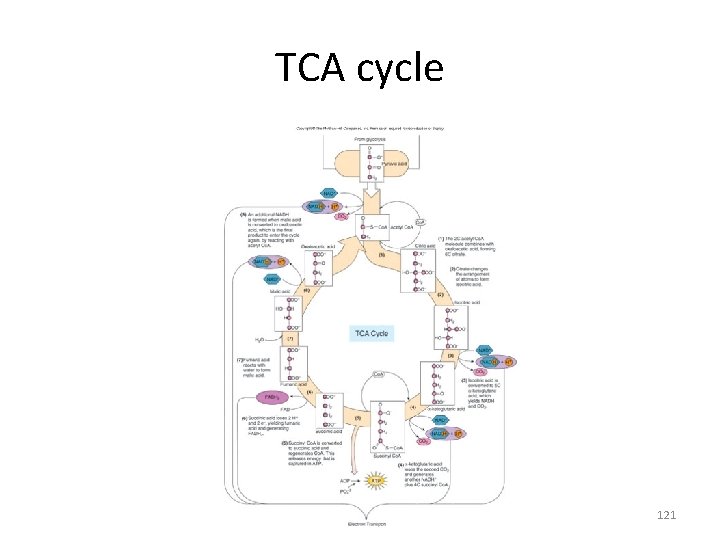
TCA cycle 121
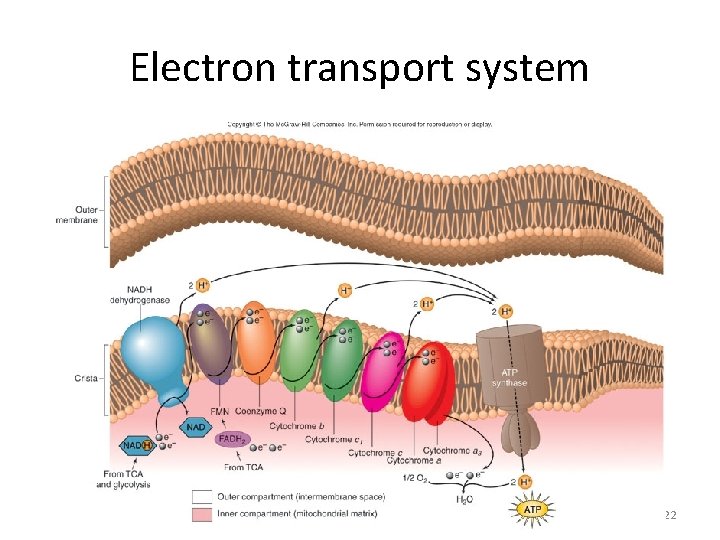
Electron transport system 122
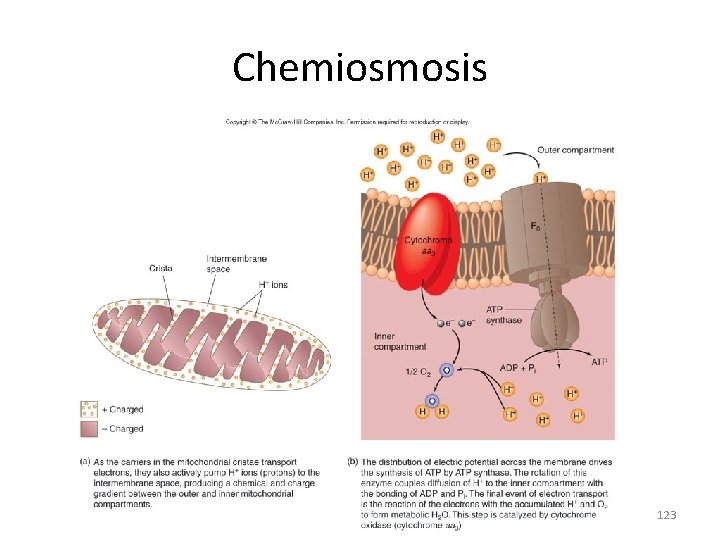
Chemiosmosis 123

Fermentation • Incomplete oxidation of glucose or other carbohydrates in the absence of oxygen • Uses organic compounds as terminal electron acceptors • Yields a small amount of ATP • Production of ethyl alcohol by yeasts acting on glucose • Formation of acid, gas & other products by the action of various bacteria on pyruvic acid 124
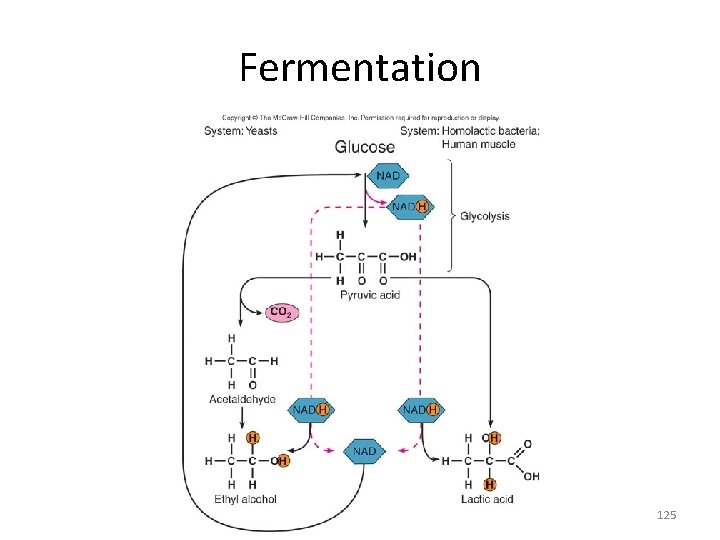
Fermentation 125
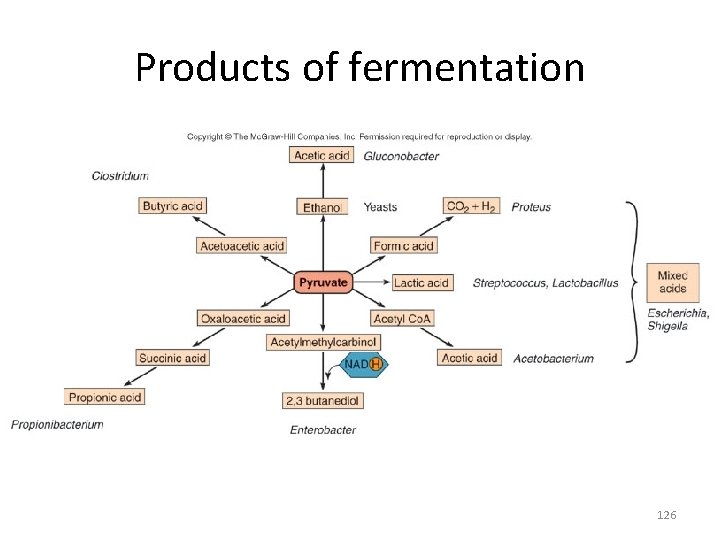
Products of fermentation 126

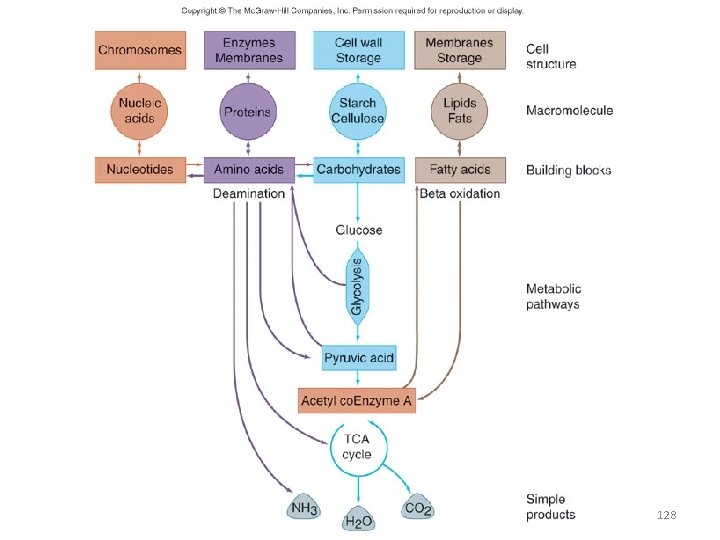
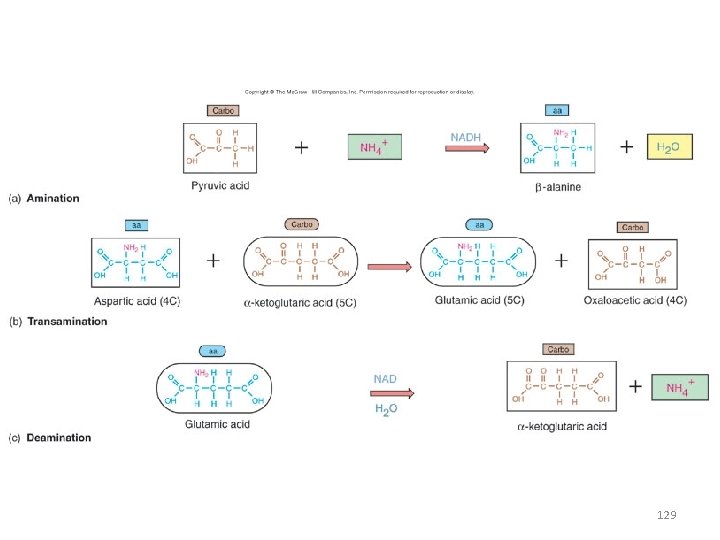
• Many pathways of metabolism are bi-directional or amphibolic • Metabolites can serve as building blocks or sources of energy – Pyruvic acid can be converted into amino acids through amination – Amino acids can be converted into energy sources through deamination – Glyceraldehyde-3 -phosphate can be converted into precursors for amino acids, carbohydrates and fats 127
128
129
- Slides: 129