MATA KULIAH DASAR BOBOT SKS SEMESTER 20102011 DOSEN

MATA KULIAH DASAR BOBOT SKS SEMESTER 2010/2011 DOSEN PENGASUH PRATIWI KODE MK : KIMIA : 4 : GENAP : IRNANDA : FT – 213

PERSAMAAN KIMIA � Suatu pereaksi adalah zat-zat apa saja yang mula- mula terdapat dan kemudian diubah selama suatu reaksi kimia � Suatu hasil reaksi adalah zat apa saja yang dihasilkan selama reaksi kimia. � 2 H 2 + O 2 2 H 2 O � Dua molekul hidrogen bereaksi dengan satu molekul oksigen, menghasilkan satu molekul air � Rumus molekul menyatakan banyaknya atom yang sebenarnya dalam suatu molekul atau satuan terkecil suatu senyawaan � Rumus empiris menyatakan angka banding bilangan bulat terkecil dari atom-atom suatu senyawaan

� Rumus molekul = H 2 O 2 � Rumus empiris = HO � Rumus unsur, misalnya : Na = Natrium Ag = Perak Fe = besi …etc Namun terdapat tujuh unsur diatom : H 2 = hidrogen N 2 = nitrogen O 2 = oksigen …. F 2, Cl 2, Br 2, I 2

�Rumus empiris dari suatu senyawa dan persentase komposisi berdasar massa dari unsur-unsur penyusunnya hanya dihubungkan oleh konsep mol semata, misalnya rumus empiris etilena (rumus molekul C 2 H 4) ialah CH 2. komposisi berdasar-massa dihitung dari massa karbon dan hidrogen dalam 1 mol unit rumus CH 2 :

�Massa C = 1 mol C x (12, 011 g/mol) = 12, 011 gr �Massa H = 2 mol H x (1, 00794 g/mol) = 2, 0159 gr Penjumlahannya menghasilkan massa total 14, 027 gr. dengan demikian, persentase massa karbon dan hidrogen dalam senyawa dihitung dengan membagi setiap massa nya dengan massa total ini dan mengalikannya dengan 100%, yang menghasilkan 85, 628 % C dan 14, 372% H.

�Contoh : sebanyak 60 gr cairan cuci- kering dianalisis dan diketahui mengandung 10, 80 gr C; 1, 36 gr H dan 47, 84 gr Cl. Tentukan rumus empiris senyawa tersebut dengan menggunakan tabel massa atom. �Penyelesaian : Banyaknya unsur kimia dalam sampel adalah Untuk karbon =

Untuk hidrogen = Untuk klorin = Nisbah jumlah bahan kimia karbon terhadap klorin (atau hidrogen) ialah 0, 8992 : 1, 35 = 0, 6666 yang mendekati 2: 3 Nisbah jumlah mol menjadi 2: 3: 3. dengan demikian rumus empirisnya ialah C 2 H 3 Cl 3

�Contoh : suatu senyawa yang digunakan dalam pengelasan hanya mengandung karbon dan hidrogen. Pembakaran sempurna sedikit sampel itu dengan oksigen menghasilkan 3, 38 g CO 2; 0, 692 g air, serta tidak ada produk lain. Tentukan rumus empiris senyawa tersebut. �Penyelesaian : Pertama-tama hitunglah jumlah bahan kimia CO 2 dan H 2 O. Oleh karena semua karbon telah terkonversi menjadi CO 2, dan semua hidrogen menjadi air, maka banyaknya bahan kimia C dan H dalam gas yang belum terbakar dapat ditentukan :

�Mol C = mol CO 2 = �Mol H = 2(mol H 2 O) = Perhatikan bahwa jumlah mol air dikalikan 2, untuk mendapatkan jumlah mol atom hidrogen , karena setiap molekul air mengandung dua atom hidrogen. Oleh karena senyawa tersebut mengandung jumlah bahan kimia (jumlah mol) karbon dan hidrogen yang sama, maka rumus empirisnya ialah CH.

� Persamaan berimbang : Ag + Cl Ag. Cl Na + Cl Na. Cl � Persamaan tidak berimbang : CH 4 + O 2 CO 2 + H 2 O Menjadi …. CH 4 + 2 O 2 CO 2 + 2 H 2 O � Reaksi gabungan langsung adalah suatu reaksi dari dua unsur yang menghasilkan suatu senyawaan Contoh : aluminium + brom aluminium bromida � Reaksi penukargantian sederhana adalah reaksi suatu unsur dengan suatu senyawaan yang menghasilkan unsur dan senyawaan lain Contoh : magnesium + feri klorida magnesium klorida + besi

� Reaksi penukargantian rangkap adalah reaksi dari dua senyawaan yang menghasilkan dua senyawaan berlainan dengan saling menukarkan komponennya Contoh : perak nitrat + kalsium klorida perak klorida + kalsium nitrat

STOIKIOMETRI �Kajian mengenai hubungan antara massa reaktan dan produknya disebut stoikiometri yang berasal dari kata Yunani stoicheion yang berarti unsurdan metron yang berarti ukuran �Stoikiometri merupakan dasar dalam semua jenis ilmu kimia �Koefisien-koefisien dalam suatu persamaan kimia yang balans memberikan “ faktor konversi kimia” antara jumlah zat kimia yang dikonsumsi atau diproduksi dalam suatu reaksi.

� Bobot atom (atomic weight) : satuan massa atom H = 1, 0079 sma ≈ 1 O = 15, 999 sma ≈ 16 C = 12, 011 sma ≈ 12 � Bobot molekul : jumlah bobot atom-atom yang ditunjukkan dalam rumusnya H 2 = 2 O 2 = 32 H 2 O = 18

� Contoh : hitung bobot molekul hidrogen sulfat, H 2 SO 4, dari bobot atom berikut : H = 1, O = 16, S = 32 Larutan. Dalam satu molekul H 2 SO 4 Bobot H = 2 x 1 = 2 sma Bobot O = 4 x 16 = 64 sma Bobot S = 1 x 32 = 32 sma = 98 sma Jadi, bobot satu molekul H 2 SO 4 adalah 98 sma

� Hubungan bobot dalam reaksi kimia : 2 Al + 3 Br 2 2 Al. Br 3 2 satuan + 3 satuan 2 satuan 2 (27 sma) + 3[2(80 sma)] = 2[ 27 +3(80)]sma 54 sma + 480 sma = 533 sma 533 sma = 533 sma � Bobot molar adalah bobot satu mol suatu zat � Bobot molar dalam gram suatu zat secara numeris sama dengan bobot molekul dalam satuan massa atom

� Bobot molar dan persamaan kimia 2 O 2 + 3 Fe Fe 3 O 4 2 mol + 3 mol 1 mol 2[2(16)]g + 3(56) g [3(56) + 4 (16)]g 64 g O 2 + 168 g Fe 232 g Fe 3 O 4

� Contoh : kalsium hipoklorit, Ca(OCl)2, digunakan sebagai bahan pemutih. Senyawa ini dihasilkan dari natrium hidroksida, kalsium hidroksida dan klorin yang menurut persamaan keseluruhannya adalah : 2 Na. OH + Ca(OH)2 + 2 Cl 2 Ca(OCl)2 + 2 Na. Cl + 2 H 2 O Berapa gram klorin dan natrium hidroksida yang bereaksi dengan 1067 g Ca(OH)2 dan berapa gram kalsium hipoklorit yang dihasilkan? Penyelesaian : Jumlah bahan kimia Ca(OH)2 yang dikonsumsi adalah

� Dimana massa molar Ca(OH)2 telah ditentukan dari massa molar kalsium, oksigen dan hidrogen sebagai 40, 08 + 2(15, 999) + 2 (1, 0079)` = 74, 09 g mol-1 � Menurut persamaan yang balans, 1 mol Ca(OH)2 bereaksi dengan 2 mol Na. OH dan 2 mol Cl 2 menghasilkan 1 mol Ca(OCl)2, jika 14, 40 mol Ca(OH)2 bereaksi maka : � Mol Na. OH =
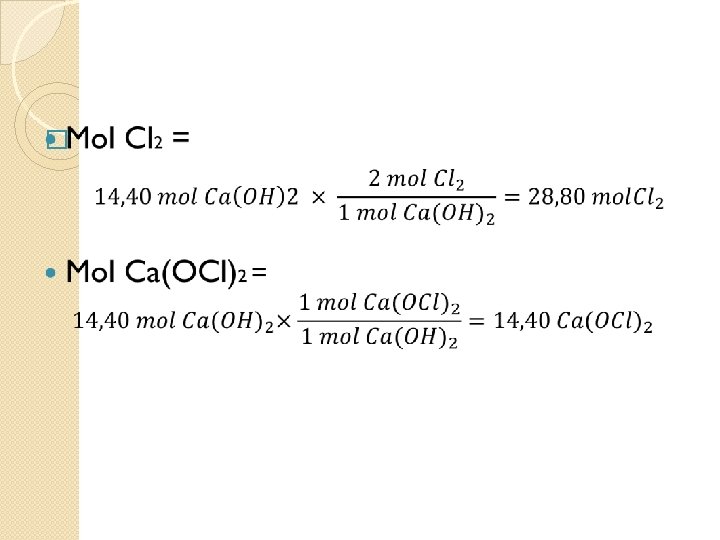

�Massa Na. OH yang bereaksi = (28, 80 mol) x (40, 00 gr/mol) = 1152 gr �Massa Cl 2 yang bereaksi = (28, 80 mol) x (70, 91 gr/mol) = 2042 gr �Mol Ca(OCl)2 yang dihasilkan = (14, 40 mol) x (142, 98 gr/mol) = 2059 gr
- Slides: 20