Master de Physique Mdicale Bases physiques de lutilisation

Master de Physique Médicale Bases physiques de l’utilisation médicale des rayonnements ionisants La Radioactivité Guillaume BONNIAUD – bonniaud@igr. fr Service de Physique Médicale, Service de Médecine Nucléaire - Institut Gustave-Roussy

Enjeux du cours § Comprendre la radioactivité Ø Appréhender les objets subatomiques Ø Comprendre la physique nucléaire § Comprendre les applications médicales de la radioactivité Ø Production de radioéléments artificiels Ø Radiothérapie métabolique Ø Imagerie Ø Radioprotection Cours de physique appliquée

La radioactivité : définition (1) Propriété de certains éléments chimiques d’émettre des rayonnements, , cette propriété est due à l’instabilité du rayonnements noyau atomique Ø Objets mis en jeu : - noyau atomique Échelle nucléaire 10 -14 m - rayonnements Énergie = Forme spontanée de transport de l’énergie

La radioactivité : définition (2) Propriété de certains éléments chimiques d’ émettre des rayonnements, cette propriété est due à l’instabilité du noyau atomique Ø Mot clef : instabilité => lien entre instabilité du noyau et rayonnement Rayonnement (énergie) Noyau instable i. e. lien entre instabilité du noyau et énergie!

Plan du cours I. Le noyau Question : Que cache la structure nucléaire ? II. La radioactivité Question : Pourquoi cette instabilité nucléaire ? Énergie Noyau instable III. Les applications médicales de la radioactivité Question : Comment tirer profit de l’énergie du noyau en médecine ? Cours ponctué de Questions (pour y répondre & pour réfléchir)

I. Le noyau Que cache la structure nucléaire ?

Le noyau : plan § Introduction : matière et interactions § Histoire de la conquête du noyau § Le noyau : structure, stabilité Visualisation tridimensionnelle de la superposition lineaire de 6 etats propres de l'atome d'Hydrogene (calcul tridimensionnel) Copyright (c) 1995 -2004 Jean-Francois Colonna Copyright (c) 1995 -2004 France Telecom R&D and CMAP / Ecole Polytechnique
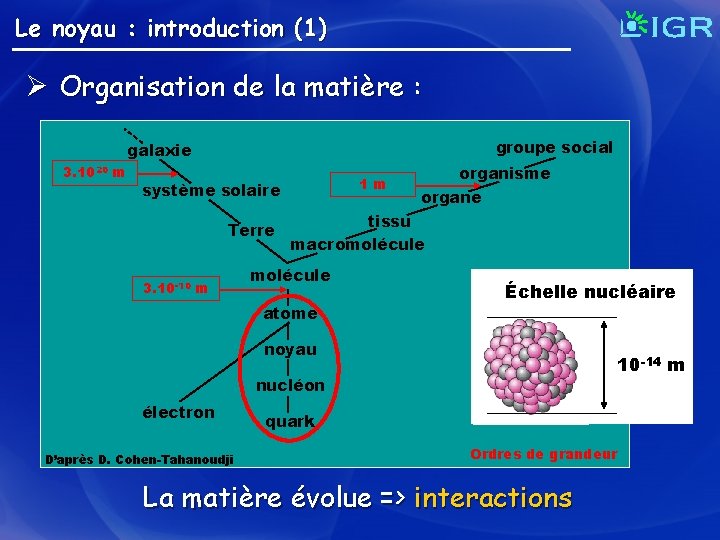
Le noyau : introduction (1) Ø Organisation de la matière : groupe social galaxie 3. 1020 m 1 m système solaire Terre 3. 10 -10 m organisme organe tissu macromolécule atome Échelle nucléaire noyau 10 -14 m nucléon électron D’après D. Cohen-Tahanoudji quark Ordres de grandeur La matière évolue => interactions

Le noyau : introduction (2) Ø Interactions : Induites par 4 types de forces (= les agents du changement) : * la force gravitationnelle * la force électromagnétique * l’interaction forte ou nucléaire * la force faible (tous les objets terrestres restent liés à la planète) (lie les objets tels que les atomes, les molécules donc les plantes et nous) (lie les quarks pour former les nucléons i. e. la matière) (transforme par exemple les nucléons)

Le noyau : introduction (3) Ø Détails des différentes forces : (classée par ordre croissant d’intensité) Force Agit sur Intensité relative* Portée Gravitationnelle Toutes les particules 1 illimitée Faible La plupart des particules 1032 10 -17 m Électromagnétique Les particules chargées 1036 illimitée Nucléaire (forte) Les quarks et les particules qu’ils constituent 1038 10 -14 m * Normalisée par rapport à la force gravitationnelle entre deux protons séparés par une distance égale à leur diamètre La force la plus intense est la force nucléaire

Le noyau : introduction (4) Pour comprendre le noyau, il faut donc : Ø Se placer à une échelle infinitésimale De l’ordre du 100 ième de fentomètre (10 -14 m) Jouer avec des forces de courte portée et d’une intensité colossale au regard de l’échelle nucléaire : Ø i. e. 50 Newton appliqué à une masse de 10 -26 kg sur 10 -14 m (1 Newton énergie à fournir pour soulever 1 pomme d’ 1 m) Comment tout cela a-t-il été possible ?

Histoire de la conquête du noyau atomique (1) Ø Concepts « Philosophiques » : 450 ans Av. J. C. § Leucippe, Démocrite (~400 ans av. JC. ) Il y a une limite à la division des corps Naissance du mot moderne d’atome (du grec atomos = « qui ne peut être coupé » ) 1811 § A. Avogadro (1811) Élaboration de la notion de molécule Notion de mole i. e. de nombre de molécules par unité de volume ou de masse (Nombre d’Avogadro A=6, 02. 1023 molécules/mole) 1881 § H. Helmholtz (1881) Il existe un quantum de charge e (l’électricité est divisée en « atomes » d’électricité) Plus tard, on déterminera : e = 1, 602. 10 -19 C Temps

Histoire de la conquête du noyau atomique (2) Ø Concepts physico-chimiques : § D. Mendeleïv (1870) : Classification périodique des éléments en fonction de leur masse atomique 1. Les éléments disposés d'après la grandeur de leur poids atomique présentent une périodicité des propriétés. 2. Les éléments qui se ressemblent par leurs fonctions chimiques présentent des poids atomiques voisins (Pt, Ir, Os), ou bien croissant uniformément (K, Rb, Cs) … 6. Il faut attendre la découverte de plusieurs corps simples encore inconnus, ressemblant, par exemple, à Al et Si et ayant un poids atomique entre 65 et 75 … 1870 8. Certaines analogies des éléments peuvent être découvertes d'après la grandeur du poids de leurs atomes. Temps
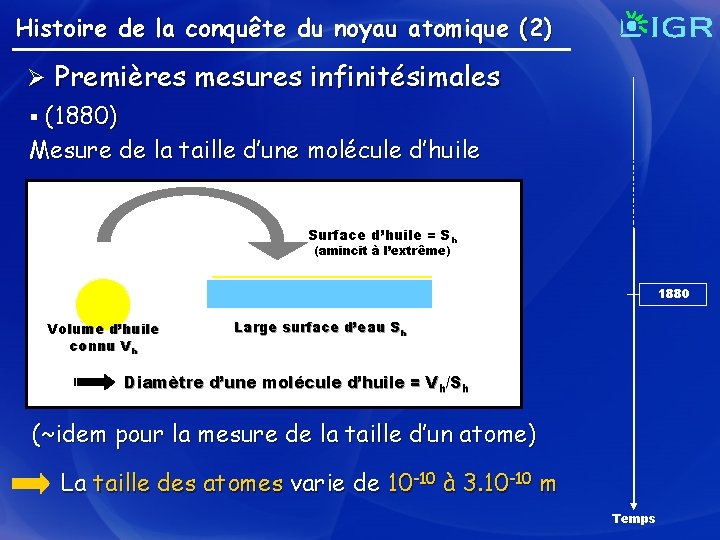
Histoire de la conquête du noyau atomique (2) Ø Premières mesures infinitésimales § (1880) Mesure de la taille d’une molécule d’huile Surface d’huile = Sh (amincit à l’extrême) 1880 Volume d’huile connu Vh Large surface d’eau Sh d’une molécule d’huile = Vhd’huile /Sh ? Question : Diamètre comment mesurer la taille d’une molécule (~idem pour la mesure de la taille d’un atome) La taille des atomes varie de 10 -10 à 3. 10 -10 m Temps
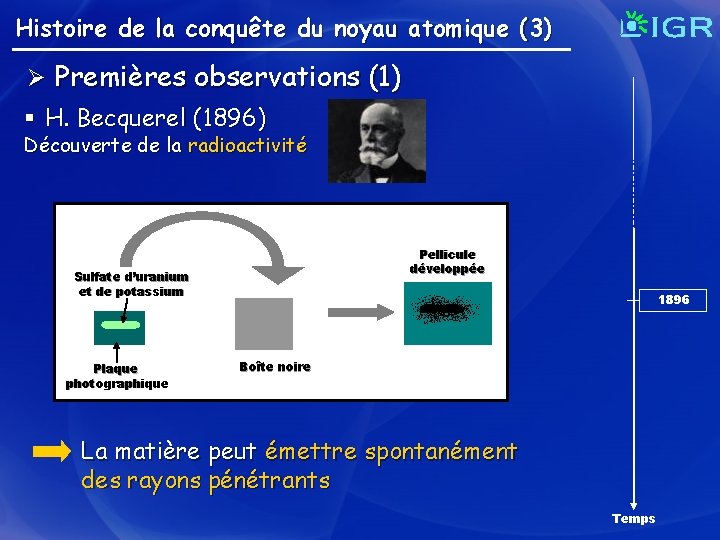
Histoire de la conquête du noyau atomique (3) Ø Premières observations (1) § H. Becquerel (1896) Découverte de la radioactivité Pellicule développée Sulfate d’uranium et de potassium Plaque photographique 1896 Boîte noire La matière peut émettre spontanément des rayons pénétrants Temps

Histoire de la conquête du noyau atomique (4) Ø Premières observations (2) § P. & M. Curie (1898) Extraction d’ 1 g de sel de radium pur par distillation d’ 1 tonne de minerai d’uranium La radioactivité est une propriété atomique § E. Rutherford (1898) Étude des rayons de Becquerel (uranium), ils sont de deux types distincts : - le rayonnement alpha ( ) (facilement absorbé) - le rayonnement bêta ( ) (plus pénétrant) 1898 § P. Villard (1900) Le radium émet des rayons très pénétrants : Les rayons gamma ( ) Temps
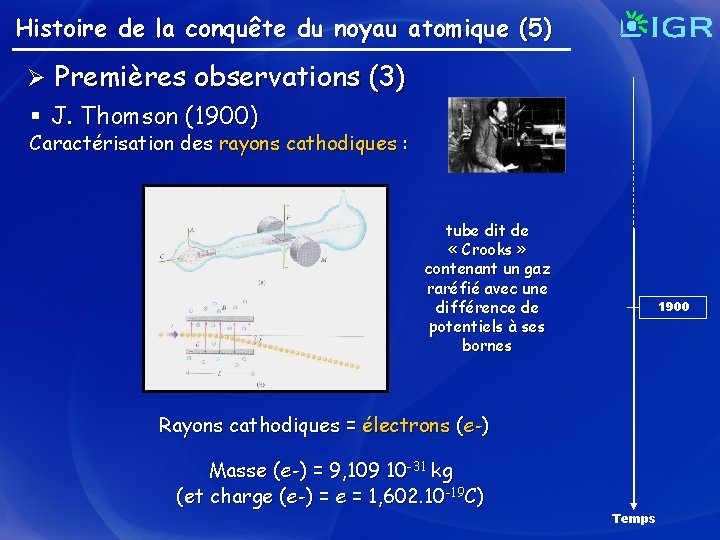
Histoire de la conquête du noyau atomique (5) Ø Premières observations (3) § J. Thomson (1900) Caractérisation des rayons cathodiques : tube dit de « Crooks » contenant un gaz raréfié avec une différence de potentiels à ses bornes 1900 Rayons cathodiques = électrons (e-) Masse (e-) = 9, 109 10 -31 kg (et charge (e-) = e = 1, 602. 10 -19 C) Temps

Histoire de la conquête du noyau atomique (6) Ø Premières observations (4) § E. Rutherford (1903) Caractérisation des rayons de Becquerel (uranium) : - les particules sont chargées positivement - les rayons sont des électrons - la masse des particules est très grande devant la masse des électrons Masse = 6, 64 10 -27 kg ~ 7300 masse e- 1903 Les rayons et sont déviés par un champ électrique Temps
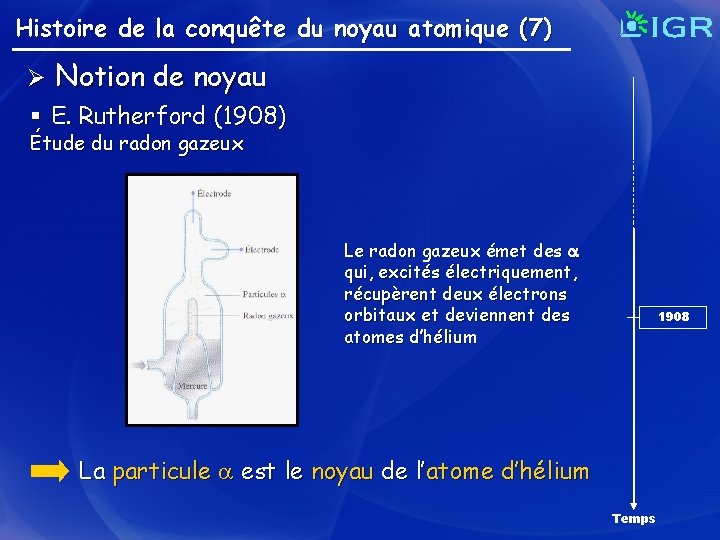
Histoire de la conquête du noyau atomique (7) Ø Notion de noyau § E. Rutherford (1908) Étude du radon gazeux Le radon gazeux émet des qui, excités électriquement, récupèrent deux électrons orbitaux et deviennent des atomes d’hélium 1908 La particule est le noyau de l’atome d’hélium Temps
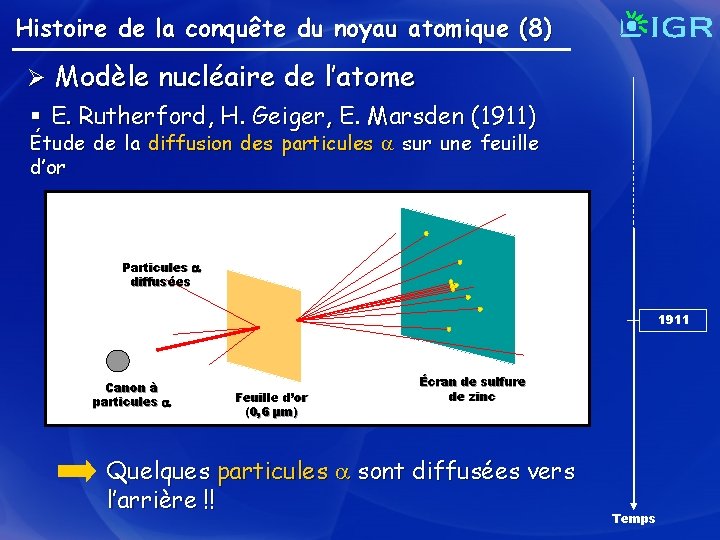
Histoire de la conquête du noyau atomique (8) Ø Modèle nucléaire de l’atome § E. Rutherford, H. Geiger, E. Marsden (1911) Étude de la diffusion des particules sur une feuille d’or Particules diffusées 1911 Canon à particules Feuille d’or (0, 6 µm) Écran de sulfure de zinc Quelques particules sont diffusées vers l’arrière !! Temps
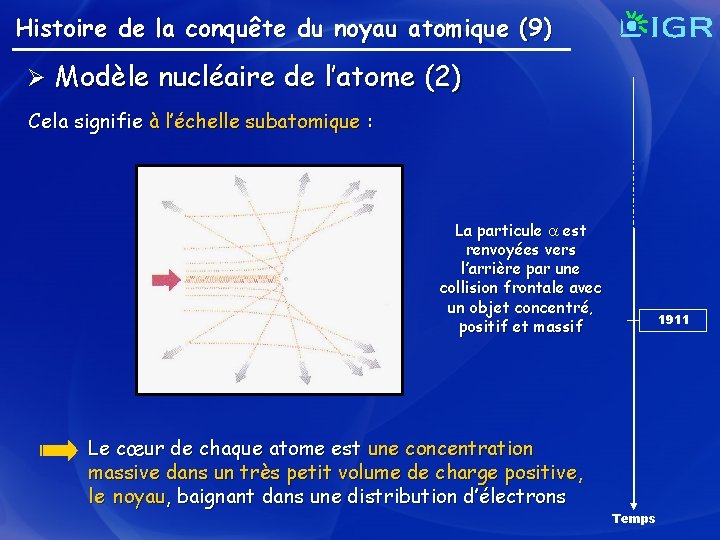
Histoire de la conquête du noyau atomique (9) Ø Modèle nucléaire de l’atome (2) Cela signifie à l’échelle subatomique : La particule est renvoyées vers l’arrière par une collision frontale avec un objet concentré, positif et massif Le cœur de chaque atome est une concentration massive dans un très petit volume de charge positive, le noyau, baignant dans une distribution d’électrons 1911 Temps

Histoire de la conquête du noyau atomique (11) Ø Question : quelle est la taille du noyau ? § Indice : Énergie cinétique (Ec) / Énergie potentielle (Ep) En P : Ep = Ec § Calcul : P § Données : 1. m. v ² k. (Ze). (2 e) = R 2 Vitesse des : 1, 5. 107 m. s-1 -27 kg * Masse des : 6, 6. 10 -19 C * Quantum de charge : 1, 6. 10 9 2 -2 * Constante de la force de Coulomb : 9. 10 N. m. C Hypothèses : Z de l‘or = 99 * § Résultat : 1911 4. k. Z. 2. e 2 R= m. v 2 La taille du noyau est ~ de 10 -14 m Temps

Histoire de la conquête du noyau atomique (12) Ø Premier modèle de l’atome § N. Bohr (1912) : Élaboration de la première théorie atomique : Les atomes sont composés d’électrons gravitant autour du noyau. Les électrons atomiques n’existent que sur certains orbites stables et durables autour du noyau, ce sont les états stationnaires. 1912 Noyau Électron orbital Li Temps
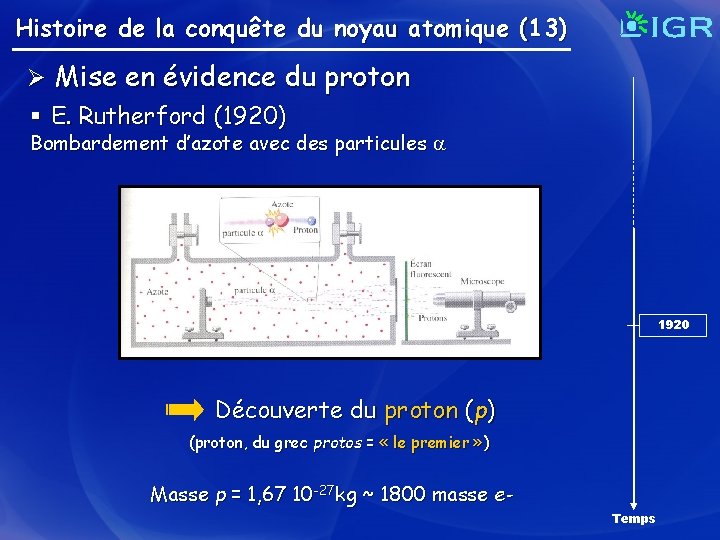
Histoire de la conquête du noyau atomique (13) Ø Mise en évidence du proton § E. Rutherford (1920) Bombardement d’azote avec des particules 1920 Découverte du proton (p) (proton, du grec protos = « le premier » ) Masse p = 1, 67 10 -27 kg ~ 1800 masse e. Temps

Histoire de la conquête du noyau atomique (14) Ø Le point sur l’atome en 1920 Exemple des atomes d’hydrogène (H) et d’hélium (He): - un noyau formé de Z protons (~10 -14 m) - Z électrons orbitaux liés par attraction coulombienne (~10 -10 m) e- e- p Particule 1920 e- H, 1 p et 1 e- He, 2 p et 2 e- Problème : [e/m]particule = ½. [e/m]noyau H et charge particule = +2 e La particule a donc 4 masses ! Temps

Histoire de la conquête du noyau atomique (15) Ø Mise en évidence du neutron § I. & F. Joliot-Curie, J Chadwick (1932) Bombardement d’une cible de béryllium avec des particules 1932 Découverte du neutron (n) Masse n = 1, 67 10 -27 kg ~ 1800 masse e. Temps

Histoire de la conquête du noyau atomique (16) Ø Les concepts évoluent…(1) § A. Einstein (1905) : L’énergie de rayonnement est discontinue. Équivalence entre masse et énergie. § L. De Broglie (1923) : La matière en mouvement a une longueur d’onde ( ) : = h/mv (ou = h/p) i. e. les particules sont des ondes 1905 1923 § N. Bohr (1925) : Dualité Onde-corpuscule : les entités microscopiques (électrons, protons, photons, …) se propagent comme des ondes et échangent de l’énergie comme des particules. i. e. E/f = p = h = quantum de l’action (=4, 13. 10 -15 e. V. s) Temps
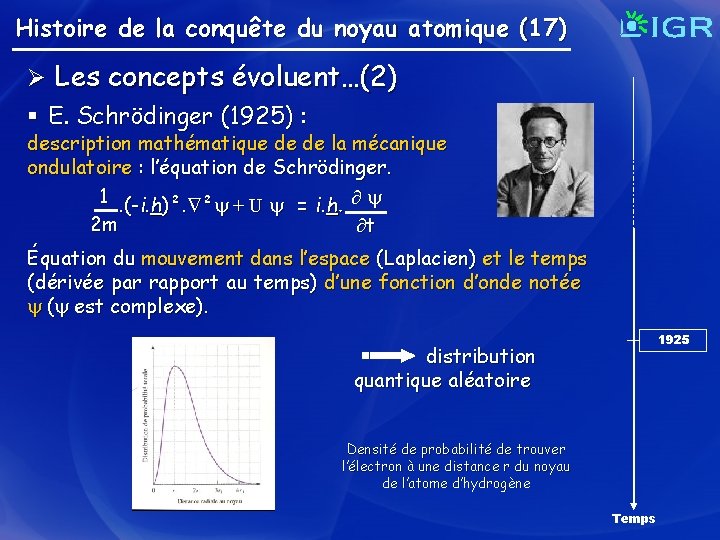
Histoire de la conquête du noyau atomique (17) Ø Les concepts évoluent…(2) § E. Schrödinger (1925) : description mathématique de de la mécanique ondulatoire : l’équation de Schrödinger. 1. (-i. h)². ² + U = i. h. 2 m t Équation du mouvement dans l’espace (Laplacien) et le temps (dérivée par rapport au temps) d’une fonction d’onde notée ( est complexe). 1925 distribution quantique aléatoire Densité de probabilité de trouver l’électron à une distance r du noyau de l’atome d’hydrogène Temps

Histoire de la conquête du noyau atomique (18) Ø Le modèle atomique en couches (1) § N. Bohr (1912…) et autres (… 1925) : structure électronique en couches : - un état (les 4 nombres quantiques n, l, ml et ms) - une orbitale (groupe d’états qui ont les mêmes valeurs de n, l et ml) - une sous-couche (groupe d’états qui ont les mêmes valeurs de n et l. Ces souscouches sont désignées par les lettres minuscules s, p, d, f, g, h, …) - une couche (groupe d’états qui ont le même nombre quantique principal n. Ces couches sont désignées par les lettres majuscules K, L, M, N, O, …) (1, 0, 0) (2, 1, 1) Densité de probabilité | ²| pour l’électron dans l’état fondamental et dans plusieurs états excités de l’atome d’hydrogène. 1925 Notation = (n, l, m) (3, 1, 0) (3, 2, 1) § W. Pauli (1924) : Principe d’exclusion : deux électrons atomiques ne peuvent occuper le même état Temps

Histoire de la conquête du noyau atomique (19) Ø Le modèle atomique en couches (2) § N. Bohr (1912…) et autres (… 1925) : Structure énergétique de l’atome : - À chaque orbite correspond à un niveau d’énergie - Et l’état fondamental est l’état de plus basse énergie Exemple de l’atome d’hydrogène -État fondamental : E 1 = -13, 6 e. V 1925 -1 er état excité : E 2 = -3, 4 e. V Question : quelle longueur d’onde un photon doit posséder pour amener l’hydrogène à son 1 er état excité ? Temps

Histoire de la conquête du noyau atomique (20) Ø Modèle du noyau atomique § W. Heisenberg (1932) : Modèle du noyau atomique : Tous les noyaux sont composés exclusivement de neutrons et de protons : les nucléons. Ø Facteurs d’échelle : 1932 Temps
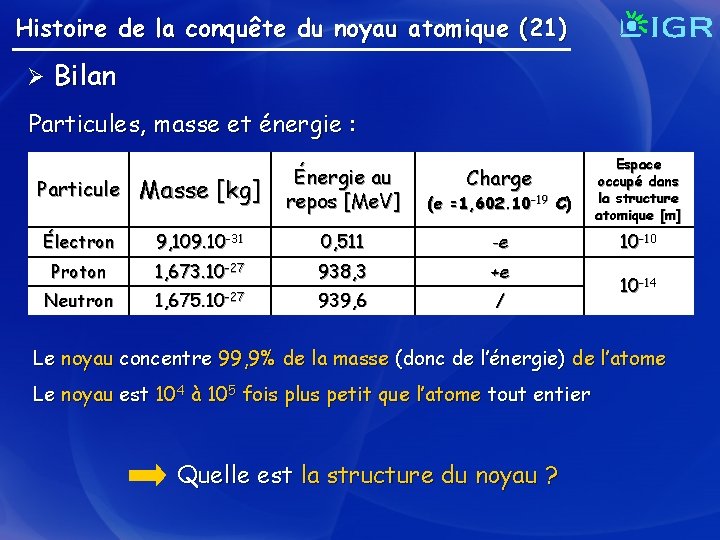
Histoire de la conquête du noyau atomique (21) Ø Bilan Particules, masse et énergie : Particule Masse [kg] Énergie au repos [Me. V] (e =1, 602. 10 -19 C) Électron 9, 109. 10 -31 0, 511 -e Proton 1, 673. 10 -27 938, 3 +e Neutron 1, 675. 10 -27 939, 6 / Charge Espace occupé dans la structure atomique [m] 10 -10 10 -14 Le noyau concentre 99, 9% de la masse (donc de l’énergie) de l’atome Le noyau est 104 à 105 fois plus petit que l’atome tout entier Quelle est la structure du noyau ?

Le noyau : structure, stabilité (1) Ø Carte d’identité § Nucléide Une espèce particulière de noyau est appelée nucléide Les nucléides sont caractérisés par : - le numéro atomique (i. e. le nombre de proton Z) - le nombre de masse ou nombre de nucléons (A) A La notation la plus courante pour un nucléide X est : Z Il existe 1500 nucléides artificiels et naturels X § Unité de masse atomique (uma) Calculée de sorte que l’atome de carbone neutre (126 C) ait une masse exactement égale à 12, 000000 uma. 1 uma = 1, 660540. 10 -27 kg = 931, 494 Me. V/c².

Le noyau : structure, stabilité (2) Ø Isotopes Il existe plusieurs type de nucléides d’un élément donné: les isotopes (du grec « isos » signifiant le même et « topos » qui veut dire place, cf le tableau périodique). Différents isotopes ont le même nombre de protons Z (i. e. la même charge) mais un nombre de neutrons différents A-Z Les isotopes d’un élément ont les mêmes propriétés chimiques Exemple : les 3 isotopes de l’hydrogène, Hydrogène Deutérium A 1 H, A = {1, 2, 3} Tritium

Le noyau : structure, stabilité (3) Ø Taille du noyau Déterminée à partir de la densité de charge en fonction de la distance au centre du noyau (R. Hofstadter 1950) Pour le Germanium 70 : R ~ 4, 9 10 -15 m L’unité employée habituellement est le fermi : 1 fermi = 10 -15 m Le rayon des noyaux est compris entre 1 et 10 fermi

Le noyau : structure, stabilité (4) Ø Densité nucléaire Question : Comment la calculer ? Hypothèse : densité du noyau indépendante du nombre de masse ! Donc [kg. m-3] = m 4. . R 3 3 Exemple : densité du noyau de Germanium 70 = 2, 3. 1017 kg. m-3 La densité de matière nucléaire est énorme Ø Forme du noyau (R. Hofstadter 1950) presque sphérique, souvent ellipsoïdale et allongée, mais parfois un peu aplatis en forme de poire ou de deux soucoupes accolées Il en est de même pour la densité de masse (i. e. les neutrons et les protons sont distribués de la même façon) Distribution spatiale des charges du noyau (ou densité de charge qui est une densité de probabilité !)

Le noyau : structure, stabilité (5) Ø Spin des noyaux Rappel : - spin = moment cinétique d’une particule - protons et neutrons = fermions : spin ½ entier Et le principe d’exclusion s’applique aux couches du noyau (pas entre protons et neutrons!) Spin total d’un noyau (J) : Somme des moments cinétiques orbitaux de ses constituants (L, L est un entier) et de leurs spins (S) Si A est pair => le noyau est un boson (J est un entier) Si A est impair => le noyau est un fermion (J est ½ entier) L’existence d’un spin nucléaire suggère la possibilité d’un moment magnétique du noyau (dépendant du nombre de nucléons et de leur arrangement)

Le noyau : structure, stabilité (6) Ø La force nucléaire (1) § W. Heisenberg (1932) Il existe une force de répulsion entre protons : environ 50 N (énorme au regard de la masse du proton!) il existe une force appelée force nucléaire qui lie les neutrons et les protons pour former les noyaux (interactions p-p, p-n, n-n) § Ordres de grandeur - de faible portée : quelques fermis - très intense : 100 à 1000 fois plus intense que la force électromagnétique et 1038 fois plus intense que la force gravitationnelle
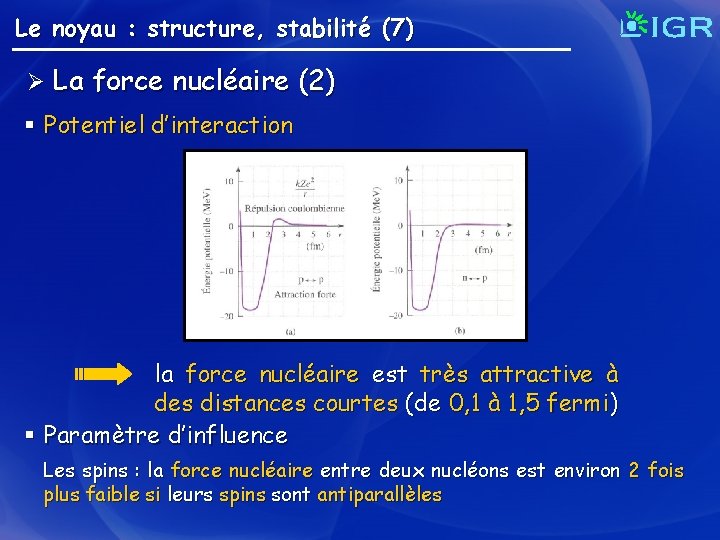
Le noyau : structure, stabilité (7) Ø La force nucléaire (2) § Potentiel d’interaction la force nucléaire est très attractive à des distances courtes (de 0, 1 à 1, 5 fermi) § Paramètre d’influence Les spins : la force nucléaire entre deux nucléons est environ 2 fois plus faible si leurs spins sont antiparallèles

Le noyau : structure, stabilité (8) Ø Les nucléons § Taille le rayon du nucléon est actuellement approximé entre 0, 7 et 0, 8 fermi § Distance inter-nucléons De l’ordre d’ 1 fermi (comparable à la portée de la force nucléaire) § L. Rainwater (1949) Modèle de la goutte d’eau : Le noyau subit une tension de surface Les nucléons de surface sont attirés vers l’intérieur (la surface du noyau a une épaisseur comparable à la portée de la force nucléaire)
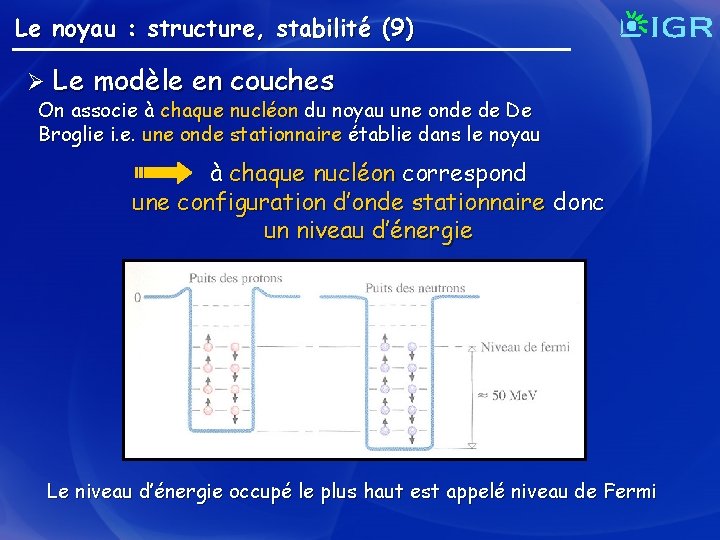
Le noyau : structure, stabilité (9) Ø Le modèle en couches On associe à chaque nucléon du noyau une onde de De Broglie i. e. une onde stationnaire établie dans le noyau à chaque nucléon correspond une configuration d’onde stationnaire donc un niveau d’énergie Le niveau d’énergie occupé le plus haut est appelé niveau de Fermi

Le noyau : structure, stabilité (10) Ø Stabilité du noyau § Les nombres magiques Certains noyaux très stables ont des nombres N et Z sont égaux : ils forment la série des nombres magiques (2, 8, 20 28, 50, 82 et 126) Ils correspondent au nombre total d’états dans les couches totalement occupées (les noyaux formés de couches pleines sont particulièrement stables) § Spin Un spin et un moment magnétique global nuls pour un noyau favorisent sa stabilité 2 protons et 2 neutrons de spins opposés ont tendance à s’apparier
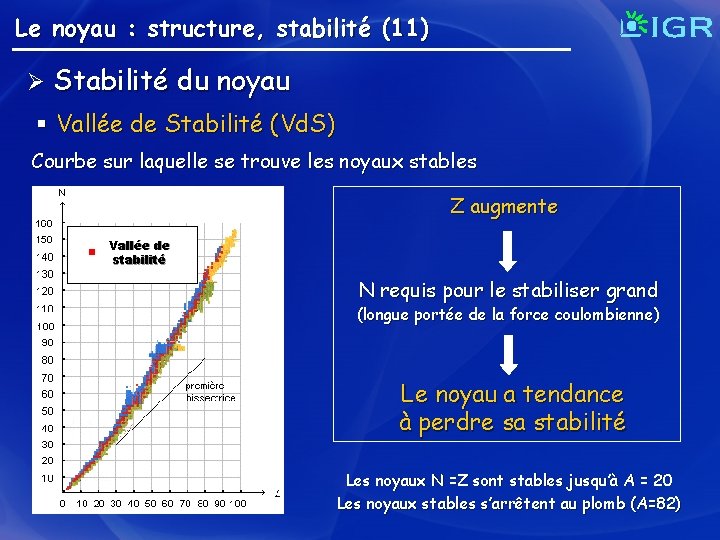
Le noyau : structure, stabilité (11) Ø Stabilité du noyau § Vallée de Stabilité (Vd. S) Courbe sur laquelle se trouve les noyaux stables Z augmente Vallée de stabilité N requis pour le stabiliser grand (longue portée de la force coulombienne) Le noyau a tendance à perdre sa stabilité Les noyaux N =Z sont stables jusqu’à A = 20 Les noyaux stables s’arrêtent au plomb (A=82)

Le noyau : structure, stabilité (12) Ø Énergie de liaison § M. Planck (1905) Masse d’un Système lié < Somme des masses de ses constituants Le défaut de masse pour un noyau correspond à l’énergie de liaison totale du nucléide (EL) § Ordre de grandeur Le deutéron, isotope de l‘hydrogène : - mp + mn = 1, 007276 uma + 1, 08665 uma = 2, 015941 uma - mdeutéron = 2, 13553 uma donc m = 0, 002388 uma donc EL = m. c² = 2, 224 Me. V (Contre 12. 7 e. V pour l’ EL de son électron)
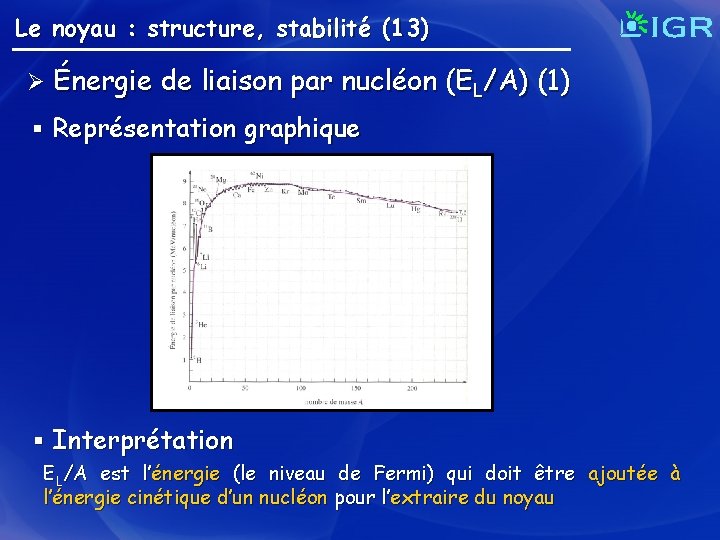
Le noyau : structure, stabilité (13) Ø Énergie de liaison par nucléon (EL/A) (1) § Représentation graphique § Interprétation EL/A est l’énergie (le niveau de Fermi) qui doit être ajoutée à l’énergie cinétique d’un nucléon pour l’extraire du noyau

Le noyau : structure, stabilité (14) Ø Énergie de liaison par nucléon (EL/A) (2) § Fission / Fusion Sélectionner un nucléide d’un côté ou d’un autre du maximum de la courbe de EL/A et modifier sa structure de façon à le déplacer vers le Nickel libère donc une grande quantité d’énergie. C’est ce que l’on fait lors de la fission et de la fusion nucléaire Le centre du soleil est une « chaudière nucléaire » activée par une réaction de fusion gigantesque : 4 1 H transformés en 4 He Libérant une énergie 24, 7 Me. V Depuis 5 milliards d’année et encore pour une durée équivalente …

Le noyau Ø Question pour réfléchir : le déterminisme A propos de l’équation de Schrödinger Définissant une distribution quantique aléatoire (1, 0, 0) (2, 1, 1) Densité de probabilité | ²| pour l’électron dans l’état fondamental et dans plusieurs états excités de l’atome d’hydrogène. Notation = (n, l, m) (3, 1, 0) (3, 2, 1) Il apparaît que des particules identiques ne comportent pas identiquement dans des situations identiques…

Abstraction en physique et art abstrait Ø Les concepts évoluent … : Évolution des concepts en physique rime avec évolution de la pensée « tout court » : la représentation du monde n’est plus réduite à notre perception « optique » … Mark Rothko

Le noyau : conclusion § Le noyau : - est 104 à 105 fois plus petit que l’atome tout entier (10 -15 m) - concentre 99, 9% de la masse (donc de l’énergie) de l’atome - il est composé de protons et de neutrons (nucléons) - possède une structure énergétique en couches § La force nucléaire (interaction forte) qui le lie les nucléons est : - très intense - de faible portée (quelques fermi) § La stabilité du noyau dépend : - du rapport Z, N du noyau - du spin et du moment magnétique global du noyau Pourquoi cette instabilité nucléaire ?

II. La radioactivité Pourquoi le noyau atomique peut-il être instable ?

La radioactivité : plan § La radioactivité : une instabilité nucléaire § Les différents types de désintégration § Les transitions gamma § Notion de demi-vie / Schéma de désintégration Traces de particules issues de la désintégration de pions positifs (CERN, chambre à fil)

La radioactivité : une instabilité nucléaire (1) Ø Définitions Les noyaux se transforment spontanément en des configurations énergétiques plus favorables par émission de particules dans un processus appelé désintégration radioactive Une désintégration radioactive donnée peut être une étape dans une longue suite de transformation d’un nucléide instable à un autre et qui aboutissent finalement à un nucléide stable Ø Désintégration et conservation Dans toute désintégration, il y a conservation : - de la charge - du nombre de nucléons (A) - de la quantité de mouvement - du moment cinétique - de l’énergie de masse

La radioactivité : une instabilité nucléaire (2) Ø nucléides radioactifs § Parmi les 1500 nucléides existants : - 280 sont stables - 1200 sont radioactifs (artificiels et naturels) Tous les éléments de Z = 93 à 112 sont produits artificiellement et radioactifs § Exemple : - Le granite de Bretagne (contient naturellement du Potassium 40)

Les radioactivités Ø La radioactivité naturelle (1836) : Désintégrations affectant les nucléides radioactifs existant dans la nature. Ils sont classés en 3 groupes. 1 - Les radionucléides de très longue période radioactive (vs à l'âge de la Terre). Ils sont généralement à l'origine d'une famille radioactive 2 - Les radionucléides de période radioactive courte : ce sont des noyaux fils des radionucléides précédents 3 - Les radionucléides formés par impact : leur formation est provoquée par l'impact, sur un noyau stable, de particules cosmiques ou de particules issues de la désintégration de l'un des nucléides prècédents Ø La radioactivité artificielle (1934) : Désintégrations obtenues en laboratoire ou dans des réacteurs nucléaires.
![Les unités de la radioactivité Ø L’unité historique : le Curie [Ci] 1 Ci Les unités de la radioactivité Ø L’unité historique : le Curie [Ci] 1 Ci](http://slidetodoc.com/presentation_image_h/1e9fa14ebf81922ac3b70fb8d0d4c3ae/image-55.jpg)
Les unités de la radioactivité Ø L’unité historique : le Curie [Ci] 1 Ci = radioactivité d’un gramme de radium é b i i. e. 37 milliards de désintégrations par seconde h o r P (unité énorme) Ø L’unité SI : le Becquerel [Bq] 1 Bq = 1 désintégration par seconde (unité très petite) Pour information : 1 m. Ci = 37 MBq
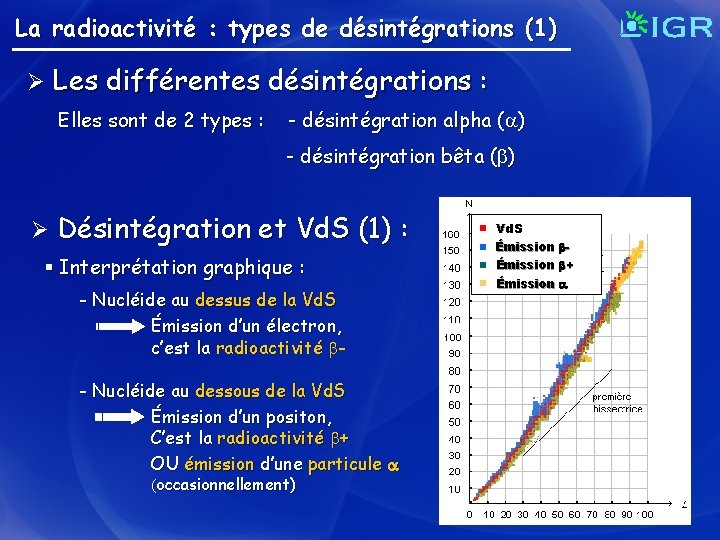
La radioactivité : types de désintégrations (1) Ø Les différentes désintégrations : Elles sont de 2 types : - désintégration alpha ( ) - désintégration bêta ( ) Ø Désintégration et Vd. S (1) : § Interprétation graphique : - Nucléide au dessus de la Vd. S Émission d’un électron, c’est la radioactivité - Nucléide au dessous de la Vd. S Émission d’un positon, C’est la radioactivité + OU émission d’une particule (occasionnellement) Vd. S Émission + Émission
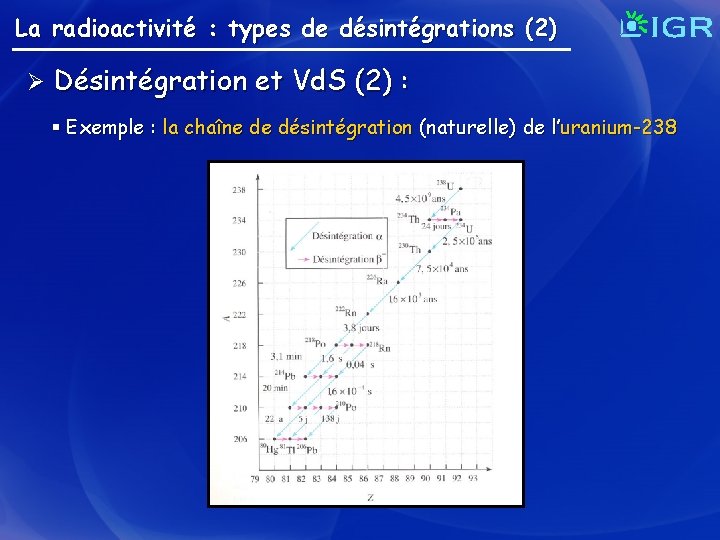
La radioactivité : types de désintégrations (2) Ø Désintégration et Vd. S (2) : § Exemple : la chaîne de désintégration (naturelle) de l’uranium-238

La radioactivité : types de désintégrations (3) Ø Désintégration (1) : § Rare pour les nucléides légers (à partir de Z = 60 et surtout à partir de Z = 82) ; § Équation : A X Z A-4 Z-2 Y + 42 He + Q avec X = noyau père, Y = noyau fils Q = énergie de liaison = (m. X-m. Y-m ). c² ([Q] = Me. V, Q transféré en énergie cinétique à )

La radioactivité : types de désintégrations (4) Ø Désintégration (2) : § Spectre d’émission : Exemple du radium-226 § Exemple : désintégration du radon (sol terrestre) 226 Ra 88 22286 Rn + 42 He + 4, 78 Me. V

La radioactivité : types de désintégrations (5) Ø Désintégration (1) : § 3 formes : - Désintégation - : 0 e -1 est émis par le noyau lorsqu’un neutron se transforme en proton - Désintégation + : 0+1 e est émis par le noyau lorsqu’un proton se transforme en neutron - Capture électronique (CE) : un électron orbital d’une couche interne est attiré par le noyau et transforme un proton en neutron § Spectre d’émission : Exemple de l’azote-13

La radioactivité : types de désintégrations (6) Ø Désintégration (2) : § Question : Écrire les équations de désintégration - Désintégration - : AZX AZ+1 Y + 0 -1 e + Q - Désintégration + : AZX AZ-1 Y + 0+1 e + Q - Capture électronique : AZX + 0 -1 e AZ-1 Y + Q (Q = énergie cinétique des particules émergentes) Et les conservations : problème théorique ! Violation de la loi de conservation de la quantité de mouvement (le noyau fils et l’électron ne se déplacent pas dans des directions opposées) Violation de la loi de conservation du moment cinétique (le spin du neutron initial vaut ½ et le spin du système proton-électron vaut 1) Violation de la loi de conservation de l’énergie (l’énergie des électrons émis suit un spectre d’énergie maximum ECmax=(mn-mp-me). c² = 0, 738 Me. V)

La radioactivité : types de désintégrations (7) Ø Désintégration (3) : § E. Fermi (1930) Hypothèse, aujourd’hui vérifiée, de l’existence d’une tierce particule impliquée dans le processus de désintégration bêta : le neutrino § Le neutrino ( e) : - Charge neutre (conservation de la charge) - Pas influencés par l’interaction forte ni par l’interaction électromagnétique, - Spin ½ (conservation du moment cinétique) - Masse de 27 e. V/c² (19000 fois moins que celle de l’électron) - Se déplace à une vitesse proche de c § L. De Broglie (1934) Le neutrino possède son antiparticule, l’antineutrino ( e)

La radioactivité : types de désintégrations (8) Ø Désintégration (4) : § Équations : - Désintégration - : A X Z AZ+1 Y + 0 -1 e + Q - Désintégration + : A X Z AZ-1 Y + 0+1 e + Q - Capture électronique : A X Z + 0 -1 e AZ-1 Y + e + Q § Exemple : désintégration de l’yttrium-90 ( - pure) : 90 Y 39 9040 Zr + 0 -1 e + 1, 76 Me. V Y 90 couplé à un anticorps pour le traitement des cancers hématologiques

La radioactivité : types de désintégrations (8) Ø Désintégration (5) : § Interaction faible : Nécessité de concevoir une nouvelle force qui pourrait transmuter un neutron en proton et vice et versa : l’interaction faible Interaction faible : - De très courte portée (de 0, 01 fermi) - Un million de fois plus faible que l’interaction forte Structure des quarks et des gluons d’un nucléon Copyright (c) 1995 -2004 Jean-Francois Colonna Copyright (c) 1995 -2004 France Telecom R&D and CMAP / Ecole Polytechnique

La radioactivité : transition gamma Ø Transition gamma : § Après une désintégration alpha ou bêta, un noyau peut se trouver dans un état excité (i. e. avec un nucléon dans un niveau d’énergie plus haut que l’état fondamental) Le noyau se relaxe en émettant un photon gamma Relaxation rapide pour atteindre la plus basse configuration énergétique possible § Ordre de grandeur : de ~1 ke. V à 1 Me. V.

La radioactivité : demie-vie (1) Ø Premières observations : § Ernest Rutherford (1920) L’intensité de rayonnement du Radon-220 diminue avec le temps de façon précise et prévisible (décroissance radioactive) § La quantité de rayonnement émise par un échantillon d’un élément radioactif donné est apparemment indépendante de l’environnement qui l’entoure (composition chimique de l’échantillon, température, pression, …) Ø Le Becquerel : La mesure quantitative de l’intensité radioactive est mesurée en : nombre de désintégration par seconde ou taux de désintégration activité radioactive L’unité du taux de désintégration est le becquerel (Bq)

La radioactivité : demie-vie (2) Ø Calcul de décroissance (1) : § Constante de décroissance Soit un élément radioactif donné, possédant N noyau radioactifs à un instant donné t : | N/ t|/N = constante = est appelée constante de désintégration, [ ] = s-1 § En pratique : La constant de décroissance caractérise une décroissance radioactive (décroissance de N exponentielle, solution de l’équation d. N = - . N. d. T) On utilise plutôt la période T, [T] = s-1, correspondant au temps au bout duquel la moitié des noyaux se sont désintégrés (- . T = Log 1/2 ) Pour un radioélément, de période T, possédant N 0 noyaux radioactifs au temps t 1, le nombre de noyaux radioactifs N au temps t 2 est donné par : 1 N = N 0. 2 t 2 -t 1 T [T] doit être égale à [ti], [N] sera égale à [N 0]

La radioactivité : demie-vie (3) Ø Calcul de décroissance (2) : § Période : Les périodes respectives de chaque nucléide radioactif, appelée également demie-vie, sont tabulées … § Question : La demie-vie du radium-226 est de 5, 096. 1010 s, sachant que les Curie avaient environ 200 g de radium en 1898, combien en reste-t-il aujourd’hui ?

La radioactivité : Schéma de désintégration Ø Représentation de la désintégration § Schéma de désintégration : il est commode de représenter sur un schéma la suite des transitions énergétiques qui conduisent du noyau père au noyau fils ainsi que la nature de l’émission correspondante et éventuellement la période de désintégration § Exemples : Schéma de désintégration simple (cobalt-60) Schéma de désintégration complexe (étain-131, lanthane-131)

La radioactivité Ø Question pour réfléchir : simultanéité et temps A propos de la désintégration radioactive Un noyau vieux de 10000 ans est absolument identique a un noyau de même espèce qui n’a que dix secondes. A partir de ce moment, l’un d’entre eux peut vivre 10000 ans et l’autre dix secondes et nous ne pouvons jamais savoir lequel ?

La radioactivité : conclusion § Transformation spontanée du noyau en configurations énergétiques stables par émission de particules : § Différentes formes de radioactivité : - émission : +, -, capture électronique auxquelles s’ajoute la transition gamma § L’intensité de rayonnement suit une loi de décroissance exponentielle caractérisée par une période (ou demie-vie) § Les énergie rayonnées sont très grandes : i. e. supérieures au Me. V Comment tirer profit de cette énergie ?

III. Les applications médicales de la radioactivité Comment tirer profit de l’émission d’énergie de la radioactivité ?

Applications médicales : introduction (1) Ø La radioactivité et l’Homme (1) § Radioactivité = source d’énergie Le rayonnement issu de la radioactivité est - (très) énergétique - de nature variée (plus ou moins pénétrant) - bien caractérisé (période, production, …) § Effet biologique des radiations Les rayonnements (donc la radioactivité) interagit avec la matière (donc avec les tissus humains) suivant deux types d’interaction : - excitation - ionisation Ces interactions induisent un dépôt d’énergie dans les tissus : la dose [dose] = Gray (Gy) (1 Gy = 1 J. kg-1)

Applications médicales : introduction (2) Ø La radioactivité et l’Homme (2) § Radioactivité vs l’Homme Le rayonnement traverse les tissus Lorsqu’il traverse les tissus il dépose de la dose différent suivant le type de rayonnement Dépôt de dose Ordre de grandeur : une dose de 10 Gy tue la quasi totalité des cellules d’un tissu donné par absorption de 0, 01 J par gramme de tissu i. e. 2. 106 ionisations par cellule

Applications médicales : introduction (2) Ø Risques comparés (Tableau basé en partie sur les données de E. POCHIN) Risque de 1 mort sur un million n n 650 km en avion 100 km en voiture la consommation d’une cigarette 1, 5 minutes d’alpinisme deux heures de séjour dans une pièce avec des fumeurs 1, 5 semaines de travail dans une usine standard 1 heure de pêche en mer 1/2 bouteille de vin exposition radiologique à 0, 1 m. Sv (millisieverts) séjour pendant 3 ans au voisinage d’une centrale nucléaire dose reçue en moyenne par trimestre du fait du radiodiagnostic

Applications médicales : introduction (3) Ø La radioactivité en médecine § Traitement par « rayons » (l’effet biologique de la dose résulte d’une chaîne de réactions physico-chimique déclenchée par les ionisations et qui induit des dommages aux grosses molécules indispensable à la vie cellulaire) § Imagerie (diagnostic) Caméra (Diagnostic) Traitement § Radioprotection !

Applications médicales (App. Med. ) : plan § Radiothérapie métabolique § L’imagerie § Production de radio-éléments artificiels § La Radioprotection Image de Tomographie par Émission de Positons couplée à un Tomodensitomètre (TEP-TDM) (Maximum Intensity Projection)

App. Med. : radiothérapie métabolique (1) Ø Le traitement par la radioactivité § Traitement par « rayons » § Utilisation d’un radio pharmaceutique : i. e - une molécule cible (spécifique d’une pathologie) - un radio-élément (pour le dépôt de dose) § But : provoquer la mort cellulaire des tissus pathologique, par irradiation, de manière ciblée § Comment : en injectant (ou ingérant) un radio pharmaceutique qui va se distribuer spécifiquement dans le corps § Exemple : Traitement du cancer de la thyroïde par Iode-131 (capsule par exemple)

App. Med. : radiothérapie métabolique (2) Quel radio-élément ? § Ce qu’on cherche : Ø dépôt de dose le plus ciblé possible et local possible § Problèmes : - dépôt de dose sur la zone pathologique en épargnant les tissus sains - radioprotection (des professionnels) § Exemple : le Traitement du cancer de la thyroïde par Iode-131 Question : pourquoi l’Iode 131 ?

App. Med. : radiothérapie métabolique (3) Ø Critères de choix du radio pharmaceutique § le pharmaceutique : le plus spécifique de la pathologie Iode : - capté en majorité par la thyroïde - MAIS captation par le digestif passage par le circuit d’élimination urinaire § le radio élément : - Émission de particules peu pénétrantes et directement ionisantes - Schéma de désintégration le plus sobre possible - Demie-vie adaptée (plutôt courte) Iode-131 : - émetteur - MAIS émetteur gamma - ½ vie de 8, 12 jours

App. Med. : radiothérapie métabolique (4) Ø Le réflexe : § la cinétique de fixation du pharmaceutique Cinétique de l’iode Source : MIRD § le schéma de désintégration du radio-élément:
App. Med. : radiothérapie métabolique (5) Ø L’iode-131 comme radio pharmaceutique § Ingestion de 3, 7 GBq (capsule) § La cinétique de l’iode : Distribution non totalement spécifique

App. Med. : imagerie (1) Ø L’imagerie d’émission § Réalisation d’images diagnostiques grâce à l’injection d’un radio traceur et une caméra adaptée § Utilisation d’un radio traceur : i. e. - une molécule cible (spécifique d’une pathologie) - un radio-élément (émettant les rayons à détecter) § But : visualiser pathologie par une méthode non invasive § Comment : en injectant (inhalant ou ingérant) un radio traceur qui va se distribuer spécifiquement dans le corps § Exemple : La Tomographie par Émission de Positons (TEP) au fluorodéoxyglucose marqué au fluor-18 (18 FDG) pour le diagnostic du cancer

App. Med. : imagerie (2) Quel radio élément ? § Ce qu’on cherche : Ø traceur la plus ciblé possible et rayonnement le plus pénétrant possible § Problèmes : - dépôt de dose à l’échelle du corps - rayonnement secondaire parasite (interactions rayons-matières) - radioprotection (des professionnels) § Exemple : La TEP dans le diagnostic des cancers Question : pourquoi l’ 18 FDG ?

App. Med. : imagerie (3) Ø Critères de choix du radio pharmaceutique § le traceur : le plus spécifique de la pathologie FDG (analogue du glucose) : - consommation exacerbée par les tumeurs - MAIS captation par la plupart des cellules humaines passage par le circuit d’élimination urinaire § le radio élément : - Émission de particules pénétrantes et d’énergie adaptée - Schéma de désintégration le plus sobre possible - Demie-vie la plus courte possible Fluor-18 : - émetteur +/détection gamma 511 kev d’annihilation - ½ vie de 2 heures

App. Med. : imagerie (4) Ø Le réflexe : § la cinétique de fixation du traceur Cinétique du FDG Source : MIRD § le schéma de désintégration du radio élément

App. Med. : imagerie (5) Ø Le 18 FDG comme radio traceur : résultat (1) § En pratique - Déroulement d’un examen : Ý Injection du 18 FDG (à jeun) Ý Repos de 45 minutes au minimum Ý Examen TEP (45 minutes environ) - Une caméra TEP : (le Biograph de Siemens)
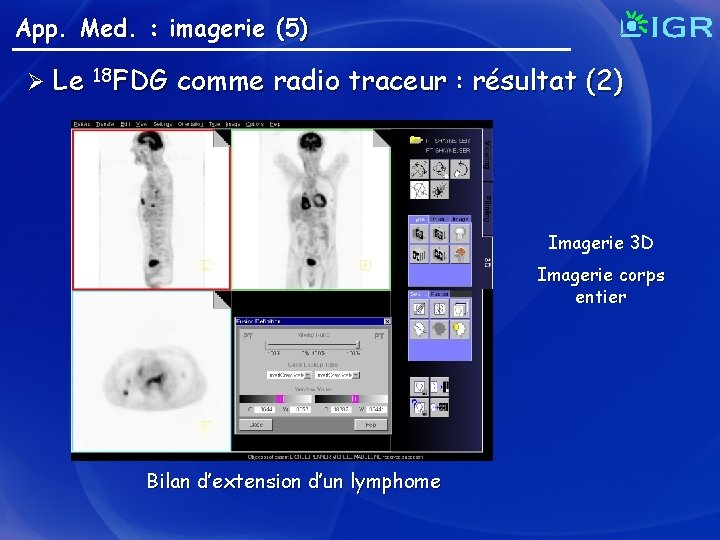
App. Med. : imagerie (5) Ø Le 18 FDG comme radio traceur : résultat (2) Imagerie 3 D Imagerie corps entier Bilan d’extension d’un lymphome
App. Med. : imagerie (6) Ø L’iode-131 comme radio traceur : Dose traceuse d’ l’iode-131 pour la détermination de l’activité thérapeutique d’un traitement de cancer de la thyroïde Ø Imagerie d’émission = imagerie fonctionnelle

App. Med. : production des radio éléments (1) Ø Quelques chiffres : § en Europe et par an plus de 12 millions de procédures médicales (diagnostic et thérapie) utilisant des radioisotopes, (soit plus de 30 000 procédures par jour) § Proportion de l’utilisation des radio éléments : - 90 % des radio éléments des fins diagnostiques - 10 % pour de la thérapie Méthodes de production ?

App. Med. : production des radio éléments (2) Ø Méthodes § Par réaction nucléaires provoquées (utilisation de cyclotrons par exemple) § Par désintégration « naturelle » (Voies de désintégration)
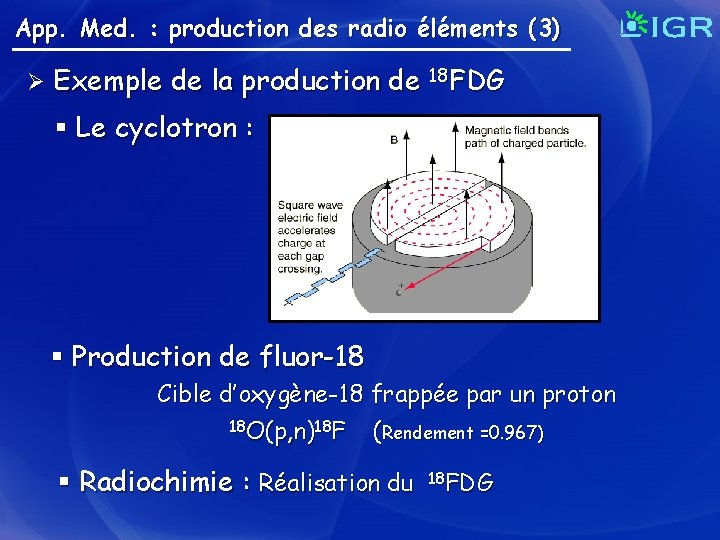
App. Med. : production des radio éléments (3) Ø Exemple de la production de 18 FDG § Le cyclotron : § Production de fluor-18 Cible d’oxygène-18 frappée par un proton 18 O(p, n)18 F (Rendement =0. 967) § Radiochimie : Réalisation du 18 FDG

App. Med. : radioprotection (1) Ø Définition : C’est l’ensemble des dispositions prises pour protéger les travailleurs et le public. Ø Principes : - justification - optimisation (ALARA) - limitation des doses individuelles Ø Un sigle :

App. Med. : radioprotection (2) Ø Radioprotection et radioactivité § Enjeux : - Protection contre des scellées/sources non scellées - Types de sources variées (thérapie/diagnostic) § Méthodes : - Circuits de gestion des déchets (liquides/solides/infectieux) - Principe temps / écran / distance

App. Med. : radioprotection (3) Ø En pratique § Consulter le schéma de désintégration § Questions à se poser : - Quel type d’émetteur (alpha, bêta, gamma) - Quelle est l’énergie de/des émissions - Quelle la période du radio élément en jeu - Quelle mesure prendre pour s’en protéger § Exemple de l’iode-131

Conclusion § Utiliser les radionucléides en médecine c’est : - savoir les produire - savoir les marquer (association avec un produit radiopharmaceutique) - connaître les caractéristiques tant physique biologique du radiopharmaceutique - savoir les détecter - savoir s’en protéger

Bibliographie § La physique : Heugène Hecht § Noyaux et particules : Luc Valentin § Biophysique des radiations et imagerie médicale : Jean Dutreix/Alain Desgrez/Bernard Bok/Jean-Marc Vinot Une question => bonniaud@igr. fr
- Slides: 97