Massas Atmicas e Massas Moleculares parte I 1











- Slides: 24


Massas Atômicas e Massas Moleculares – parte I 1ª Série – Ensino Médio Professora Simone Silva Cotrin

Habilidade Calcular massas moleculares das substâncias a partir das massas atômicas dos elementos químicos constituintes.

Combinados • • • Realize as atividades propostas Anote suas dúvidas Caderno do Aluno – volume 3

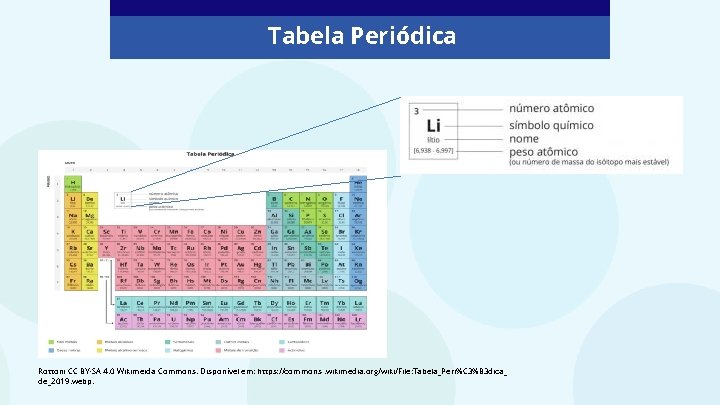
Tabela Periódica Rottoni CC BY-SA 4. 0 Wikimeida Commons. Disponível em: https: //commons. wikimedia. org/wiki/File: Tabela_Peri%C 3%B 3 dica_ de_2019. webp.

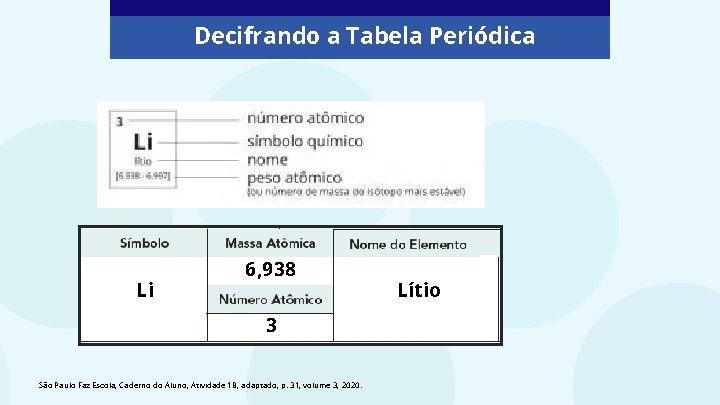
Decifrando a Tabela Periódica Li 6, 938 3 São Paulo Faz Escola, Caderno do Aluno, Atividade 1 B, adaptado, p. 31, volume 3, 2020. Lítio

Massa Atômica

Isótopos são átomos de um mesmo elemento químico que possuem a mesma quantidade de prótons (mesmo número atômico), mas diferenciam-se pelo número de massa. (A = prótons + nêutrons) Z X A O carbono possui dois isótopos estáveis: • 6 C 12 – carbono 12, mais abundante na Terra (cerca de 98, 89%). • 6 C 13 – carbono 13, menos abundante (cerca de 1, 01 a 1, 14%).

Massa Atômica Média Z X A O carbono possui dois isótopos estáveis: • 6 C 12 – carbono 12, mais abundante na Terra (cerca de 98, 89%). • 6 C 13 – carbono 13, menos abundante (cerca de 1, 01 a 1, 14%). Calcula-se a média ponderada de todos os isótopos estáveis. Massa atômica = [12. (98, 89) + 13. (1, 11)] / 100 Massa atômica = 12, 0111 u

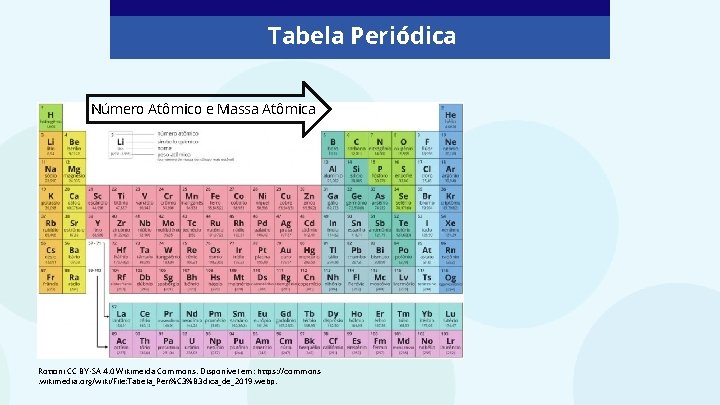
Tabela Periódica Número Atômico e Massa Atômica Rottoni CC BY-SA 4. 0 Wikimeida Commons. Disponível em: https: //commons. wikimedia. org/wiki/File: Tabela_Peri%C 3%B 3 dica_de_2019. webp.

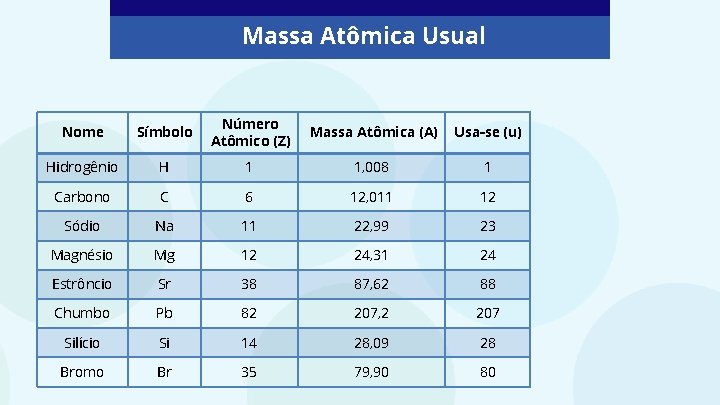
Massa Atômica Usual Nome Símbolo Número Atômico (Z) Massa Atômica (A) Usa-se (u) Hidrogênio H 1 1, 008 1 Carbono C 6 12, 011 12 Sódio Na 11 22, 99 23 Magnésio Mg 12 24, 31 24 Estrôncio Sr 38 87, 62 88 Chumbo Pb 82 207, 2 207 Silício Si 14 28, 09 28 Bromo Br 35 79, 90 80

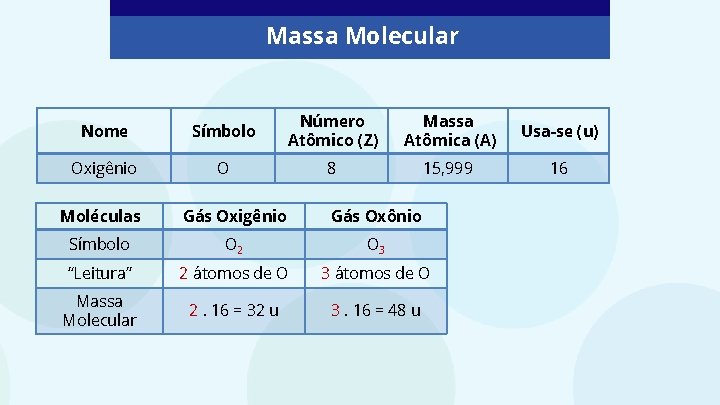
Massa Molecular Nome Símbolo Número Atômico (Z) Massa Atômica (A) Usa-se (u) Oxigênio O 8 15, 999 16 Moléculas Gás Oxigênio Gás Oxônio Símbolo O 2 O 3 “Leitura” 2 átomos de O 3 átomos de O Massa Molecular 2. 16 = 32 u 3. 16 = 48 u

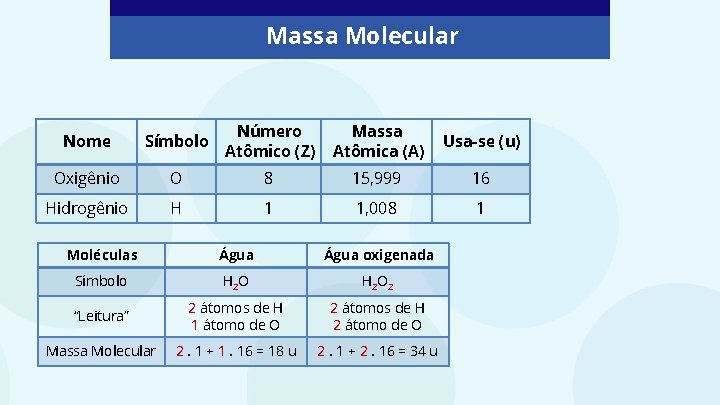
Massa Molecular Nome Símbolo Número Atômico (Z) Massa Atômica (A) Usa-se (u) Oxigênio O 8 15, 999 16 Hidrogênio H 1 1, 008 1 Moléculas Água oxigenada Símbolo H 2 O 2 “Leitura” 2 átomos de H 1 átomo de O 2 átomos de H 2 átomo de O Massa Molecular 2. 1 + 1. 16 = 18 u 2. 1 + 2. 16 = 34 u

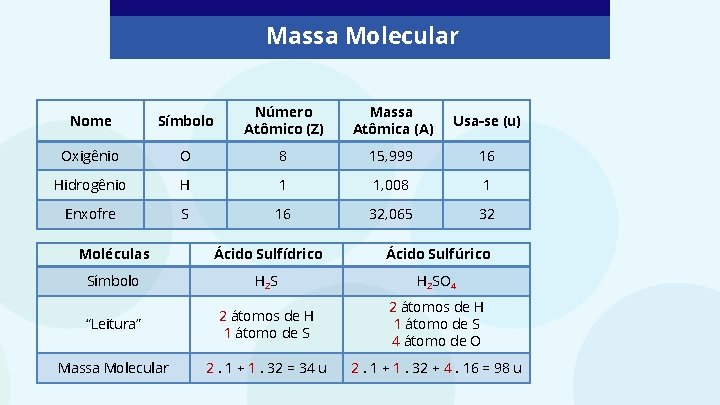
Massa Molecular Nome Símbolo Número Atômico (Z) Massa Atômica (A) Usa-se (u) Oxigênio O 8 15, 999 16 Hidrogênio H 1 1, 008 1 Enxofre S 16 32, 065 32 Moléculas Ácido Sulfídrico Ácido Sulfúrico Símbolo H 2 SO 4 “Leitura” 2 átomos de H 1 átomo de S 4 átomo de O Massa Molecular 2. 1 + 1. 32 = 34 u 2. 1 + 1. 32 + 4. 16 = 98 u

Agora é sua vez. . . Pesquise na tabela periódica as massas atômicas e os símbolos dos elementos hidrogênio, oxigênio, cálcio, cobre, enxofre, carbono e ferro. São Paulo Faz Escola, Caderno do Aluno, Atividade 3 F, adaptado, p. 37 e 38, volume 3, 2020.

Agora é sua vez. . . Pesquise na tabela periódica as massas atômicas e os símbolos dos elementos: hidrogênio, oxigênio, cálcio, cobre, enxofre, carbono e ferro. São Paulo Faz Escola, Caderno do Aluno, Atividade 3 F, adaptado, p. 37 e 38, volume 3, 2020.

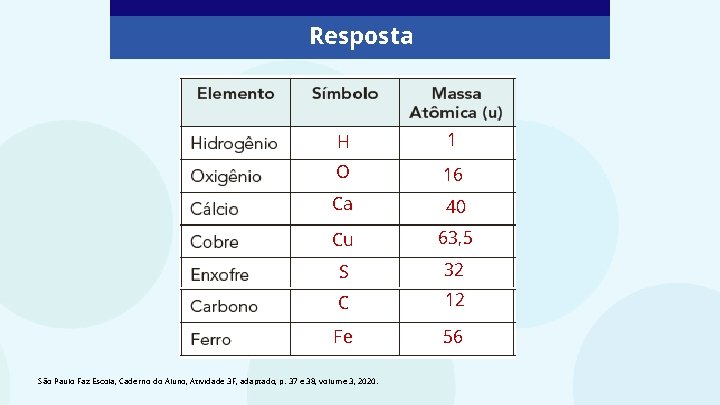
Resposta H 1 O 16 Ca 40 Cu 63, 5 S 32 C 12 Fe 56 São Paulo Faz Escola, Caderno do Aluno, Atividade 3 F, adaptado, p. 37 e 38, volume 3, 2020.

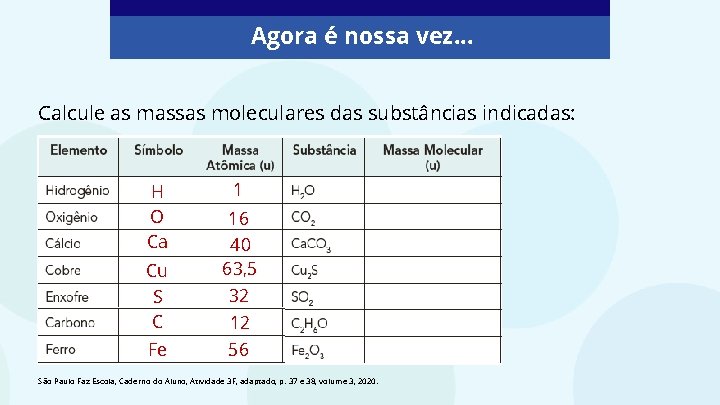
Agora é nossa vez. . . Calcule as massas moleculares das substâncias indicadas: H O Ca Cu S C Fe 1 16 40 63, 5 32 12 56 São Paulo Faz Escola, Caderno do Aluno, Atividade 3 F, adaptado, p. 37 e 38, volume 3, 2020.

Resposta 18 44 100 159 64 46 160 São Paulo Faz Escola, Caderno do Aluno, Atividade 3 F, adaptado, p. 37 e 38, volume 3, 2020.

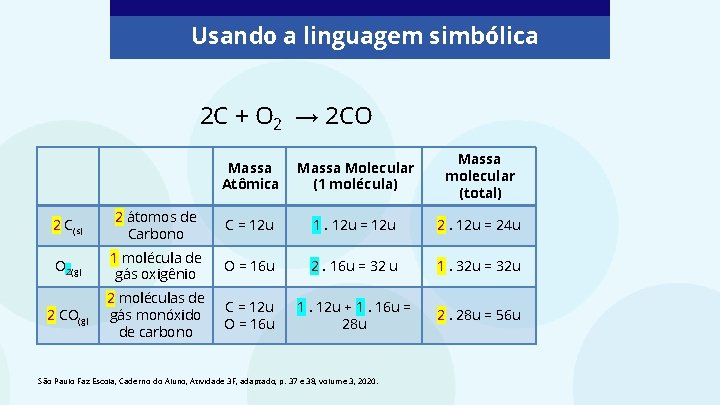
Usando a linguagem simbólica 2 C + O 2 → 2 CO Massa Atômica Massa Molecular (1 molécula) Massa molecular (total) 2 C(s) 2 átomos de Carbono C = 12 u 1. 12 u = 12 u 2. 12 u = 24 u O 2(g) 1 molécula de gás oxigênio O = 16 u 2. 16 u = 32 u 1. 32 u = 32 u 2 CO(g) 2 moléculas de gás monóxido de carbono C = 12 u O = 16 u 1. 12 u + 1. 16 u = 28 u 2. 28 u = 56 u São Paulo Faz Escola, Caderno do Aluno, Atividade 3 F, adaptado, p. 37 e 38, volume 3, 2020.

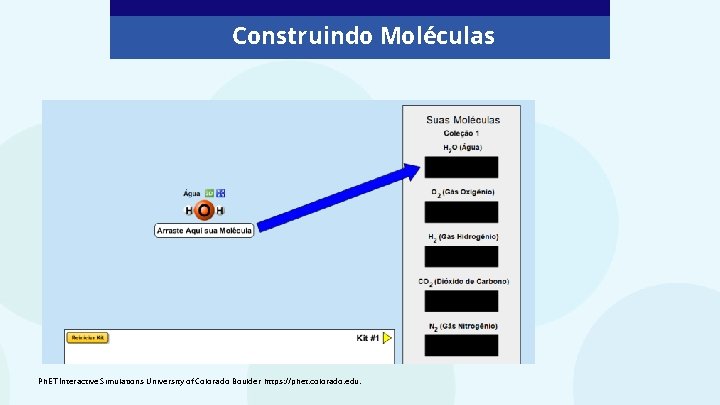
Construindo Moléculas Ph. ET Interactive Simulations University of Colorado Boulder https: //phet. colorado. edu.

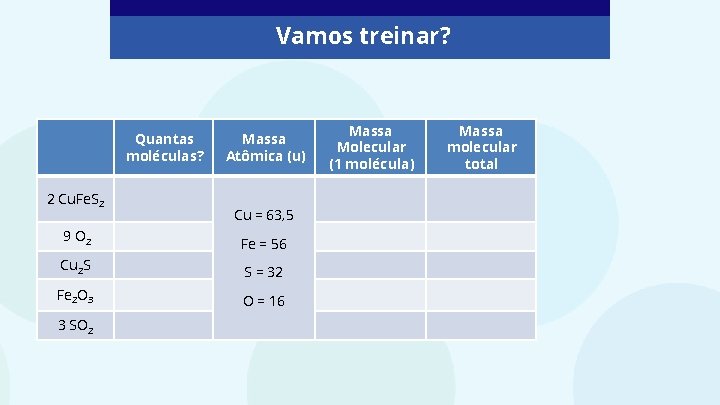
Vamos treinar? Quantas moléculas? 2 Cu. Fe. S 2 Massa Atômica (u) Cu = 63, 5 9 O 2 Fe = 56 Cu 2 S S = 32 Fe 2 O 3 O = 16 3 SO 2 Massa Molecular (1 molécula) Massa molecular total

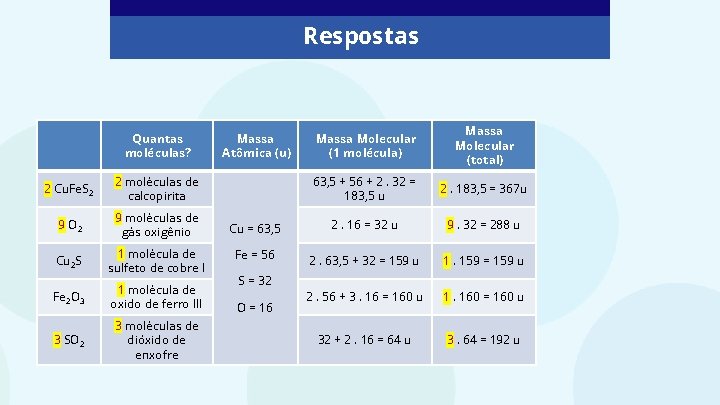
Respostas Quantas moléculas? Massa Atômica (u) Massa Molecular (1 molécula) Massa Molecular (total) 63, 5 + 56 + 2. 32 = 183, 5 u 2. 183, 5 = 367 u 2 Cu. Fe. S 2 2 moléculas de calcopirita 9 O 2 9 moléculas de gás oxigênio Cu = 63, 5 2. 16 = 32 u 9. 32 = 288 u Cu 2 S 1 molécula de sulfeto de cobre I Fe = 56 2. 63, 5 + 32 = 159 u 1. 159 = 159 u Fe 2 O 3 1 molécula de oxido de ferro III 2. 56 + 3. 16 = 160 u 1. 160 = 160 u 3 SO 2 3 moléculas de dióxido de enxofre 32 + 2. 16 = 64 u 3. 64 = 192 u S = 32 O = 16

Obrigada