Maria Luisa Tutino Dip Chimica Organica e Biochimica

Maria Luisa Tutino Dip. Chimica Organica e Biochimica tutino@unina. it Tel 081674317 Gilda Parrilli Dip. Chimica Organica e Biochimica erparril@unina. it Tel 081674114

Modulo di chimica e biotecnologie delle fermentazioni (corso di biotecnlogie microbiche e delle fermentazioni corso di laurea magistrale in biotecnologie del farmaco) • INTRODUZIONE • MODELLI CINETICI. Cinetica della crescita microbica. Cinetica della formazione del prodotto. Cinetica del consumo del substrato. Il bilancio di massa. Velocità volumetrica e specifica di reazione. Crescita microbica. Resa di crescita. Modello di Monod. Principali metodi di determinazione della biomassa. • MODALITA’ OPERATIVE DI CONDUZIONE DEL BIOPROCESSO. Fermentazione batch, continua, fedbatch. Vantaggi e limitazioni. • BIOREATTORI. Stirred tank reactor. Bioreattori a colonna di bolle. Bioreattori Air Lift. Bioreattori a letto impaccato. Bioreattori a letto fluidificato • TECNOLOGIA DELLE FERMENTAZIONI: Biocatalizzatori. Formulazione terreni di coltura. Sterilizzazione. Aerazione ed agitazione. • APPLICAZIONI: produzione di antibiotici Testi consigliati: • Appunti delle lezioni • Donadio S. e Marino G: Biotecnologie Microbiche Casa Editrice Ambrosiana 2008 • S. O. Enfors and L. Haggstrom: Bioprocess technology: fundamentals and applications, Hogskoletryckeriet, Stockolm, 1998.
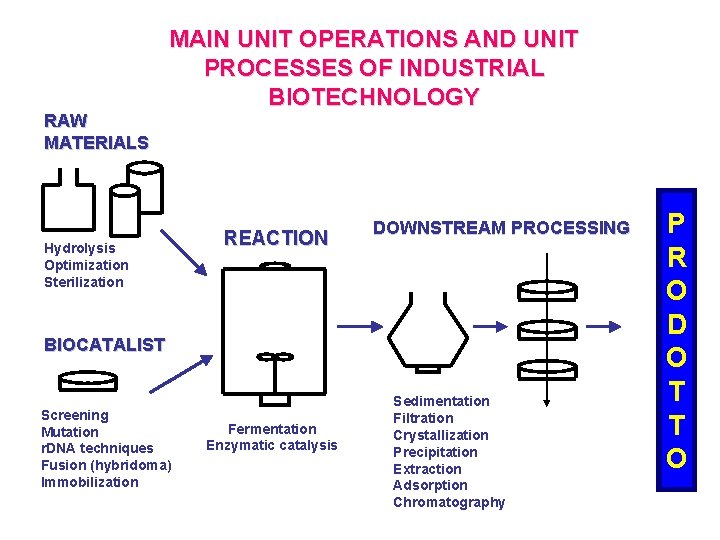
RAW MATERIALS MAIN UNIT OPERATIONS AND UNIT PROCESSES OF INDUSTRIAL BIOTECHNOLOGY Hydrolysis Optimization Sterilization REACTION DOWNSTREAM PROCESSING BIOCATALIST Screening Mutation r. DNA techniques Fusion (hybridoma) Immobilization Fermentation Enzymatic catalysis Sedimentation Filtration Crystallization Precipitation Extraction Adsorption Chromatography P R O D O T T O
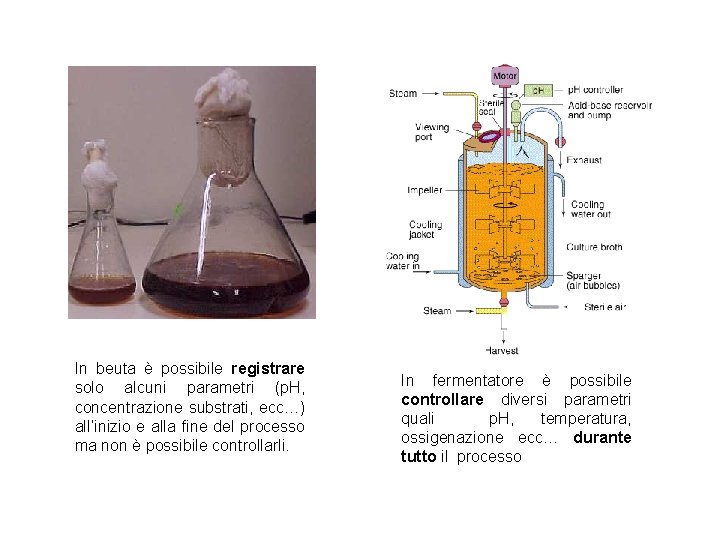
In beuta è possibile registrare solo alcuni parametri (p. H, concentrazione substrati, ecc…) all’inizio e alla fine del processo ma non è possibile controllarli. In fermentatore è possibile controllare diversi parametri quali p. H, temperatura, ossigenazione ecc… durante tutto il processo

BIOREATTORI BIOREATTORE: ambiente controllato in cui si allestisce una reazione biochimica FERMENTATORE: un bioreattore nel quale si realizza una fermentazione Scala da laboratorio Scala pilota Scala industriale 1 -10 L 50 -1000 L 100, 000 -300, 000 L

Fermentatori I fermentatori vanno da semplici a sistemi integrati complessi che coinvolgono diversi livelli di controllo. Si distinguono due tipi di fermentatori: sistemi non-asettici dove non è necessario operare con colture pure di microrganismi; sistemi asettici usati per la produzione di composti come antibiotici, amminoacidi, polisaccaridi ecc. . . L’obiettivo di qualsiasi fermentatore è di ottimizzare la crescita dell’organismo e/o la formazione di un prodotto da parte di un organismo.

Un fermentatore deve… üescludere l’ingresso di organismi contaminanti ücontenere gli organismi desiderati ümantenere il volume della coltura costante ümantenere il livello di ossigeno disciolto sopra valori critici di aerazione e agitazione per organismi aerobici üControllare parametri come temperatura e p. H üConsentire una buona miscelazione della coltura

In un fermentatore… – I materiali che sono in contatto con le soluzioni che entrano nel fermentatore o con la coltura devono • essere resistenti alla corrosione. • essere non-tossici perchè la dissoluzione del materiale non inibisca la crescita. • sopportare ripetuti cicli di sterilizzazione ad alta pressione. – Il sistema di agitazione, le porte d’ingresso devono essere sufficientemente rigidi da non essere deformati o rotti per lo stress meccanico. – L’ispezione visiva del mezzo e della coltura è vantaggiosa, per cui se possibile dovrebbero essere usati materiali trasparenti.

TIPOLOGIE DI BIOREATTORI üStirred tank reactor üBioreattori a colonna di bolle üBioreattori Air Lift üBioreattori a letto impaccato üBioreattori a letto fluidificato
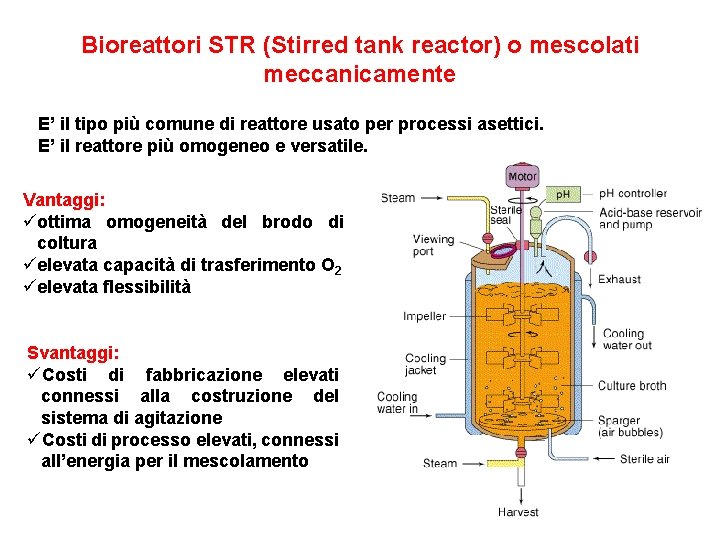
Bioreattori STR (Stirred tank reactor) o mescolati meccanicamente E’ il tipo più comune di reattore usato per processi asettici. E’ il reattore più omogeneo e versatile. Vantaggi: üottima omogeneità del brodo di coltura üelevata capacità di trasferimento O 2 üelevata flessibilità Svantaggi: üCosti di fabbricazione elevati connessi alla costruzione del sistema di agitazione üCosti di processo elevati, connessi all’energia per il mescolamento
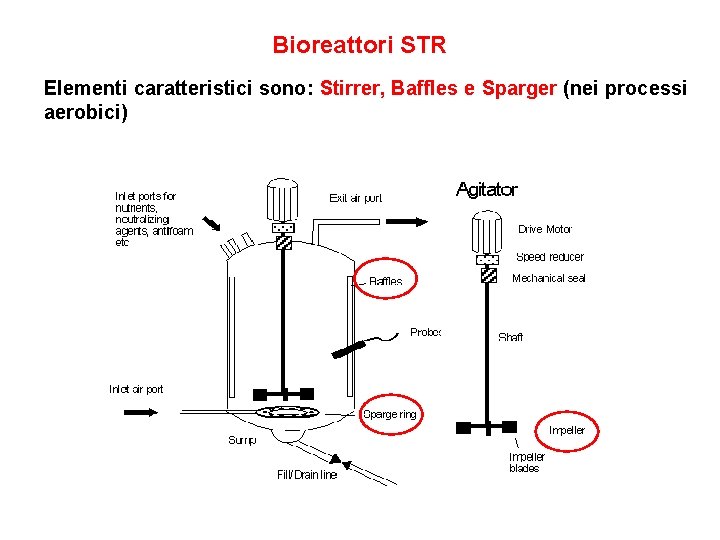
Bioreattori STR Elementi caratteristici sono: Stirrer, Baffles e Sparger (nei processi aerobici)
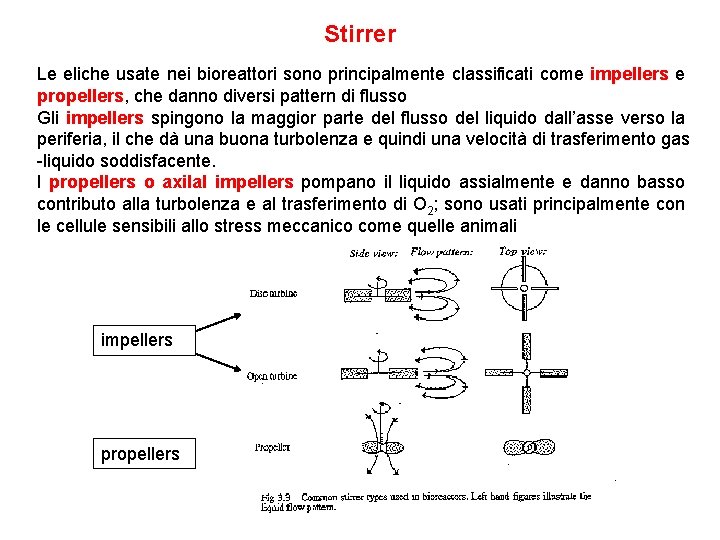
Stirrer Le eliche usate nei bioreattori sono principalmente classificati come impellers e propellers, che danno diversi pattern di flusso Gli impellers spingono la maggior parte del flusso del liquido dall’asse verso la periferia, il che dà una buona turbolenza e quindi una velocità di trasferimento gas -liquido soddisfacente. I propellers o axilal impellers pompano il liquido assialmente e danno basso contributo alla turbolenza e al trasferimento di O 2; sono usati principalmente con le cellule sensibili allo stress meccanico come quelle animali impellers propellers

Stirrer I due tipi di stirrer più usati nei fermentatori sono: La Rushton Turbine è una turbina con lame poste perpendicolarmente, ha lame piatte, con un disco o perno centrale, e un numero variabile di alette attaccate con un angolo di 90 gradi al perno. Questi impellers forzano il flusso all’esterno in direzione radiale e causano cicli nel reattore poiché il flusso colpisce le pareti. L’A 310 Airfoil è un axilal impeller (propeller) più simile a un motore marino con lame angolate. Alcuni hanno lame dritte attaccate all’asse del motore ad angolo, altri hanno lame curve. Questi forzano il flusso verso il basso, creando un pattern di flusso giù al centro del reattore che sale su lungo le pareti. Rushton Turbine Impeller A 310 Airfoil
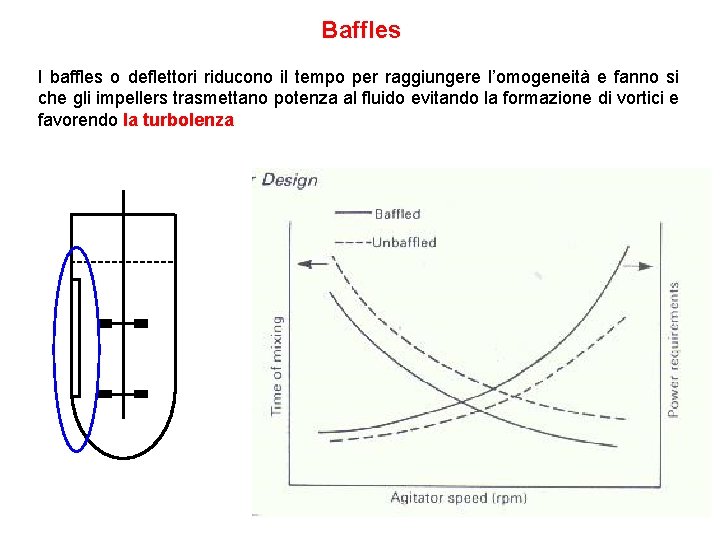
Baffles I baffles o deflettori riducono il tempo per raggiungere l’omogeneità e fanno si che gli impellers trasmettano potenza al fluido evitando la formazione di vortici e favorendo la turbolenza
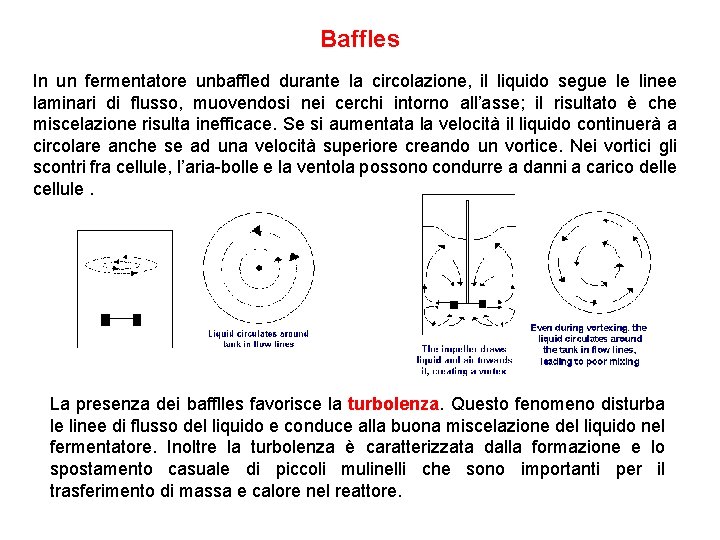
Baffles In un fermentatore unbaffled durante la circolazione, il liquido segue le linee laminari di flusso, muovendosi nei cerchi intorno all’asse; il risultato è che miscelazione risulta inefficace. Se si aumentata la velocità il liquido continuerà a circolare anche se ad una velocità superiore creando un vortice. Nei vortici gli scontri fra cellule, l’aria-bolle e la ventola possono condurre a danni a carico delle cellule. La presenza dei bafflles favorisce la turbolenza. Questo fenomeno disturba le linee di flusso del liquido e conduce alla buona miscelazione del liquido nel fermentatore. Inoltre la turbolenza è caratterizzata dalla formazione e lo spostamento casuale di piccoli mulinelli che sono importanti per il trasferimento di massa e calore nel reattore.
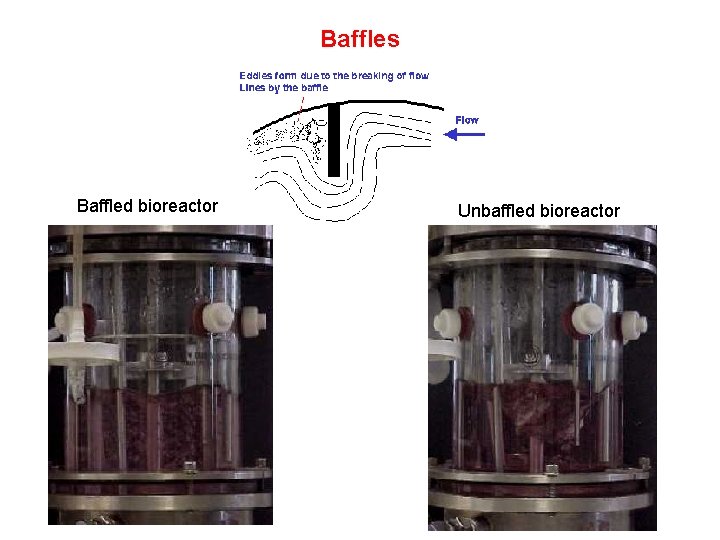
Baffles Baffled bioreactor Unbaffled bioreactor
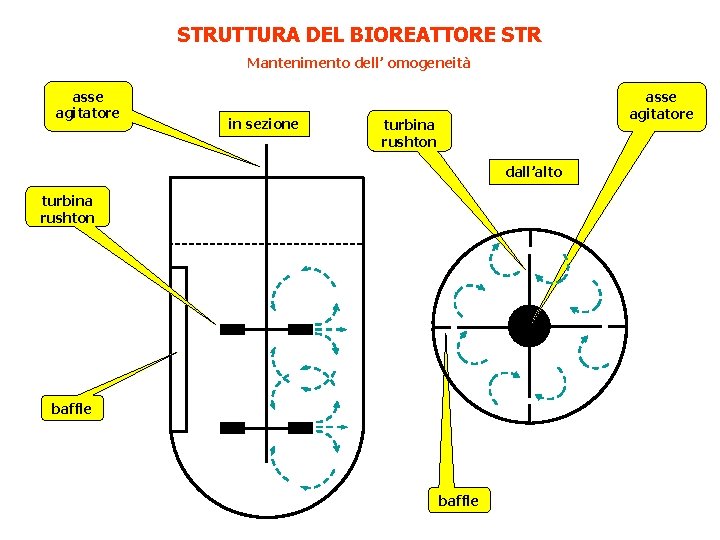
STRUTTURA DEL BIOREATTORE STR Mantenimento dell’ omogeneità asse agitatore in sezione asse agitatore turbina rushton dall’alto turbina rushton baffle

Spargers Gli spargers servono ad introdurre bolle più piccole nel fermentatore. Il tipo più semplice è a singolo-orifizio. All’aumentare delle dimensioni del fermentatore aumentano le richieste di aerazione. Se occorre una maggiore aerazione, si usa lo sparger ad anello ha molti buchi. Ciascun buco è quindi considerato come un orefizio critico. Lo Sparger è localizzato direttamente sotto il disco dell’impeller più basso cosicché la corrente d’aria è immessa direttamente attraverso gli impellers.
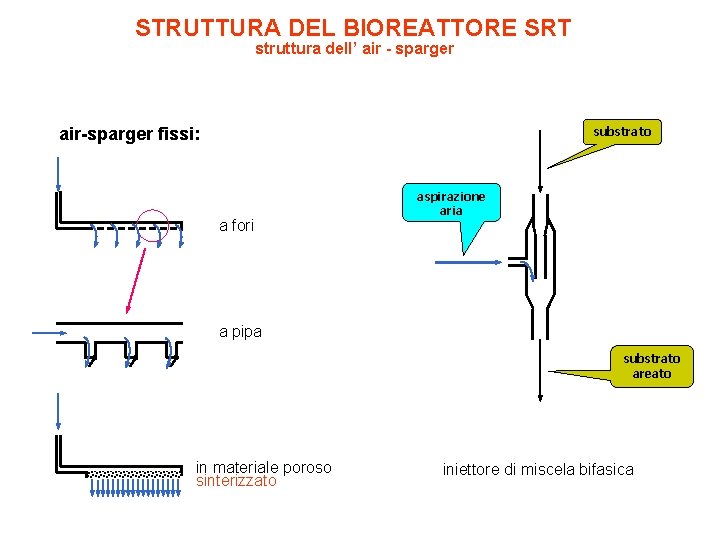
STRUTTURA DEL BIOREATTORE SRT struttura dell’ air - sparger air-sparger fissi: substrato a fori aspirazione aria a pipa substrato areato in materiale poroso sinterizzato iniettore di miscela bifasica
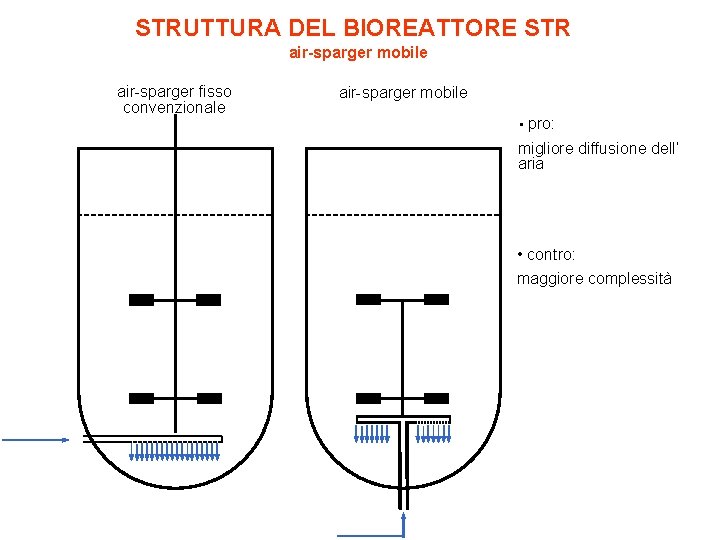
STRUTTURA DEL BIOREATTORE STR air-sparger mobile air-sparger fisso convenzionale air-sparger mobile • pro: migliore diffusione dell’ aria • contro: maggiore complessità

Oxygen delivery system I dispositivi coinvolti nel sistema di ossigenazione oltre agli insufflatori comprendono: il compressore e sistemi per l’ingresso e l’uscita dell’aria L’aria contiene tipicamente 103 -104 microrganismi/m 3; l’aria in ingresso è sterilizzata per filtrazione; il filtro è sterilizzato a vapore
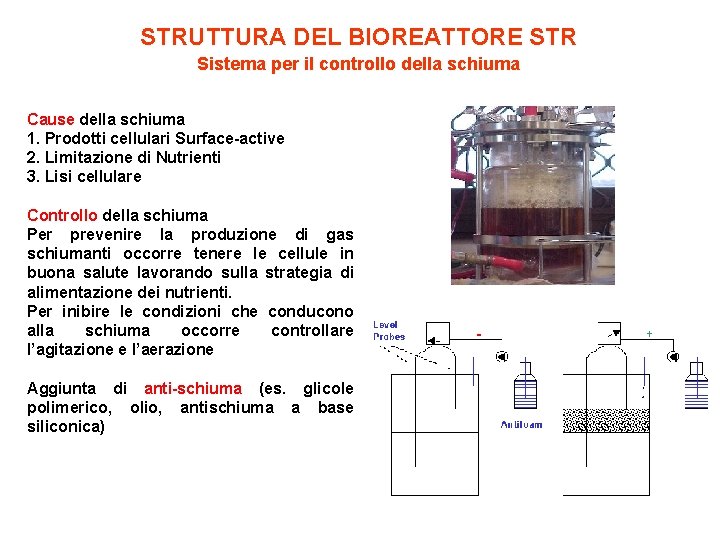
STRUTTURA DEL BIOREATTORE STR Sistema per il controllo della schiuma Cause della schiuma 1. Prodotti cellulari Surface-active 2. Limitazione di Nutrienti 3. Lisi cellulare Controllo della schiuma Per prevenire la produzione di gas schiumanti occorre tenere le cellule in buona salute lavorando sulla strategia di alimentazione dei nutrienti. Per inibire le condizioni che conducono alla schiuma occorre controllare l’agitazione e l’aerazione Aggiunta di anti-schiuma (es. glicole polimerico, olio, antischiuma a base siliconica)
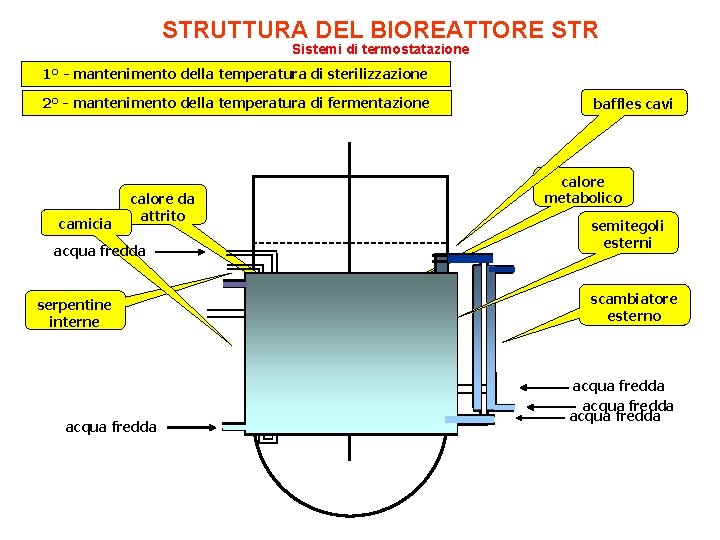
STRUTTURA DEL BIOREATTORE STR Sistemi di termostatazione 1° - mantenimento della temperatura di sterilizzazione 2° - mantenimento della temperatura di fermentazione camicia calore da attrito acqua fredda serpentine interne acqua fredda baffles cavi calore metabolico semitegoli esterni scambiatore esterno acqua fredda
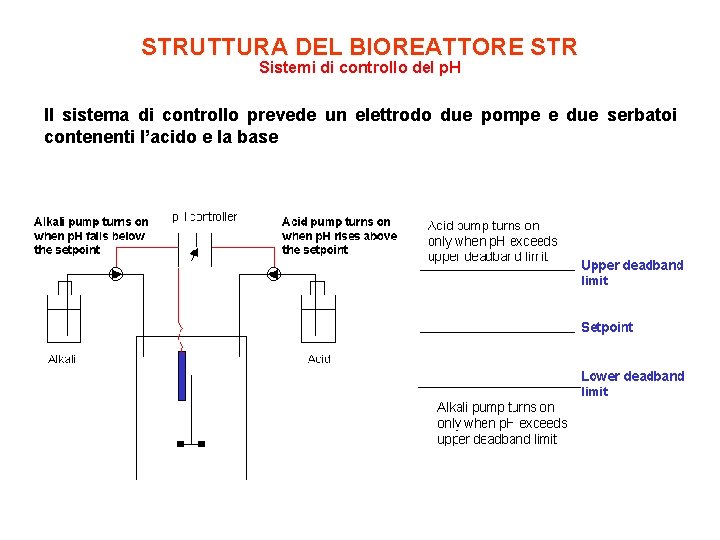
STRUTTURA DEL BIOREATTORE STR Sistemi di controllo del p. H Il sistema di controllo prevede un elettrodo due pompe e due serbatoi contenenti l’acido e la base
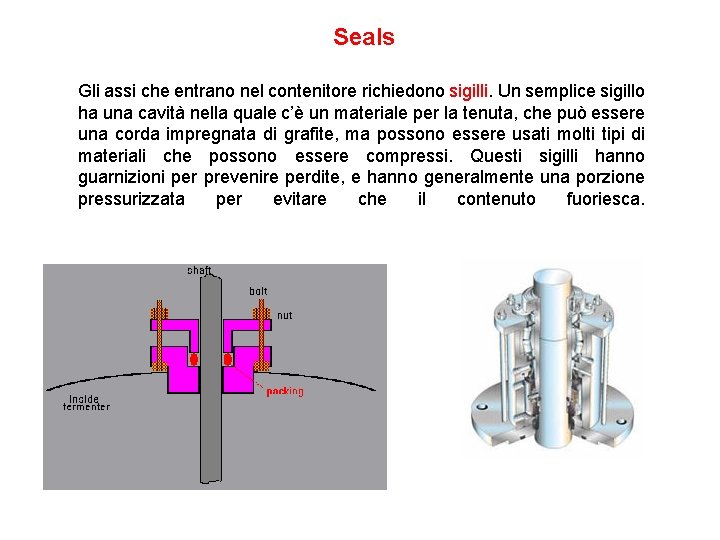
Seals Gli assi che entrano nel contenitore richiedono sigilli. Un semplice sigillo ha una cavità nella quale c’è un materiale per la tenuta, che può essere una corda impregnata di grafite, ma possono essere usati molti tipi di materiali che possono essere compressi. Questi sigilli hanno guarnizioni per prevenire perdite, e hanno generalmente una porzione pressurizzata per evitare che il contenuto fuoriesca.

STERILIZZAZIONE • Una delle principali difficoltà nel condurre una fermentazione su larga scala è connessa alla funzione asettica del reattore • I reattori di laboratorio sono spesso di vetro e sono sterilizzati con il mezzo (se non è termolabile), tubi, e elettrodi in autoclave • Alcuni reattori di laboratorio e tutti quelli su larga scala sono recipienti a pressione, che operano ad almeno 1. 2 bar sulla pressione ambiente. Questi sono sterilizzati in situ con un iniziale riscaldamento con un getto di vapore attraverso una camicia esterna finché la temperatura del mezzo è circa 90 °C, seguita da iniezione diretta di vapore nel mezzo per aumentare la temperatura a 120 °C, per evitare la condensazione dell’acqua nel mezzo. Tubi, valvole e filtri sono sterilizzati da continua immissione di vapore sotto pressione durante la sterilizzazione. • Sono disponibili sonde sterilizzabili a vapore per monitorare il p. H, l’O 2 disciolto, la temperatura e la pressione



Fermentatori Da Stauffer Chemical Co. Monosodium Glutamate plant in San Jose, CA. . 8 fermentatori di 30. 000 gal (110. 000 l) ciascuno.

TIPOLOGIE DI BIOREATTORI üStirred tank reactor üBioreattori a colonna di bolle üBioreattori Air Lift üBioreattori a letto impaccato üBioreattori a letto fluidificato
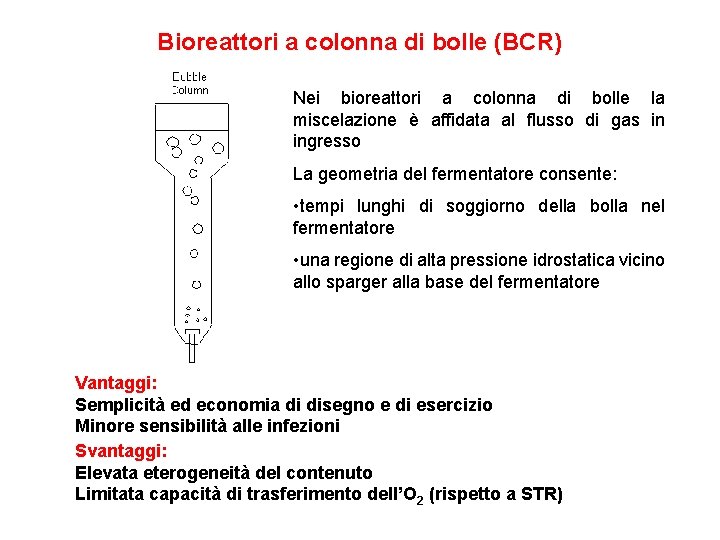
Bioreattori a colonna di bolle (BCR) Nei bioreattori a colonna di bolle la miscelazione è affidata al flusso di gas in ingresso La geometria del fermentatore consente: • tempi lunghi di soggiorno della bolla nel fermentatore • una regione di alta pressione idrostatica vicino allo sparger alla base del fermentatore Vantaggi: Semplicità ed economia di disegno e di esercizio Minore sensibilità alle infezioni Svantaggi: Elevata eterogeneità del contenuto Limitata capacità di trasferimento dell’O 2 (rispetto a STR)
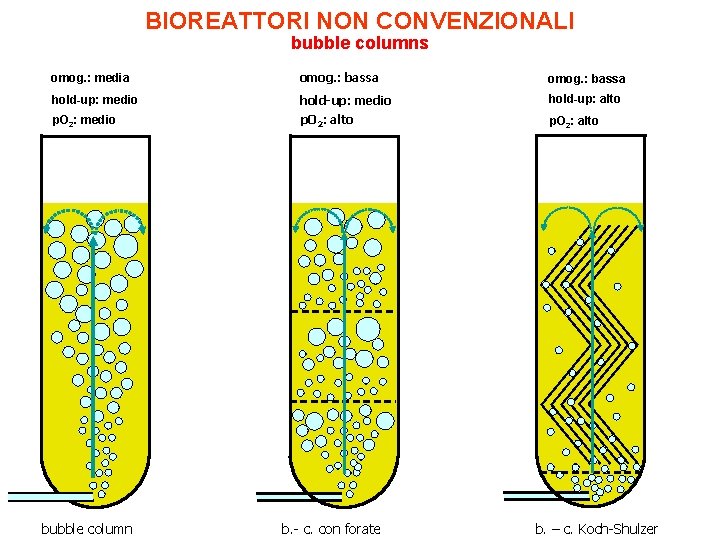
BIOREATTORI NON CONVENZIONALI bubble columns omog. : media omog. : bassa hold-up: medio hold-up: alto p. O 2: medio p. O 2: alto bubble column b. - c. con forate b. – c. Koch-Shulzer
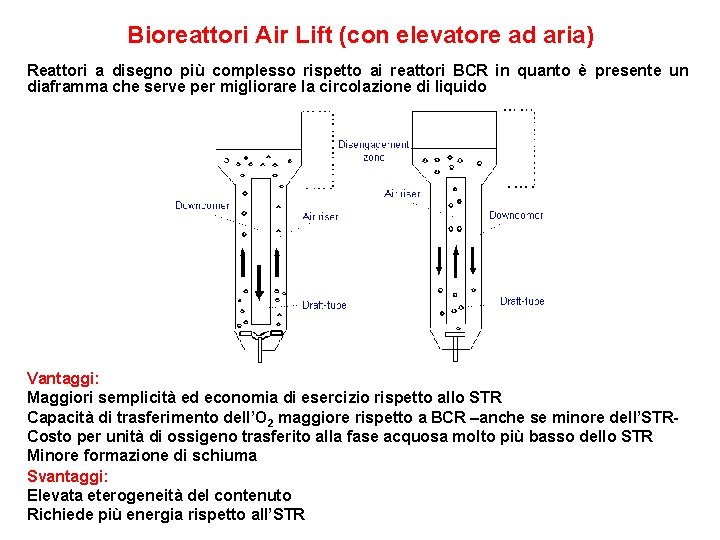
Bioreattori Air Lift (con elevatore ad aria) Reattori a disegno più complesso rispetto ai reattori BCR in quanto è presente un diaframma che serve per migliorare la circolazione di liquido Vantaggi: Maggiori semplicità ed economia di esercizio rispetto allo STR Capacità di trasferimento dell’O 2 maggiore rispetto a BCR –anche se minore dell’STRCosto per unità di ossigeno trasferito alla fase acquosa molto più basso dello STR Minore formazione di schiuma Svantaggi: Elevata eterogeneità del contenuto Richiede più energia rispetto all’STR
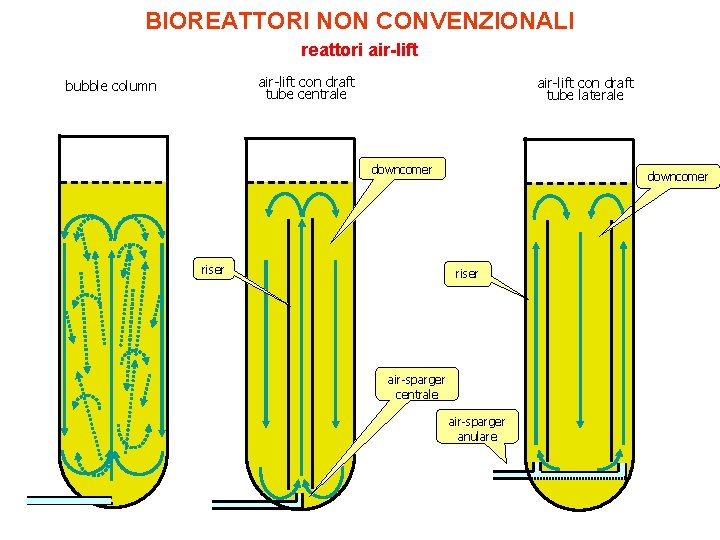
BIOREATTORI NON CONVENZIONALI reattori air-lift con draft tube centrale bubble column air-lift con draft tube laterale downcomer riser air-sparger centrale air-sparger anulare
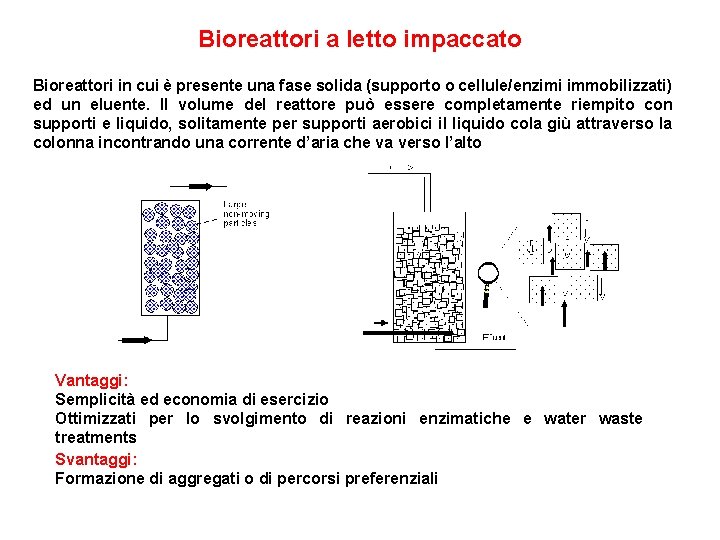
Bioreattori a letto impaccato Bioreattori in cui è presente una fase solida (supporto o cellule/enzimi immobilizzati) ed un eluente. Il volume del reattore può essere completamente riempito con supporti e liquido, solitamente per supporti aerobici il liquido cola giù attraverso la colonna incontrando una corrente d’aria che va verso l’alto Vantaggi: Semplicità ed economia di esercizio Ottimizzati per lo svolgimento di reazioni enzimatiche e water waste treatments Svantaggi: Formazione di aggregati o di percorsi preferenziali
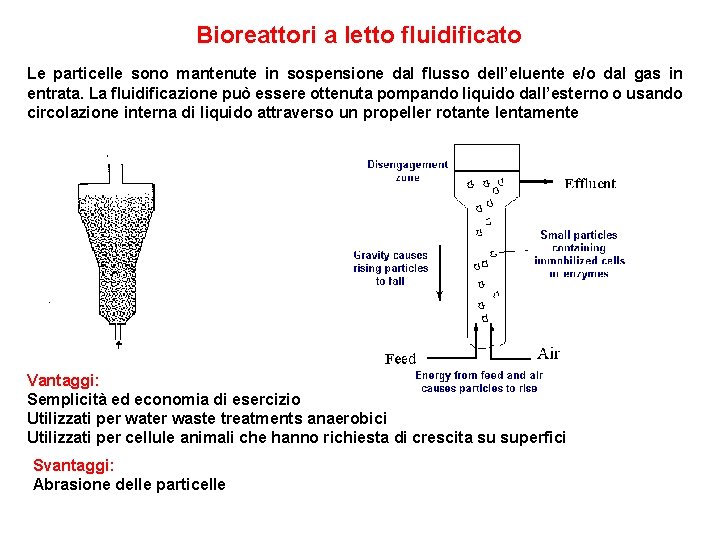
Bioreattori a letto fluidificato Le particelle sono mantenute in sospensione dal flusso dell’eluente e/o dal gas in entrata. La fluidificazione può essere ottenuta pompando liquido dall’esterno o usando circolazione interna di liquido attraverso un propeller rotante lentamente Vantaggi: Semplicità ed economia di esercizio Utilizzati per water waste treatments anaerobici Utilizzati per cellule animali che hanno richiesta di crescita su superfici Svantaggi: Abrasione delle particelle
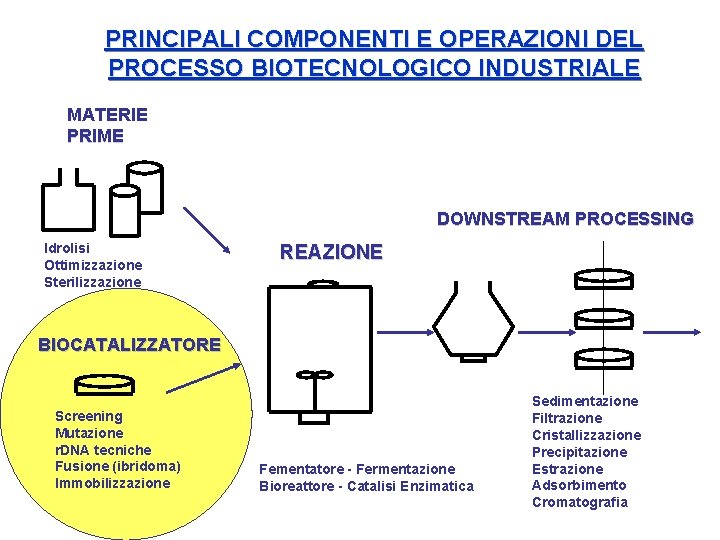
PRINCIPALI COMPONENTI E OPERAZIONI DEL PROCESSO BIOTECNOLOGICO INDUSTRIALE MATERIE PRIME DOWNSTREAM PROCESSING Idrolisi Ottimizzazione Sterilizzazione REAZIONE BIOCATALIZZATORE Screening Mutazione r. DNA tecniche Fusione (ibridoma) Immobilizzazione Fementatore - Fermentazione Bioreattore - Catalisi Enzimatica Sedimentazione Filtrazione Cristallizzazione Precipitazione Estrazione Adsorbimento Cromatografia
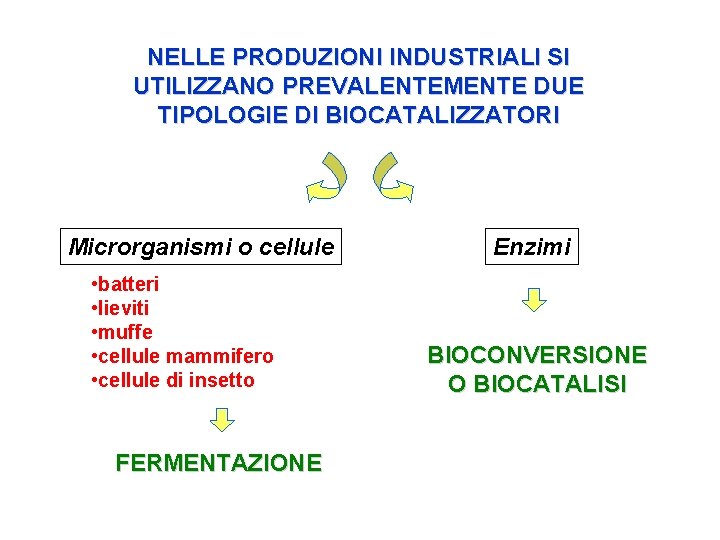
NELLE PRODUZIONI INDUSTRIALI SI UTILIZZANO PREVALENTEMENTE DUE TIPOLOGIE DI BIOCATALIZZATORI Microrganismi o cellule • batteri • lieviti • muffe • cellule mammifero • cellule di insetto FERMENTAZIONE Enzimi BIOCONVERSIONE O BIOCATALISI

FERMENTAZIONE nei processi industriali È un processo produttivo che prevede la crescita dei microrganismi o delle cellule che catalizzano il processo; è un processo autocatalitico. E’ storicamente l’area più importante in biotecnologia. C’è stato un estensivo sviluppo con nuovi prodotti come farmaci, solventi, prodotti alimentari, etc. Questo include anche la ricerca di differenti design di fermentazione per ottimizzare il processo. in biochimica Via metabolica di produzione di energia in cui una sostanza organica è utilizzata come accettore di elettroni in condizioni anaerobiche, in luogo dell’ossigeno.

BIOCONVERSIONE • L’applicazione industriale degli BIOCONVERSIONE o BIOCATALISI • Nuove tecnologie come la “mutagenesi sito-diretta” e il “DNAshuffling” permettono di sviluppare nuovi enzimi fatti su misura per specifiche applicazioni enzimi prende il nome di

I PARAMETRI CHE DETERMINANO LA SCELTA DEL BIOCATALIZZATORE Ø Ø Ø finalità del processo tipologia dell’impianto condizioni sperimentali del processo produttività sostenibilità ambientale Facciamo un esempio….

… Il lavaggio automatico della biancheria! @ finalità del processo Ä Rimozione delle macchie (lipidi, proteine) @ tipologia dell’impianto Ä lavatrice Ä temperatura variabile, tensioattivi, alti @ condizioni sperimentali del processo @ produttività @ sostenibilità ambientale valori di p. H Ä %sporco rimosso/tempo di lavaggio Ä minor uso possibile di detergenti Idrolisi enzimatica delle macchie di sporco! Lipasi e proteasi quali additivi detersivi per il bucato

QUALI PROPRIETA’ DEVONO AVERE QUESTI ENZIMI? 4 termoresistenti 4 funzionare bene ad alto p. H 4 resistenti alla denaturazione da detergenti 4 avere una elevata efficienza catalitica Enzimi estratti da microrganismi estremofili come termoalofili! Ma siamo sicuri che questo bioprocesso non possa essere migliorato?

Il lavaggio efficiente della biancheria a temperatura ambiente! Ä Risparmio di energia per raggiungere alte temperature Ä preserva l’integrità ed i colori degli indumenti Per realizzare questo bioprocesso, gli enzimi da aggiungere devono: 4 4 funzionare bene ad alto p. H resistere alla denaturazione da detergenti 4 avere una elevata efficienza catalitica alle basse temperature! Enzimi estratti da microrganismi psicrofili!
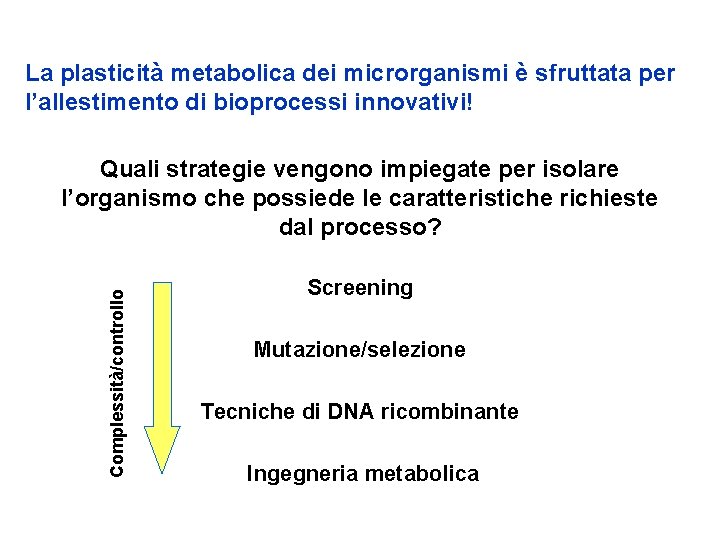
La plasticità metabolica dei microrganismi è sfruttata per l’allestimento di bioprocessi innovativi! Complessità/controllo Quali strategie vengono impiegate per isolare l’organismo che possiede le caratteristiche richieste dal processo? Screening Mutazione/selezione Tecniche di DNA ricombinante Ingegneria metabolica

Screening: opportune strategie di selezione sono richieste (es. produzione di antibiotici) Mutazione/selezione: ciclo costituito da due fasi 1) mutagenesi random (uso mutageni) 2) selezione di individui con proprietà migliori DNA ricombinante: conoscenza della sequenza di gene/i Produzione ricombinante dei prodotti genici o di opportune varianti con proprietà migliori Ingegneria metabolica: miglioramento mirato della formazione di prodotto o delle proprietà cellulari attraverso la modifica di specifiche reazioni biochimiche o l’introduzione di nuove reazioni mediante combinazione multifattoriale di tecniche di analisi metabolica, r-DNA, e bioprocessi fermentativi avanzati Genesi di nuovi organismi con proprietà metaboliche innovative!

Una volta ottenuto, l’organismo che catalizza il bioprocesso deve essere conservato! I metodi di conservazione sono efficaci se: • assicurano la vitalità del biocatalizzatore • assicurano la stabilità genetica del biocatalizzatore I metodi più spesso impiegati sono: • liofilizzazione • criopreservazione tra -20 e -80°C per i batteri -196°C in azoto liquido per cellule eucariotiche In entrambi i casi è essenziale l’uso di crioprotettivi (glicerolo o DMSO) QUESTE METODOLOGIE SONO SPESSO COPERTE DA SEGRETO INDUSTRIALE!
- Slides: 47