Maraviroc antagonista del CCR 5 Inibitore noncompetitivo del
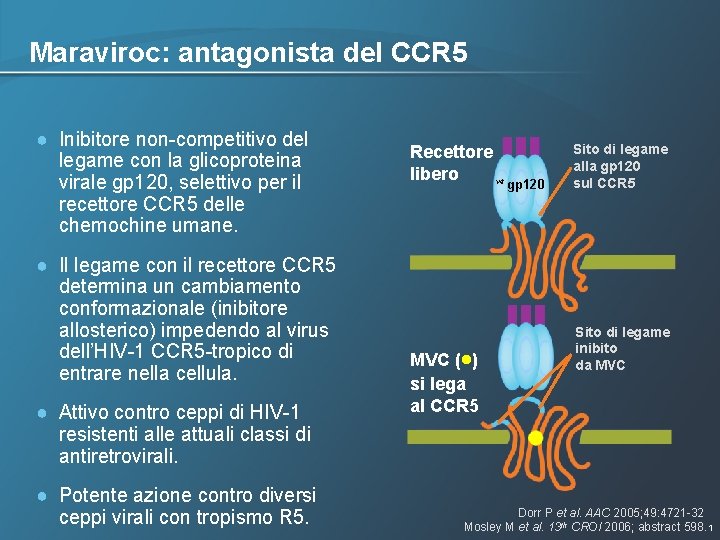
Maraviroc: antagonista del CCR 5 ● Inibitore non-competitivo del legame con la glicoproteina virale gp 120, selettivo per il recettore CCR 5 delle chemochine umane. ● Il legame con il recettore CCR 5 determina un cambiamento conformazionale (inibitore allosterico) impedendo al virus dell’HIV-1 CCR 5 -tropico di entrare nella cellula. ● Attivo contro ceppi di HIV-1 resistenti alle attuali classi di antiretrovirali. ● Potente azione contro diversi ceppi virali con tropismo R 5. Recettore libero wt gp 120 • MVC ( ) si lega al CCR 5 Sito di legame alla gp 120 sul CCR 5 Sito di legame inibito da MVC Dorr P et al. AAC 2005; 49: 4721 -32 Mosley M et al. 13 th CROI 2006; abstract 598. 1

STUDI MOTIVATE 1 e 2: analisi combinata di efficacia dopo 48 settimane 2

MOTIVATE 1 e 2: disegno dello studio OBT* + placebo Randomizzazione 1: 2: 2 MOTIVATE 1 N=601 MOTIVATE 2 N=475 OBT* + MVC (150 mg† QD) OBT* + MVC (150 mg† BID) 4 -6 sett. Periodo di screening 0 24 sett. Analisi ad interim Pazienti stratificati in base all’uso di enfuvirtide e HIV-1 RNA < e ≥ 100. 000 copie/m. L * † 48 sett. Endpoint primario: Variazione della carica virale vs basale OBT = terapia di base ottimizzata con 3 -6 ARV (ritonavir utilizzato come booster non considerato come ARV). I pazienti la cui OBT comprendeva un PI (escluso TPV) e/o delavirdina sono stati trattati con dosi di MVC da 150 mg; tutti gli altri con dosi da 300 mg di MVC. MOTIVATE 1 e 2 Lalezari J, et al. 14 th CROI 2007. Abstract 104 b. LB Nelson M, et al. 14 th CROI 2007. Abstract 104 a. LB 3
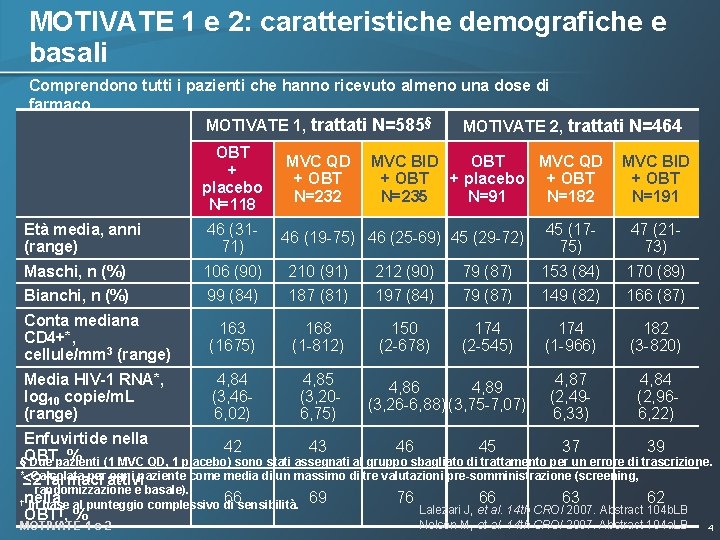
MOTIVATE 1 e 2: caratteristiche demografiche e basali Comprendono tutti i pazienti che hanno ricevuto almeno una dose di farmaco MOTIVATE 1, trattati N=585§ MOTIVATE 2, trattati N=464 OBT + placebo N=118 Età media, anni (range) 46 (3171) Maschi, n (%) 106 (90) Bianchi, n (%) MVC QD + OBT N=232 MVC QD MVC BID OBT + placebo + OBT N=182 N=235 N=91 MVC BID + OBT N=191 46 (19 -75) 46 (25 -69) 45 (29 -72) 45 (1775) 47 (2173) 210 (91) 212 (90) 79 (87) 153 (84) 170 (89) 99 (84) 187 (81) 197 (84) 79 (87) 149 (82) 166 (87) Conta mediana CD 4+*, cellule/mm 3 (range) 163 (1675) 168 (1 -812) 150 (2 -678) 174 (2 -545) 174 (1 -966) 182 (3 -820) Media HIV-1 RNA*, log 10 copie/m. L (range) 4, 84 (3, 466, 02) 4, 85 (3, 206, 75) 4, 87 (2, 496, 33) 4, 84 (2, 966, 22) 4, 86 4, 89 (3, 26 -6, 88) (3, 75 -7, 07) Enfuvirtide nella 46 45 42 43 37 39 % (1 MVC QD, 1 placebo) sono stati assegnati al gruppo sbagliato di trattamento per un errore di trascrizione. §OBT, Due pazienti *≤ 2 Calcolata per attivi ogni paziente come media di un massimo di tre valutazioni pre-somministrazione (screening, farmaci randomizzazione e basale). 76 66 66 69 63 62 †nella In base al punteggio complessivo di sensibilità. Lalezari J, et al. 14 th CROI 2007. Abstract 104 b. LB OBT†, % MOTIVATE 1 e 2 Nelson M, et al. 14 th CROI 2007. Abstract 104 a. LB 4
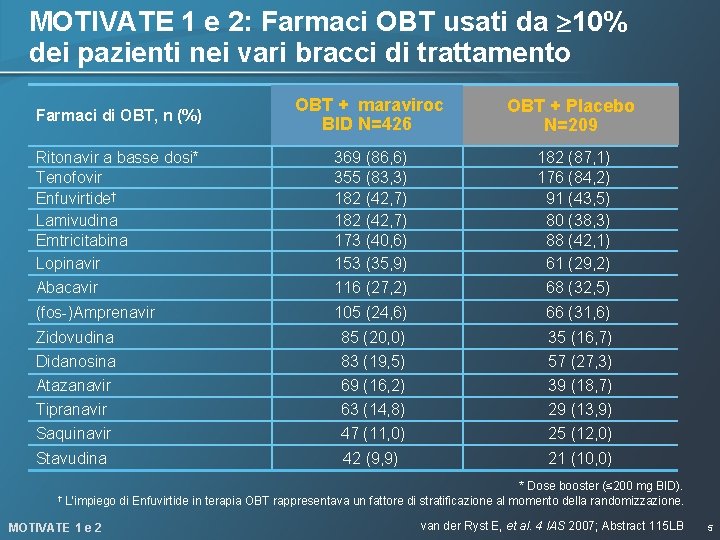
MOTIVATE 1 e 2: Farmaci OBT usati da 10% dei pazienti nei vari bracci di trattamento Farmaci di OBT, n (%) OBT + maraviroc BID N=426 OBT + Placebo N=209 Ritonavir a basse dosi* Tenofovir Enfuvirtide† Lamivudina Emtricitabina Lopinavir 369 (86, 6) 355 (83, 3) 182 (42, 7) 173 (40, 6) 153 (35, 9) 182 (87, 1) 176 (84, 2) 91 (43, 5) 80 (38, 3) 88 (42, 1) 61 (29, 2) Abacavir 116 (27, 2) 68 (32, 5) (fos-)Amprenavir 105 (24, 6) 66 (31, 6) Zidovudina 85 (20, 0) 35 (16, 7) Didanosina 83 (19, 5) 57 (27, 3) Atazanavir Tipranavir 69 (16, 2) 63 (14, 8) 39 (18, 7) 29 (13, 9) Saquinavir 47 (11, 0) 25 (12, 0) Stavudina 42 (9, 9) 21 (10, 0) † L’impiego MOTIVATE 1 e 2 * Dose booster (≤ 200 mg BID). di Enfuvirtide in terapia OBT rappresentava un fattore di stratificazione al momento della randomizzazione. van der Ryst E, et al. 4 IAS 2007; Abstract 115 LB 5
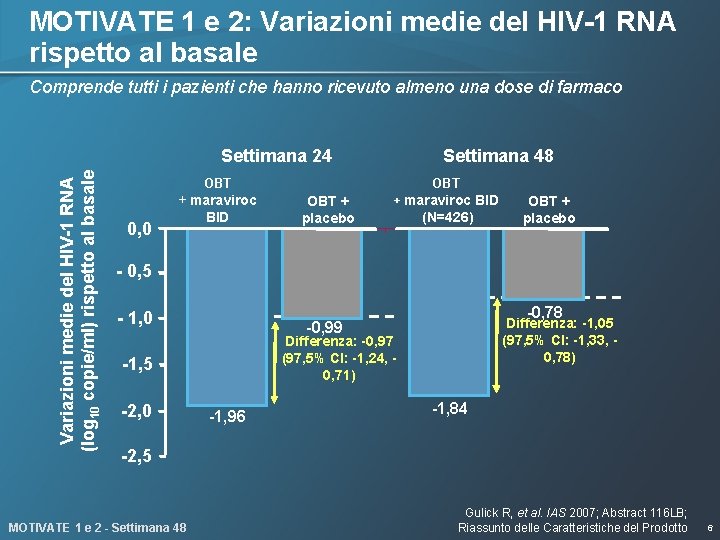
MOTIVATE 1 e 2: Variazioni medie del HIV-1 RNA rispetto al basale Comprende tutti i pazienti che hanno ricevuto almeno una dose di farmaco Variazioni medie del HIV-1 RNA (log 10 copie/ml) rispetto al basale Settimana 24 Settimana 48 OBT + maraviroc 0, 0 BID (N=426) OBT + placebo (N=209) + maraviroc BID (N=426) OBT + placebo (N=209) - 0, 5 - 1, 0 -0, 99 Differenza: -0, 97 (97, 5% CI: -1, 24, 0, 71) -1, 5 -2, 0 -0, 78 Differenza: -1, 05 (97, 5% CI: -1, 33, 0, 78) -1, 96 -1, 84 -2, 5 MOTIVATE 1 e 2 - Settimana 48 Gulick R, et al. IAS 2007; Abstract 116 LB; Riassunto delle Caratteristiche del Prodotto 6
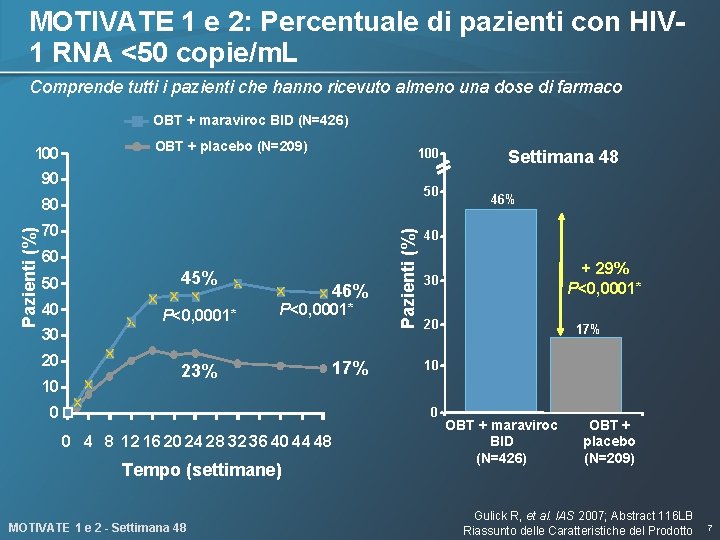
MOTIVATE 1 e 2: Percentuale di pazienti con HIV 1 RNA <50 copie/m. L Comprende tutti i pazienti che hanno ricevuto almeno una dose di farmaco OBT + maraviroc BID (N=426) 100 OBT + placebo (N=209) 100 90 50 70 60 50 45% 40 P<0, 0001* 46% P<0, 0001* 30 20 10 23% 17% 0 Pazienti (%) 80 Tempo (settimane) MOTIVATE 1 e 2 - Settimana 48 46% 40 + 29% P<0, 0001* 30 20 17% 10 0 0 4 8 12 16 20 24 28 32 36 40 44 48 Settimana 48 OBT + maraviroc BID (N=426) OBT + placebo (N=209) Gulick R, et al. IAS 2007; Abstract 116 LB Riassunto delle Caratteristiche del Prodotto 7
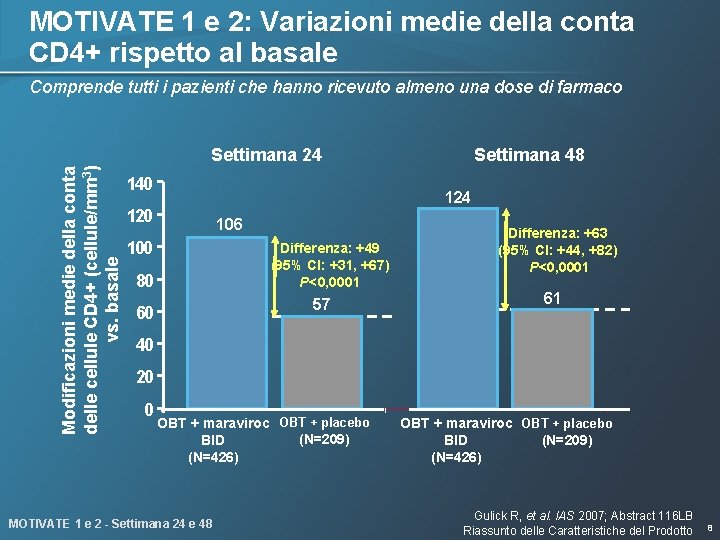
MOTIVATE 1 e 2: Variazioni medie della conta CD 4+ rispetto al basale Comprende tutti i pazienti che hanno ricevuto almeno una dose di farmaco Modificazioni medie della conta delle cellule CD 4+ (cellule/mm 3) vs. basale Settimana 24 140 Settimana 48 124 120 106 100 Differenza: +49 (95% CI: +31, +67) P<0, 0001 80 57 60 Differenza: +63 (95% CI: +44, +82) P<0, 0001 61 40 20 0 OBT + maraviroc OBT + placebo (N=209) BID (N=426) MOTIVATE 1 e 2 - Settimana 24 e 48 OBT + maraviroc OBT + placebo BID (N=209) (N=426) Gulick R, et al. IAS 2007; Abstract 116 LB Riassunto delle Caratteristiche del Prodotto 8

STUDI MOTIVATE 1 e 2: analisi combinata di efficacia dopo 24 settimane per sottogruppi 9
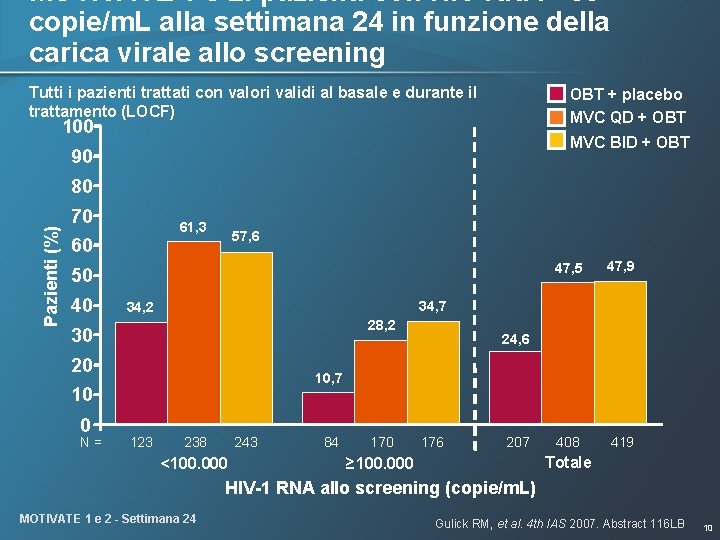
MOTIVATE 1 e 2: pazienti con HIV RNA <50 copie/m. L alla settimana 24 in funzione della carica virale allo screening Tutti i pazienti trattati con valori validi al basale e durante il trattamento (LOCF) OBT + placebo MVC QD + OBT 100 MVC BID + OBT 90 Pazienti (%) 80 70 61, 3 57, 6 60 50 40 28, 2 20 408 419 24, 6 10, 7 10 N= 47, 9 34, 7 34, 2 30 0 47, 5 123 238 243 <100. 000 84 170 176 207 Totale ≥ 100. 000 HIV-1 RNA allo screening (copie/m. L) MOTIVATE 1 e 2 - Settimana 24 Gulick RM, et al. 4 th IAS 2007. Abstract 116 LB 10
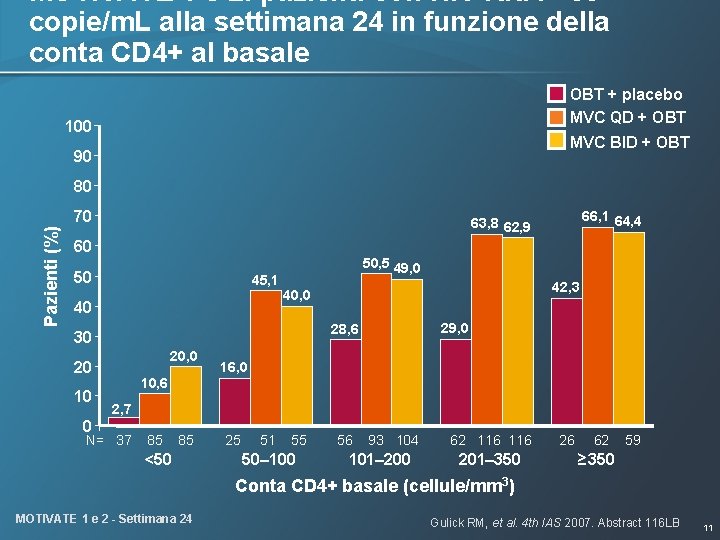
MOTIVATE 1 e 2: pazienti con HIV RNA <50 copie/m. L alla settimana 24 in funzione della conta CD 4+ al basale OBT + placebo MVC QD + OBT 100 MVC BID + OBT 90 80 Pazienti (%) 70 66, 1 64, 4 63, 8 62, 9 60 50 45, 1 40 50, 5 49, 0 20 0 29, 0 28, 6 30 10 42, 3 40, 0 16, 0 10, 6 2, 7 N= 37 85 85 <50 25 51 55 50– 100 56 93 104 101– 200 62 116 201– 350 26 62 59 ≥ 350 Conta CD 4+ basale (cellule/mm 3) MOTIVATE 1 e 2 - Settimana 24 Gulick RM, et al. 4 th IAS 2007. Abstract 116 LB 11
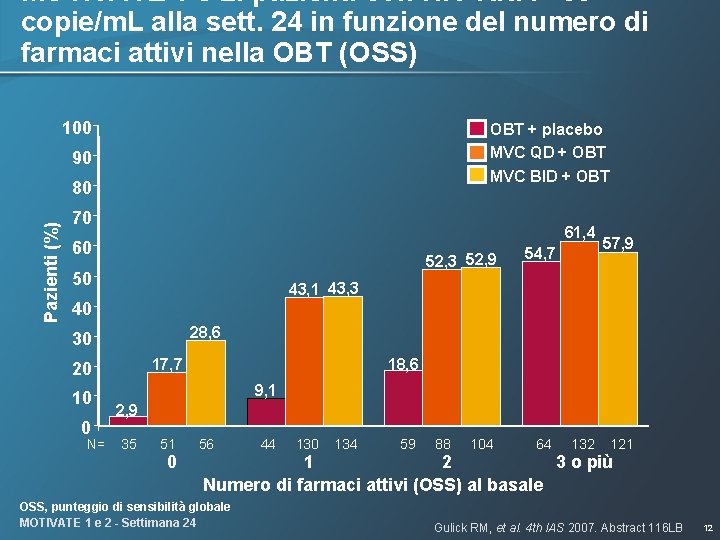
MOTIVATE 1 e 2: pazienti con HIV RNA <50 copie/m. L alla sett. 24 in funzione del numero di farmaci attivi nella OBT (OSS) 100 OBT + placebo MVC QD + OBT 90 MVC BID + OBT Pazienti (%) 80 70 61, 4 60 52, 3 52, 9 50 54, 7 57, 9 43, 1 43, 3 40 28, 6 30 10 0 N= 18, 6 17, 7 20 9, 1 2, 9 35 51 0 56 44 130 134 59 88 104 64 132 121 1 2 3 o più Numero di farmaci attivi (OSS) al basale OSS, punteggio di sensibilità globale MOTIVATE 1 e 2 - Settimana 24 Gulick RM, et al. 4 th IAS 2007. Abstract 116 LB 12

STUDI MOTIVATE 1 e 2: Analisi combinata di tollerabilità dopo 48 settimane
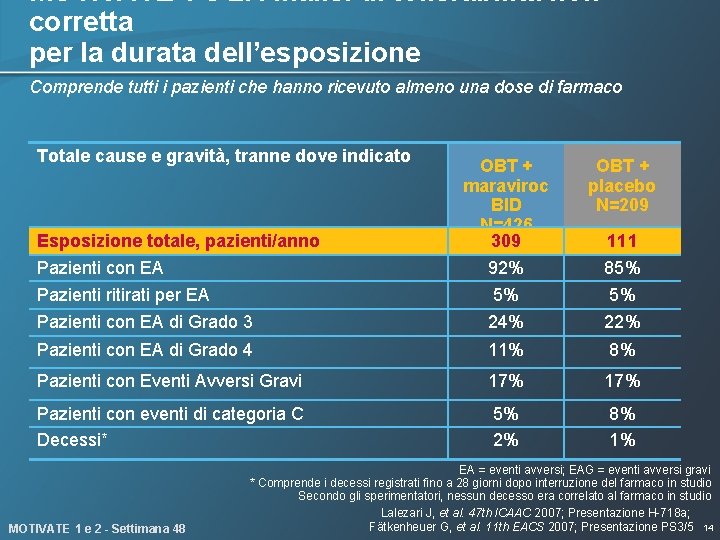
MOTIVATE 1 e 2: Analisi di tollerabilità non corretta per la durata dell’esposizione Comprende tutti i pazienti che hanno ricevuto almeno una dose di farmaco Totale cause e gravità, tranne dove indicato OBT + maraviroc BID N=426 309 OBT + placebo N=209 Pazienti con EA Pazienti ritirati per EA 92% 5% 85% 5% Pazienti con EA di Grado 3 24% 22% Pazienti con EA di Grado 4 11% 8% Pazienti con Eventi Avversi Gravi 17% Pazienti con eventi di categoria C Decessi* 5% 2% 8% 1% Esposizione totale, pazienti/anno MOTIVATE 1 e 2 - Settimana 48 111 EA = eventi avversi; EAG = eventi avversi gravi * Comprende i decessi registrati fino a 28 giorni dopo interruzione del farmaco in studio Secondo gli sperimentatori, nessun decesso era correlato al farmaco in studio Lalezari J, et al. 47 th ICAAC 2007; Presentazione H-718 a; Fätkenheuer G, et al. 11 th EACS 2007; Presentazione PS 3/5 14
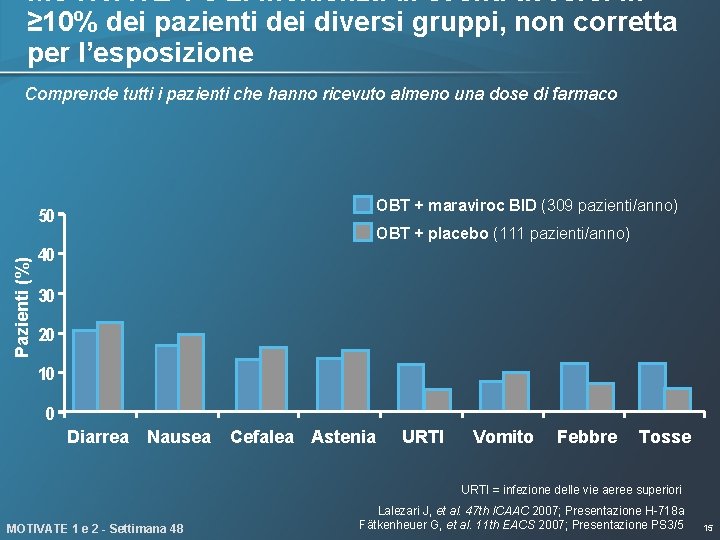
MOTIVATE 1 e 2: incidenza di eventi avversi in ≥ 10% dei pazienti dei diversi gruppi, non corretta per l’esposizione Comprende tutti i pazienti che hanno ricevuto almeno una dose di farmaco OBT + maraviroc BID (309 pazienti/anno) Pazienti (%) 50 OBT + placebo (111 pazienti/anno) 40 30 20 10 0 Diarrea Nausea Cefalea Astenia URTI Vomito Febbre Tosse URTI = infezione delle vie aeree superiori MOTIVATE 1 e 2 - Settimana 48 Lalezari J, et al. 47 th ICAAC 2007; Presentazione H-718 a Fätkenheuer G, et al. 11 th EACS 2007; Presentazione PS 3/5 15
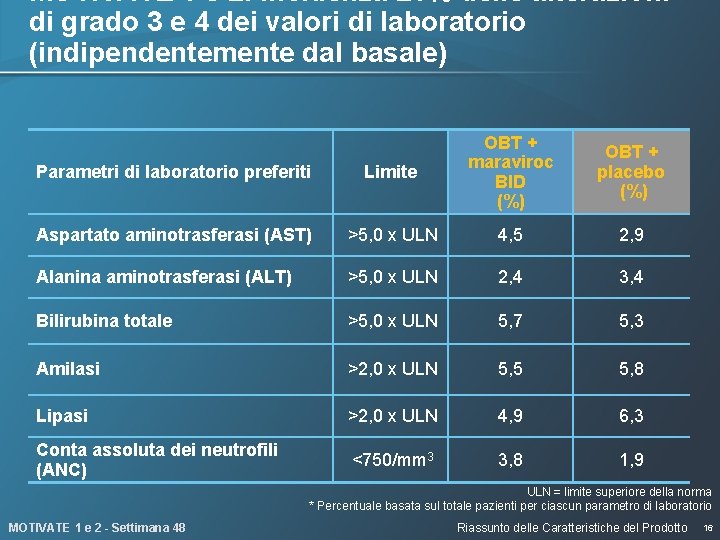
MOTIVATE 1 e 2: incidenza ≥ 1% delle alterazioni di grado 3 e 4 dei valori di laboratorio (indipendentemente dal basale) Parametri di laboratorio preferiti Limite OBT + maraviroc BID (%) Aspartato aminotrasferasi (AST) >5, 0 x ULN 4, 5 2, 9 Alanina aminotrasferasi (ALT) >5, 0 x ULN 2, 4 3, 4 Bilirubina totale >5, 0 x ULN 5, 7 5, 3 Amilasi >2, 0 x ULN 5, 5 5, 8 Lipasi >2, 0 x ULN 4, 9 6, 3 Conta assoluta dei neutrofili (ANC) <750/mm 3 3, 8 1, 9 OBT + placebo (%) ULN = limite superiore della norma * Percentuale basata sul totale pazienti per ciascun parametro di laboratorio MOTIVATE 1 e 2 - Settimana 48 Riassunto delle Caratteristiche del Prodotto 16
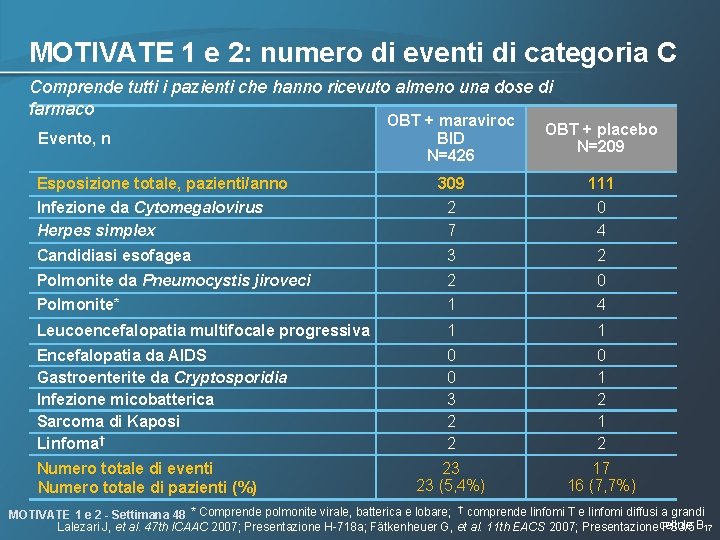
MOTIVATE 1 e 2: numero di eventi di categoria C Comprende tutti i pazienti che hanno ricevuto almeno una dose di farmaco OBT + maraviroc BID N=426 OBT + placebo N=209 309 2 7 111 0 4 Candidiasi esofagea 3 2 Polmonite da Pneumocystis jiroveci 2 0 Polmonite* 1 4 Leucoencefalopatia multifocale progressiva 1 1 Encefalopatia da AIDS Gastroenterite da Cryptosporidia Infezione micobatterica Sarcoma di Kaposi Linfoma† 0 0 3 2 2 0 1 2 23 23 (5, 4%) 17 16 (7, 7%) Evento, n Esposizione totale, pazienti/anno Infezione da Cytomegalovirus Herpes simplex Numero totale di eventi Numero totale di pazienti (%) † MOTIVATE 1 e 2 - Settimana 48 * Comprende polmonite virale, batterica e lobare; comprende linfomi T e linfomi diffusi a grandi Lalezari J, et al. 47 th ICAAC 2007; Presentazione H-718 a; Fätkenheuer G, et al. 11 th EACS 2007; Presentazionecellule PS 3/5 B 17

MOTIVATE 1 e 2: sintesi dei risultati aggregati a 48 settimane ● I dati di efficacia nei pazienti trattati con maraviroc BID + OBT alla 48 a settimana confermano quanto già dimostrato a 24 settimane. ● Il profilo di tollerabilità alla 48 a settimana è risultato simile a quello rilevato alla 24 a settimana. ● Questi risultati dimostrano che il trattamento con maraviroc + OBT garantisce una prolungata efficacia e tollerabilità nei pazienti “experienced”. Lalezari J, et al. 47 th ICAAC 2007; Presentazione H-718 a Fätkenheuer G, et al. 11 th EACS 2007; Presentazione PS 3/5 18

Impatto della terapia con maraviroc sul tropismo di HIV
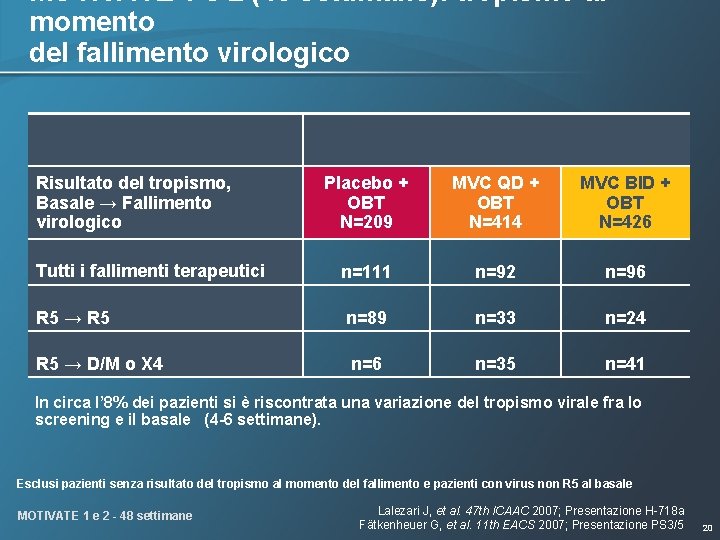
MOTIVATE 1 e 2 (48 settimane): tropismo al momento del fallimento virologico Risultato del tropismo, Basale → Fallimento virologico Placebo + OBT N=209 MVC QD + OBT N=414 MVC BID + OBT N=426 Tutti i fallimenti terapeutici n=111 n=92 n=96 R 5 → R 5 n=89 n=33 n=24 R 5 → D/M o X 4 n=6 n=35 n=41 In circa l’ 8% dei pazienti si è riscontrata una variazione del tropismo virale fra lo screening e il basale (4 -6 settimane). Esclusi pazienti senza risultato del tropismo al momento del fallimento e pazienti con virus non R 5 al basale MOTIVATE 1 e 2 - 48 settimane Lalezari J, et al. 47 th ICAAC 2007; Presentazione H-718 a Fätkenheuer G, et al. 11 th EACS 2007; Presentazione PS 3/5 20
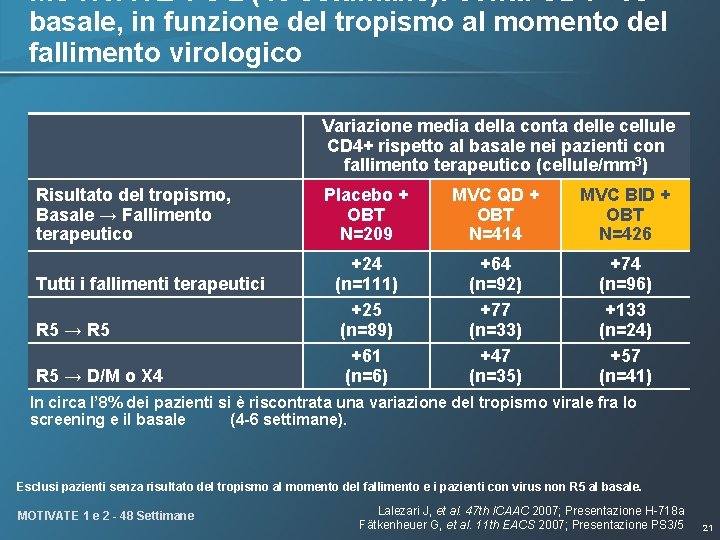
MOTIVATE 1 e 2 (48 settimane): conta CD 4+ vs basale, in funzione del tropismo al momento del fallimento virologico Variazione media della conta delle cellule CD 4+ rispetto al basale nei pazienti con fallimento terapeutico (cellule/mm 3) Risultato del tropismo, Basale → Fallimento terapeutico Tutti i fallimenti terapeutici R 5 → D/M o X 4 Placebo + OBT N=209 MVC QD + OBT N=414 MVC BID + OBT N=426 +24 (n=111) +25 (n=89) +61 (n=6) +64 (n=92) +77 (n=33) +47 (n=35) +74 (n=96) +133 (n=24) +57 (n=41) In circa l’ 8% dei pazienti si è riscontrata una variazione del tropismo virale fra lo screening e il basale (4 -6 settimane). Esclusi pazienti senza risultato del tropismo al momento del fallimento e i pazienti con virus non R 5 al basale. MOTIVATE 1 e 2 - 48 Settimane Lalezari J, et al. 47 th ICAAC 2007; Presentazione H-718 a Fätkenheuer G, et al. 11 th EACS 2007; Presentazione PS 3/5 21

MOTIVATE 1 e 2: quale tropismo dopo la sospensione del trattamento? Valutazione del tropismo virale all’ultima visita di osservazione, dopo la sospensione del trattamento, nei pazienti che avevano un tropismo D/M o X 4 al fallimento Virus con tropismo D/M o Virus con tropismo R 5 X 4 all’ultima visita di follow. Trattamen follow-up up N to N di Giorni pazienti (mediana) OBT + 4 14 16 30 203 § Il 68% (30/44) MVC 4 dei pazienti trattati con maraviroc e in cui, al fallimento, era stato documentato un virus con tropismo D/M o X 4, sono ritornati ad avere un tropismo R 5, dopo la sospensione OBTdella + terapia 3(tempo mediano: 2 1 20 203 giorni). 22 Placebo § Il tempo mediano dell’ultima visita di osservazione, per pazienti ai quali era stato sospeso il trattamento e che avevano ancora un virus con tropismo D/M o X 4 era più breve: 16 giorni. § Se si considerano i pazienti con un follow-up, dopo la sospensione del trattamento, >1 mese: 30/31 pazienti, il cui tropismo era D/M o X 4 al momento del fallimento, sono ritornati ad essere R 5. MOTIVATE 1 e 2 Van der Ryst E, et al. 47 ICAAC 2007; 22
- Slides: 22