Mangelernhrung Ein verborgenes Risiko rechtzeitiges Handeln und Erkennen

„Mangelernährung – Ein verborgenes Risiko – rechtzeitiges Handeln und Erkennen“ Claudia Hoppe, Dipl. Oecotrophologin

1. Teil: Assessment bei Mangelernährung in der Praxis 2. Teil: Fallvorstellung mangelernährter Patienten unterschiedlicher Altersgruppen 23. 01. 2022

Service – die Therapiebereiche Geschultes Fachpersonal und Experten in allen Therapiebereichen:

Geschichte der klinischen Ernährung 23. 01. 2022

Parenterale Ernährung • Bedeutet Verabreichung von Nährstoffen direkt in das Blut • über großkalibrige Katheter, meist mit Zugang in zentrale Vene • Hintergrund: rektale Gabe von Nährstoffen führte zu einer unzureichenden Ernährung. Deshalb beschäftigten sich Wissenschaftler frühzeitig mit der Möglichkeit der parenteralen Ernährung. • war lange Zeit erfolglos (Hygiene, falsche Nährstoffzusammensetzung) • 1926: erste industriell hergestellte Infusionslösung (Tutofusin: E-lyte) • 1937: Erste Infusion von Aminosäurelösungen • 1961: erste verwertbare und sichere Fettemulsion für den klinischen Gebrauch • 1970: erstmalig ambulante parenterale Ernährungstherapie

Was sehen Sie? Albrecht Dürer: Porträt seiner Mutter (14. Jahrhundert) • Extremer Schwund des subkutanen Fettgewebes • Atrophie der Kau- und Gesichtsmuskulatur. • Typische Zeichen einer Eiweißkatabolie 23. 01. 2022
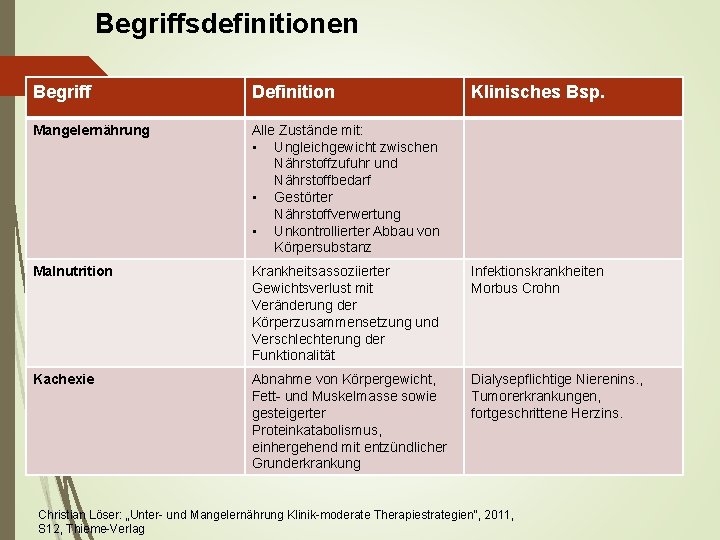
Begriffsdefinitionen Begriff Definition Klinisches Bsp. Mangelernährung Alle Zustände mit: • Ungleichgewicht zwischen Nährstoffzufuhr und Nährstoffbedarf • Gestörter Nährstoffverwertung • Unkontrollierter Abbau von Körpersubstanz Malnutrition Krankheitsassoziierter Gewichtsverlust mit Veränderung der Körperzusammensetzung und Verschlechterung der Funktionalität Infektionskrankheiten Morbus Crohn Kachexie Abnahme von Körpergewicht, Fett- und Muskelmasse sowie gesteigerter Proteinkatabolismus, einhergehend mit entzündlicher Grunderkrankung Dialysepflichtige Nierenins. , Tumorerkrankungen, fortgeschrittene Herzins. Christian Löser: „Unter- und Mangelernährung Klinik-moderate Therapiestrategien“, 2011, S 12, Thieme-Verlag

Was ist Kachexie?

Kachexie? • Im Prinzip nur Beschreibung eines Zustandes • Kommt aus dem griechischen • „Kaktos“ = schlecht • „hexis“ = Zustand

Kachexie? Was sagen die Ärzte? • Bekannter Ausdruck • Unvermeidlich bei malignen Tumoren • Gehört dazu • Es ist eben so • Hat jeder Tumorpatient im Endstadium? • Gewicht verliert jeder Patient mit einer malignen Erkrankung

Erkrankungen mit Kachexie • • AIDS Chronische Lungenerkrankungen Chronische Herzerkrankungen Rheumatoide Arthritis Chronische Infektionen Morbus Crohn Tumorkachexie Bachmann et al. , J Gastrointest Surg 2008
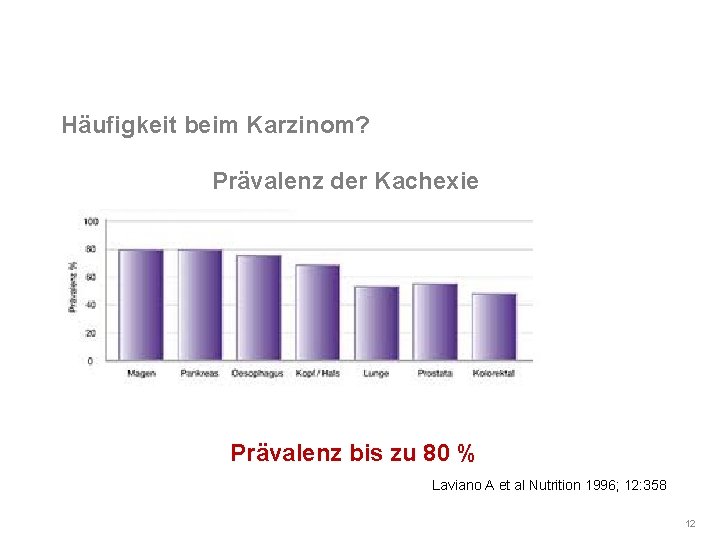
Häufigkeit beim Karzinom? Prävalenz der Kachexie Prävalenz bis zu 80 % Laviano A et al Nutrition 1996; 12: 358 12

? s o l t a Ä r n e u Gewichtsverlust = ? a h c s e t z r
Kachexie = Kachexie? ? Mangelernährung Kachexie

Definition der Kachexie? 2008 15

Definition der Kachexie? 2008 In der Klinik schwer anzubringen! 16

Definition der Kachexie? 2011 Fearon et al. Lancet Oncology 2011 17

Definition der Kachexie? 2011 Fearon et al. Lancet Oncology 2011 18

Definition der Kachexie… 2014 Das letzte Wort ist noch nicht gesprochen…. . Klinisch: • ungewollter Gewichtsverlust von mehr als 5 % des KG • BMI < 20 und Gewichtsverlust von mehr als 2 % • Muskel-Index vereinbar mit Sarkopenia ( männlich < 7, 2 kg/m 2 und weiblich< 4, 5 kg/m 2 + Gewichtsverlust > 2 % 40 % bei Patienten in einem frühen Tumorstadium (Bachmann et al 2008) 80 % beim Versterben der Patienten beteiligt (de. Wys et al 1980)

Mangelernährung in deutschen Kliniken Mangelernährung ist auch in Industrieländern wie Deutschland ein Problem, das vor allem kranke und alte Menschen betrifft. In einer deutscher Studie Pirlich et al. 2006 wurden 1886 Patienten eingeschlossen. Jeder zweite geriatrische Patient sowie jeder dritte onkologische oder gastroenterlogische Patient war bei der Klinikeinweisung schon mangelernährt. Textquelle: Pirlich et al. : The German Hospital Malnutrition Study, Clinical Nutrition (2006), 25, 563 -572

50 % der Tumorpatienten haben bereits zum Zeitpunkt der Diagnosestellung einen ungewollten Gewichtsverlust von 10 – 16 % des üblichen Gewichtes. Mehr als 45 % aller onkologischen Patienten verlieren beim stationären Aufenthalt mehr als 10 % des Ausgangsgewichts. (Albrecht 1996, De Wys 1980, Jungi 199, Müller 1991, Selberg 1992, Toomey 1995)

Mangelernährung in unseren Krankenhäusern …… Ist das ein Problem? ? ? Ja 23. 01. 2022
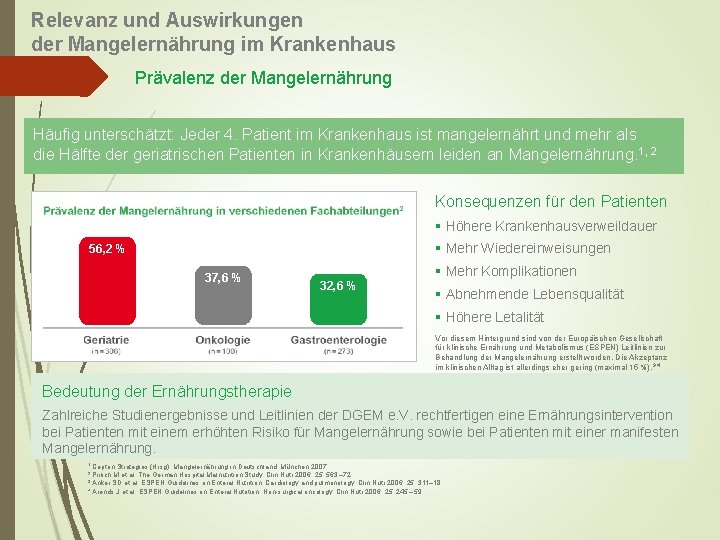
Relevanz und Auswirkungen der Mangelernährung im Krankenhaus Prävalenz der Mangelernährung Häufig unterschätzt: Jeder 4. Patient im Krankenhaus ist mangelernährt und mehr als die Hälfte der geriatrischen Patienten in Krankenhäusern leiden an Mangelernährung. 1, 2 Konsequenzen für den Patienten § Höhere Krankenhausverweildauer § Mehr Wiedereinweisungen 56, 2 % 37, 6 % 32, 6 % § Mehr Komplikationen § Abnehmende Lebensqualität § Höhere Letalität Vor diesem Hintergrund sind von der Europäischen Gesellschaft für klinische Ernährung und Metabolismus (ESPEN) Leitlinien zur Behandlung der Mangelernährung erstellt worden. Die Akzeptanz im klinischen Alltag ist allerdings eher gering (maximal 15 %). 3, 4 Bedeutung der Ernährungstherapie Zahlreiche Studienergebnisse und Leitlinien der DGEM e. V. rechtfertigen eine Ernährungsintervention bei Patienten mit einem erhöhten Risiko für Mangelernährung sowie bei Patienten mit einer manifesten Mangelernährung. Cepton Strategies (Hrsg): Mangelernährung in Deutschland, München 2007 Pirlich M et al. The German Hospital Malnutrition Study. Clin Nutr 2006, 25: 563 – 72 Anker SD et al. ESPEN Guidelines on Enteral Nutrition: Cardiology and pulmonology. Clin Nutr 2006, 25: 311– 18 4 Arends J et al. ESPEN Guidelines on Enteral Nutrition: Non-surgical oncology. Clin Nutr 2006, 25: 245 – 59. 1 2 3

Relevanz und Auswirkungen der Mangelernährung im Krankenhaus Ökonomische Auswirkungen der Mangelernährung Häufigere und längere stationäre Aufenthalte sind die Folgen des verzögerten Behandlungserfolges bei mangelernährten Patienten. Die Verweildauer liegt im Mittel um 4, 5 Tage höher als bei Patienten mit gutem Ernährungszustand. 1 SGAA* SGAB** * Adäquat ernährte Patienten (Subjective Global Assessment A); ** Mäßige Mangelernährung (Subjective Global Assessment B) 1 Cepton Strategies (Hrsg): Mangelernährung in Deutschland, München 2007
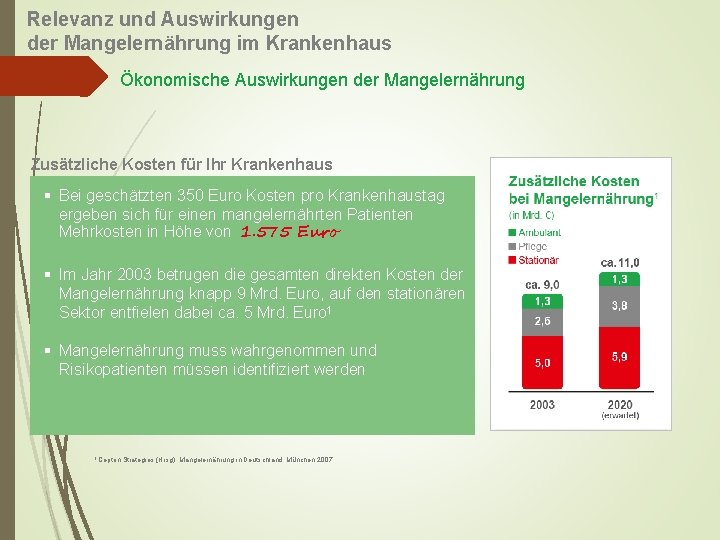
Relevanz und Auswirkungen der Mangelernährung im Krankenhaus Ökonomische Auswirkungen der Mangelernährung Zusätzliche Kosten für Ihr Krankenhaus § Bei geschätzten 350 Euro Kosten pro Krankenhaustag ergeben sich für einen mangelernährten Patienten Mehrkosten in Höhe von 1. 575 Euro § Im Jahr 2003 betrugen die gesamten direkten Kosten der Mangelernährung knapp 9 Mrd. Euro, auf den stationären Sektor entfielen dabei ca. 5 Mrd. Euro 1 § Mangelernährung muss wahrgenommen und Risikopatienten müssen identifiziert werden 1 Cepton Strategies (Hrsg): Mangelernährung in Deutschland, München 2007
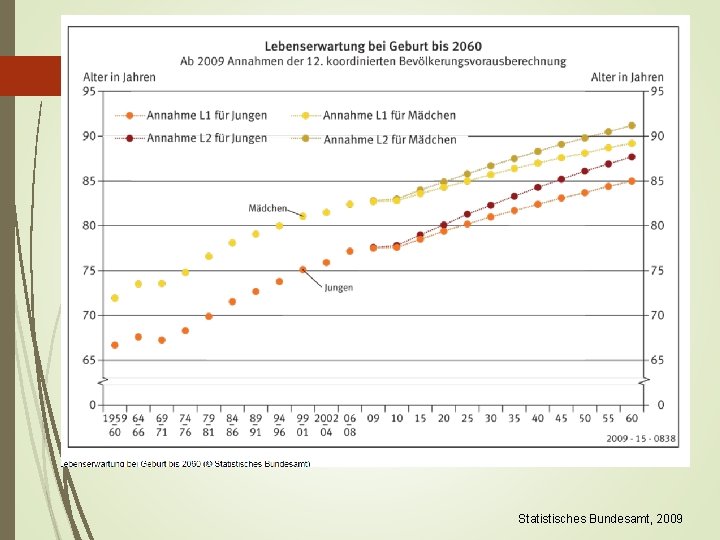
Statistisches Bundesamt, 2009
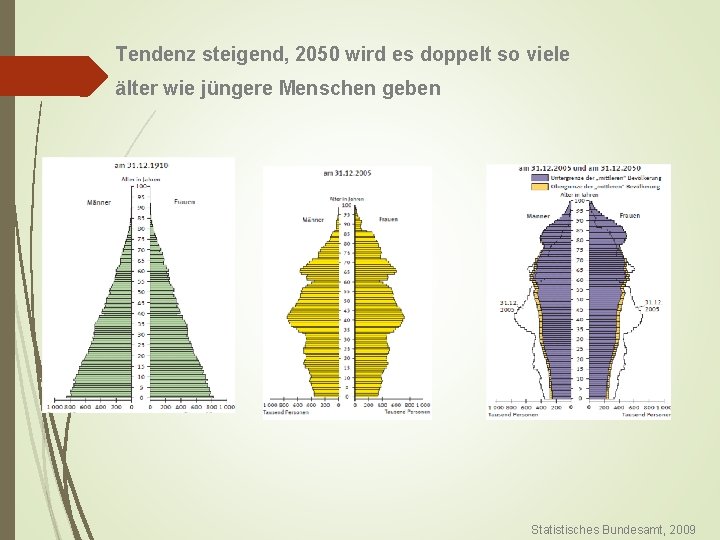
Tendenz steigend, 2050 wird es doppelt so viele älter wie jüngere Menschen geben Statistisches Bundesamt, 2009

Diagnostik Da verschiedene Aspekte des Ernährungszustandes durch verschiedene Methoden erfasst und abgebildet werden, gibt es kein international anerkanntes Standardverfahren („golden standard“) zur Erfassung des Ernährungszustandes.
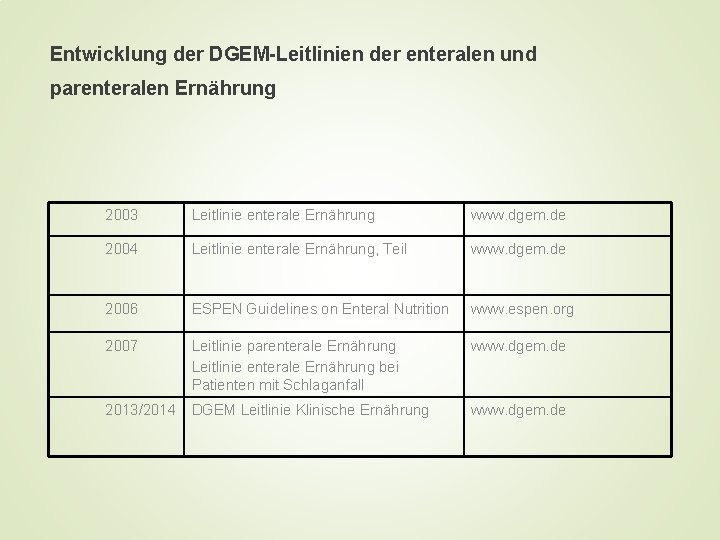
Entwicklung der DGEM-Leitlinien der enteralen und parenteralen Ernährung 2003 Leitlinie enterale Ernährung www. dgem. de 2004 Leitlinie enterale Ernährung, Teil www. dgem. de 2006 ESPEN Guidelines on Enteral Nutrition www. espen. org 2007 Leitlinie parenterale Ernährung Leitlinie enterale Ernährung bei Patienten mit Schlaganfall www. dgem. de 2013/2014 DGEM Leitlinie Klinische Ernährung www. dgem. de

Fragebögen zur Diagnostik einer Mangelernährung Scores erfassen die Zeichen einer Mangelernährung wie einen unbeabsichtigten Gewichtsverlust und den BMI (Body-Mass-Index) sowie Risikofaktoren wie verringerte Nahrungsaufnahme und Krankheitsaktivität. NRS 2002 Nutritional Risk Screening 2002: BMI, Gewichtsverlust, Nahrungszufuhr, Krankheitsschwere Punktegewichtung von Ernährungszustand und Krankheitsschwere MUST Mangelernährung Universal Screening Tool BMI, Gewichtsverlust, Nahrungskarenz SGA Subjective Global Assessment Gewichtsverlauf, Nahrungsaufnahme, gastrointestinale Symptome, Einschätzung der Leistungsfähigkeit, Auswirkungen der Erkrankung auf den Nährstoffbedarf Körperliche Untersuchung Subjektive Einschätzung des Ernährungszustandes 23. 01. 2022

Erfassung der Mangelernährung Screening nach NRS 20021 Initiales Screening Ja Nein Ist der BMI < 20, 5? (Alternativ: Ist der mittlere Oberarmumfang < 25 cm? ) Verminderte Nahrungsaufnahme in der letzten Woche? Hat der Patient innerhalb der letzten 3 Monate Gewicht verloren? Liegt eine schwere Erkrankung vor (z. B. chron. Erkrankung)? Wenn mindestens 1 x ja, dann Screening nach NRS 1 Das Wenn alle Nein, dann initiales Screening wöchentlich wiederholen Vor größeren Eingriffen, eine präventive Ernährungstherapie in Betracht ziehen Ernährungsrisiko kann in standardisierter Form mit Hilfe des NRS (Nutritional Risk Screening NRS 2002) ermittelt werden, nach Kondrup J et al. , Clinical Nutrition 2003; 22: 415 -421 (DOI: 10. 1016/S 0261 -5614(03)00098 -0), empfohlen von der Europäischen Gesellschaft für Klinische Ernährung und Stoffwechsel (ESPEN).

Erfassung der Mangelernährung Screening nach NRS 20021 Punkte Ermittlung des Ernährungszustandes Schweregrad der Erkrankung/ Therapie Alter Kein oder geringer Gewichtsverlust in 3 Monaten 0 Gewichtsverlust > 5 % in den letzten 3 Monaten oder Kostaufnahme 50 bis 75 % der gewohnten Menge während der letzten Woche 1 Gewichtsverlust > 5 % in den letzten 2 Monaten oder BMI = 18, 5 – 20, 5 + beeinträchtigter Allgemeinzustand oder Kostaufnahme 25 bis 50 % der gewohnten Menge während der letzten Woche 2 Gewichtsverlust > 5 % in einem Monat oder BMI < 18, 5 + beeinträchtigter Allgemeinzustand oder Kostaufnahme weniger als 25 % der gewohnten Menge während der letzten Woche 3 § Keine Stoffwechselerkrankung § Chronische Erkrankungen (z. B. Zirrhose, Diabetes, Z. n. Schlaganfall) speziell mit akuten Komplikationen § Akuter Schlaganfall § Schwere entzündliche Darmerkrankung § Hämatologische Erkrankung § Chemotherapie § Wiederholte chirurgische Eingriffe § Kopfverletzungen § Knochenmarktransplantationen § Intensivpatienten § Größere Apoplexien Patient 70 Jahre oder älter 0 § Normaler Nährstoffbedarf § Solide Tumore/Strahlentherapie § Cholezystektomie § Laparoskopische Chirurgie § Schwere Pneumonie § Postoperatives Nierenversagen § Größere abdominelle Operation § Ileus § Anastomoseninsuffizienz § Schwere Infektion (Sepsis) § Verbrennungen > 50 % § Schwere akute Pankreatitis 1 – 0 Punkte = derzeit kein Risiko 1 – 2 Punkte = erhöhtes Risiko Screening wöchentlich wiederholen 1 modifiziert nach Kondrup J et al. Clin Nutr. 2003; 22: 415 -421 1 2 3 1 Zur Gesamtberechnung der Punkte nur die jeweils höchsten Punktwerte aus den Blöcken addieren. Auswertung Gesamtpunktzahl: Wertung Gesamt: ≥ 3 Punkte = hohes Risiko Patienten mit einem Risikograd ≥ 3 benötigen eine supportive Ernährungstherapie Bei geplanter OP: präoperative Ernährungstherapie

Ergebnis: Hauptscreening NRS 2002 23. 01. 2022
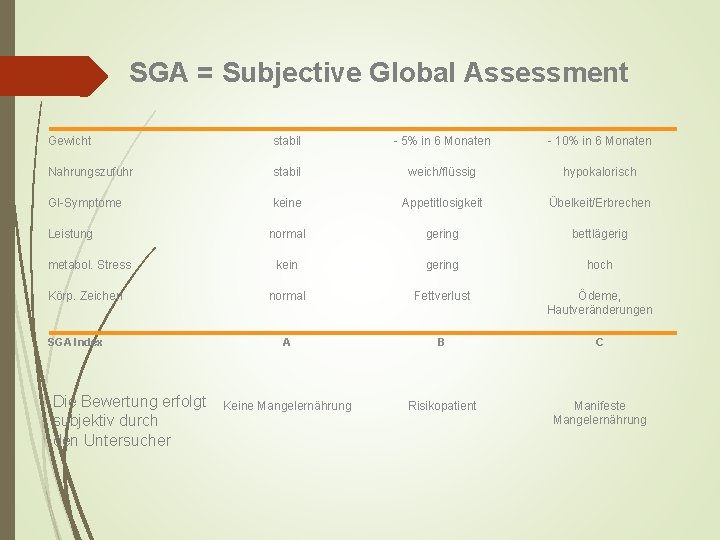
SGA = Subjective Global Assessment Gewicht stabil - 5% in 6 Monaten - 10% in 6 Monaten Nahrungszufuhr stabil weich/flüssig hypokalorisch GI-Symptome keine Appetitlosigkeit Übelkeit/Erbrechen normal gering bettlägerig kein gering hoch normal Fettverlust Ödeme, Hautveränderungen A B C Keine Mangelernährung Risikopatient Manifeste Mangelernährung Leistung metabol. Stress Körp. Zeichen SGA Index Die Bewertung erfolgt subjektiv durch den Untersucher
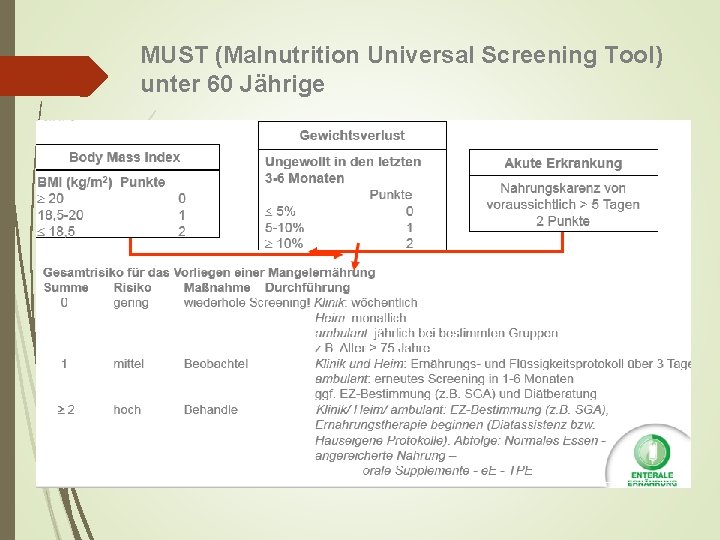
MUST (Malnutrition Universal Screening Tool) unter 60 Jährige
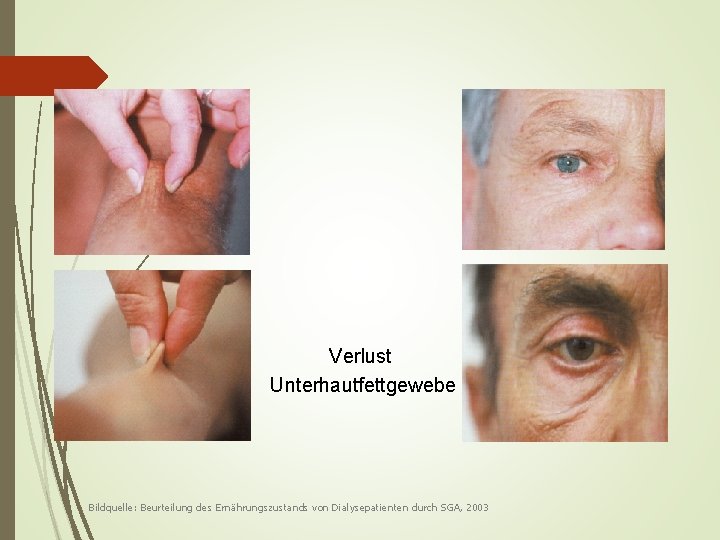
Verlust Unterhautfettgewebe Bildquelle: Beurteilung des Ernährungszustands von Dialysepatienten durch SGA, 2003
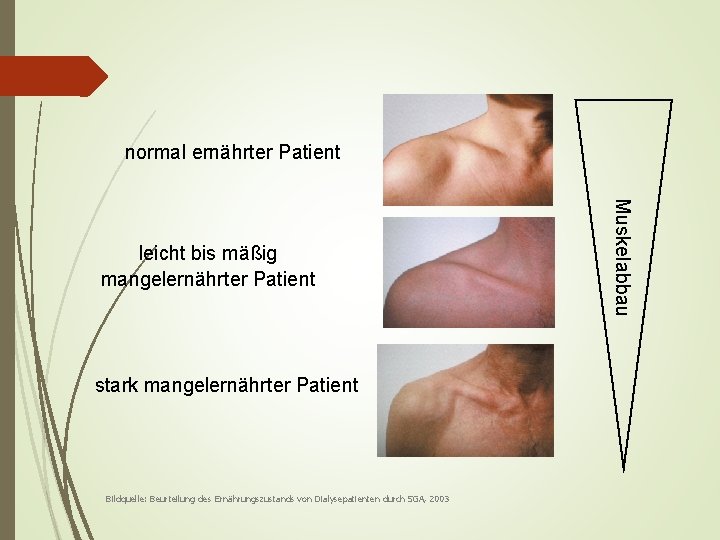
normal ernährter Patient stark mangelernährter Patient Bildquelle: Beurteilung des Ernährungszustands von Dialysepatienten durch SGA, 2003 Muskelabbau leicht bis mäßig mangelernährter Patient

BMI = Body - Mass - Index Eingruppierungen für unter 60 - Jährige: 19 - 25 normaler Ernährungszustand <18, 5 Mangelernährung Grad 1 <17, 0 Mangelernährung Grad 2 <16, 0 Mangelernährung Grad 3

Gleiche Größe, gleiches Gewicht! Manchmal sagt der BMI nichts aus! www. data-input. de
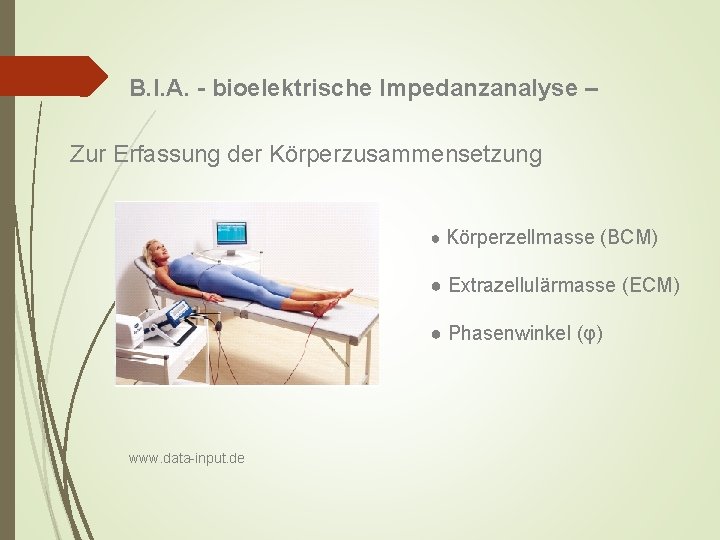
B. I. A. - bioelektrische Impedanzanalyse – Zur Erfassung der Körperzusammensetzung ● Körperzellmasse (BCM) ● Extrazellulärmasse (ECM) ● Phasenwinkel (φ) www. data-input. de
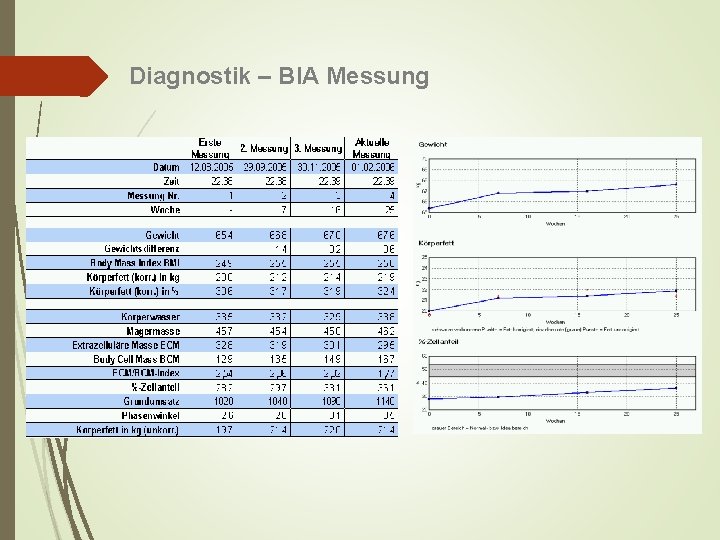
Diagnostik – BIA Messung
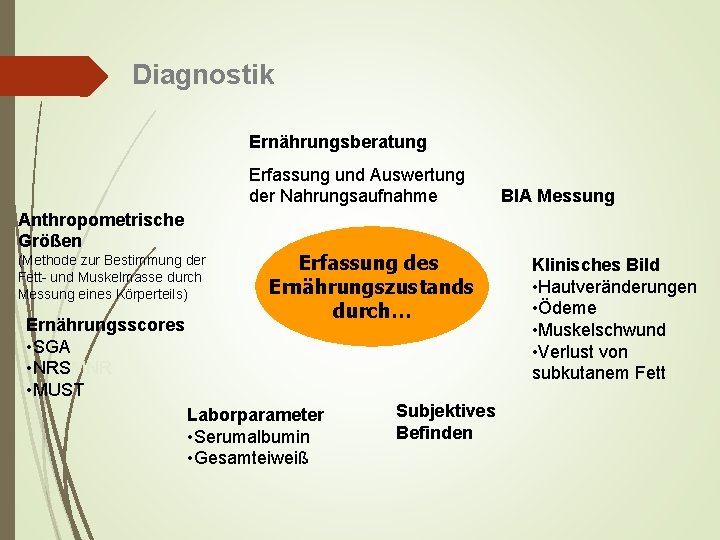
Diagnostik Ernährungsberatung Erfassung und Auswertung der Nahrungsaufnahme Anthropometrische Größen (Methode zur Bestimmung der Fett- und Muskelmasse durch Messung eines Körperteils) Ernährungsscores • SGA • NRSMNR • MUST Erfassung des Ernährungszustands durch… Laborparameter • Serumalbumin • Gesamteiweiß Subjektives Befinden BIA Messung Klinisches Bild • Hautveränderungen • Ödeme • Muskelschwund • Verlust von subkutanem Fett
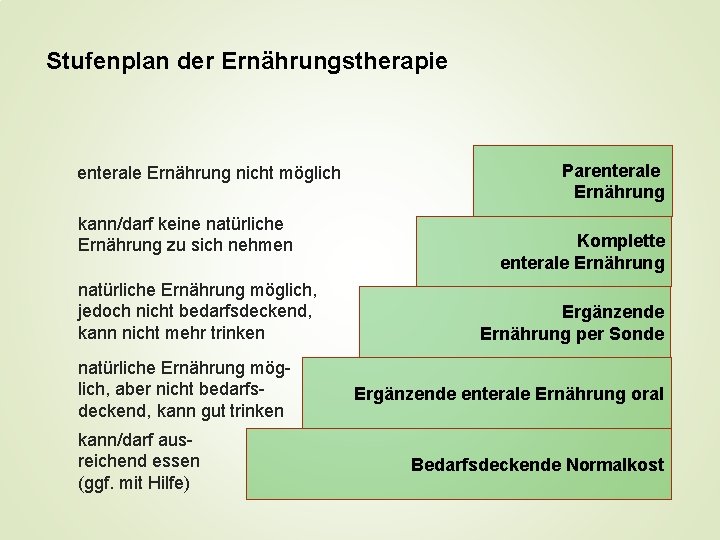
Stufenplan der Ernährungstherapie enterale Ernährung nicht möglich kann/darf keine natürliche Ernährung zu sich nehmen natürliche Ernährung möglich, jedoch nicht bedarfsdeckend, kann nicht mehr trinken natürliche Ernährung möglich, aber nicht bedarfsdeckend, kann gut trinken kann/darf ausreichend essen (ggf. mit Hilfe) Parenterale Ernährung Komplette enterale Ernährung Ergänzende Ernährung per Sonde Ergänzende enterale Ernährung oral Bedarfsdeckende Normalkost

Ernährungstherapie - was kann sie leisten? - Ziele der Ernährungstherapie: • Ernährungszustand stabilisieren • Gewichtsverlust verhindern / reduzieren • Erhöhung der Effektivität der antitumoralen Therapie • Reduktion von Nebenwirkungen der Therapie (nach: Leitlinie Parenterale Ernährung der DGEM, nichtchirurgische Onkologie) • Erhalt / Verbesserung der Lebensqualität
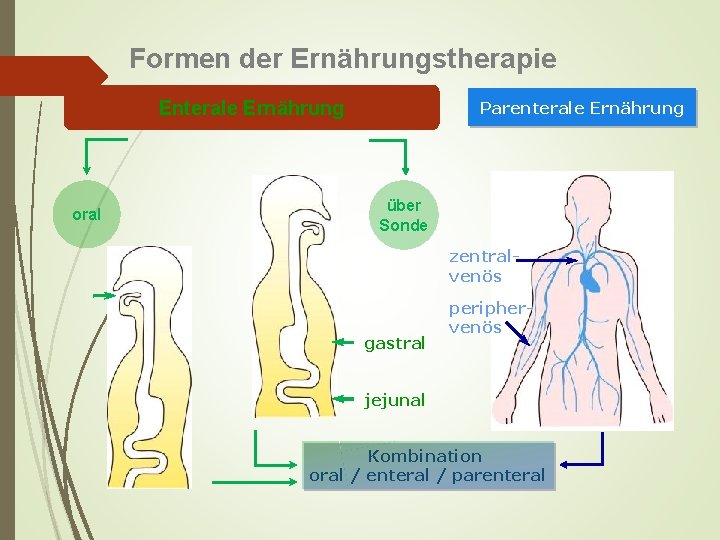
Formen der Ernährungstherapie Enterale Ernährung oral Parenterale Ernährung über Sonde zentralvenös gastral periphervenös jejunal Kombination oral / enteral / parenteral
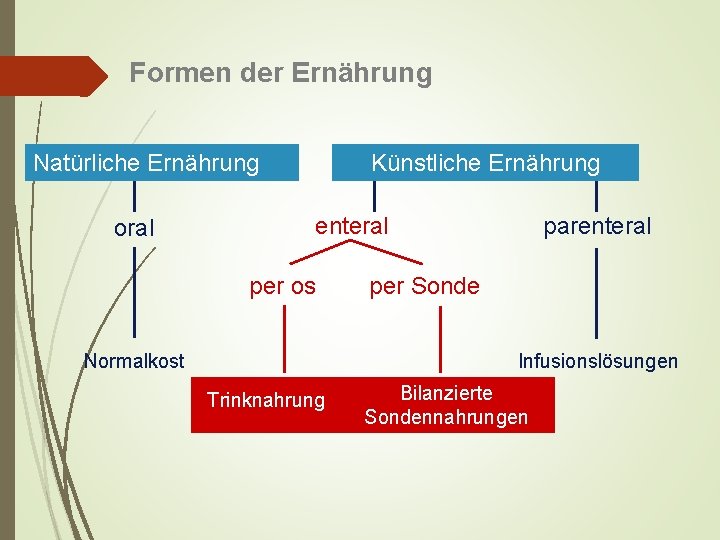
Formen der Ernährung Natürliche Ernährung oral Künstliche Ernährung enteral per os Normalkost parenteral per Sonde Infusionslösungen Trinknahrung Bilanzierte Sondennahrungen
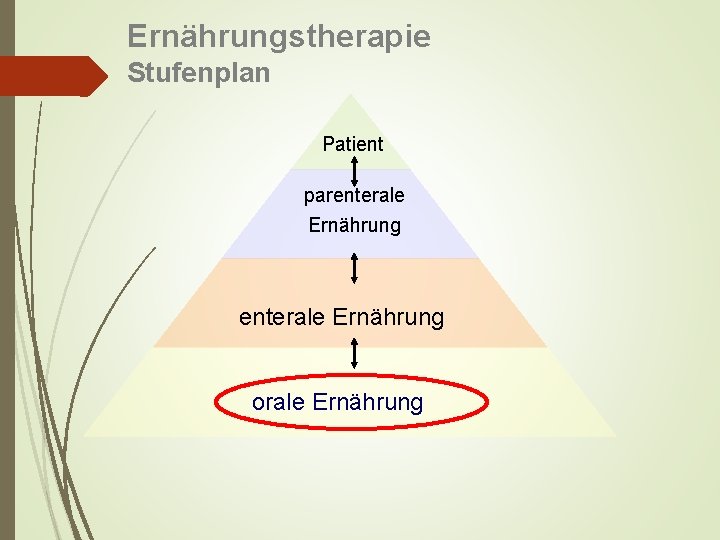
Ernährungstherapie Stufenplan Patient parenterale Ernährung orale Ernährung

Orale Ernährung • so lange wie möglich aufrecht erhalten • Wunschkost nach Bedarf des Patienten • bei Gewichtsverlust sofort reagieren Ernährungsempfehlungen / Ernährungsberatung Trinknahrung anbieten
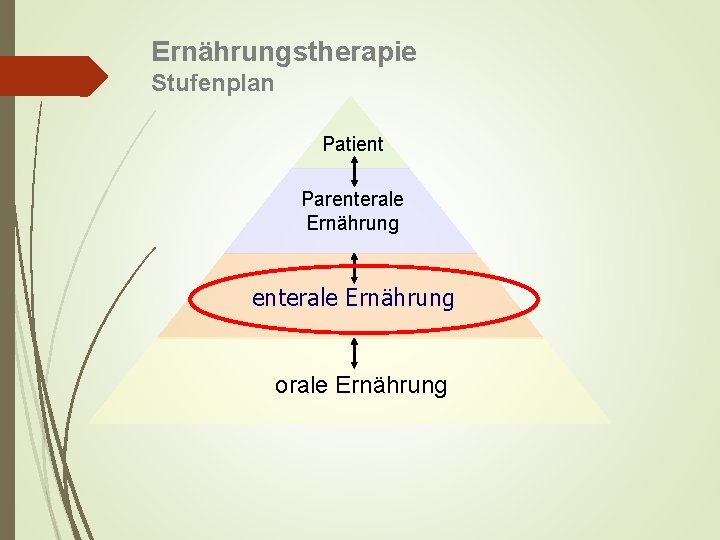
Ernährungstherapie Stufenplan Patient Parenterale Ernährung orale Ernährung

Enterale Ernährung Patient kann, darf oder will nichts mehr essen Nasale Sonden (kurzzeitige Ernährung) Gastrale Sonden (Langzeiternährung) enterale Ernährungslösung erreichen erst bei 1500 ml den Mikronährstoff-Mindestbedarf (DGE) enterale Produkte entsprechend der Indikation, Stoffwechselsituation, orale Restnährstoffmenge auswählen langsamer Kostaufbau, häufig Übelkeiten und Erbrechen

Einteilung bilanzierter Diäten AMR 15. 4 Produktspezifikationen 15. 4. 1. Standardprodukte Elementardiäten und Sondennahrungen, die bei der überwiegenden Zahl der Indikationen für enterale Ernährung einsetzbar sind 15. 4. 2. Spezialprodukte Elementardiäten und Sondennahrungen, die krankheitsadaptiert für bestimmte Indikationen ausgewiesen sind

Unterscheidungskriterien von enteraler Nahrung Energie Niederkalorisch = 0, 75 kcal/ ml Beispiele für Indikationen: Übergewicht, hoher Flüssigkeitsbedarf, Einschleichphase Normokalorisch/ Isokalorisch = 1 kcal/ ml Standardernährung Hochkalorisch = 1, 3 -2 kcal/ ml Verkostung

Enterale Ernährung – Hersteller
Ernährungstherapie Stufenplan Patient parenterale Ernährung orale Ernährung

Indikation zur parenteralen Ernährung? • operative Eingriffe (vor allem am GI) • künstliche Beatmung • Kurzdarmsyndrom (je nach Restdünndarmlänge) • schwere Malnutrition • unstillbare Diarrhoen, Erbrechen • Ösophaguskarzinome • Malabsorption • Tumorkachexie • gestörte Magen-Darm-Passage • HNO-Tumore • Chronisch entzündliche Darmerkrankungen CED • chron. terminale Niereninsuffizienz • • Stenosen im Mund-, Rachenbereich Dysphagie Bewusstlosigkeit, Koma Demenz • Anorexie-Kachexie-Syndrom
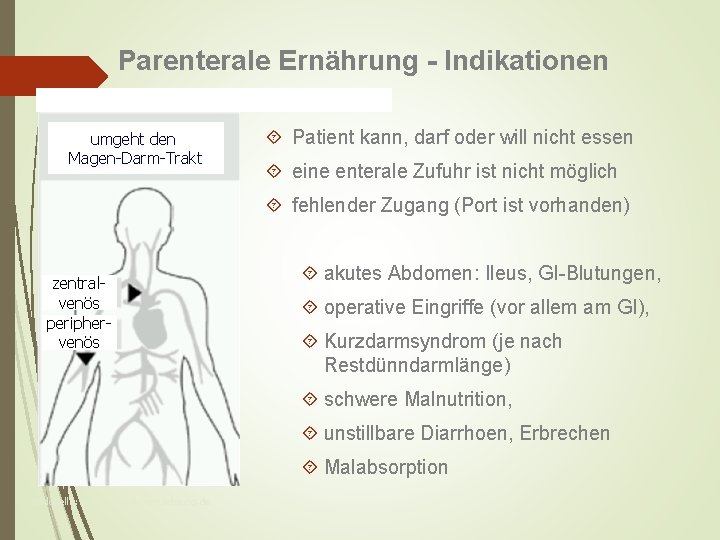
Parenterale Ernährung - Indikationen umgeht den Magen-Darm-Trakt Patient kann, darf oder will nicht essen eine enterale Zufuhr ist nicht möglich fehlender Zugang (Port ist vorhanden) zentralvenös periphervenös akutes Abdomen: Ileus, GI-Blutungen, operative Eingriffe (vor allem am GI), Kurzdarmsyndrom (je nach Restdünndarmlänge) schwere Malnutrition, unstillbare Diarrhoen, Erbrechen Malabsorption Bildquelle: www. enterale-ernaehrung. de

Faustzahlen zur künstlichen Ernährung Energiezufuhr(kcal(kg. KG/d) normokalorische Ernährung: postoperative Ernährung: Tumorpatienten: hochkalorische Ernährung: 30 30 -33 25 -35 35 -45 Flüssigkeitsbedarf (ml/kg. KG/d): 30 -35 s. Leitlinien parenterale Ernährung DGEM 2013/14

Indikation zur Ernährungstherapie von Tumorpatienten (ESPEN 2009) Ab wann ist eine Ernährungstherapie notwendig? • orale Zufuhr liegt unter 500 kcal/Tag • unzureichende orale Nahrungszufuhr unter 60 % des täglichen Bedarfs • Malnutrition liegt vor • Nebenwirkungen oder Beschwerden liegen vor

Mikronährstoffe 23. 01. 2022

Parenterale Ernährung ist auch zu Hause möglich Leitlinien der DGEM für heimparenterale Ernährung 2013/2014 Maßnahmen einleiten: die Organisation der heimparenteralen Ernährung • Indikationsstellung durch den behandelnden Arzt • Sorgfältige Informationen, Aufklärung und Einwilligung des Patienten • Erstellung einer individuellen Rezeptur • Beauftragung einer für die Maßnahmen qualifizierten Apotheke oder eines spezialisierten Versorgungsunternehmen (Lieferung der Materialien nach Hause, Durchführung der Ernährung vor Ort) • Individuelle Schulung des Patienten und seiner Angehörigen durch Ernährungsteam oder Versorgungsunternehmen für heimparenterale Ernährung • Festlegung des Monitorings (Hausarzt, Ernährungsambulanz)
Fazit Malnutrition ist weit verbreitet. Malnutrition birgt schwerwiegende Folgen. Ernährungszustand sollte routinemäßig erfasst werden alle Möglichkeiten der Ernährungstherapie ausschöpfen oral - enteral - parenteral

Fallvorstellung mangelernährter Patienten unterschiedlicher Altersgruppen 23. 01. 2022

Pädiatrie Monitoring bei (teil)parenteraler Ernährung und oder Flüssigkeitstherapie • Klinische Untersuchung, Flüssigkeitsbilanz täglich • Somatische Daten: Körpergewicht (zunächst täglich) Kopf- und Längenwachstum (Verlaufskontrolle mit Perzentiltabellen) 1 mal/Woche • Blut: Blutzucker, Blutgasanalyse, Elektrolyte zunächst täglich Blutbild, Protein gesamt, Triglyzeride, Bilirubin gesamt, alkalische Phosphatase - wenn stabil alle 14 Tage • Urin: Volumen, Eiweiß, ph-Wert, spezifisches Gewicht, Ketonkörper – wenn stabil alle 14 Tage Jochum, Ernährungsmedizin Pädiatrie, 2. Auflage, Springer 23. 01. 2022

Pädiatrie Erweiterte Methoden zur Beurteilung der Ernährung und des Ernährungsstatus • BMI Body Mass Index • Hautfaltendicke • BIA Messung Bioimpedanzanalyse • Ernährungsanamnese (24 h Protokoll, 3 -7 Tage Protokolle) • Berechnung der Nährstoffzufuhr Berechnungsgrundlage Gewicht und Körperlänge Ein Gewicht unter 2 Perzentilen unter dem Sollgewicht wird als Unterernährung bezeichnet 23. 01. 2022
Fallbeispiel einjähriges Mädchen Sude Zwillingskind, Schwester gesund Geb. im August 2013 Aktuelles Gewicht: 5, 6 kg Diagnose: Infantile systemische Hyalinosis mit progredienter Dystrophie, Gelenkkontrakturen Übernahme durch Homecare-Unternehmen September 2014 Anlass: schlechtes Gedeihen und ständiges Spucken Transnasale Sonde Infatrini Peptisorb

Fallbeispiel einjähriges Mädchen Sude November 2014 Weitere Gewichtsabnahme (ca. 500 g) Trotzt Sonde, weiter schlechtes Gedeihen und Spucken. Essen wird zum übermächtigen Thema in der Familie. Aufgrund der Diagnose (schlechte Resorption von oraler Nahrung) wird sich gegen eine PEG- Anlage und für eine TPE entschieden. Mitte November Anlage eines einlumigen Broviackatheter

Fallbeispiel einjähriges Mädchen Sude ist extrem berührungsempfindlich. Wird oral mit Chloralhydrat, Luminal und Morphin versorgt. Äußerst ängstlich und abwehrend gegen fremde Personen, aufgrund Ihrer vielen Krankenhausaufenthalte. Kind lässt sich nur von der Mutter beruhigen. Fängt an mit Kopfschütteln ein „Nein“ zu äußern. Zahnfleischwucherungen behindern die normale Nahrungsaufnahme. Mit viel Geduld, fängt Sude wieder mit oraler zusätzlicher Nahrungsaufnahme an (Fruchtzwerge) TPE Regime: 422 kcal/ 353 ml + Vitamine + Spurenelemente Zunahme von 600 g innerhalb 3 Wochen

Fallbeispiel 43 Jähriger Mann Geschlecht: männlich Alter: 43 Jahre Größe: 1, 85 m Diagnose: Ösophaguskarzinom Mai 2014 Gewichtsverlust von 25 kg innerhalb der letzten 5 Monate Aktuelles Gewicht beträgt 73 kg BMI 21, 3 kg/m², Phasenwinkel: 4, 5°, BCM: 27, 0 kg Orale Nahrungszufuhr beträgt ca. 400 kcal Energiebedarf: 2190 kcal/d (30 kcal/kg. KG) Flüssigkeitszufuhr ca. 1500 ml Schluckstörungen, ausgeprägte Inappetenz, Völlegefühl, breiige Diarrhoen 4 -5 x/d Port vorhanden 23. 01. 2022

Fallbeispiel 43 Jähriger Mann Einleitung einer TPN mit 1000 ml Olimel peri 2, 5% (700 kcal) + Zusätze Nach unauffälligem Labor erhöht auf 1500 ml Olimel 2, 5% (1050 kcal) + Zusätze Juni 2014 Gewichtszunahme von 4, 5 kg innerhalb der letzten 4 Wochen (77, 5 kg) BMI: 22, 6 kg/m², Phasenwinkel: 4, 6°, BCM: 28, 5 kg Verbesserter Schluckakt Orale Nahrungszufuhr beträgt ca. 700 kal, Flüssigkeitszufuhr weiterhin ca. 1500 ml Fortführung der TPN mit 1500 ml Olimel 2, 5% (1050 kcal) + Zusätze Juli 2014 Gewichtszunahme von 2 kg (79, 5 kg) BMI: 23, 2 kg/m², Phasenwinkel: 5, 0, BCM: 30, 6 kg Reduzierung der TPN 23. 01. 2022

Fallbeispiel 62 Jährige Frau Alter: Größe: Diagnose: 62 Jahre 1, 69 m Koloncarzinom Aktuelles Gewicht: Gewichtsverlust von Flüssigkeit Appetitlosigkeit 60 kg 15 kg innerhalb von 8 Wochen ca. 2 Liter Start mit Olimel 2, 5% 1050 kcal/ 1500 ml (ca. 20 kcal/kg KG/Tag) Verbesserte orale Aufnahme Gewichtszunahme von 11 kg innerhalb eines halben Jahres 23. 01. 2022
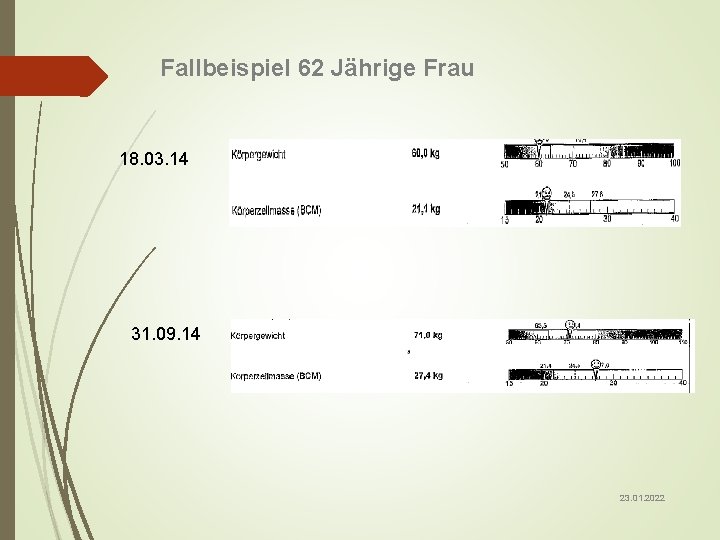
Fallbeispiel 62 Jährige Frau 18. 03. 14 31. 09. 14 23. 01. 2022

Fallbeispiel 72 Jähriger Mann Alter: Größe: Diagnose: 72 Jahre 1, 76 m Pankreascarzinom, Chemo beendet Gewicht bei Aufnahme: Orale Aufnahme: Flüssigkeit: 48 kg (BMI 15, 5) unter 500 kcal ca. 1 Liter Beginn der Ernährungstherapie: Resource Protein 250 kcal Keine Gewichtszunahme Umstellung auf PE und TN Start mit PE 800 kcal/ 900 ml + 250 kcal TN Nach einen halben Jahr Gewichtszunahme von 13 kg Orale Aufnahme hat sich verbessert Reduzierung der PE 23. 01. 2022
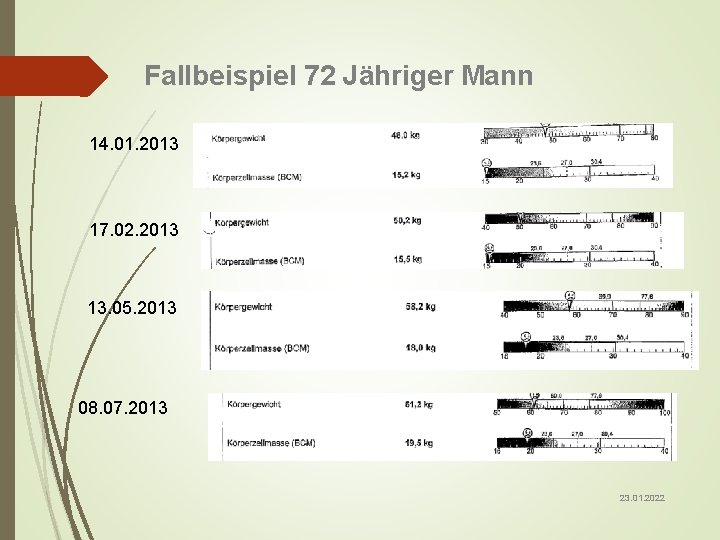
Fallbeispiel 72 Jähriger Mann 14. 01. 2013 17. 02. 2013 13. 05. 2013 08. 07. 2013 23. 01. 2022

Fallbeispiel 79 Jähriger Mann Größe: Aktuelles Gewicht: Diagnose: 1, 64 m 43 kg Bronchialcarzinom, Magencarzinom Sehr schlechter Allgemeinzustand, kaum orale Aufnahme Flüssigkeit: ca. 1 Liter Start mit: TPN 800 kcal/800 ml Nach drei Wochen keine Gewichtszunahme, Erhöhung des Regimes auf 1170 kcal/ 1000 ml Gewichtszunahme nach 10 Wochen um 5 kg TPN Regime wird weitergegeben 23. 01. 2022
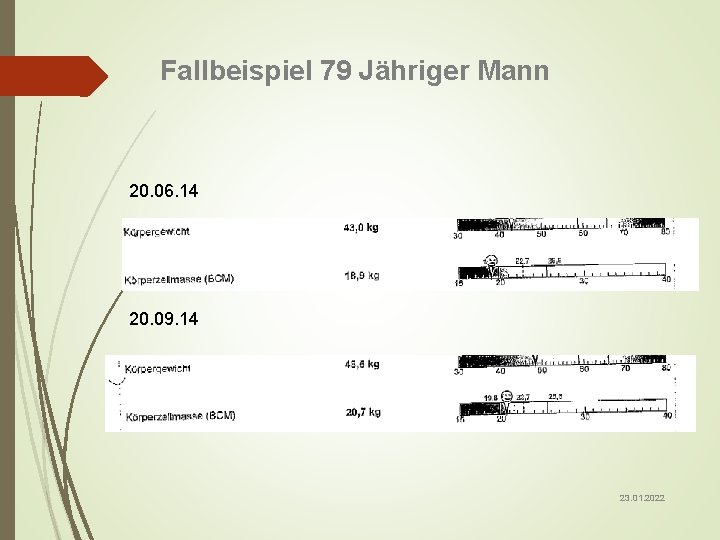
Fallbeispiel 79 Jähriger Mann 20. 06. 14 20. 09. 14 23. 01. 2022

Füllen Sie gegenseitig einen NRS Bogen anhand der mitgebrachten Beispiele aus. 23. 01. 2022

Fallbeispiel A „Paul Klaus mit Oesophagus-Ca“ Paul Klaus Oesophagus-Ca Alter 75 Jahre Größe 1, 85 m Gewicht 55 kg Gewichtsverlust 10 kg in drei Monaten Probleme Schluckstörungen, er hat in der letzten Woche kaum etwas gegessen, extreme Appetitlosigkeit Er verweigert eine PEG und hat einen Port Berechnen Sie den BMI. 15, 7 Was sagt der NRS aus? Wie würden Sie mit einer Ernährungstherapie starten? 23. 01. 2022

Fallbeispiel B „Erna Mustermann mit Magen-Ca“ Erna Mustermann Magen-Ca, terminale Niereninsuffizienz Alter 83 Jahre Größe 1, 60 m Gewichtsverlust Probleme 55 kg in drei Monaten Kauprobleme, Appetitlosigkeit, immobil, bettlägerig Berechnen Sie den BMI. Was sagt der NRS aus? Wie würden Sie mit einer Ernährungstherapie starten? 23. 01. 2022

Fallbeispiel C: Hans Müller Kurzdarmpatient Herr Hans Müller Kurzdarmsyndrom Alter 65 Jahre Größe 1, 80 m Gewicht 50 kg Gewichtsverlust von 10 kg in drei Monaten Extreme Appetitlosigkeit Patient kann oral Flüssigkeit zu sich nehmen Er hat einen Port. Berechnen Sie den BMI. Was sagt der NRS aus? Wie würden Sie mit einer Ernährungstherapie starten? 23. 01. 2022

Appetitlosigkeit Empfehlungen zur Ernährung bei Chemo- und Strahlentherapie: ð essen, wenn Appetit vorhanden ist ð starke Essensgerüche vermeiden und häufig lüften ð möglichst nicht selbst kochen ð kleine Portionen: “Wunschkost”, „Knabberteller“ ð gepflegete, appetitliche Darbietung der Speisen ð appetitanregende Getränke ð Spaziergänge an der frischen Luft 23. 01. 2022

Übelkeit und Erbrechen ð 2 -3 Stunden nach dem Erbrechen: salzige Kekse; schluckweise Flüssigkeit ð Mund vor und nach dem Essen ausspülen ð Mehrere kleine, mild gewürzte Mahlzeiten ð Langsam essen und trinken, gründlich kauen ð Essensgerüche meiden ð Kühle und lauwarme Speisen bevorzugen ð Schon vor dem Aufstehen trockenes Gebäck (Kekse, Zwieback, . . ) 23. 01. 2022

Veränderungen des Geschmacksempfinden Empfehlungen zur Ernährung bei Chemo- und Strahlentherapie: ð Geschmacksschwelle für bitter herabgesetzt ð Geschmacksschwelle für süß ist erhöht ð Abneigung gegen Fleisch und Wurst: auf Milch, Milchprodukte, Hülsenfrüchte, Eier und Fisch wechseln; Fleisch zusammen mit Süßem (z. B. Apfelmus) verzehren oder mit Fruchtsaft, Sojasoße oder Wein marinieren ð Metallgeschmack im Mund: Zitronen- und Minzbonbons oder Kaugummi (zuckerfrei); evtl. Plastikbesteck 23. 01. 2022

Alle angegebenen Beschreibungen, Bilder, Firmen- und Markennamen sowie Warenzeichen sind Eigentum ihrer Inhaber und dienen lediglich zur Identifikation und Beschreibung der Produkte. Eine Garantie für Vollständigkeit, Aktualität oder Richtigkeit der gemachten Angaben kann nicht übernommen werden, ebenso wenig wie eine Haftung für die Verwendung dieser Seiten oder deren Inhalte. Die einzelnen Artikel stellen weder eine individuelle Beratung, noch eine Empfehlung dar. Diese Präsentation ist in allen ihren Teilen urheberrechtlich geschützt. Jede Verwertung außerhalb der engen Grenzen des Urheberrechtsgesetzes ist ohne Zustimmung unzulässig.

Vielen Dank für Ihre Aufmerksamkeit! Ich wünsche Ihnen einen schönen Nikolaus
- Slides: 84