MANEJO DE SOLUCIONES PARENTERALES Y DOSIFICACIN DE MEDICAMENTOS












































- Slides: 46

MANEJO DE SOLUCIONES PARENTERALES Y DOSIFICACIÓN DE MEDICAMENTOS

LÍQUIDOS PAR ENTÉRALES • Son los líquidos administrados por cualquier vía que no sea el aparato digestivo. Necesarios cuando la enfermedad se acompaña de pérdida importante de volumen, originada por diversas causas tales como vómito, diarrea, pérdida excesiva de líquidos y electrólitos, choque hipovolémico, pérdida de la consciencia.

COMPLICACIONES DURANTE LA TERAPEÚTICA CON LÍQUIDOS PARENTERALES • • • Insuficiencia cardiaca. Dolor. Edema. Eritema. Cambio de coloración. Ausencia de retorno venoso.

MEMBRETE PARA SOLUCIONES PARENTERALES Nombre del paciente. Número de cama. Fecha. Componentes de la solución expresados con Mililitros, y mili equivalentes en caso de agregarles algún electrolito. Volumen real de la solución. Hora de inicio. Goteo por minuto. Nombre de la enfermera responsable de la preparación.

METABOLISMO DEL AGUA ORGANISMO DEL NIÑO 79% AGUA NACIMIENTO SE MANTIENE HASTA EL 60% EDAD ADULTA ANCIANIDAD 55%

DISTRIBUCIÓN DEL AGUA • INTRACELULAR} 30 – 50 % • EXTRACELULAR} 20 – 28 % A SU VEZ SE DIVIDE EN: • • • 5% PLASMA SANGUÍNEO 15% LÍQUIDO INTERSTICIAL 3 % AGUA TRANSCELULAR V A R I A N Edad Tejido graso

FUENTES DE PROVICION DE AGUA • INGERIDOS} alimentos y agua de oxidación. • • • 1 GR CARBOHIDRATOS = 0. 55 ml de H 2 O 1 GR PROTEÍNAS = 0. 45 ml DE H 2 O 1 GR LÍPIDOS = 1 ml de H 2 O

AGUA INGERIDA Tracto gastrointestinal 90% por difusión pasiva A nivel intravascular se mantiene intercambio por defecto de presión hidrostática ( BOMBA CARDIACA) PRESIÓN ONCÓTICA ( PROTEÍNAS PLASMÁTICAS) Zona de gradiente depresión (equilíbrio de straling)

AGUA INGERIDA ESPACIO INTRACELULAR Y EXTRACELULAR INTERCAMBIO BASADO EN LA OSMOSIS (EQUILIBRIO DE DONAN) LIQUIDO DE UNA ZONA DE > < CONCENTRACIÓN

METABOLISMO DEL AGUA LÍQUIDOS LLEGAN AL CAPILAR GLOMERULAR Asa de Henle ( ascendente) Favorece la salida de Na y K Disminuye la osmolaridad

METABOLISMO DEL AGUA LÍQUIDOS LLEGAN AL CAPILAR GLOMERULAR Asa de Henle ( descendente) Favorece la entrada de Na y K Aumenta la osmolaridad Mecanismo renal provee tonicidad y osmolaridad urinaria

MECANISMO RENAL 1 Osmolaridad Libera HAD Favorece reabsorción de líquidos Uresis (concentrada) Si no libera HAD (uresis diluida)

MECANISMO RENAL 2 Neurohumoral de control liq orgánicos Efecto secundario filtrado glomerular Favorece liberación de renina (yuxtaglomerular y aldosterona) Vasopresor estimula reabsorción de Na y Cl en túbulo distal

MECANISMO RENAL * 50 % agua ingerida (orina) * Gasto urinario normal (0. 5 – 2 -3 ml/kg. /hr. (15 ml /M 2 SC). * Piel elimina 31 %. * Ventilación pulmonar 10 % * Heces 6 % * P insensibles 400 - 600 ml/M 2 SC/ día ( condiciones físicas externas o patológicas)

PÉRDIDAS DE LÍQUIDOS BÁSICAS • Existen básicamente 3 clases de pérdida que pueden llevar al choque. • • Pérdida importante de solución salina sola. • Una por pérdida de solución salina y sangre. • Y por pérdida de sangre sola. • Puede esperarse una pérdida importante de solución salina sola en pacientes con quemaduras, peritonitis, contusiones múltiples y obstrucción intestinal.

LIQUIDOS SUGERIDOS • Volumen de líquido Rango de 80 – 120 ml / kg / día. Dependerá del estado clínico por ejemplo en niños con, PCA, ICC y edema agudo pulmonar se puede considerar un incremento de 10 – 20 ml /kg / día. • Los lactantes y los prematuros que pesan < 1. 000 gr. necesitan más líquido y menos glucosa en los niños pretérmino de 800 – 1. 000 gr.

LIQUIDOS SUGERIDOS • Se inicia líquidos a un ritmo de 80 – 100 ml / kg / día y se agrega en promedio de 5 -6 mg / kg /min. de dextrosa al 7. 5%. • Los niños que pesan < 800 gr habitualmente necesitan un ingreso de líquidos de 120 – 140 ml / kg / día. Para compensar las pérdidas insensibles mayores y evitar descompensación electrolítica. .

TIPOS DE SOLUCIONES • COLOIDE: Substancias no cristalinas, difusible • • pero no soluble en agua; incapaz de pasar a través de una membrana animal. Compuestas por dextrano, hidroxietilalmidón, poligelina, cloruro sódico, cloruro de potasio, cloruro de calcio. Su osmolaridad va de 275 – 308 mosm / l. Su Ph va de 5 – 7 dependiendo el tipo de solución. Las marcas comerciales más conocidas son: Rheomacrodex 10%, Expafusin, Hemacel.

TIPOS DE SOLUCIONES • CRISTALOIDE: Substancias que por su composición química disueltas atraviesan los tabique porosos. Compuestas por glucosa, cloro, sodio, potasio, calcio y lactato. • Su osmolaridad va de 273 – 307 mosm / l. • Su Ph va de 3. 5 a 7 dependiendo el tipo de solución y el laboratorio. • Las marcas comerciales más conocidas son: dextrosa al 5 o 10 %, Cloruro de sodio, y Lactato de Ringer.

TIPOS DE SOLUCIONES • HIPEROSMOLARES: son las soluciones que ejercen una presión osmótica mas elevada que la otra. (suele hacerse comparación con el plasma normal). • HIPERTÓNICAS: G. Hiper (encima) Tonos (tensión). soluciones con mayor presión osmótica que el líquido fisiológico normal del organismo. • ISOTÓNICAS: G. Isos (igual) Tonos (tensión). se aplica a soluciones con la misma presión osmótica que la sangre (salina al 0. 9% de sal en agua).

DOSIFICACIÓN DE MEDICAMENTOS • CONCEPTO: Procedimiento que consiste en ministrar fármacos al paciente pediátrico de una manera racional y segura. • OBJETIVO: Lograr la máxima eficacia y seguridad al ministrar pequeñas dosis de medicamentos.

GENERALIDADES • Existe un límite promedio de dosificación. • El ajuste de la dosis en pacientes pediátricos es el tamaño. • Casi todas las dosis de medicamentos para esta población se administran Mcg / Kg. O Mg/Kg. • Algunas veces se requiere calcular en M 2 de superficie corporal. • El recién nacido y el pretérmino requieren ajustes adicionales ya que la absorción por vía oral es incompleta o se encuentra alterada. (distribución de agua, retrasos en el metabolismo, inmadurez de las funciones hepáticas y renales).

GENERALIDADES • SOLVENTE: Agente capaz de disolver otras substancias. • SOLUTO: Sustancia que se disuelve en un líquido. • SOLUCIÓN: Líquido que contiene una sustancia disuelta. • MEZCLA: Incorporar o juntar varias cosas obteniendo una homogeneidad total o aparente. • DILUIR: Procedimiento que consiste en Disolver las partes de un cuerpo líquido (ejem. PSC polvo diluirlo en 3 ml sol inyectable).

GENERALIDADES • AFORAR: Procedimiento que consiste en llevar un volumen de medicamento hasta un nivel deseado de solución. (Calcular la capacidad de líquido en una unidad de volumen). • SUPERFICIE CORPORAL: (SC) Para calcular superficie corporal en M 2 con base a talla y peso.

CALCULO DE SUPERFICIE CORPORAL • Menos de 10 Kg. = Peso X 4 + 9 / 100 = SC • Mas de 10 Kg. = Peso X 4 + 7 / 90 + Peso = SC superficie corporal • SC del niño M 2 /SC del adulto M 2 X Dosis corriente del adulto=Dosis pediátrica.

CÁLCULO POR SUPERFICIE CORPORAL • EJEMPLO: PENTOBARBITAL de 100 mg calcular dosis a un niño de 0. 4 M 2 de SC. 0. 4 / 1. 7 x 100 Mg = 40 / 1. 7 = 23. 5 MG. Nota: De la fracción pueden eliminarse los puntos decimales y hacer la conversión en enteros: 4 / 17 X 100 MG = 23. 5 MG.

CALCULO PARA DOSIS DE MEDICAMENTOS VÍA ORAL • DOSIS DESEADA / DOSIS DISPONIBLE = DOSIS ADMINISTRADA • EJEMPLO: AC ascórbico 100 mg VO C/8 HR. Dosis disponible tabletas de 50 MG. 100 mg / 50 mg = Adm. 2 tabletas de AC ascórbico

CALCULO PARA DOSIS DE MEDICAMENTOS VÍA ORAL • PROPANOLOL 7. 5 MG VO C / 12 HR. Dosis disponible tabletas de 20 mg. • 7. 5 MG / 20 MG = 0. 37 MG de tableta. • NOTA: Debido a la presentación de algunos medicamentos es recomendable que sean fraccionados molidos o diluidos para ser exactos

CALCULO PARA MEDICAMENTOS PRESENTADOS EN JERINGAS O CARTUCHOS DESECHABLES • FORMULA: DOSIS DESEADA / DOSIS DISPONIBLE X CANTIDAD PRESENTADA = DOSIS MINISTRADA • EJEMPLO: Diacepam 5 Mg. C/12 Hr. (presentación jeringa 2 ml C/ 10 Mg) • 5 Mg / 10 Mg X 2 ml = 1 ml a ministrar.

CALCULO PARA MEDICAMENTOS PRESENTADOS EN JERINGAS O CARTUCHOS DESECHABLES • ENOXOPARINA SUBCUTÁNEA: 5 Mg SC C/24 Hr. (presentación jeringa. 2 ml con 20 Mg) • 5 Mg / 20 Mg X. 2 ml = 0. 05 ml a ministrar.

REGLA DE CLARK • Basada en peso en libras (primero haga la conversión a peso en gramos) • Peso del niño en libras / Peso del adulto en libras X Dosis adulto = Dosis del niño. • (1 libra es igual a 454 grs). • EJEMPLO: 6 libras (2. 724 Kg. ) / 150 libras (68. 100 Kg. ) X 5 gr. = 0. 07 gr.

REGLA DE YOUNG • Basada en edad y se utiliza en niños de entre 12 meses a 12 años. • Edad / Edad + 12 (constante) X Dosis adulto = Dosis del niño. • EJEMPLO: Digital p/ adulto de 0. 1 gr. (100 mg) Calculé dosis para niño de 4 años • 4 / 4 + 12 = 4 / 16 X 100 = 25 Mg.

REGLA DE 3 • Es un método para expresar igualdad entre 2 proporciones, y se usa para calcular una cantidad desconocida y se le asigna por lo general el valor * X *. PASO 1 • Volumen real de medicamento ----- Mg totales (reales) de medicamento • Valor desconocido * X * ----- Dosis solicitada (requerida)

REGLA DE 3 PASO 2 • Volumen real de medicamento X Dosis solicitada / Mg reales = dosis a aplicar. • EJEMPLO: Midazolam 5 Mg. Aforado en 50 ml de solución glucosada 5 % y pasar 1 ml por hora. • Presentación del medicamento. Ampolletas de 3 ml con 15 Mg. • 3 ml X 5 Mg /15= 1 ml (dosis aforar en 50 ml de SG 5 %.

REGLA DE 3 • EJEMPLO: Dopamina 20 Mg Aforar en 80 ml SG 5 % • Presentación: Dopamina 200 Mg en 5 ml. • 5 ml X 20 Mg / 200=. 5 ml (dosis a aforar en 80 ml SG 5%)

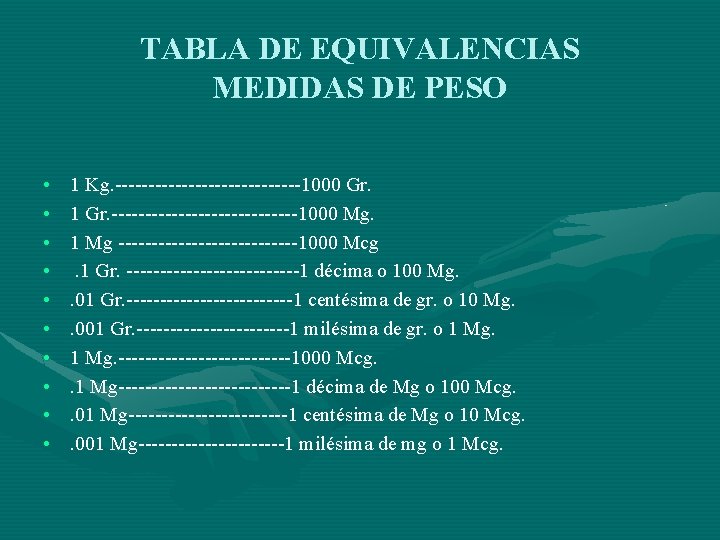
TABLA DE EQUIVALENCIAS MEDIDAS DE PESO • • • 1 Kg. --------------1000 Gr. 1 Gr. --------------1000 Mg. 1 Mg --------------1000 Mcg. 1 Gr. -------------1 décima o 100 Mg. . 01 Gr. -------------1 centésima de gr. o 10 Mg. . 001 Gr. ------------1 milésima de gr. o 1 Mg. -------------1000 Mcg. . 1 Mg-------------1 décima de Mg o 100 Mcg. . 01 Mg------------1 centésima de Mg o 10 Mcg. . 001 Mg-----------1 milésima de mg o 1 Mcg.

MEDIDAS DE VOLUMEN • • 1 Lt -------------1000 ml. ½ Lt ------------ 500 ml. ¼ Lt ------------- 250 ml. 1 onza ------------ 30 ml. 1 ml -------------10 décimas. ½ ml ------------5 décimas o. 5 ml. ¼ ml ------------0. 25 ml.

CALCULO PARA EXCEDENTE DE SOLUCIONES INTRAVENOSAS • Proporción de soluciones que conforman un total, misma que es utilizada para purgar un equipo que se instala en un total de soluciones intravenosas a ministrar.

CALCULO PARA EXCEDENTE DE SOLUCIONES INTRAVENOSAS • EJEMPLO: SOL GLUC 10% 35 ml + SOL FISIOLÓGICA 15 ML + KCL 2 Meq = 51 ML TOTALES. • EQUIPO DE 12 ML + 8 ML DE LLAVE DE 3 VÍAS. = 20 ML • DESARROLLO: • SOL GLUC 10% 35 ML X 20 ML (DE PURGA) / 51 ML DE VOL TOTAL • 1. - 35 X 20 / 51 = 13. 7 ML 2. - 35 ML + 13. 7 (EXCED SG 10%) = 48. 7 ML

CALCULO PARA EXCEDENTE DE SOLUCIONES INTRAVENOSAS • 1. - 15 X 20 / 51 = 5. 8 ML 2. - 15 ML + 5. 8 ML (EXCED SOL FISIOLOG)= 20. 8 ML • K. C. L. 2 Meq = 1 ML • 1. - 1 ML X 20 / 51 =0. 3 ML KCL) = 1. 3 ML 2. - 1 ML + 0. 3 ML (EXCED • SOLUCIÓN REAL A PREPARAR: ES IGUAL A LA SUMA DE TODOS LOS TOTALES • SG 10 % 48. 7 ML + SOL FIS 20. 8 ML + 1. 3 ML = 70. 8 ML DE SOL REAL A PREPARAR

CALCULO PARA EXCEDENTE DE SOLUCIONES INTRAVENOSAS COMPROBACIÓN: sol total con excedente MENOS sol real sin excedente igual a total de ml para purgar el equipo. • COMPROBACIÓN DE LA OPERACIÓN: 48. 7 ml + 20. 8 ml + 1. 3 ml =71 ml totales menos 51 ml de sol total Real indicada = 20 ml (que son con los que se purga el equipo). nota: ( a la cifra resultante de los excedentes mayor en decimales se eleva a la siguiente cifra (20. 8 ml se eleva a 21 ml).

CALCULO PARA SOLUCIONES HIPEROSMOLARES • G. hiper arriba. Osmos. Impulso Son soluciones que ejercen una presión osmótica más elevada que la otra (se considera el plasma normal). • FÓRMULA: PASO 1 SOL DE MENOR CONCENTRACIÓN - SOL DE MAYORCONCENTRACIÓ = CONSTANTE CANTIDAD DESEADA FÓRMULA : PASO 2 SOL MENOR CONCENTRACIÓN – CANTIDAD DESEADA= CANT DE DEXTRABOT CONSTANTE NECESARIA

CALCULO PARA SOLUCIONES HIPEROSMOLARES • • EJEMPLO Solución glucosada 20 % 500 ml + Dextrabot 25 mg (presentación 50 ml) PASO 1 Sg 10% - 50 ml= 40 ml= 0. 08 (constante) 500 ml • PASO 2 • SG 10% - 20% = 10 = 125 ML 0. 08 • 500 DE UNA SOLUCIÓN ML SE LE TIRAN 125 ML Y SE LE AGREGA 25 ML DE DEXTRABOTT PARA QUEDE LA SOLUCION AL 20 %.

PREPARACIÓN DE SOLUCIONES INTRAVENOSAS A DOSIS ½, ¾, DOBLE . • DOBLE esta soluciones se preparara si es al doble lo doble de cada elemento de la solución indicada. • DOSIS ½: se prepara la solución indicada más la mitad de cada componente que la conforman. • DOSIS ¾: se prepara la solución indicada más las ¾ partes de cada elemento que la compone.

PREPARACIÓN DE SOLUCIONES INTRAVENOSAS A DOSIS ½, ¾, DOBLE . • EJEMPLO: SOLUCIÓN GLUCOSA 5% 60 ML + SOLUCIÓN FISIOLÓGICA 20 ML + KCL 2 MEQ = 81 ML. • DOBLE: SG 5% 120 ML + S FIS 40 ML + KCL 4 Meq = TOTAL 162 ML SE PURGA A DEJAR LA SOLUCIÓN CON VOLUMEN REAL DE LA INDICACIÓN INICIAL (81 ML) • DOSIS ½: SG 5% 90 ML + S FIS 30 ML + KCL 3 Meq = 121. 5 ML Y SE PURGA A DEJAR LOS 81 ML DE VOLÚMEN INICIAL. • DOSIS ¾: SG 5% 75 ML + S FIS 25 ML + KCL 2. 5 Meq = 101. 2 ML Y SE PURGA A DEJAR LOS 81 ML DEL VOLÚMEN INICIAL

LUCHA MUY DURAMENTE DA LO MEJOR DE TI. . HAZ LO CORRECTO DEJARAS HUELLA A TU PASO… Y MARCARAS LA DIFERENCIA