MANEJO DE LAS INMUNODEFICIENCIAS PRIMARIAS EN EL LABORATORIO

MANEJO DE LAS INMUNODEFICIENCIAS PRIMARIAS EN EL LABORATORIO

Introducción • Las inmunodeficiencias primarias (IDP) son enfermedades o deficiencias del sistema inmunitario, de carácter hereditario, por lo general autosómicas recesivas, aunque también ligadas al cromosoma X, en las que existe una alteración de los mecanismos en la respuesta inmunológica. • Afectan a la inmunidad celular ( linfocitos T ) y humoral ( linfocitos B ) o mecanismos no específicos ( células fagocíticas, citocinas, proteínas del Complemento etc. )

Introducción • Esto origina predisposición a infecciones, pero también a procesos autoinmunes. • Muchas IDP tienen manifestaciones en sangre periférica, fundamentalmente citopenias. • Lactantes < 1 año, con linfocitos < 2. 500 – 3. 000 /μL , puede ser signo de IDP.

Introducción • Las manifestaciones son muy variadas, dependiendo del déficit inmunológico. Se suelen presentar a los pocos meses de vida o en la primera infancia, también en adultos. • Los defectos que implican alteraciones en la función de los L B, dan lugar a infecciones pulmonares recurrentes; también meningitis crónica y giardiasis intestinal. • Los L T, son esenciales para el control de la enfermedad viral y fúngica, también tienen función de colaboración con L B, mediante liberación de citocinas, que promueve una respuesta inmune adecuada y efectiva.

Introducción • Desordenes como Inmunodeficiencia Combinada Severa ( IDCS ) de L T y L B, da como resultado, susceptibilidad aumentada a patógenos virales, fúngicos y bacterianos. • Otros signos o síntomas más difíciles de relacionar con IDP: - úlceras o aftas gigantes de mucosas. - rasgos dismórficos faciales. - alteraciones cutáneas o del pelo ( albinismo, vitíligo, manchas hipercrómicas, petequias, telangiectasias, alopecia ) eritrodermias y dermatitis.

Prevalencia de IDP

Clasificación de las IDP • Ligadas a X. • Autosómicas recesivas, asociadas a Inmunodeficiencia Combinada Severa ( IDCS ). • Autosómicas recesivas, no asociadas a ( IDCS ).
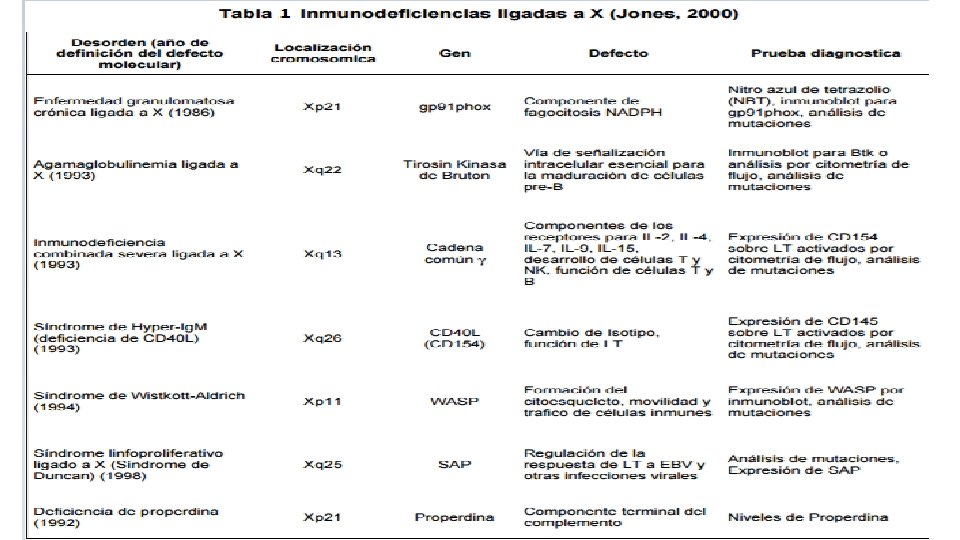
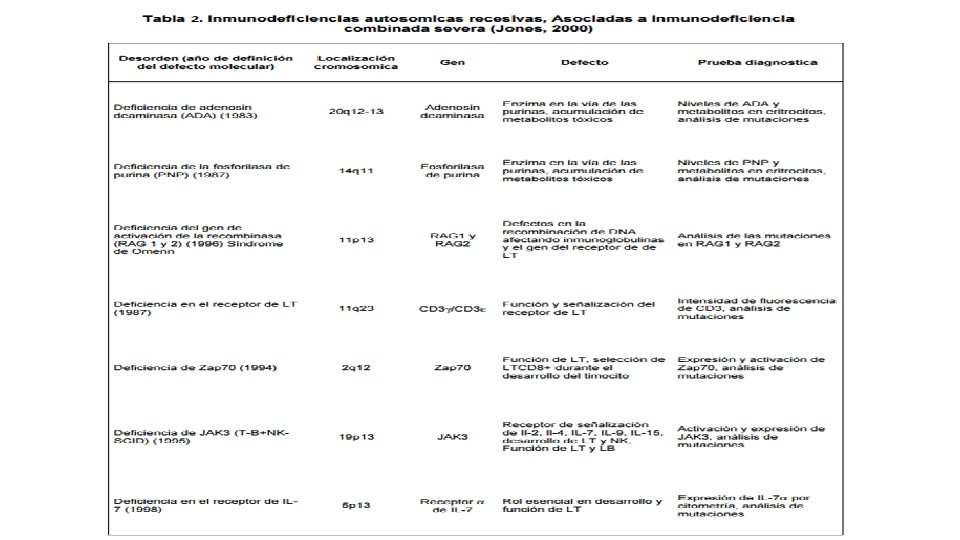
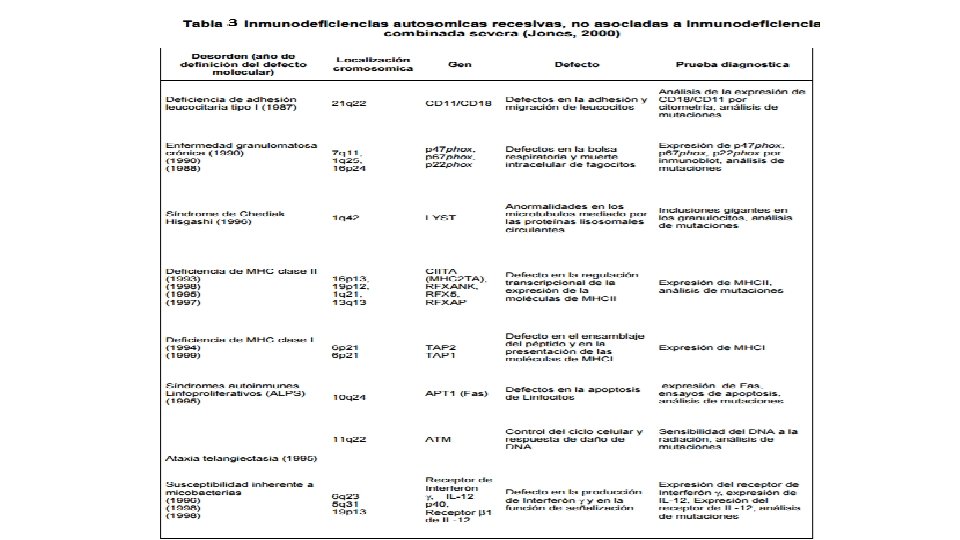

DIAGNOSTICO DE IDP • Debe estar centrado en el paciente, solicitando paso a paso las Pruebas de laboratorio, teniendo en cuenta la historia personal y familiar y la exploración física. • El escrutinio inicial incluye: Hemograma, Frotis de sangre periférica, velocidad de sedimentación globular, recuento plaquetario. Bioquímica general. Electroforesis de proteínas plasmáticas. Poblaciones de linfocitos T, B y NK.
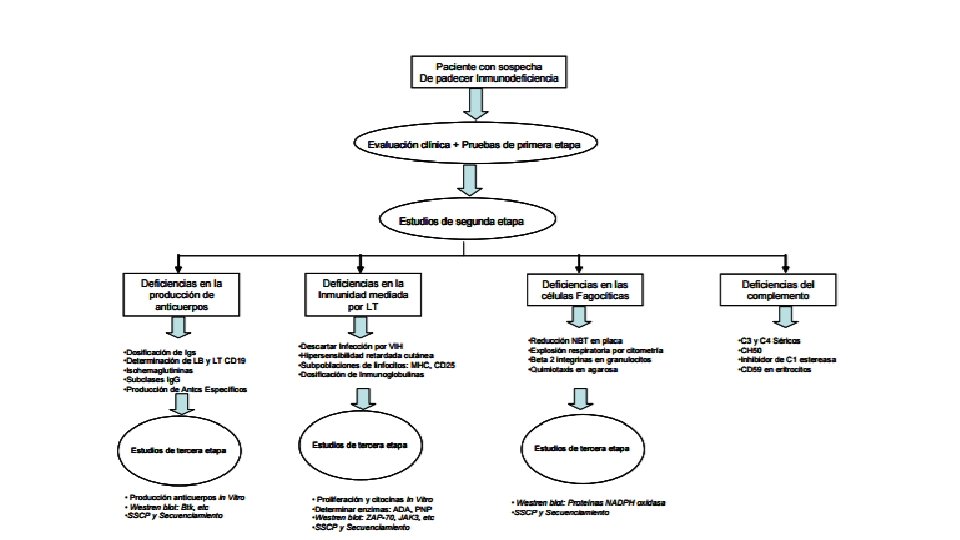

PRUEBAS DE PRIMERA ETAPA • Cuadro hemático con frotis de sangre periférica Recuento plaquetario Velocidad de sedimentación La sangre constituye la mejor ventana al sistema inmunitario y muchas IDP tienen expresión en sangre periférica. El FSP es una herramienta de gran valor para la orientación diagnóstica inicial de una IDP. Las citopenias que afectan a una o más de las tres series, son frecuentes en IDP. Síndrome de Di George, deficiencias de ADA (adenosindeaminasa) o nucleotidofosforilasa, pueden cursar con citopenias. En el Síndrome de Wiskott-Aldrich, hay trombocitopenia, con plaquetas de pequeño tamaño.
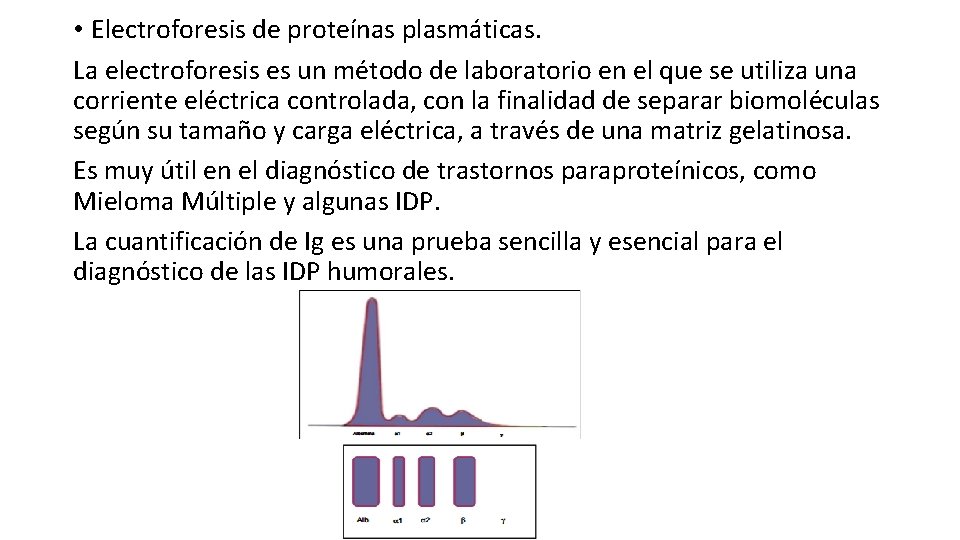
• Electroforesis de proteínas plasmáticas. La electroforesis es un método de laboratorio en el que se utiliza una corriente eléctrica controlada, con la finalidad de separar biomoléculas según su tamaño y carga eléctrica, a través de una matriz gelatinosa. Es muy útil en el diagnóstico de trastornos paraproteínicos, como Mieloma Múltiple y algunas IDP. La cuantificación de Ig es una prueba sencilla y esencial para el diagnóstico de las IDP humorales.

PRUEBAS DE SEGUNDA ETAPA • A) PRUEBAS PARA MEDIR LA PRODUCCIÓN DE ANTICUERPOS -A-1 Cuantificación de los niveles séricos de Ig: Ig. G; Ig. M; Ig. A. (Turbidimetría) -A-2 Medición de subclases de Ig. G: Ig. G 1; Ig. G 2; Ig. G 3; Ig. G 4. (Nefelometría) -A-3 Isohemaglutininas (Ig. M) -A-4 Producción de Ac Ig. G específicos (ELISA, Inmunoenzimoensayo) -A-5 Cuantificación de LB. CD 19, CD 20, HLA-DR (Citometría de Flujo)

A-1 Cuantificación de los niveles séricos de Ig: Ig. G; Ig. M; Ig. A. • TURBIDIMETRIA Es la medición de la luz transmitida a través de una suspensión. Tiene la ventaja de permitir la valorización cuantitativa, sin separar el producto, de la solución. Las mediciones pueden efectuarse con cualquier espectrofotómetro.

A-2 Medición de subclases de Ig G • Las Ig se han agrupado en diferentes subclases, de acuerdo a diferencias en las cadenas pesadas. La Ig. G se subdivide en: Ig. G 1; Ig. G 2; Ig. G 3; Ig. G 4. La Ig. G 2 es el isotipo de Ac predominante en respuesta a determinados polisacáridos, niveles disminuidos de Ig. G 2 dan como resultado una menor respuesta a bacterias encapsuladas. Su cuantificación en el laboratorio es por Nefelometría.

Nefelometría • La Nefelometría se utiliza para medir las reacciones Ag-Ac. La determinación de los Ag, se lleva acabo por la adición de cantidades constantes de Ac específico, a diversas cantidades de Ag. Los reactantes resultantes de Ag-Ac, se colocan en un recipiente, bajo un rayo de luz y el grado de dispersión de la luz, se mide en una célula fotoeléctrica como densidad óptica. Permite la valoración cuantitativa, se compara la intensidad del rayo emergente, con la del incidente; mide la luz dispersada con un ángulo entre ( 15º - 90º ). Se usa para diluciones más diluidas que la Turbidimetría y tiene mayor sensibilidad y exactitud.

A-3 Isohemaglutininas • Dependiendo de la edad del paciente y su grupo sanguíneo, es posible medir la presencia de Ac naturales o Isohemaglutininas anti-A y anti-B. Estos Ac. Son predominantemente de clase Ig. M dirigidos contra Ag del grupo sanguíneo. Es una prueba útil en casos de inmunodeficiencias con falla selectiva para la formación de Ig. M por ejemplo el síndrome de Wis. Kott Aldrich.
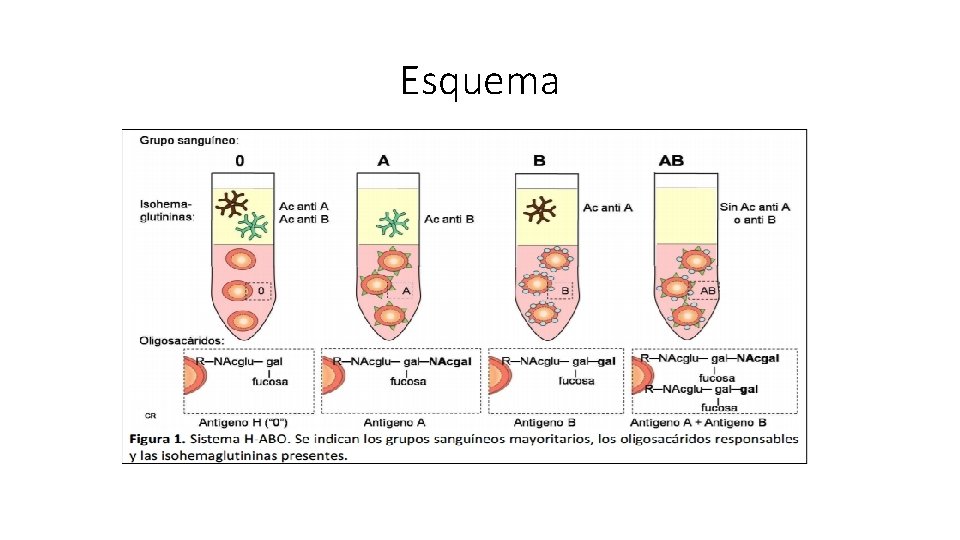
Esquema

A-4 Producción de Ac Ig. G específicos. ( ELISAInmunoensayo) • La identificación Ag-Ac, se hace mediante el empleo de enzimas, unidas al Ag o al Ac. La enzima se detecta al añadir el sustrato correspondiente y observar los cambios que en éste se producen. Generalmente se utilizan enzimas que inducen en el sustrato, cambios de coloración, con lo cual se detecta fácilmente por colorimetría, la presencia de la enzima y por lo tanto, del complejo Ag-Ac. Como enzimas se suelen utilizar: peroxidasa, beta-galactosidasa o glucosaoxidasa. Esta técnica permite la detección de sustancias a muy bajas concentraciones.

A-5 Cuantificación de LB. (CF) • Los LB expresan diversas moléculas de superficie que se pueden detectar por medio de Ac monoclonales. Los LB maduros expresan CD 19, CD 20 y HLA-DR. Los LB inmaduros pueden expresar moléculas adicionales como CD 10. • Los Ac monoclonales marcados con fluorocromos se utilizan para detectar células que tienen los marcadores de LB. La cuantificación de los LB se realiza mediante Citometría de Flujo.

Citometría de flujo • Es una técnica de análisis celular multiparamétrico. Se basa en hacer pasar una suspensión de partículas (células) alineadas por delante de un haz de laser focalizado. El impacto de cada célula con el rayo de luz produce señales que corresponden a diferentes parámetros de la célula y que son recogidos por distintos detectores. -Parámetros relacionados con características intrínsecas de la célula, como su tamaño y la complejidad de su núcleo y citoplasma. -Parámetros relacionados con características antigénicas de cada célula (Inmunofenotipo). Por lo tanto, la CMF es capaz de identificar una célula por medio de sus características antigénicas y/o por sus características morfológicas.


PRUEBAS DE SEGUNDA ETAPA • B ) PRUEBAS PARA MEDIR LA INMUNIDAD MEDIADA POR LT • B-1 Hipersensibilidad cutánea retardada • B-2 Subpoblaciones de LT ( CF ) • B-3 Cuantificación de moléculas de superficie ( CF ) • B-4 Citotoxicidad mediada por LT CD 8+ y NK • B-5 Cuantificación de células NK ( CF )

B-1 Hipersensibilidad cutánea retardada • La prueba de hipersensibilidad cutánea retardada es considerada como una correlación In Vivo, de la inmunidad mediada por células, puede ser usada como método de monitoreo para defectos en la inmunidad mediada por células. • Consiste en la inoculación intracutánea, de una cantidad definida, de un Ag conocido como PPD ( derivado proteico purificado ) o Candida albicans. El sitio de la inyección se observa entre 48 y 72 horas, observando la aparición de una pápula, si esta pápula tiene un diámetro mayor de 2 mm, se considera positiva. • Los individuos con inmunodeficiencia presentan resultados negativos.

B-2 Subpoblaciones de LT ( CF ) • Los Linfocitos T poseen dos subgrupos que pueden distinguirse por dos proteínas de superficie, específicas para cada uno. Los L T ayudadores expresan en su superficie la molécula CD 4+. Son cooperadores de la proliferación, maduración y función inmunitaria de otros tipos celulares mediante la secreción de citocínas. Los L T citotóxicos expresan CD 8+. Son importantes en la defensa contra infecciones virales, células neoplásicas y células alogénicas en trasplante de órganos. Aproximadamente el 70% de los L T de sangre periférica son CD 4+ o CD 8+

B-3 Cuantificación de moléculas de superficie ( CF ) • Los L T expresan en su superficie diversas moléculas como las Caherinas, Inmunoglobulinas, Integrinas, Selectinas y Proteoglicano. También moléculas coestimuladoras como el CD 28. Todas estas moléculas pueden ser identificadas mediante ( CF ), siempre que exista el Ac monoclonal específico para cada una.

B-4 Citotoxicidad mediada por LT CD 8+ y NK • La citotoxicidad celular consiste en la capacidad para interaccionar con otras células y destruirlas. Este mecanismo de defensa interviene en la defensa frente a infecciones víricas y células neoplásicas, así como en la destrucción de células alogénicas en trasplante de órganos. Se consideran especializados en dicha función a los L T CD 8+ y a las células natural killer ( NK ).

B-5 Cuantificación de células NK ( CF ) • Las células NK son un componente importante del sistema inmune innato, son capaces de lisar las células infectadas por virus o células tumorales y son la fuente de una gran variedad de citocinas. Cuando se presentan defectos en estas células, se incrementa la posibilidad de presentar mayor susceptibilidad a infecciones virales. La cuantificación de las células NK se realiza por ( CF ), estas células coexpresan en su superficie las moléculas CD 16/CD 56, por lo que es sencilla su cuantificación en sangre periférica.

PRUEBAS DE SEGUNDA ETAPA • C ) PRUEBAS PARA MEDIR LA FUNCIÓN DE LAS CÉLULAS FAGOCÍTICAS ( Neutrófilos ) La función principal de los neutrófilos es la defensa contra infecciones ocasionadas por microorganísmos. (fagocitosis ) C-1 Reducción de NBT ( azul de tetrazolio nitrado) C-2 Medición de radicales libres de oxígeno C-3 Quimiotaxis C-4 Fagocitosis y actividad bactericida de los neutrófilos C-5 Adherencia

C-1 Reducción de NBT ( azul de tetrazolio nitrado ) • La muerte de un microorganismo después de su fagocitosis se debe a la producción de iones superóxido, que ayudan a la destrucción del mismo. En algunas patologías esto no ocurre, por lo que la destrucción no se lleva a cabo correctamente. • El ( NBT ) es un compuesto claro, amarillo y soluble en agua, que al reducirse, se vuelve azul oscuro. Es una prueba útil para analizar la integridad metabólica de los neutrófilos. La falta de reducción se asocia con enfermedad granulomatosa crónica.

C-2 Medición de radicales libres de oxígeno • El desbalance en la producción de especies reactivas de oxígeno y la defensa antioxidante provoca un daño oxidativo, conocido como estrés oxidativo, que lleva a una gran cantidad de cambios fisiológicos y bioquímicos, los cuales provocan el deterioro y muerte celular. Se puede medir este tipo de daño mediante métodos indirectos: Espectrometría UV. Cromatografía líquida de alta presión.

C-3 Quimiotaxis • El movimiento de los neutrófilos hacia diversos estímulos quimiotácticos se cuantifican mediante el uso de la cámara de boyden. Las células por analizar se colocan en la parte superior y se separan de la cámara inferior que contiene la sustancia quimiotáctica mediante una membrana de filtro de poro pequeño. Los neutrófilos pueden atravesar el filtro, pero se atrapan en el tránsito hacia la membrana y después de un periodo de incubación, el filtro se tiñe y se observa al microscopio. • C-4 Fagocitosis • C-5 Adherencia Mediados por una serie de citocinas y factores químicos que los inducen a llevar a cabo el proceso de fagocitosis.

PRUEBAS DE SEGUNDA ETAPA • D ) PRUEBAS PARA MEDIR EL SISTEMA DEL COMPLEMENTO El sistema del complemento esta formado por más de 40 glicoproteínas que trabajan en cascada y existen en el plasma en forma de precursores. D-1 CH 50. Cuando el complemento es activado por los Ac que se encuentran fijados sobre la superficie de los glóbulos rojos, estos son lisados y la hemoglobina es liberada. Los resultados son expresados en base a la última dilución del suero que causa la lisis del 50% de las células. D-2 Cuantificación de C 3 y C 4. ( Turbidimetría) D-3 Inhibidor de C 1 esterasa. D-4 CD 59 en eritrocitos. ( CF )

PRUEBAS DE TERCERA ETAPA • A) Pruebas para medir la producción de Anticuerpos. A-1 In Vitro. La activación de los LB por Ag o mitógenos genera cantidades pequeñas pero detectables de Ig policlonales (ELISA) A-2 Western blot para BTK; BLNK; NEMO; están relacionadas con la maduración y proliferación del linfocito B y se pueden determinar por Western Blot.

PRUEBAS DE TERCERA ETAPA A-3 Análisis de polimorfismos conformacionales de cadena sencilla (SSCP). Detección de mutaciones: el DNA es separado en dos hebras y por electroforesis, si existe alguna mutación, migrará de manera diferente. Estas mutaciones son detectadas como bandas nuevas, ya sea por tinción de plata o por el uso de primers fluorescentes que posteriormente se analizaran en un secuenciador automatizado.

Western blot • Western blot es una técnica analítica para identificar proteínas específicas en una mezcla compleja de proteínas. Consta de tres etapas: 1 - Separación por tamaños mediante electroforesis en gel. 2 - Transferencia a un soporte sólido (membrana de nitrocelulosa) por difusión o por electrotransferencia. Bloqueo de los lugares que han quedado libres (con albúmina) 3 - Visualización mediante la marcación de proteínas con anticuerpos. Se detecta la unión Ag-Ac por actividad enzimática o por fluorescencia.

PRUEBAS DE TERCERA ETAPA • B) Pruebas para medir la inmunidad mediada por LT B-1 Linfoproliferación con mitógenos. Se cultivan linfocitos en microplaca, con fitohemaglutinina, se añaden mitógenos a distintas concentraciones. Se añade Timidina tritiada, que es un precursor de nucleósido que se incorpora en el DNA que se acaba de sintetizar. Se determina la cantidad de Timidina incorporada al DNA en un tiempo determinado, que es relativa a la velocidad de síntesis del DNA y se determina por la cuenta de centelleos en un espectrofotómetro de líquido de centelleo.

PRUEBAS DE TERCERA ETAPA • B-2 Cuantificación de la producción de citocinas in vitro. (CF) • B-3 Western blot para ZAP-70; JAK-3 y STAT-1 Estas proteínas están alteradas en la Inmunodeficiencia combinada severa ( IDCS ) por lo que su análisis es muy importante en el diagnóstico de esta patología. Se cuantifica utilizando Ac monoclonales anti-ZAP-70; JAK-3 y STAT-1. • C ) Pruebas para medir la función de células fagocíticas Western blot para proteínas del sistema NADPHoxidasa.

GRACIAS
- Slides: 41