Malign pemna buky Tyto procesy jsou u vych

Maligní přeměna buňky Ø Tyto procesy jsou u vyšších organismů regulovány mnohastupňovými mechanismy, které zahrnují intracelulární a extracelulární kontrolní dráhy. Ø Proces onkogeneze na buněčné úrovni je úzce spjat s kontrolou buněčné proliferace, diferenciace a programované smrti buněk. Ø Většina, pokud ne všechny, nádorové buňky obsahují mnohočetné genetické změny, které pravděpodobně podporují proces tumorigeneze právě poškozováním důležitých kontrolních drah.

U nádorových onemocnění se takřka pravidelně setkáváme se dvěma základními typy genetických poškození Ø Prvním typem poškození jsou poruchy jejímž cílem jsou protoonkogeny. Ø Tato poškození jsou zodpovědné za vyvolání stimulačních účinků na růst buněk Ø Druhým typem poškození jsou poruchy, se kterými se setkáváme u antionkogenů. Ø Poruchy ovlivňující antionkogeny jsou zodpovědné za ztrátu jejich inhibiční funkce.

ONKOGENY – definice Genetická informace inkorporovaná v genomu hostitelské buňky (protoonkogen = potenciální onkogen), která po své aktivaci (onkogen) je schopna vyvolat její neoplastickou transformaci. Protoonkogen může být aktivován bodovou mutací, amplifikací, translokací (delece, přestavba chromosomu), transdukcí, inzerční mutagenezí.

Aktivace onkogenů 1. 2. 3. 4. Změny ve struktuře genu mající za následek syntézu abnormálního genového produktu (onkoproteinu), který má změněnou funkci. Změny ovlivňující regulaci genové exprese, které vedou ke zvýšené nebo nepřiměřené produkci strukturně nezměněné formy normálního proteinu podporujícího růst. a) Inserce retrovirů do buněčného genomu ovlivňuje kontrolu buněčných genů silnými retrovirovými promotory což má za následek konstitutivní produkci normálního proteinu. b) Klasickým případem mutační aktivace protoonkogenů jsou bodové mutace ve specifických kodonech genu ras, se kterými se setkáváme u mnoha typů nádorových onemocnění. Genové amplifikace protoonkogenů jsou zodpovědné za zvýšení produkci DNA matrice pro tvorbu RNA což má za následek nesprávnou expresi kódovaných proteinů. Chromosomální translokace protoonkogenů mohou mít za následek abnormální transkripční regulaci postižených genů nebo vznik zkrácených nebo fúzovaných genů s abnormální funkcí.

ONKOGENY – aktivace bodovou mutací Bodová mutace – prostá záměna nukleotidu v sekvenci NA vedoucí ke změně v pořadí aminokyselin produktu. Nejlépe demonstrováno na genech rodiny ras, kde bodová mutace má vliv na vazbu proteinových produktů genů ras k proteinu GAP (GTPase activating protein).

ONKOGENY – aktivace amplifikací Amplifikace – zmnožení genu (někdy zaměňováno se zvýšenou expresí genu – overexpresí). Důsledky jsou podobné. Příčiny nejasné. Protože amplifikace bývá spojena se zřetelnými chromosomálními abnormitami a strukturálními alteracemi genů, nevylučuje se, že příčinami mohou být mnohočetné mutace a genová přeskupení (rearrangement). Amplifikace byla prokázána v četných nádorech. Příkladem je amplifikace N-myc v neuroblastomu nebo L-myc v malobuněčném karcinomu plic.

ONKOGENY – aktivace translokací Translokace – přesuny, mohou mít vli buď na expresi nebo funkci protoonkogenů. Např. při translokaci během níž dojde k připojení c-myc či c-bcl-2 ke genům pro syntézu Ig (Burkittův lymfom, folikulární ML) nebo c-abl k oblasti bcr (break-point cluster region) (CML).

ONKOGENY – aktivace transdukcí Transdukce – implantace buněčného protoonkogenu do virového genomu. Tato inkorporace způsobuje zpravidla vysokou expresi transdukovaného genu (overexpresi) a z toho vyplývající nepříznivý vliv na buněčnou homeostázu. Jako transduktory se uplatňují zejména tzv. akutně transformující retroviry jako např. virus Rausova sarkomu.

ONKOGENY – aktivace izerční mutagenezí Inzerční mutageneze – vložení (inzerce) retrovirových promotorů a zesilovačů (enhancerů) do genomu hostitelské buňky, zpravidla do blízkosti protoonkogenu (např. c-myc nebo c-erb. B). Obvykle to vede ke vzniku nesmrtelné buněčné linie, ale nestačí to k zahájení kompletní maligní transformace.

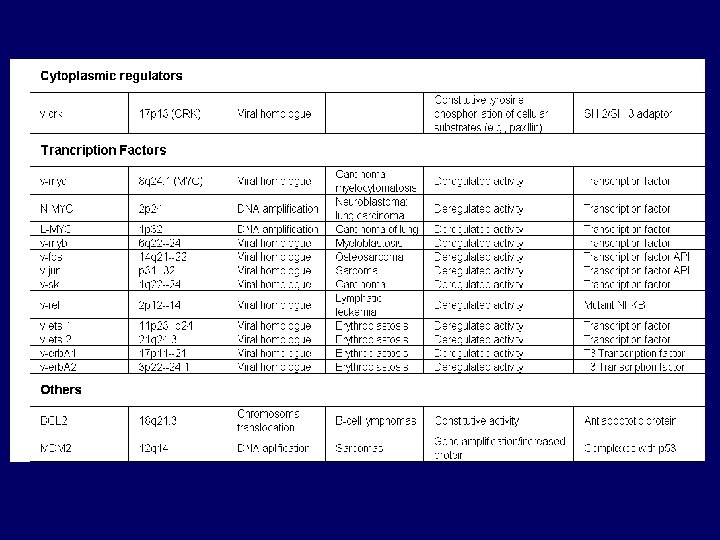
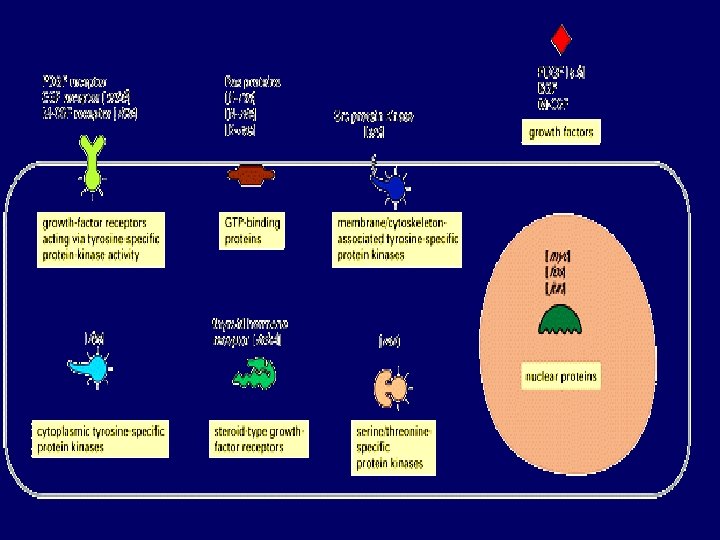
ONKOGENY – rozdělení Ø Onkogeny kódující faktory regulující transkripci myc, jun, fos. . Ø Onkogeny kódující protein-kinázy src, abl, erb. . Ø Onkogeny kódující růstové faktory int, sis. . Ø Onkogeny kódující signální transduktory ras. . Ø Onkogeny inaktivující supresorové geny E 6, E 7, mdm-2. . Ø Onkogeny blokující apoptózu bcl-2, bcl-X. . . Ø Defektní supresorové a antimetastatické geny p 53, Rb, WT 1, DCC, NF 1, APC. . nm-23. .

Onkogeny - I Ø Původní poznatky o podstatě molekulární kontroly tvorby nádorů a objevení onkogenů jsou spojeny se studiemi zabývajícími se RNA nádorovými retroviry. Ø Virové onkogeny jsou segmenty virového genomu, které vyvolávají neoplastickou buněčnou transformaci in vitro a podporují patogenézu virem indukovaných nádorů in vivo. Ø Shodné homologní sekvence byly nalezeny v genomu většiny eukaryotických buněk. Ø Tyto sekvence jsou evolučně zachovány mezi různými druhy organismů, což potvrzuje jejich důležitost pro základní buněčné funkce. Ø Homology všech těchto virových a buněčných genů majících transformační účinky a vyskytujících se v normálních buňkách se nazývají protoonkogeny.
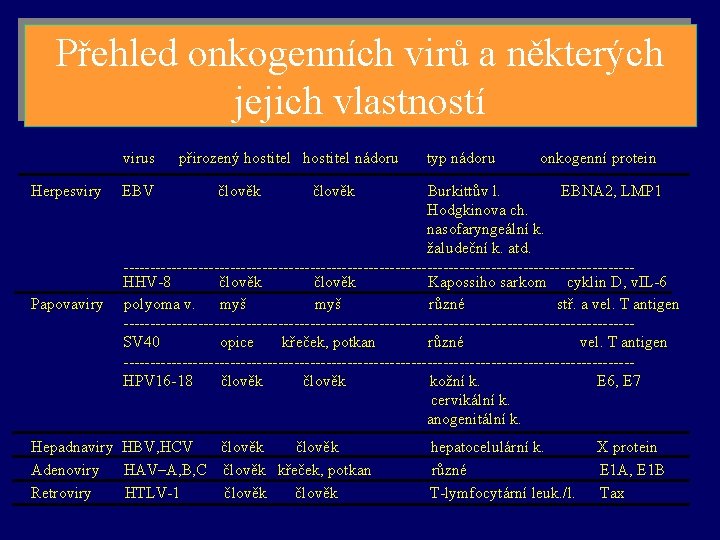
Přehled onkogenních virů a některých jejich vlastností virus přirozený hostitel nádoru typ nádoru onkogenní protein Herpesviry EBV člověk Burkittův l. EBNA 2, LMP 1 Hodgkinova ch. nasofaryngeální k. žaludeční k. atd. ------------------------------------------------ HHV-8 člověk Kapossiho sarkom cyklin D, v. IL-6 Papovaviry polyoma v. myš různé stř. a vel. T antigen ------------------------------------------------ SV 40 opice křeček, potkan různé vel. T antigen ------------------------------------------------ HPV 16 -18 člověk kožní k. E 6, E 7 cervikální k. anogenitální k. Hepadnaviry HBV, HCV člověk hepatocelulární k. X protein Adenoviry HAV–A, B, C člověk křeček, potkan různé E 1 A, E 1 B Retroviry HTLV-1 člověk T-lymfocytární leuk. /l. Tax

Onkogeny - II Ø Proteiny kódované protoonkogeny modulují celou řadu biochemických drah, které kontrolují genovou expresi, cytoskeletální architekturu a buněčný metabolismus tedy procesy zodpovědné za regulaci progrese buněčného cyklu a buněčných diferenciačních programů. Ø Obecně je známo, že proliferační kapacita se snižuje se stupněm diferenciace buněk. Ø Jinak lze říci, že zvýšená buněčná proliferace indukovaná jakýmkoliv onkogenem nemusí representovat přímý efekt na regulaci buněčného cyklu, ale může být důsledkem snížení diferenciačního potenciálu buňky. Ø Cytogenetické poruchy, které jsou zodpovědné za přeměnu normální regulační funkce protoonkogenů na jejich transformující funkci se podílejí na aktivaci onkogenů.

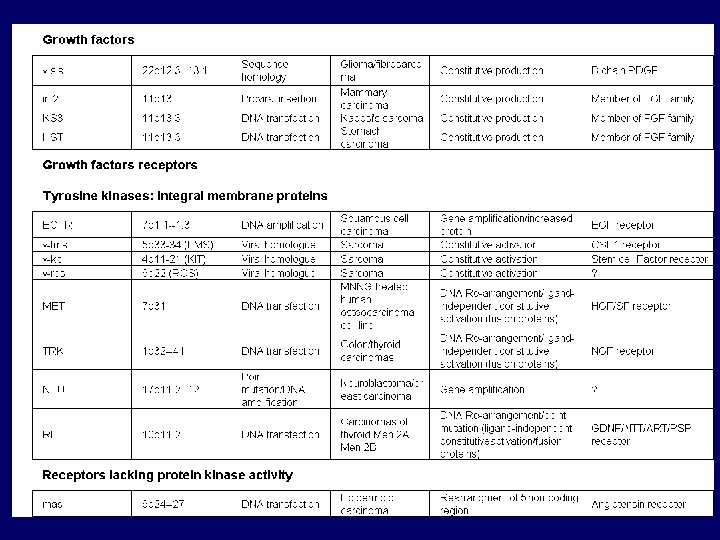
Přehled nejznámějších onkogenů – I 1. Geny pro růstové faktory jako onkogeny Růstové faktory, které stimulují proliferaci normálních buněk hrají důležitou roli při procesu maligní přeměny buňky [TGF (transforming growth factor ), se vyskytují u celé řady nádorů různorodého histogenetického původu, c-sis kóduje -řetězec PDGF (platelet-derived growth factor); produkce PDGF byla nalezena u celé řady nádorů zejména pak u astrocytomů a osteosarkomů] 2. Geny pro receptory růstových faktorů jako onkogeny Některé onkogeny byly identifikovány jako deletované nebo nepatřičně exprimované receptory růstových faktorů [Mezi nejznámější členy rodiny EGFR (epidermal growth factor receptor) patří tři geny (c-erb B 1, c-erb B 2, c-erb B 3)]; c-erb B 1 aberantně exprimován u spinocelulárního karcinomu plic a méně často u karcinomů močového měchýře, GIT a astrocytomů; c-erb B 2 (nebo c-neu) je amplifikován u vysokého procenta lidských karcinomů prsu, ovária, adenokarcinomů plic, žaludku a slinných žláz; c-erb B 3 je možno sledovat u karcinomů prsu;

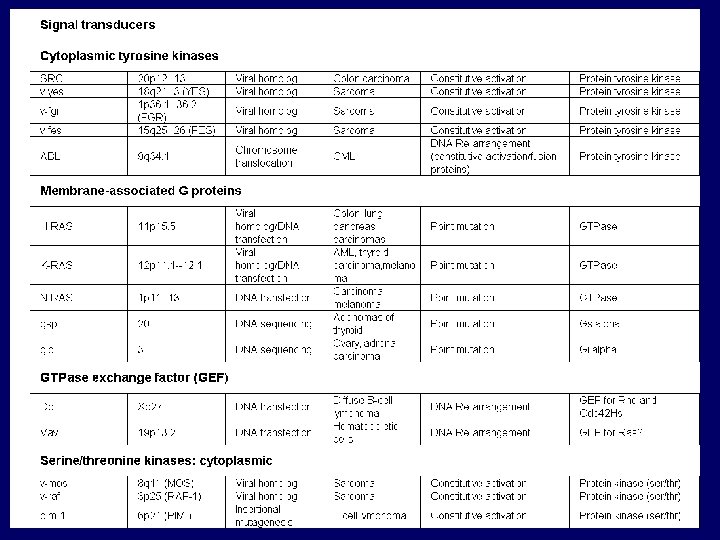
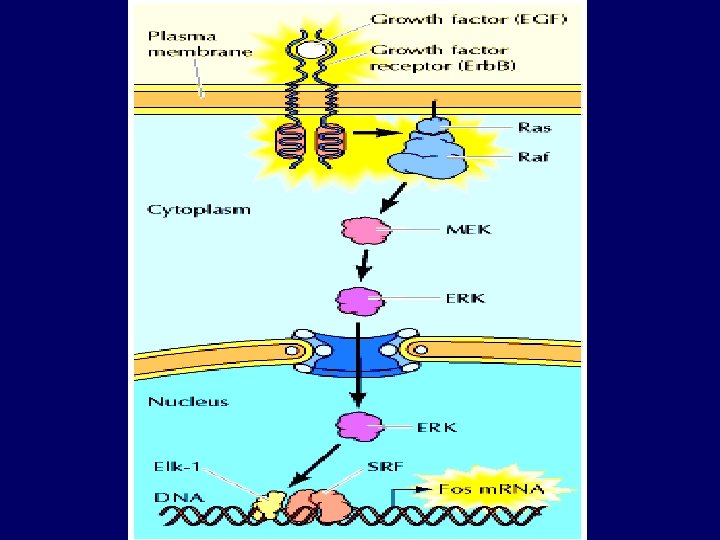
Přehled nejznámějších onkogenů – II 3. Geny pro přenašeče signálů jako onkogeny a) Onkogeny s aktivitou přenašečů signálu vázaných na membránu Tyto onkogeny můžeme rozdělit podle povahy produktů na skupinu s aktivitou tyrozin kinázovou a skupinu s aktivit GTPázovou b) Cytoplasmatické přenašeče signálů jako onkogeny Tyto onkogeny a jejich buněčné homology kódují cytoplasmické proteiny mající serin/treonin kinázovou aktivitu. 4. Jaderné transkripční faktory jako onkogeny Všechny dráhy podílející se na přenosu signálů vstupují do jádra a ovlivňují velkou skupinu genů, které řídí buňku. Tento proces (např. DNA replikace a buněčného dělení) je regulován geny, jejichž produkty jsou lokalizovány v jádře kde kontrolují transkripci genů regulujících buněčný růst.

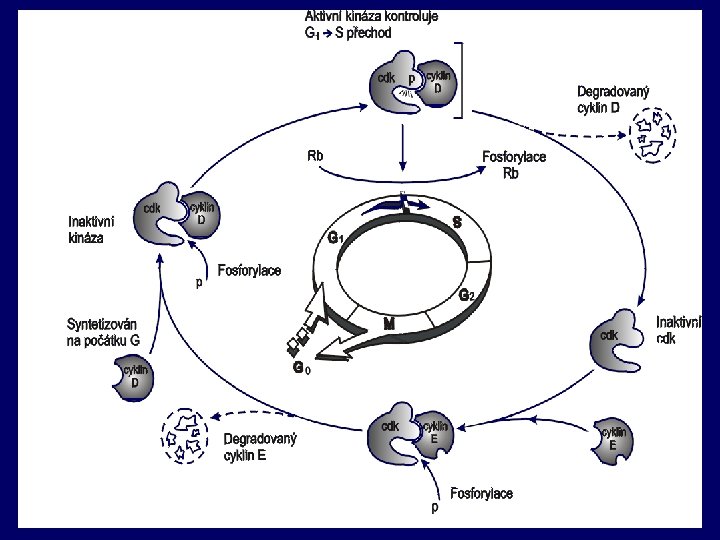
Přehled nejznámějších onkogenů – III 5. Geny pro cykliny a cyklin-dependentní kinázy (cdk) jako onkogeny Postup buněčného cyklu u savčích buněk je koordinován aktivací cyklinů a cyklin-dependentních kináz. Z těchto důvodů jsou cykliny a některé cyklin-dependentní kinázy považovány za potenciální onkogeny. Cyklin D 1 byl identifikován jako první z potenciálních onkogenů (PRAD 1) stejně jako cyklin-dependentní kináza cdk 4.
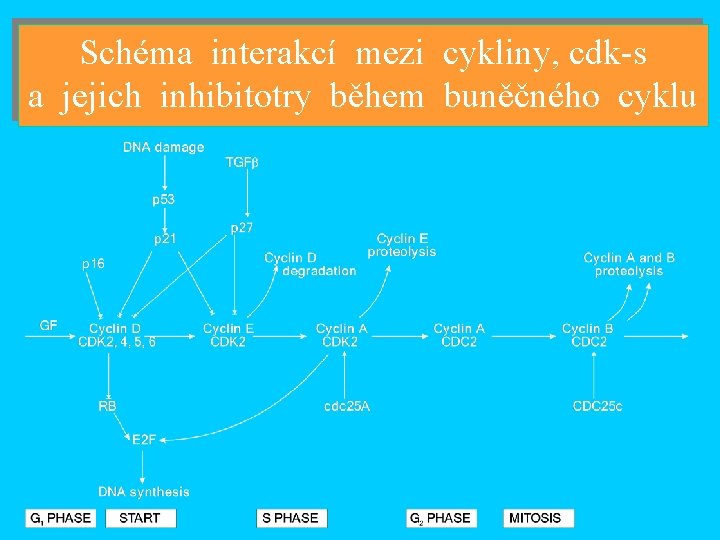
Schéma interakcí mezi cykliny, cdk-s a jejich inhibitotry během buněčného cyklu

ONKOGENY – význam v histopatologii Detekce produktů onkogenů, supresorových genů, antimetastatických genů popř. genů ovlivňujících lékovou rezistenci může přinést důležité informace o: Ø Ø onkogenních drahách vedoucích ke vzniku nádoru prognóze onemocnění nejvhodnějším způsobu terapie případné cílené genové terapii (např. antisense)

Antionkogeny Ø Nádory suprimující geny se od předchozích onkogenů odlišují tím, že kódují proteiny, které se podílejí na kontrole buněčného růstu a procesu diferenciace a ztráta jejich funkce je zodpovědná přímo za změněný fenotyp nádorové buňky. Ø Antionkogeny lze tedy definovat jako geny jejichž represe, inaktivace, dysfunkce nebo ztráta má za následek buněčnou transformaci. Ø Identifikace těchto antionkogenů byla prováděna s využitím cytogenetických studií vrozených chromosomálních změn u pacientů s nádorem, studií analýz vedoucích k lokalizaci genů zodpovědných za predispozici k tvorbě určitého typu nádorů a studií sledujících ztráty heterozygozity (LOH) nebo ztráty alel při srovnávání normální a nádorové tkáně. Ø Přes všechny doposud získané výsledky, molekulární mechanismy nádorové suprese pomocí proteinových produktů antionkogenů na buněčné úrovni, nejsou zcela prostudovány.

Retinoblastomový (Rb) gen Ø Retinoblastomový gen je prototyp nádorového antionkogenu, který byl objeven jako první a jeho inaktivace je klíčovým bodem ve vývoji celé řady lidských nádorů. Ø Je exprimován v každé buňce a existuje v různě fosforylovaných formách což závisí na stádiu buněčného cyklu. Ø V G 0 fázi protein Rb: Ø nefosforylovaná forma působí jako supresor buněčného dělení Ø hyperfosforylováná forma ztrácí tuto svoji antiproliferační – antionkogenní funkci. Ø Molekulární účinek tohoto proteinu je založen na inaktivaci proteinů důležitých proces buněčné proliferace a v jádře je závislý především na interakci hypofosforylované formy Rb s rodinou transkripčních faktorů E 2 F. Ø Z předcházejících poznatků lze uzavřít, že nepřítomnost funkčního Rb proteinu, vede k uvolnění kontrolních bodů buněčného dělení a bezprostřednímu snadnému přechodu buněk do S fáze.

Retinoblastoma Gene Family Proteins p 130 p 107 Rb 1 1139 1 1 1068 H 1 H 2 PD-A PD-B 928 Highly conserved domains include: H 1, H 2 and the large pocket subdominains, PD-A and PS-B
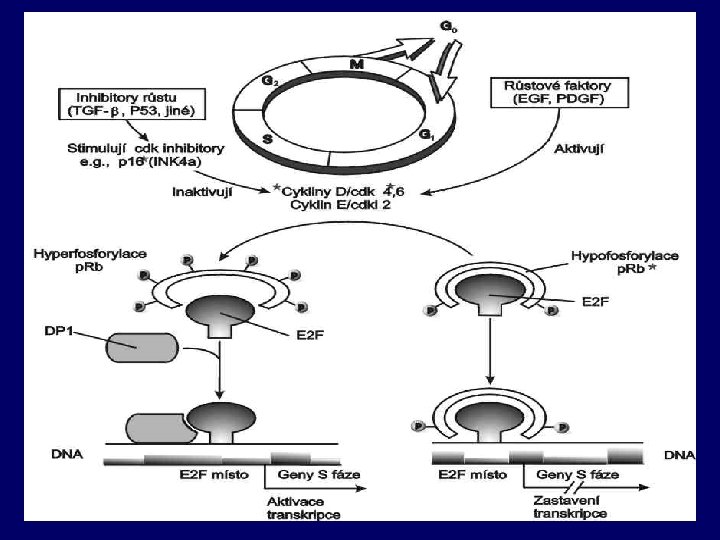

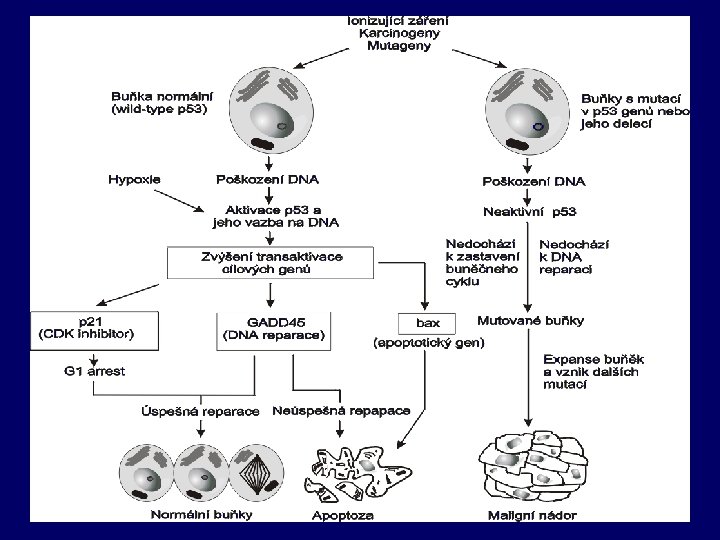
p 53 gen Ø Mezi nejčastěji se vyskytující mutace u lidských nádorů patří ty, které postihují antionkogen p 53 nacházející se na chromosomu 17 p 13. 1. Ø Tento gen kóduje jaderný fosfoprotein o molekulové hmotnosti 53 k. Da, který je negativním regulátorem přechodu G 1/S fáze buněčného dělení. Ø Inaktivace obou alel genu p 53 byla nalezena u většiny typů nádorů a zejména u karcinomů plic, tlustého střeva a prsu. Ø Současný model funkce proteinu p 53 je spojen s jeho aktivací vyvolanou poruchami v DNA, které jsou způsobeny různými typy záření, UV světlem nebo mutagenními látkami. Ø Takto akumulovaný protein se váže na specifické sekvence DNA, stimuluje expresy celé řady genů, které zprostředkovávají dva důležité efekty p 53: Ø zastavení buněčného cyklu v pozdní G 1 fázi a Ø programovanou smrt buňky.
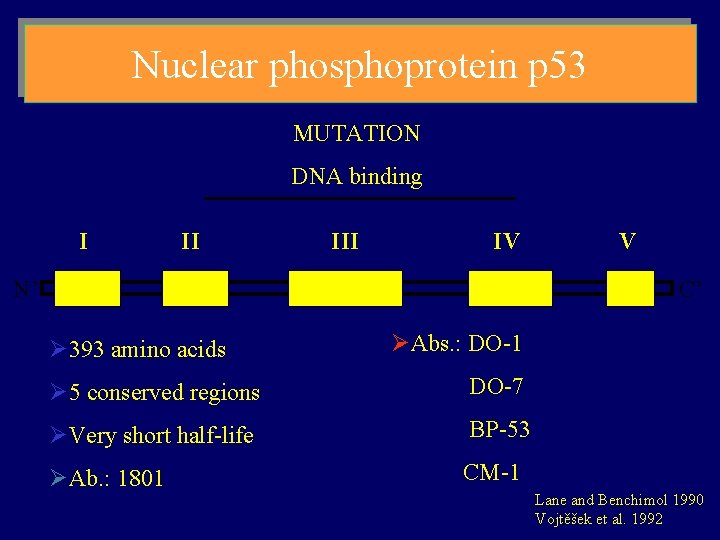
Nuclear phosphoprotein p 53 MUTATION DNA binding I II IV N’ V C’ Ø 393 amino acids ØAbs. : DO-1 Ø 5 conserved regions DO-7 ØVery short half-life BP-53 ØAb. : 1801 CM-1 Lane and Benchimol 1990 Vojtěšek et al. 1992

Anti-p 53 antibodies P + DO-1 hum, mon, bov + DO-2 hum, mov, bov P + DO-7 hum, mon, bov + DO-11 hum + DO-12 hum + DO-13 hum + DO-14 hum P + BP-53 hum, mon P + CM-1 non-spec + + 421 mou, hum + 240 mou P + + 1801 hum, mou + + 1005 hum, mou + mutant+wild + wild The end of 1994

Přehled některých produktů nádorových supresorů protein nádor funkce proteinu ____________________________________ p 53 četné typy nejčastějších nádorů transkripční faktor p. Rb retinoblastom, osteosarkom regulátor transkripce NF-1 neurofibrom, gliální nádory protein aktivující GTPázu NF-2 neurinom, meningiom cytoskeletální spoj k membráně APC karcinom tlustého střeva suspektní regulátor -cateninu WT 1 Wilmsův nádor transkripční faktor PTEN četné typy nejčastějších tumorů fosfatáza BRCA 1 karcinom mléčné žlázy, ovarií atd. oprava DNA BRCA 2 karcinom mléčné žlázy oprava DNA p 16 melanoblastom, karcinom pankreatu inhibitor cdk TSC 2 tuberózní skleróza protein aktivující GTPázu DPC 4 karcinom pankreatu signální dráha TGF
- Slides: 33