Malattie neurodegenerative Progressiva e irreversibile perdita di neuroni

Malattie neurodegenerative • Progressiva e irreversibile perdita di neuroni in specifiche aree del cervello – Ippocampo e corteccia: perdita delle capacità mnesiche e cognitive – Alzheimer – Gangli della base: anomalie nel controllo dei movimenti – M. di Parkinson, corea di Huntington – Motoneuroni spinali, corticali e bulbari: debolezza muscolare - SLA

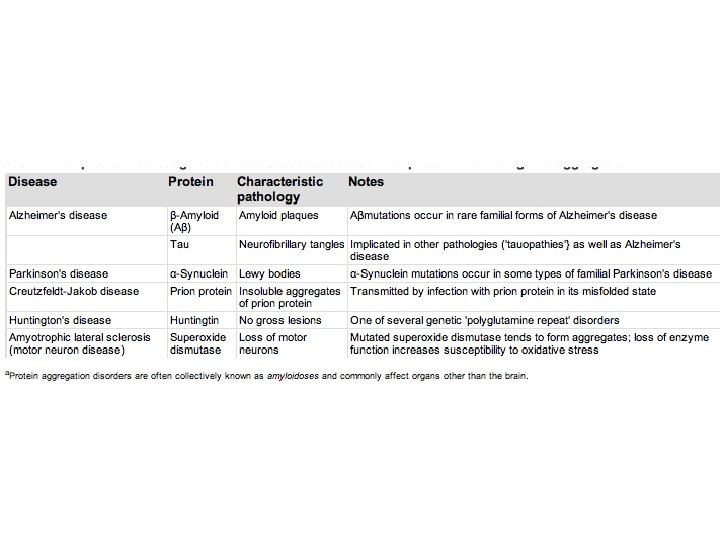
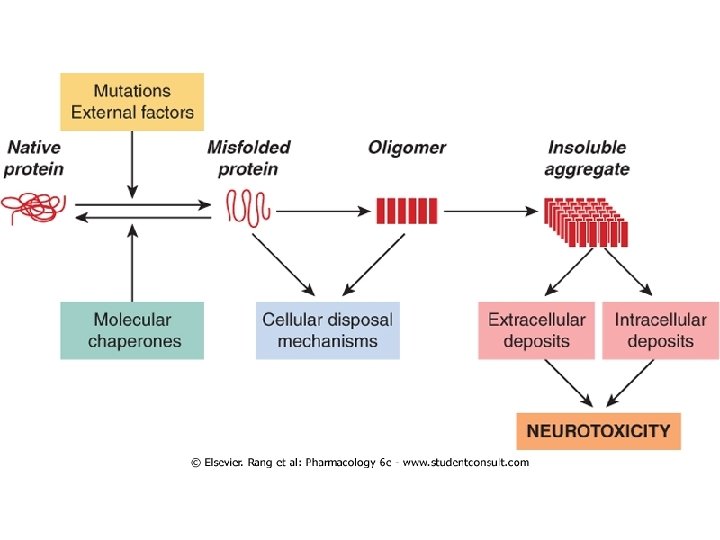
Misfolding delle proteine • Molte malattie neurodegenerative coinvolgono il ripiegamento non corretto delle forme normali o mutate di proteine fisiologiche • Le proteine ripiegate in maniera errata sono di norma rimosse da processi di degradazione intracellulare, che potrebbero essere alterate nelle malattie neurodegenerative. • Le proteine ripiegate in maniera errata tendono ad aggregarsi, dando origine all’inizio ad oligomeri solubili, i quali successivamente diventano grossi aggregati insolubili e si accumulano a livello intracellulare o extracellulare come depositi microscopici stabili e resistenti alla proteolisi. • Le proteine ripiegate in maniera errata spesso presentano residui superficiali idrofobici che favoriscono l’aggregazione e l’interazione con membrane. • I meccanismi responsabili della morte cellulare non sono stati ancora chiariti, ma molte evidenze suggeriscono che gli aggregati solubili e i depositi microscopici possano essere neurotossici.
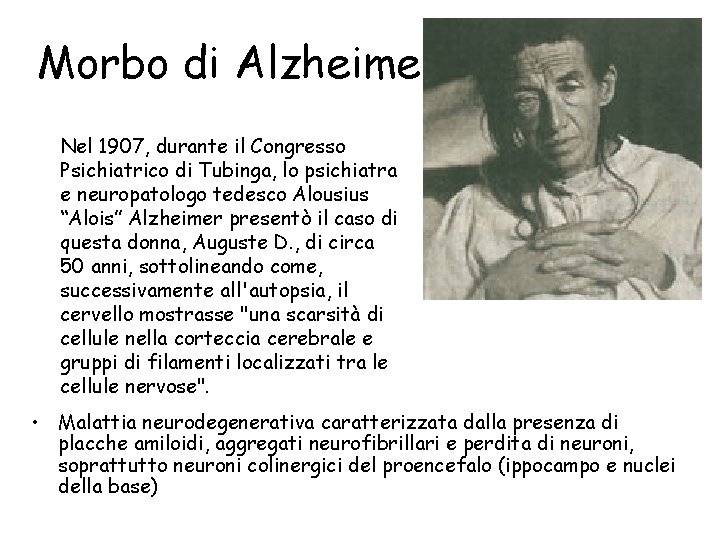
Morbo di Alzheimer Nel 1907, durante il Congresso Psichiatrico di Tubinga, lo psichiatra e neuropatologo tedesco Alousius “Alois” Alzheimer presentò il caso di questa donna, Auguste D. , di circa 50 anni, sottolineando come, successivamente all'autopsia, il cervello mostrasse "una scarsità di cellule nella corteccia cerebrale e gruppi di filamenti localizzati tra le cellule nervose". • Malattia neurodegenerativa caratterizzata dalla presenza di placche amiloidi, aggregati neurofibrillari e perdita di neuroni, soprattutto neuroni colinergici del proencefalo (ippocampo e nuclei della base)
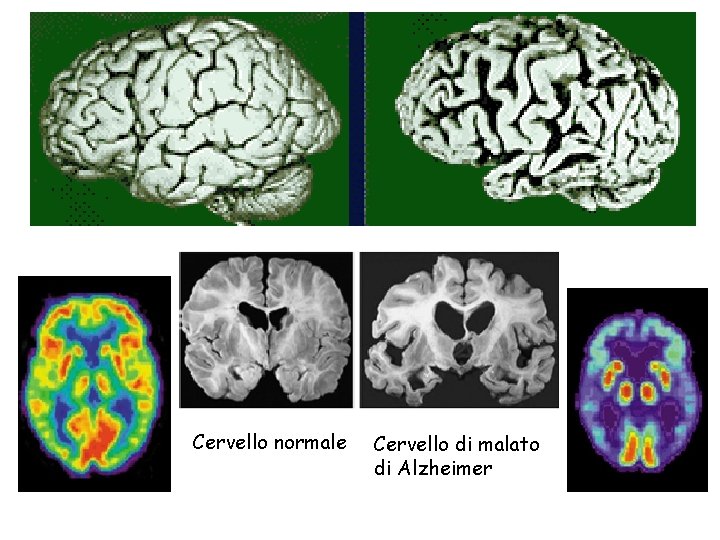
PET scan Cervello normale Cervello di malato di Alzheimer
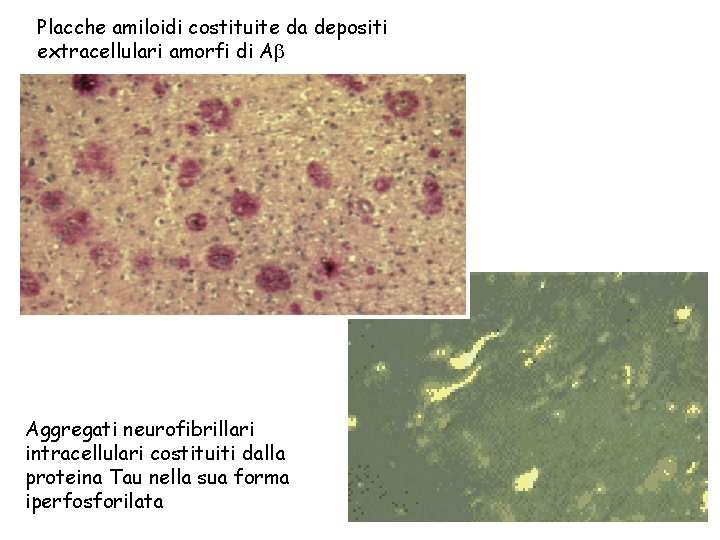
Placche amiloidi costituite da depositi extracellulari amorfi di A Aggregati neurofibrillari intracellulari costituiti dalla proteina Tau nella sua forma iperfosforilata
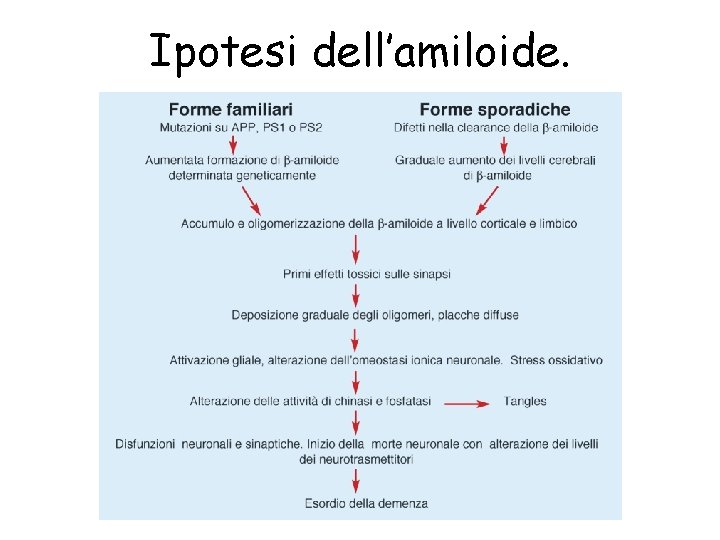
Ipotesi dell’amiloide.
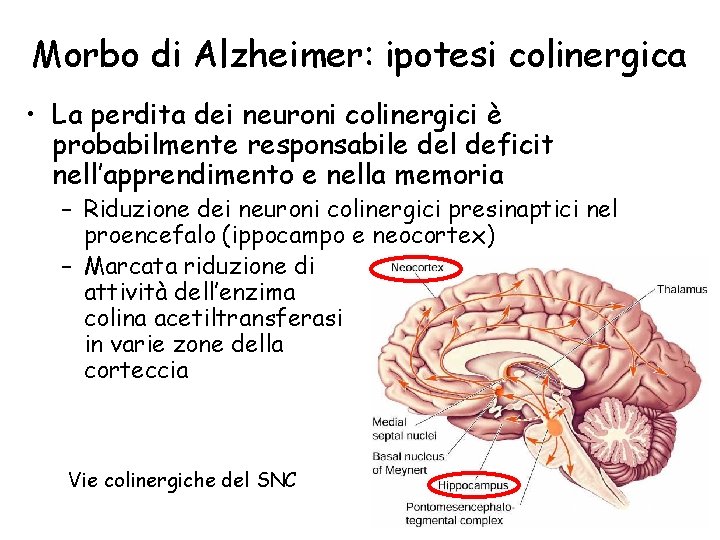
Morbo di Alzheimer: ipotesi colinergica • La perdita dei neuroni colinergici è probabilmente responsabile del deficit nell’apprendimento e nella memoria – Riduzione dei neuroni colinergici presinaptici nel proencefalo (ippocampo e neocortex) – Marcata riduzione di attività dell’enzima colina acetiltransferasi in varie zone della corteccia Vie colinergiche del SNC
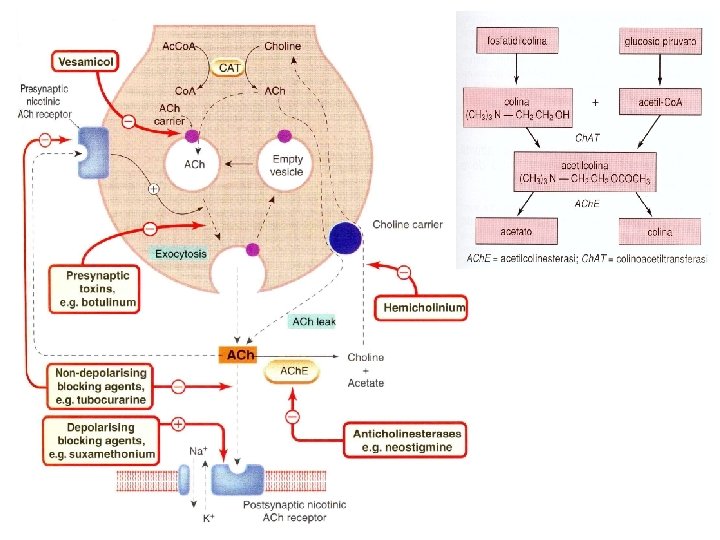

Approccio sintomatico • Mira ad aumentare i livelli dei neurotrasmettitori che sono deficitari
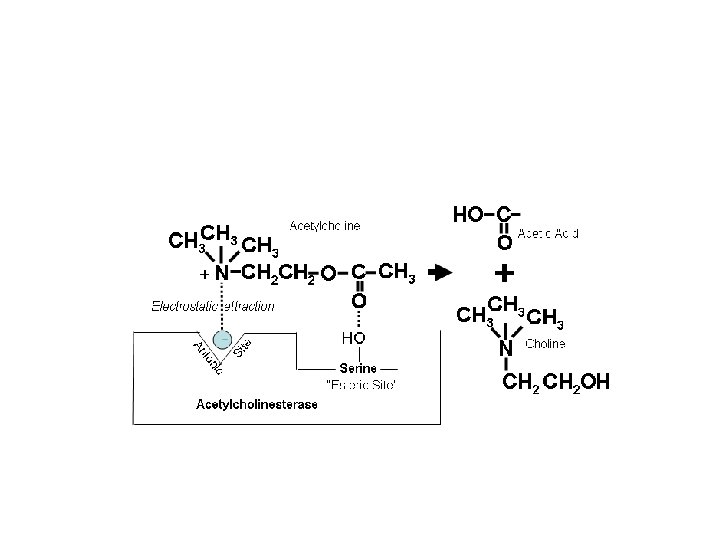
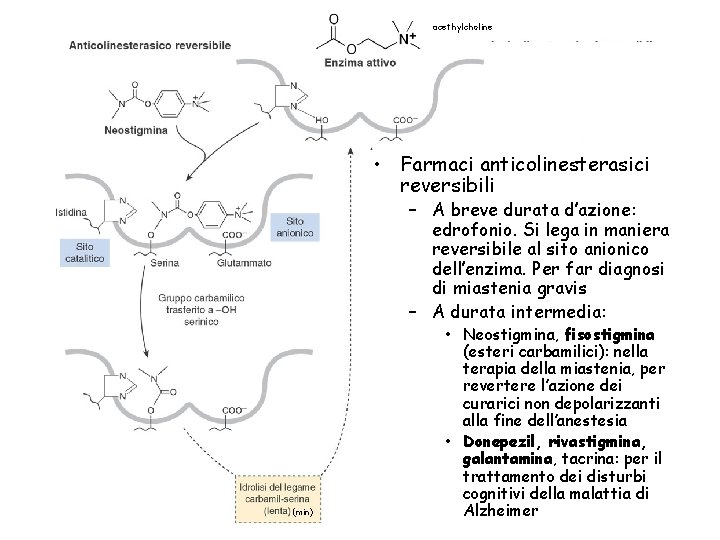
acethylcholine • Farmaci anticolinesterasici reversibili – A breve durata d’azione: edrofonio. Si lega in maniera reversibile al sito anionico dell’enzima. Per far diagnosi di miastenia gravis – A durata intermedia: (min) • Neostigmina, fisostigmina (esteri carbamilici): nella terapia della miastenia, per revertere l’azione dei curarici non depolarizzanti alla fine dell’anestesia • Donepezil, rivastigmina, galantamina, tacrina: per il trattamento dei disturbi cognitivi della malattia di Alzheimer
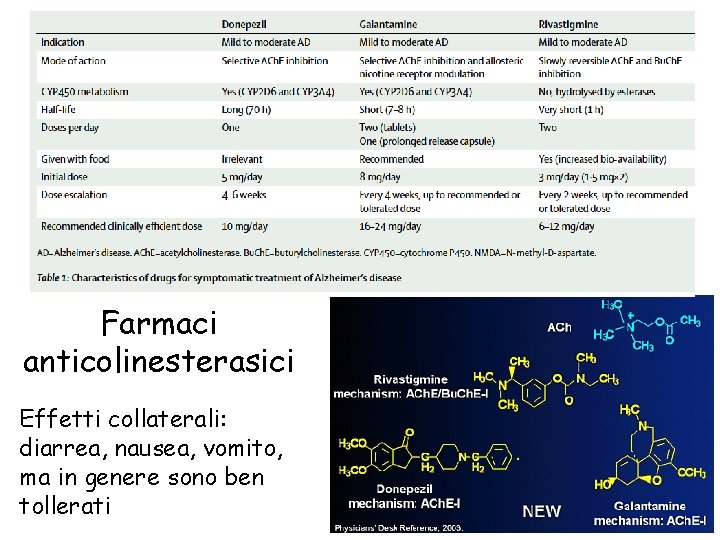
Farmaci anticolinesterasici Effetti collaterali: diarrea, nausea, vomito, ma in genere sono ben tollerati
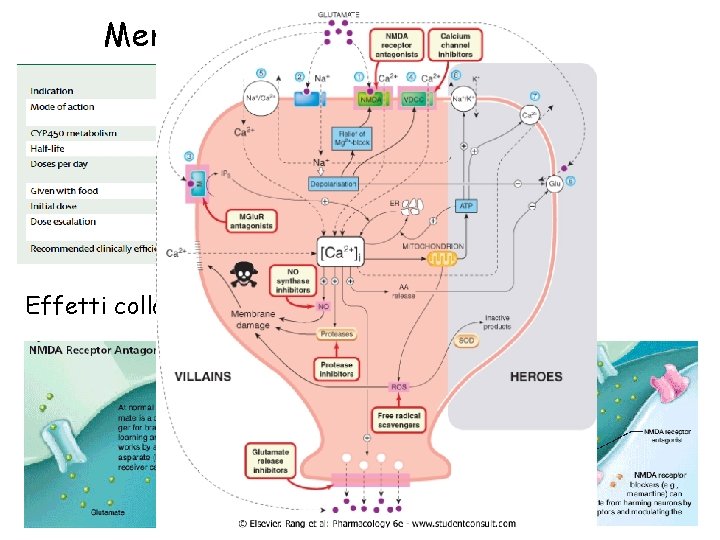
Memantina Effetti collaterali: cefalea

Morbo di Parkinson • Malattia neurodegenerativa caratterizzata da – – Tremori (a riposo) Rigidità muscolare Bradicinesia Compromissione dell’equilibrio posturale James Parkinson, 1817
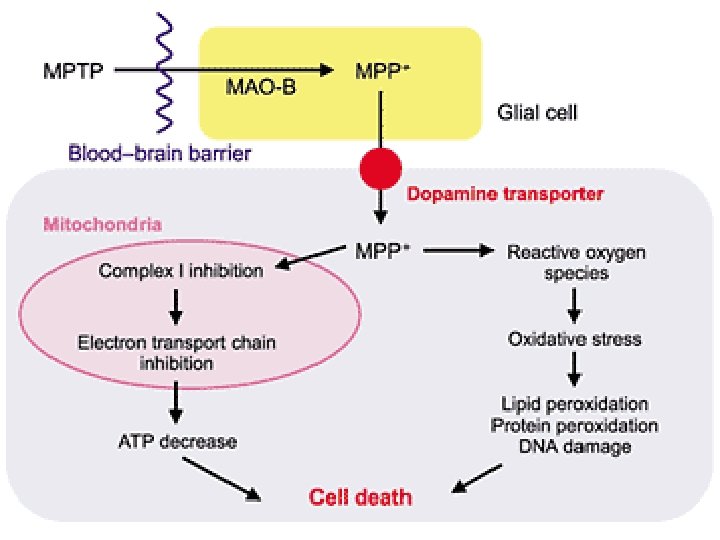
Eziologia • • Idiopatico Genetico (10 -15%, sinucleina e parkina) Encefalite virale? Tossico – Farmaci che riducono la quantità di dopamina nel cervello (reserpina) – Farmaci che inibiscono i recettori dopaminergici (neurolettici) – MPTP (1 -metil-4 -fenil-1, 2, 3, 6 -tetraidropiridina), 1982 – Rotenone (diserbante)
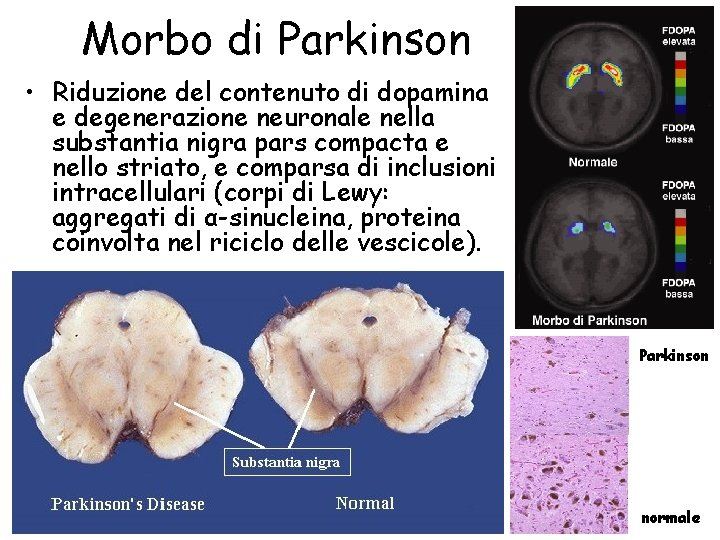
Morbo di Parkinson • Riduzione del contenuto di dopamina e degenerazione neuronale nella substantia nigra pars compacta e nello striato, e comparsa di inclusioni intracellulari (corpi di Lewy: aggregati di α-sinucleina, proteina coinvolta nel riciclo delle vescicole). Parkinson normale
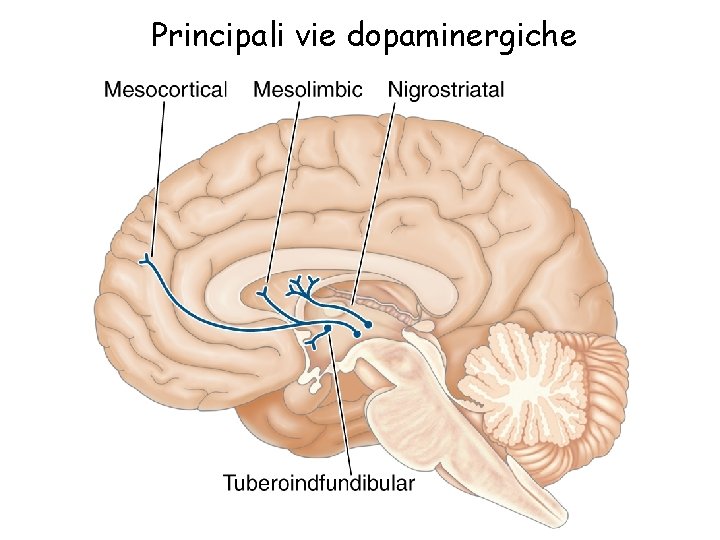
Principali vie dopaminergiche
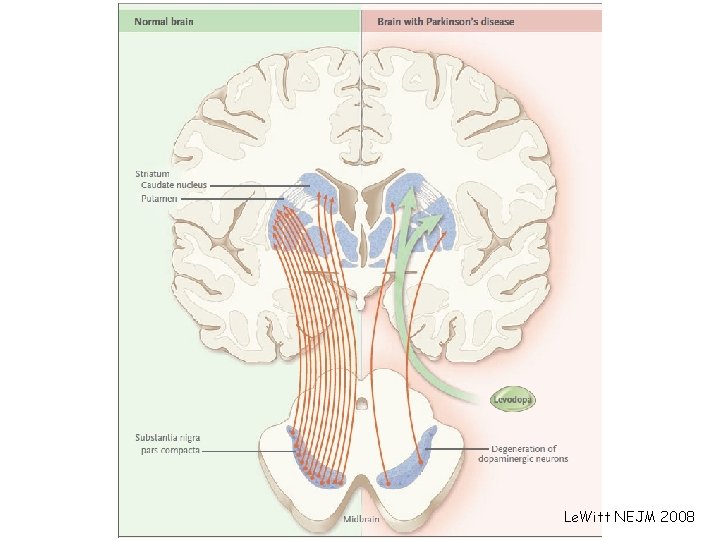
Le. Witt NEJM 2008
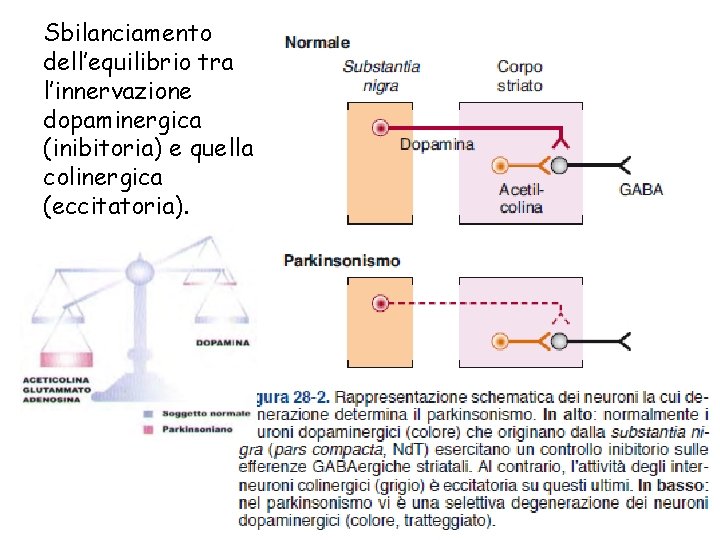
Sbilanciamento dell’equilibrio tra l’innervazione dopaminergica (inibitoria) e quella colinergica (eccitatoria).
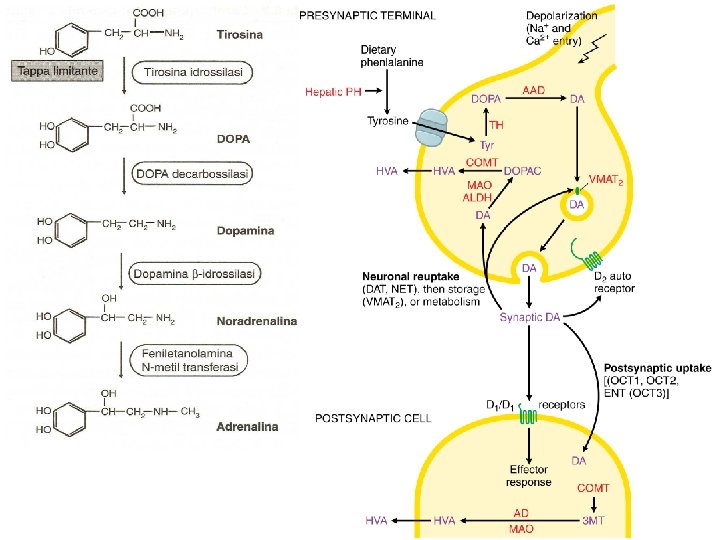
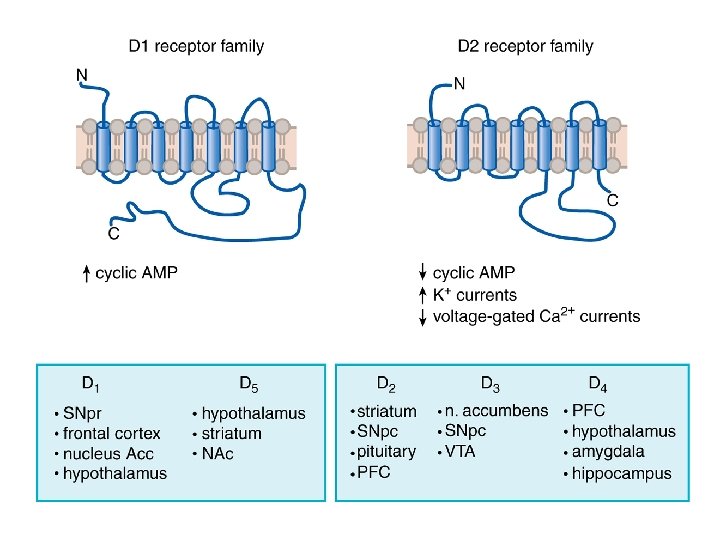
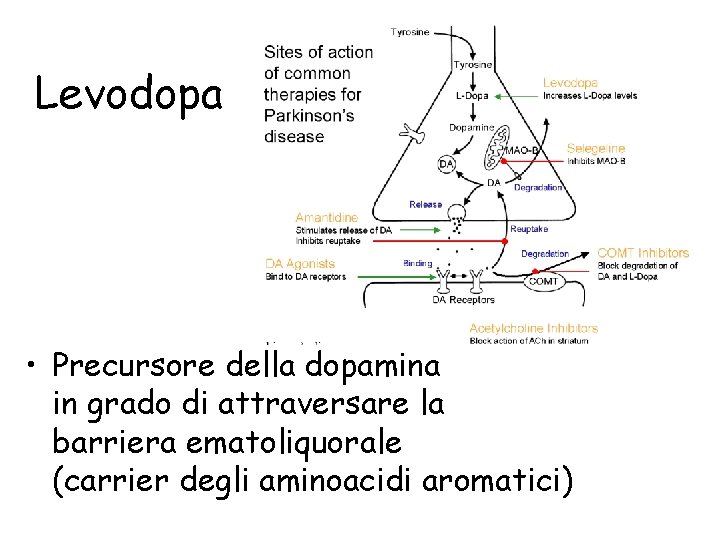
Levodopa • Precursore della dopamina in grado di attraversare la barriera ematoliquorale (carrier degli aminoacidi aromatici)
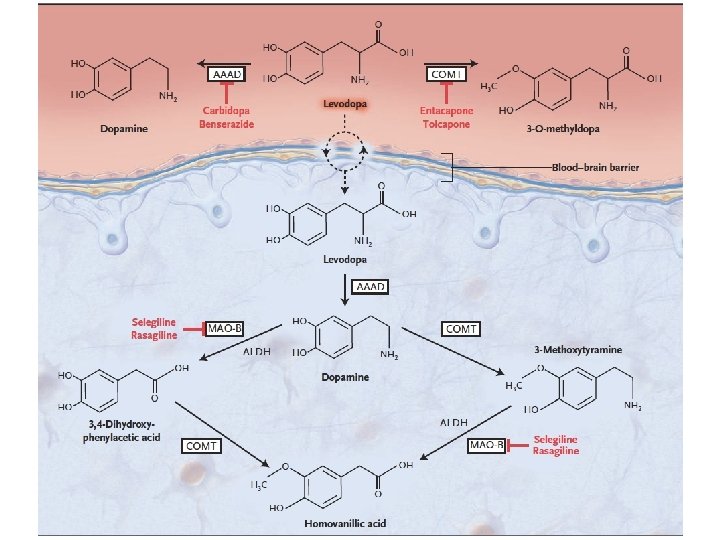
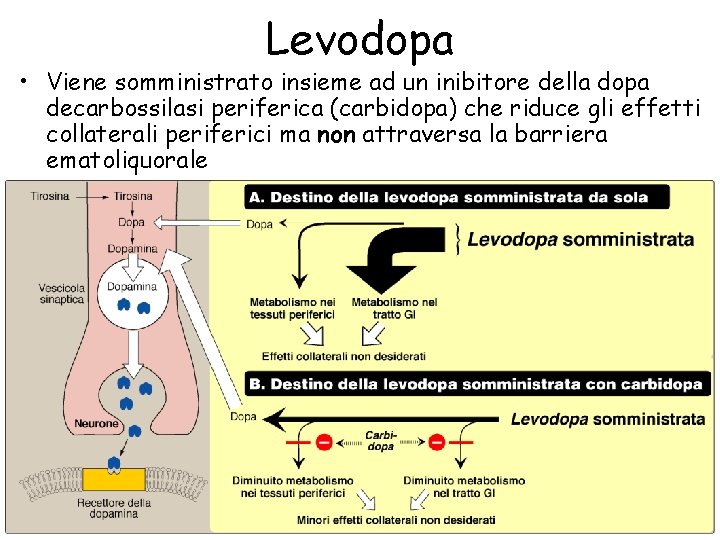
Levodopa • Viene somministrato insieme ad un inibitore della dopa decarbossilasi periferica (carbidopa) che riduce gli effetti collaterali periferici ma non attraversa la barriera ematoliquorale
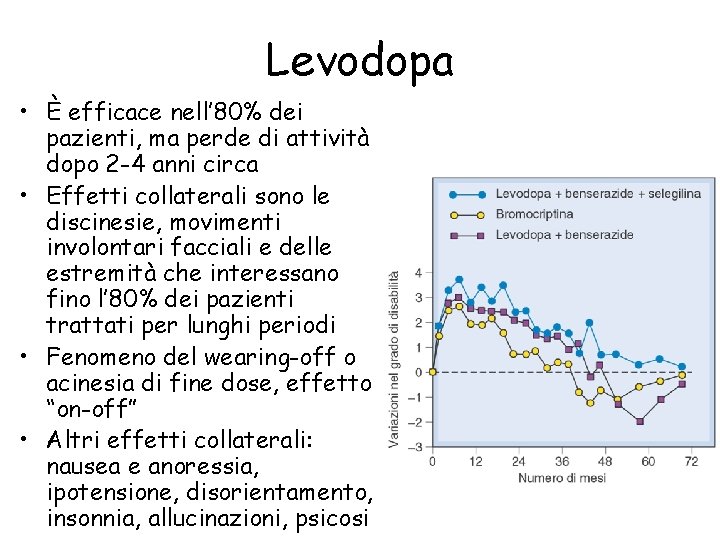
Levodopa • È efficace nell’ 80% dei pazienti, ma perde di attività dopo 2 -4 anni circa • Effetti collaterali sono le discinesie, movimenti involontari facciali e delle estremità che interessano fino l’ 80% dei pazienti trattati per lunghi periodi • Fenomeno del wearing-off o acinesia di fine dose, effetto “on-off” • Altri effetti collaterali: nausea e anoressia, ipotensione, disorientamento, insonnia, allucinazioni, psicosi
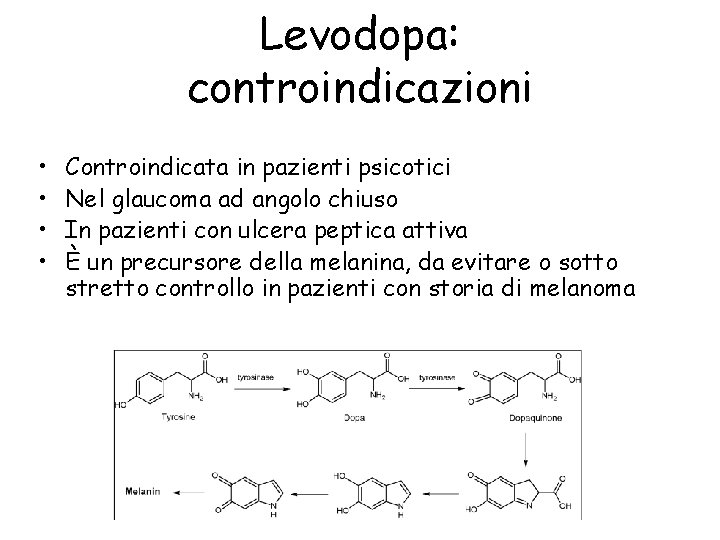
Levodopa: controindicazioni • • Controindicata in pazienti psicotici Nel glaucoma ad angolo chiuso In pazienti con ulcera peptica attiva È un precursore della melanina, da evitare o sotto stretto controllo in pazienti con storia di melanoma
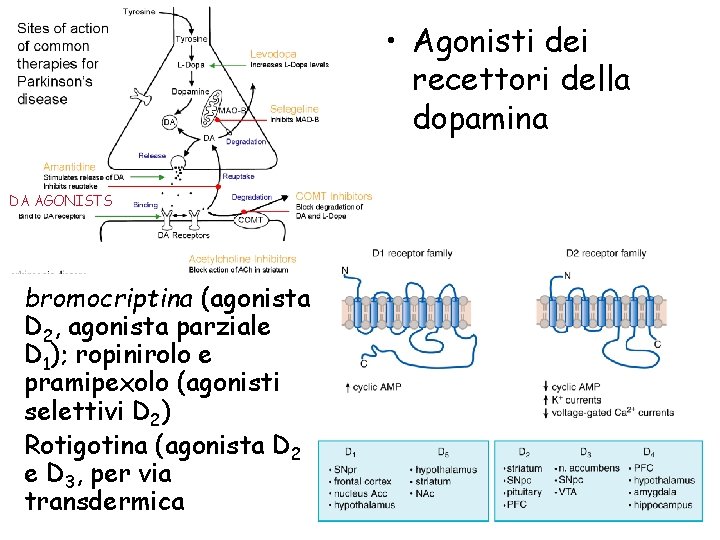
• Agonisti dei recettori della dopamina DA AGONISTS bromocriptina (agonista D 2, agonista parziale D 1); ropinirolo e pramipexolo (agonisti selettivi D 2) Rotigotina (agonista D 2 e D 3, per via transdermica

Agonisti recettoriali, vantaggi • La loro attività non dipende dall’attività funzionale dei neuroni nigro striatali • Hanno una durata d’azione più lunga della l-dopa, minore frequenza di fluttuazioni motorie e discinesie • La terapia dovrebbe essere iniziata con questi farmaci • Possono modificare il decorso del Parkinson?

Agonisti recettoriali, svantaggi • Anoressia, nausea e vomito, stipsi e dispepsia • Ipotensione posturale (all’inizio della terapia) • Discinesie • Convulsioni, allucinazioni, disturbi psichiatrici
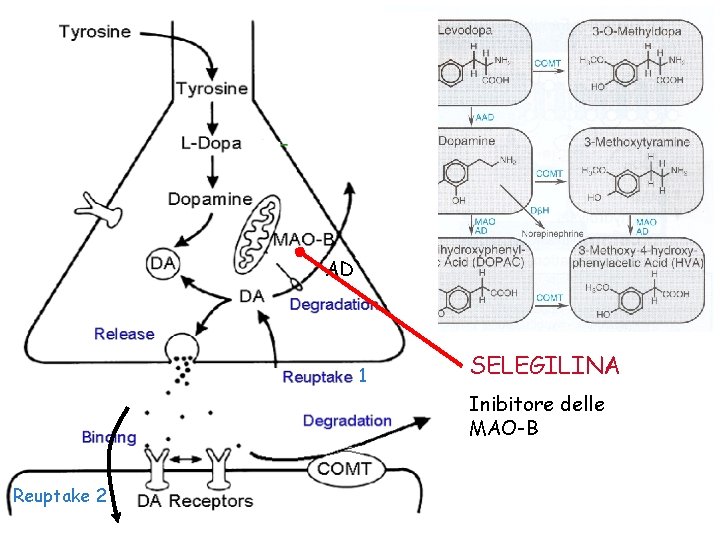
AD 1 SELEGILINA Inibitore delle MAO-B Reuptake 2

• Selegilina • Rasagligina • Sempre in associazione a L-DOPA di cui prolungano l’azione • Rallentano il catabolismo della dopamina e sono utili per ridurne la dose e attenuare i fenomeni “on off” e “wearing off” di grado lieve
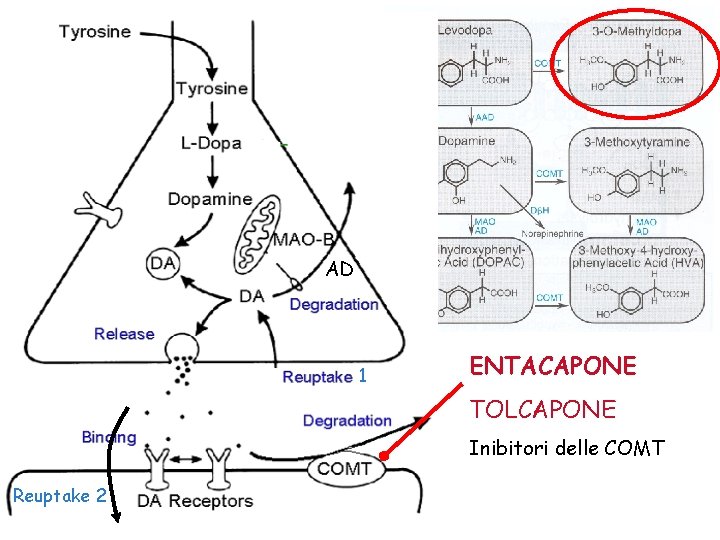
AD 1 ENTACAPONE TOLCAPONE Inibitori delle COMT Reuptake 2

Apomorfina • Potente agonista dopaminergico efficace per il sollievo temporaneo dei periodi off di acinesia nei pazienti in terapia con levodopa • Somministrato per via sottocutanea, efficace dopo 10 min e per 2 ore • È un potente emetico
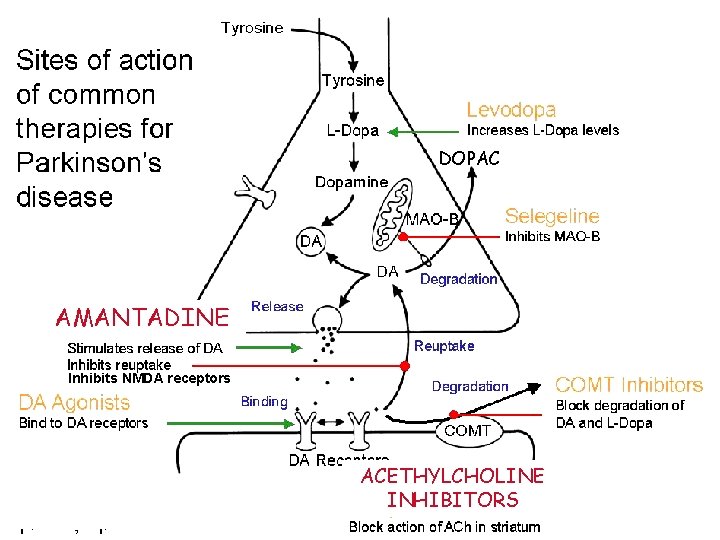
DOPAC AMANTADINE Inhibits NMDA receptors ACETHYLCHOLINE INHIBITORS

Farmaci anticolinergici • Migliorano il tremore e la rigidità ma sono poco efficaci sulla bradicinesia • Effetti collaterali antimuscarinici

• Procedure chirurgiche – Stimolazione encefalica profonda ad alta frequenza del nucleo subtalamico e del globus pallidus – Trapianto di tessuto dopaminergico (substantia nigra fetale) – Terapia cellulare • Terapia genica (studi di fase I); iniezione nel corpo striato di un adenovirus tipo 2 come vettore di geni: – Gene codificante la decarbossilasi dell’acido glutammico (precursore del GABA) – Gene della decarbossilasi degli aminoacidi aromatici; – Gene della neurturina, fattore di crescita che aumenta la sopravvivenza dei neuroni dopaminergici
- Slides: 38