Magorzata Inglot Katedra i Klinika Chorb Zakanych AM

Małgorzata Inglot Katedra i Klinika Chorób Zakaźnych AM we Wrocławiu Koinfekcja HIV/HCV/HBV

Impact of HIV and HCV HIV • Prevalence HCV • Prevalence World - 40 million World - 170 million USA - 1 million (0. 4%) USA - 3 million (1. 4%) • About 15, 000 deaths • About 10, 000 deaths yearly in U. S. A. • Death rate stable or declining yearly in U. S. A. • Number of deaths expected to increase 23 fold by 2030

HIV a HCV • HIV przyspiesza progresję do marskości Czas od nabycia zakażenia HCV do marskości 6. 9 lat u pacjentów HIV(+) vs. 23. 2 lat u pacjentów HIV(-) Soto B, et al. J Hepatol. 1997 Jan; 26(1): 1 -5. Ryzyko śmierci z powodu ESLD u pacjentów HIV(+)/HCV(+) 3. 81 razy wyższe vs HIV(-) /HCV(+) Ragni MV, et al. J Infect Dis. 2001 Apr 1; 183(7): 1112 -5
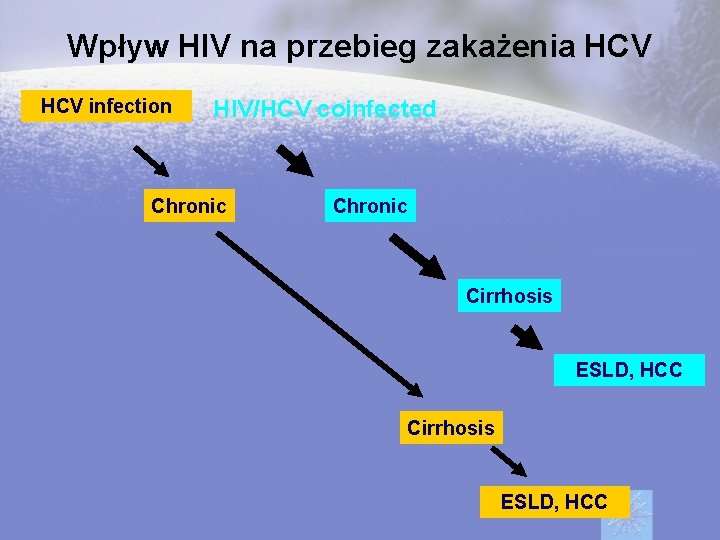
Wpływ HIV na przebieg zakażenia HCV infection HIV/HCV coinfected Chronic Cirrhosis ESLD, HCC

EUROSIDA: HBV a HIV • W grupie n=5728 odsetek zakażeń HBV - 8, 7% • • • (HBs. Ag +) Brak korelacji koinfekcji HBV z progresją do AIDS U osób z koinfekcją znacząco wyższa śmiertelność Brak wpływu koinfekcji na odpowiedź na HAART Outcome HBs. Ag-negative (n = 5230) HBs. Agpositive (n = 498) Incidence Ratio P Value Global mortality, deaths/100 person-yrs 2. 6 3. 7 1. 53 . 0001 Liver-related mortality, deaths/100 person-yrs 0. 2 0. 7 3. 58 <. 0001
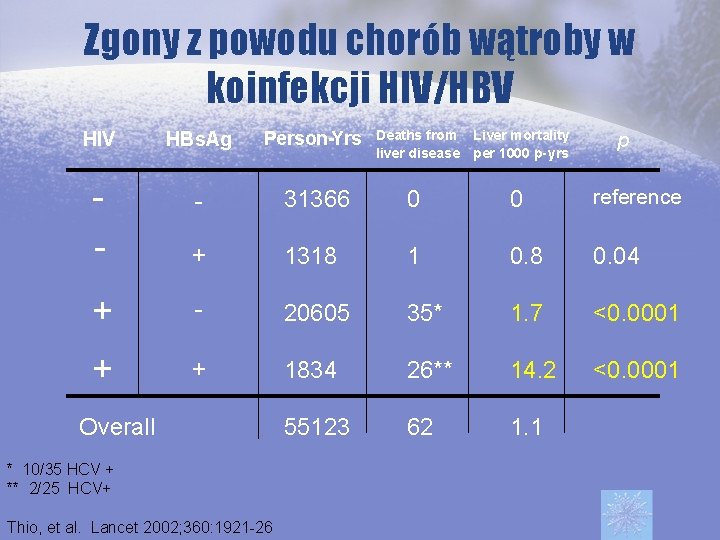
Zgony z powodu chorób wątroby w koinfekcji HIV/HBV HIV HBs. Ag Person-Yrs Deaths from Liver mortality liver disease per 1000 p-yrs p - - 31366 0 0 reference + 1318 1 0. 8 0. 04 + - 20605 35* 1. 7 <0. 0001 + + 1834 26** 14. 2 <0. 0001 55123 62 1. 1 Overall * 10/35 HCV + ** 2/25 HCV+ Thio, et al. Lancet 2002; 360: 1921 -26
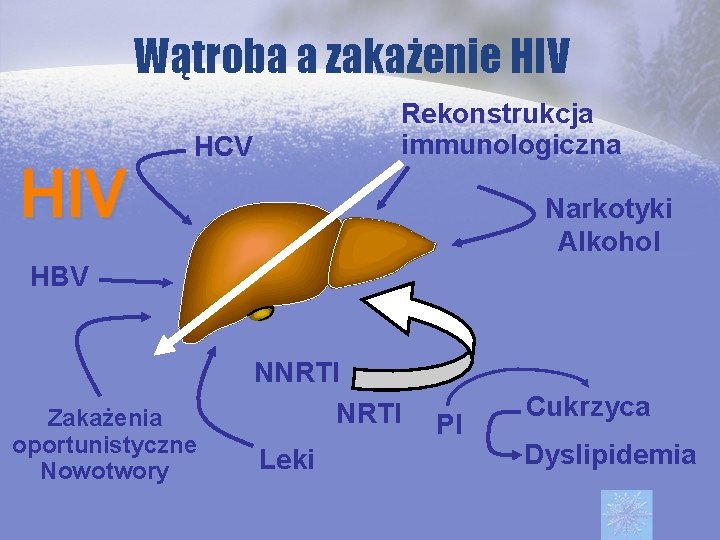
Wątroba a zakażenie HIV Rekonstrukcja immunologiczna HCV Narkotyki Alkohol HBV Zakażenia oportunistyczne Nowotwory NNRTI Leki PI Cukrzyca Dyslipidemia

EUROSIDA: Ryzyko zgonu z powodu niewydolności wątroby • Ryzyko zgonu z powodu niewydolności • • • wątroby rośnie w badanej grupie w latach 1995 -2004 Dłuższy czas trwania HAART wiąże się z większym ryzykiem zgonu z powodu niewydolności wątroby u pacjentów ze zbliżonymi wartościami CD 4 Każdy rok HAART – ryzyko zgonu z powodu niewydolności wątroby wzrasta o 12% Lundgren J, Mocroft A, Soriano V, et al. Is there evidence for an increase in the death rate from liver-related disease in patients with HIV? The Euro. SIDA study. Program and abstracts of the 10 th European AIDS Conference; November 17 -20, 2005; Dublin, Ireland. Abstract PS 7/2
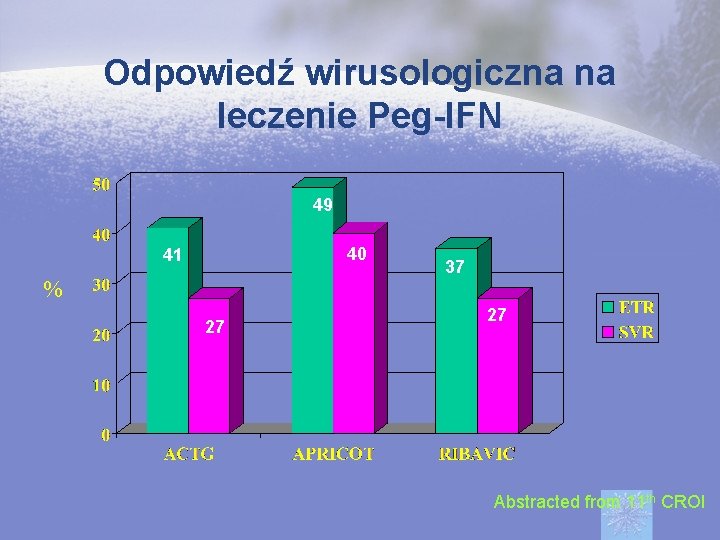
Odpowiedź wirusologiczna na leczenie Peg-IFN 49 40 41 % 27 37 27 Abstracted from 11 th CROI

Opcje terapeutyczne w zakażeniu HBV • Interferon – standardowy lub • • pegylowany Lamiwudyna = 3 TC Adefowir = ADV Tenofowir = TDF Emtrycytabina = FTC
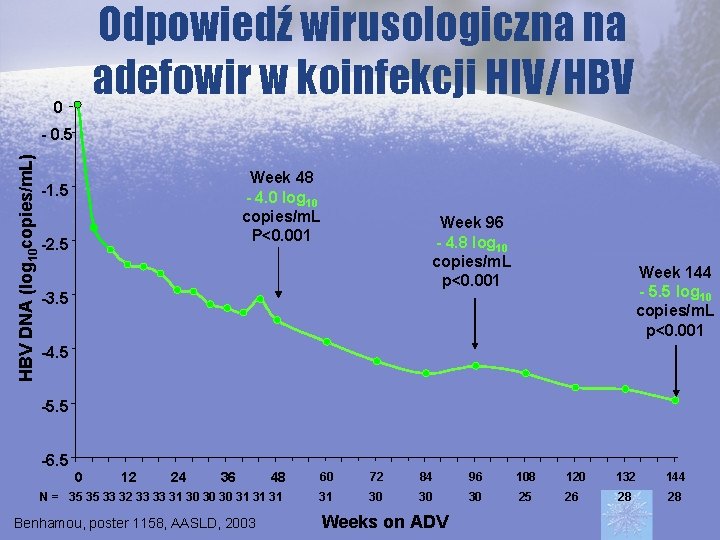
Odpowiedź wirusologiczna na adefowir w koinfekcji HIV/HBV 0 HBV DNA (log 10 copies/m. L) - 0. 5 Week 48 - 4. 0 log 10 copies/m. L P<0. 001 -1. 5 -2. 5 Week 96 - 4. 8 log 10 copies/m. L p<0. 001 -3. 5 Week 144 - 5. 5 log 10 copies/m. L p<0. 001 -4. 5 -5. 5 -6. 5 48 60 72 84 96 108 120 132 144 N = 35 35 33 32 33 33 31 30 30 30 31 31 30 30 30 25 26 28 28 0 12 24 36 Benhamou, poster 1158, AASLD, 2003 Weeks on ADV

Short Statement of the First European Consensus Conference on the Treatment of Chronic Hepatitis C and B in HIV Co-infected Patient March 1 -2, 2005 Paris, France

HBV

Zalecane badania • ALT – wielokrotnie powtarzane • • • zwłaszcza dla HBe. Ag(-) HBe. Ag/anty-HBe HBV DNA ilościowo– unifikacja testów, wyniki w IU/ml Biopsja wątroby (BII)

Wskazania do leczenia • HBV DNA > 20 000 IU/ml dla HBe. Ag(+) i • • HBV DNA >2000 IU/ml dla HBe. Ag (-) ALT >N Zmiany hist-pat. (grading) (BII)

Leki • PEG IFN alfa 2 a 180 mcg 1 x tyg 48 tyg • • (u pacjentów nie wymagających HAART) IFN alfa 5 -6 MU 3 xtyg 6 -12 msc Analogi nukleozydowe
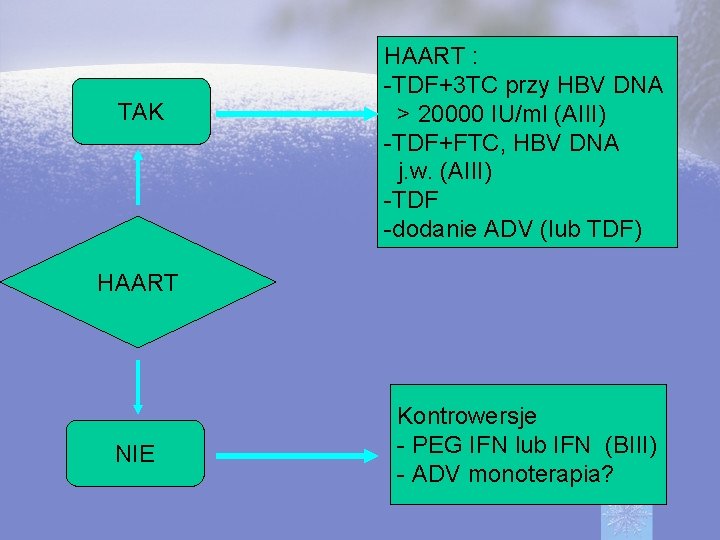
TAK HAART : -TDF+3 TC przy HBV DNA > 20000 IU/ml (AIII) -TDF+FTC, HBV DNA j. w. (AIII) -TDF -dodanie ADV (lub TDF) HAART NIE Kontrowersje - PEG IFN lub IFN (BIII) - ADV monoterapia?

HCV

Biopsja wątroby • Decyzja o wykonywaniu biopsji winna • być indywidualizowana, biopsja szczególnie wskazana u pacjentów zakażonych genotypem 1 oraz u „normal ALT” W zakażeniu genotypem 2, 3 oraz 1 z niską wiremią biopsja nie jest konieczna

Kryteria kwalifikacyjne • U pacjentów z CD 4<200 kom/mm najpierw • • • włączyć HAART (AII) Genotyp 2, 3 oraz 1 z niską wiremią – leczyć niezależnie od obrazu hist. pat. (AI) U pacjentów: zakażonych genotypem 1 z wysoką wiremią, „normal ALT” w zależności od wyniku biopsji (AII) Pacjenci uzależnieni i stosujący metadon – brak przeciwwskazań (CIII)

Schemat terapii • PEG IFN alfa 2 a 180 mcg/1 xtyg lub PEG • IFN alfa 2 b 1, 5 mcg /kg m. c. 1 x/tyg RBV: genotypy 2, 3 800 mg/dobę (AI) genotypy 1, 4 1000 -1200 mg/dobę (BIII) Czas leczenia : 48 tygodni niezależnie od genotypu ( wymaga dalszych badań) (BI)

Monitorowanie i działania niepożądane • Ocena odpowiedzi w 12 tyg. jak w • • monoinfekcji (AII) Wizyty co 2 tyg w 1 msc. a następnie co 4 tygodnie CD 4 co 4 tygodnie

Nowa Akademia Medyczna we Wrocławiu
Wstępne wyniki próby obserwacyjnej HIV/HCV (1) • Kwalifikacja: 40 pts, CD 4 > 350 • • kom/mm, HIV RNA <50 kopii/ml u leczonych, HAART co najmniej od 6 msc, brak OI w wywiadzie Genotypy: 3 a – 19 (58%) 1– 9 4– 5 Bad. hist-pat: Staging ≥ 2 – 11 osób

Wstępne wyniki próby obserwacyjnej HIV/HCV(2) • Leczenie: PEG IFN alfa 2 a 180 mcg 1 x • • • tyg + RBV 800 -1200 mg/dobę Czas leczenia: genotyp 3 – 24 tyg; genotyp 1, 4 - 48 tyg. Wizyty: co 2 tyg w 1 ms. następnie co 4 - 6 tygodni CD 4 i HIV RNA: 0 – 12 - 24 – 48 tyg

Wstępne wyniki próby obserwacyjnej HIV/HCV (3) • SVR: (n=17) – 11 osób (65%) • Przerwanie leczenia: 2 osoby z powodu SAE w pierwszym miesiącu terapii (niedokrwistość hemolityczna) 3 osoby z powodu braku EVR

Problemy

Dostępność leków • w ramach programów NFZ - wg kryteriów jak dla pacjentów HIV(-) - wg odrębnych (preferencyjnych? ) kryteriów • w ramach badań klinicznych • w ramach programu KC (? )

Biopsja wątroby • U wszystkich pacjentów jako niezbędny • • element kwalifikacji Tylko u chorych zakażonych genotypem 1 U pacjentów z prawidłową aktywnością Al. AT

Czas leczenia a genotyp HCV • wszyscy pacjenci 48 tygodni • genotyp 2, 3 - 24 tygodnie • genotyp 1 - 72 tygodni ?

Kogo leczyć? • Pacjentów ze stabilnym przebiegiem • • zakażenia HIV (CD 4 300 – 350 kom/mm, niską bądź niewykrywalną wiremią) W pierwszej kolejności z włóknieniem co najmniej 2 (? ) Dobrze współpracujących, umotywowanych

Monitorowanie leczenia • • Wizyty częściej niż u pacjentów HIV(-) Niedokrwistość!!! Depresja!!! CD 4 co 8 -12 tygodni Mleczany, anion gap, gazometria, diastaza

Wpływ terapii HCV na przebieg zakażenia HIV • Leczenie PEG-INF/RBV powoduje spadek CD 4 (o 130 -160 cells/mm ), ale liczba CD 4 wraca do wartości baseline po zakończeniu terapii 1, 2 • Wartość HIV RNA obniża się w trakcie leczenia PEGIFN/RBV u osób z wiremią wykrywalną w baseline 2 • Wewnątrzkomórkowa fosforylacja i farmakokinetyka AZT, 3 TC and D 4 T nie zmienia się przy stosowaniu rybawiryny w dawce 800 mg/dobę 3 1 Chung et al. NEJM 2004 2 Torriani et al. NEJM 2004 3 Gries et al. CROI #136 LB
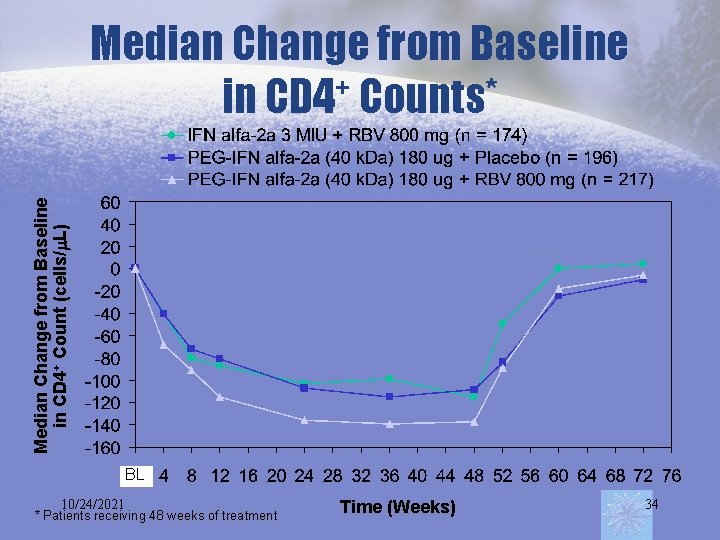
Median Change from Baseline in CD 4+ Count (cells/ L) Median Change from Baseline + in CD 4 Counts* BL 10/24/2021 * Patients receiving 48 weeks of treatment Time (Weeks) 34
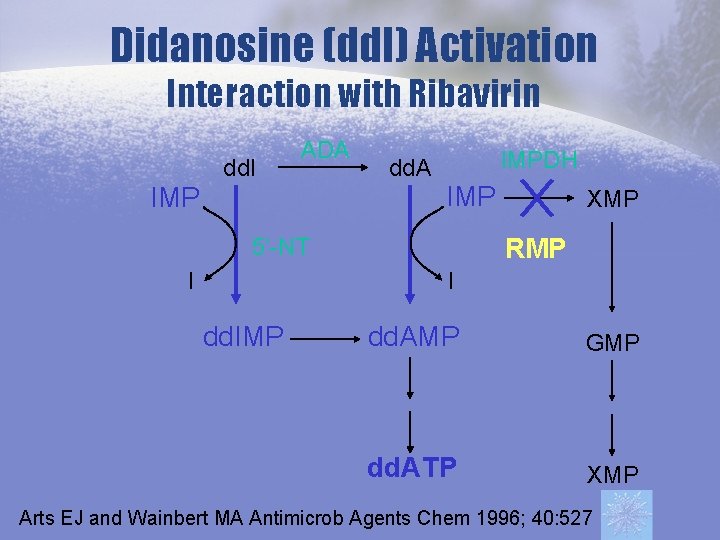
Didanosine (dd. I) Activation Interaction with Ribavirin IMP dd. I ADA dd. A IMPDH IMP XMP RMP 5’-NT I I dd. IMP dd. AMP GMP dd. ATP XMP Arts EJ and Wainbert MA Antimicrob Agents Chem 1996; 40: 527

Ryzyko toksyczności mitochondrialnej: NRTI + Ribavirin w koinfekcji HIV/HCV • US FDA Adverse Event Reporting System (2002) Pacjenci HIV/HCV Ribavirin + NRTIs • 31 przypadków (58 zgłoszeń) objawów mogących sugerować toksyczność mitochondrialną Pancreatitis i lub iwzrost lipazy (n=21) Lactic acidosis (n=20) Wzrost akt. Al. AT (n=8) Hepatic steatosis (n=6) Wzrost kreatyniny, neuropatia, Mitochondrial Toxicity Risk Ribavirin + 12. 4 Didanosine + stavudine 8. 0 3. 3 Stavudine 1. 1 Abacavir 0. 2 Lamivudine Zidovudine 0. 01 0. 06 0. 1 1. 0 10 100 Odds Ratio (95% CI) Fleischer R, et al. 2004.

Jak zapewnić adherence? • DOT? • kwalifikacja umotywowanych • pacjentów edukacja pacjentów

Kwalifikacja do OLT • Pacjent HIV(+) z ESLD – wskazanie do transplantacji wątroby

OLT u pacjentów HIV(+) - kryteria – Brak OI w wywiadzie – CD 4 >100 kom/mm 3 – HIV RNA <50 copies/m. L Roland M. Topics in HIV Medicine. 2004; 12: 73 -76.
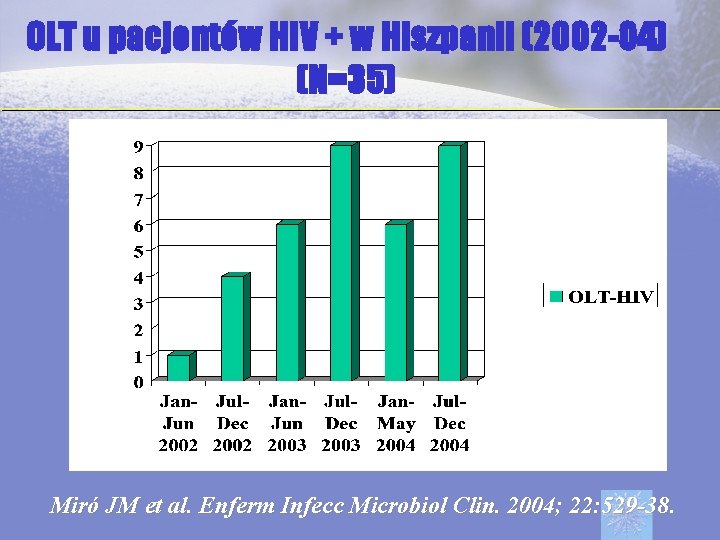
OLT u pacjentów HIV + w Hiszpanii (2002 -04) (N=35) Miró JM et al. Enferm Infecc Microbiol Clin. 2004; 22: 529 -38.
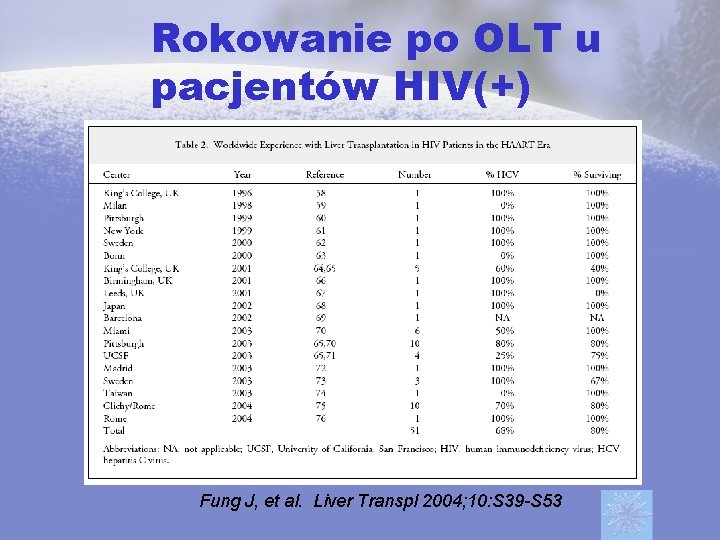
Rokowanie po OLT u pacjentów HIV(+) Fung J, et al. Liver Transpl 2004; 10: S 39 -S 53

Dziękuję za uwagę!

I wtedy motyl jakby się zatrzymał. Tak jakby zaszedł tak daleko jak mógł i dalej już nie miał sił.

Czasem walka to to, czego nam w życiu potrzeba. Jeśli Bóg pozwala nam iść przez życie bez jakichkolwiek problemów to może to zrobić z nas słabeuszy. Nie bylibyśmy tak silni jak moglibyśmy. Nie być w stanie do latania.

Hepatitis C +/- HIV Time to Cirrhosis HIV Status Time to Cirrhosis HIV + (n = 87) 6. 9 years HIV - (n = 272) 23. 2 years P < 0. 01 Soto et al. J Hepatol. 1997; 26 : 1 -5
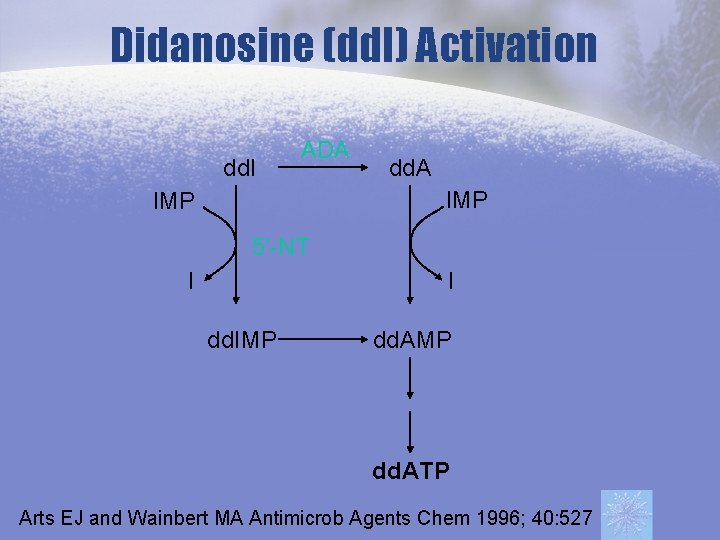
Didanosine (dd. I) Activation dd. I ADA dd. A IMP 5’-NT I I dd. IMP dd. ATP Arts EJ and Wainbert MA Antimicrob Agents Chem 1996; 40: 527
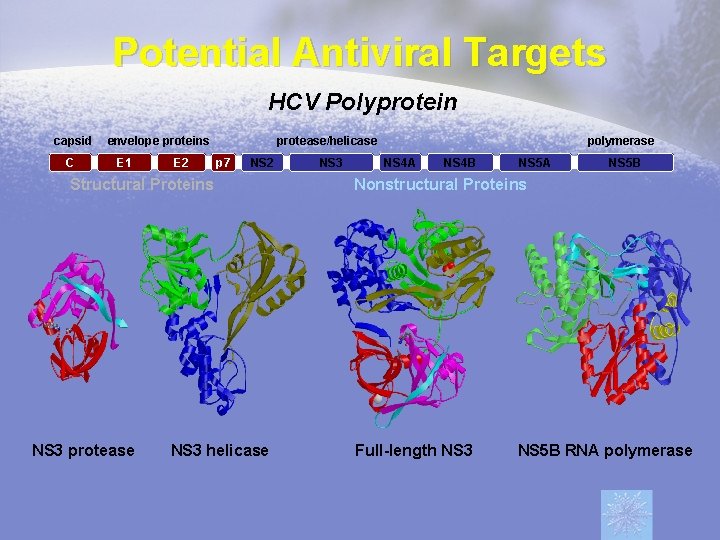
Potential Antiviral Targets HCV Polyprotein capsid C envelope proteins E 1 E 2 protease/helicase p 7 NS 2 Structural Proteins NS 3 protease NS 3 helicase NS 3 polymerase NS 4 A NS 4 B NS 5 A NS 5 B Nonstructural Proteins Full-length NS 3 NS 5 B RNA polymerase

HIV Disease Progression UK HIV Disease Progression Study • Prospective, cohort 92 HIV+ hemophiliac men 86% HCV+ coinfection Genotype 1 (70%), 2 (13%), 3 (14%) and 4 (2%) • HCV type 1 showed faster progression to AIDS (P=0. 009) and death (P=0. 007) than non-type 1 • RR 3. 1 and 3. 4, respectively Sabin, J Infect Dis. 1997; 175: 164.

Poprawa hist. pat. nieodpowiadajacych Histologic response Histologic Response (%) possible even in patients who do not 100 90 achieve SVR 80 Best response with Peg-IFN + RBV 70 60 50 40 (+) SVR (-) SVR 80% 58% Prospective study of treatment for HCVmono-infected nonresponders ongoing (HALT-C) Lissen E, et al. IAS 2005. Abstract Tu. Pe 1. 1 C 21. 100% 40% 33% 30 20 10 n=10 12 0 Peg-IFN + RBV (n = 22) 5 15 Peg-IFN (n = 20) 4 18 IFN + RBV (n = 22)
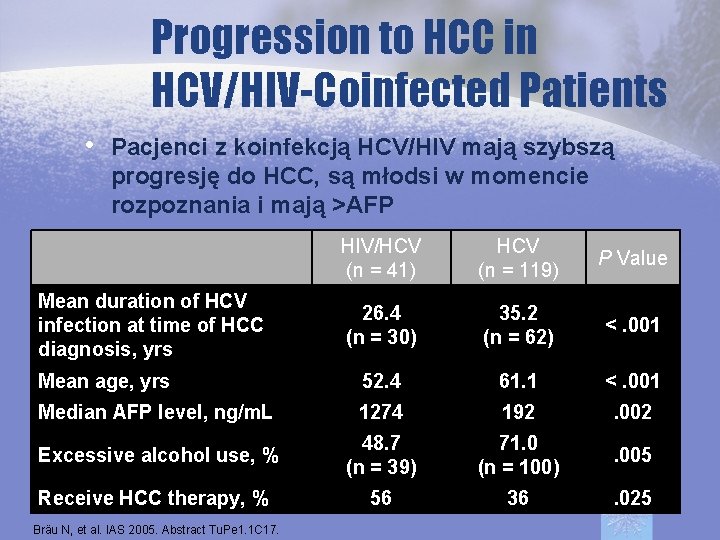
Progression to HCC in HCV/HIV-Coinfected Patients • Pacjenci z koinfekcją HCV/HIV mają szybszą progresję do HCC, są młodsi w momencie rozpoznania i mają >AFP HIV/HCV (n = 41) HCV (n = 119) P Value 26. 4 (n = 30) 35. 2 (n = 62) <. 001 Mean age, yrs 52. 4 61. 1 <. 001 Median AFP level, ng/m. L 1274 192 . 002 Excessive alcohol use, % 48. 7 (n = 39) 71. 0 (n = 100) . 005 Receive HCC therapy, % 56 36 . 025 Mean duration of HCV infection at time of HCC diagnosis, yrs Bräu N, et al. IAS 2005. Abstract Tu. Pe 1. 1 C 17.

Conflicting results from studies on influence of HCV infection on HIV disease progression (in HAART era) • Swiss Cohort study (n = 3111; 1157 HIV/HCV co-infected): Significantly smaller increases in CD 4+ cells Risk for AIDS progression or death increased • Johns Hopkins HIV Cohort (n = 1995; 44. 6% co-infected): In those receiving effective HAART, no difference in increase in death, CD 4+ cell count or %, in HCV-infected compared with HCV-uninfected
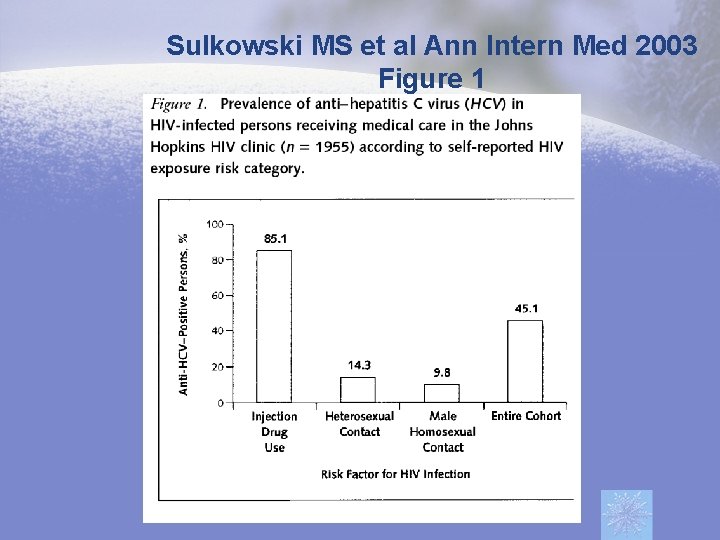
Sulkowski MS et al Ann Intern Med 2003 Figure 1
Effect of HIV on the Course of Hepatitis C HCV infection Chronic Cirrhosis ESLD, HCC

Progression to HCC in HCV/HIV-Coinfected Patients • HCV/HIV-coinfected patients progress more rapidly to HCC than HCVmonoinfected patients • Coinfected pts also younger at HCC HCVlevels, diagnosis, have. HIV/HCV higher AFP P Value (n = 41) (n = 119) receive HCC treatment more often Mean duration of HCV 26. 4 (n = 30) 35. 2 (n = 62) <. 001 Mean age, yrs 52. 4 61. 1 <. 001 Median AFP level, ng/m. L 1274 192 . 002 48. 7 (n = 39) 71. 0 (n = 100) . 005 infection at time of HCC diagnosis, yrs Excessive use, % Bräu N, et al. IAS alcohol 2005. Abstract Tu. Pe 1. 1 C 17.
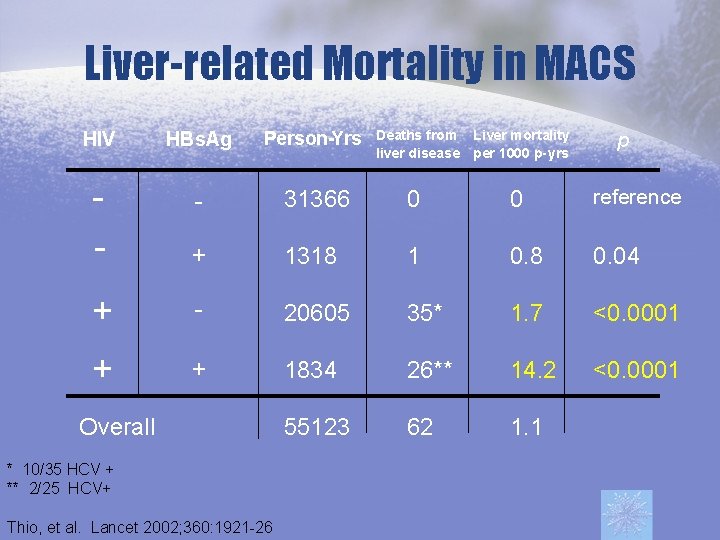
Liver-related Mortality in MACS HIV HBs. Ag Person-Yrs Deaths from Liver mortality liver disease per 1000 p-yrs p - - 31366 0 0 reference + 1318 1 0. 8 0. 04 + - 20605 35* 1. 7 <0. 0001 + + 1834 26** 14. 2 <0. 0001 55123 62 1. 1 Overall * 10/35 HCV + ** 2/25 HCV+ Thio, et al. Lancet 2002; 360: 1921 -26

Dyskusja • U osób anty-HCV i/lub anty-HBc ujemnych • • powtarzanie badań 1 x w roku U pacjentów HBs. Ag + oznaczenie HBV DNA ilościowe Biopsja wątroby zalecana przy kwalifikacji do leczenia Należy w każdym ośrodku stworzyć listę preferencyjną dla zakażonych HIV zakażonych wirusami hepatotropowymi ze względu na szybką progresję choroby wątroby Osoby z włóknieniem ≥ 2 powinny rozpoczynać terapię niezwłocznie, pozostałe w czasie nie dłuższym niż 1 rok

Dyskusja 2 • Nie przyjmujemy żadnego preferencyjnego • • schematu c. ART u osób współzakażonych HIV/HCV Należy unikać dd. I, AZT u osób, u których planujemy leczenie p wzw t. C Należy ściśle monitorować osoby współzakażone HIV/HCV Przed rozpoczęciem HAART opcjonalne oznaczenie HCV RNA i genotypu HCV, ewentualnie biopsja wątroby Leczenie pwzw t. C zgodnie z zaleceniami europejskimi (z wyjątkiem zaleceń dot. oznaczania CD 4)

Dyskusja 3 - HBV • Kryteria włączenia do leczenia pwzw t. B wg • zaleceń europejskich U pacjentów, którzy nie wymagają HAART: zalecany PEG IFN (lub IFN klasyczny) Ścisłe monitorowanie pacjentów nieleczonych IFN i ewentualne wcześniejsze wdrożenie HAART, w skład schematu powinien wchodzić TDF + (3 TC lub FTC) • Konieczne szczepienie p/HBV u pacjentów anty. HBc ujemnych zgodnie z kalendarzem szczepień Monitorowanie odpowiedzi humoralnej
- Slides: 59