MAGNEZIJUM http www wikiwand combsMagnezij https epruveticaki wordpress
MAGNEZIJUM http: //www. wikiwand. com/bs/Magnezij https: //epruveticaki. wordpress. com/category/osmi-razred/

OTKRIĆE MAGNEZIJUMA Da je magnezijum poseban element prvi je utvrdio Džozef Blek. U čistom obliku ga je otkrio Dejvi (1808). Dejvi (Sir Humphry Davy, 1778 - 1829) Blek (Joseph Black, 1728 – 1799)
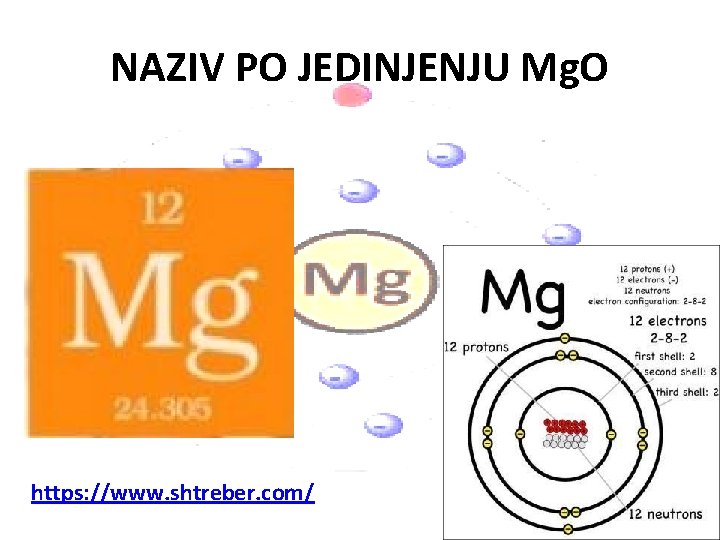
NAZIV PO JEDINJENJU Mg. O https: //www. shtreber. com/
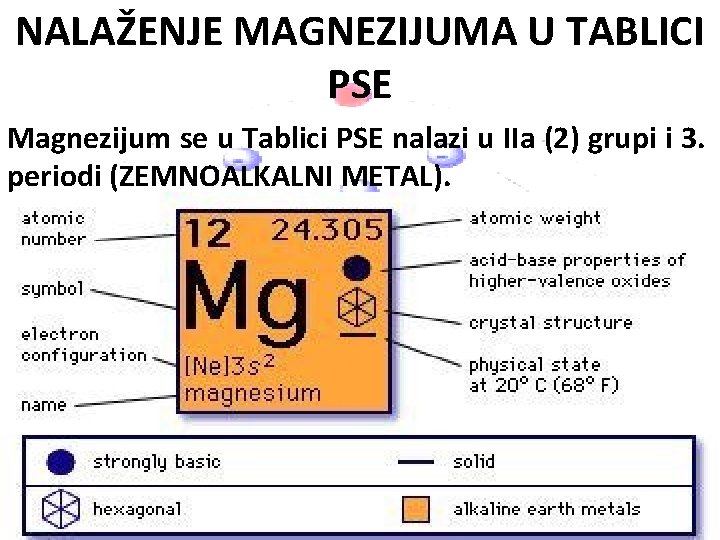
NALAŽENJE MAGNEZIJUMA U TABLICI PSE Magnezijum se u Tablici PSE nalazi u IIa (2) grupi i 3. periodi (ZEMNOALKALNI METAL).

NALAŽENJE MAGNEZIJUMA U PRIRODI - Zbog svoje reaktivnosti magnezijuma U PRIRODI NEMA U SLOBODNOM STANJU. - JEDINJENJA (RUDE, MINERALI): Magnezit Mg. CO 3 Dolomit Mg. CO 3 x Ca. CO 2 Karnalit KCl x Mg. Cl 2 x 6 H 2 O - BIOGENI ELEMENT: Magnezijum ulazi u sastav hlorofila u lišću Soli kalcijuma i magnezijuma koje su rastvorene u vodi daju joj ukus i čine je tvrdom.



IZOTOPI MAGNEZIJUMA Stabilni izotopi magnezijuma su: 24 Mg, 25 Mg i 26 Mg.
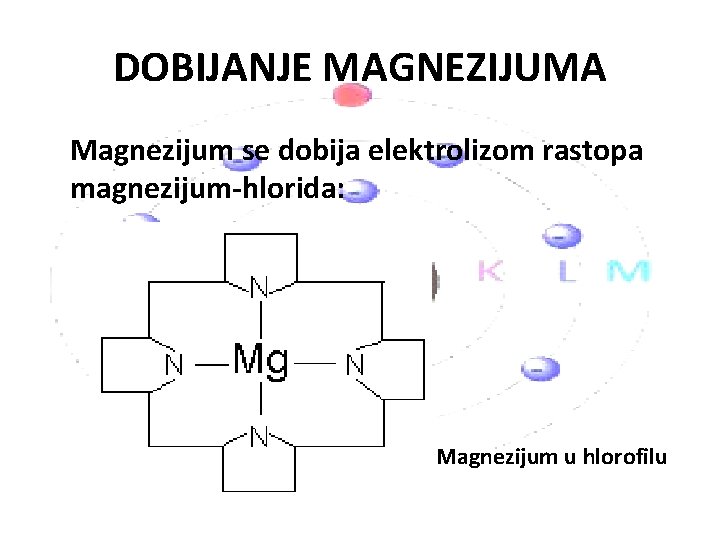
DOBIJANJE MAGNEZIJUMA Magnezijum se dobija elektrolizom rastopa magnezijum-hlorida: Magnezijum u hlorofilu

FIZIČKA SVOJSTVA MAGNEZIJUMA Sive je boje, dobro provodi toplotu i elektricitet Lak metal, male gustine (manje tvrd od kalcijuma), niske vrednosti za tačke ključanja i topljenja, zbog angažovanja samo dva elektrona u metalnoj vezi. Izvlači se u žice, kovan je, energija jonizacije i elektronegativnost imaju niske vrednosti, pa je dobro redukciono sredstvo.


HEMIJSKA SVOJSTVA MAGNEZIJUMA - Mg gori svetlo-blještavim plamenom: 2 Mg + O 2 → 2 Mg. O - U hladnoj vodi se reakcija sporo odvija, pa se magnezijum sipa u vruću vodu: Mg. O + H 2 O → Mg(OH)2 - U struji ugljen-dioksida Mg gori uz izdvajanje čađi: 2 Mg + CO 2 → Mg. O + C - Mg je dobro redukciono sredstvo. Ta se osobina koristi za dobijanje nekih drugih metala Ti, Cr.

http: //virtual-chem. blogspot. rs/2014_09_01_archive. html https: //epruveticaki. wordpress. com/category/osmi-razred/ https: //www. youtube. com/watch? v=4 oq. JHQi 4 HFg


UPOTREBA MAGNEZIJUMA Magnezijum je uključen u preko 300 reakcija u organizmu. Važan je za sve organe, a naročito za pravilan rad srca, mišića, bubrega, izgradnju zuba i kostiju. Primenjuje se kod: srčanih oboljenja, grčeva i slabosti mišića, zatvora, alkoholizma, dijabetesa, kao antacid, kod astme, hroničnog umora, osteoporoze, migrenskih glavobolja, PMS-a.

UPOTREBA JEDINJENJA MAGNEZIJUMA • Mg. O (magnezijum-oksid) se koristi za proizvodnju vatrostalnih opeka. • Mg. SO 4 (magnezim-sulfat ili gorka so) za bolje varenje • Mg. SO 4 x. H 2 O i Mg. SO 4 x 7 H 2 O upotrebljavju se u industriji kože, tekstila i medicini. http: //pt. slideshare. net/arminmasnopitay/magnezijum-ili-magnezij



- Slides: 19