Magnesium Copyright 2006 Armin Glaser Magnesium 2 hufigstes





















- Slides: 30

Magnesium Copyright 2006 Armin Glaser

Magnesium • 2. häufigstes Kation im Meerwasser • 1284 mg/kg (Ca = 412 mg/kg) • 52, 8 m. Mol/kg (Ca = 10, 28 m. Mol/kg)

Magnesium • bildet mit Carbonationen Ionenpaare • lagert sich an Kalkoberflächen an (Calcifikationsinhibitor) • verhindert Kalkausfällung in Ca. CO 3 -übersättigtem Meerwasser

Wer verbraucht Magnesium ? nein ja

Steinkorallen brauchen kein Magnesium ! Warum ?

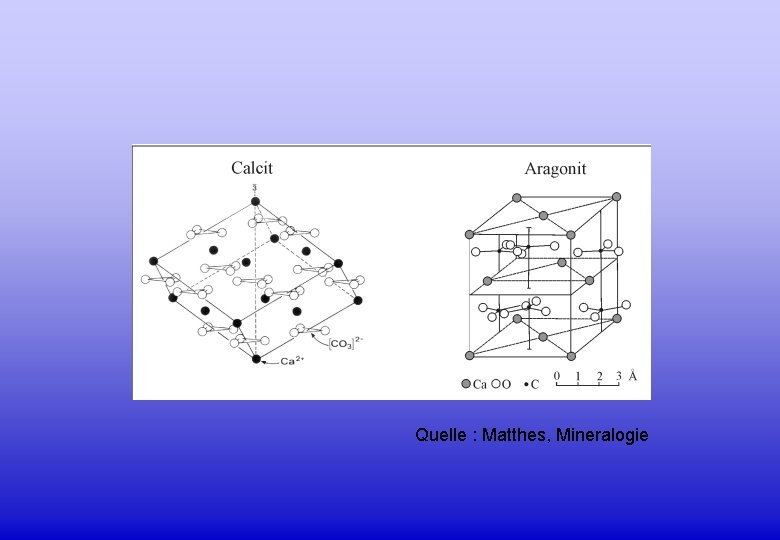
Quelle : Matthes, Mineralogie

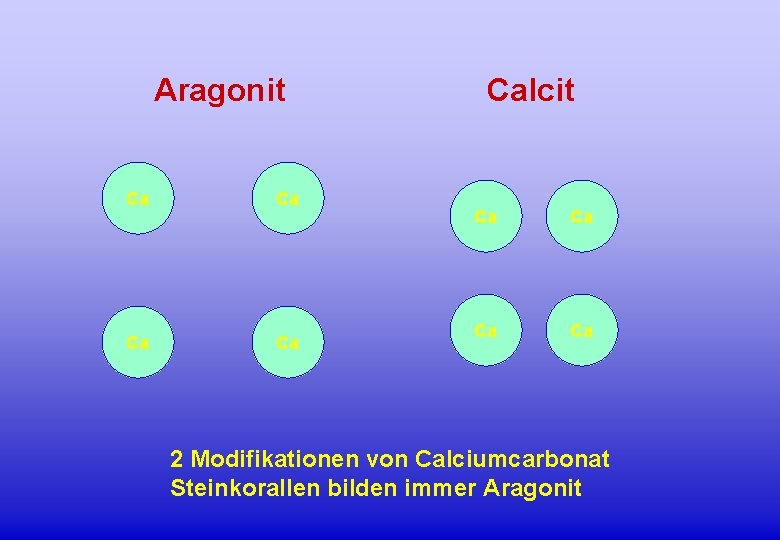
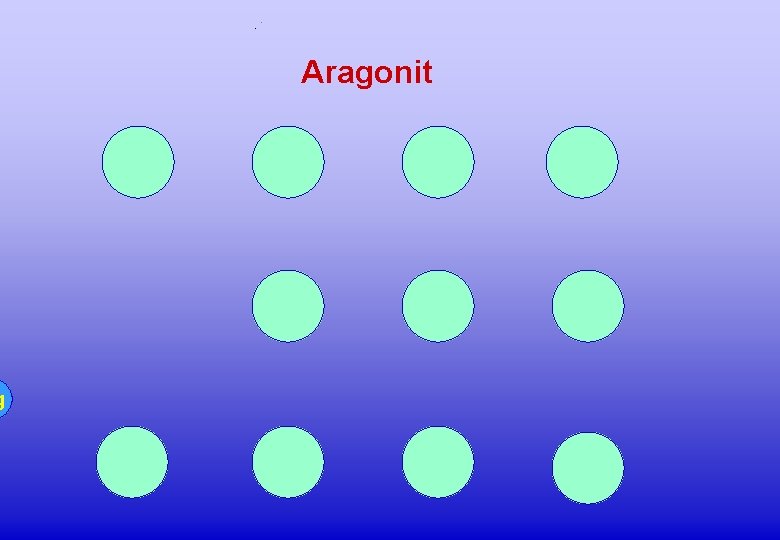
Aragonit Ca Ca Calcit Ca Ca 2 Modifikationen von Calciumcarbonat Steinkorallen bilden immer Aragonit


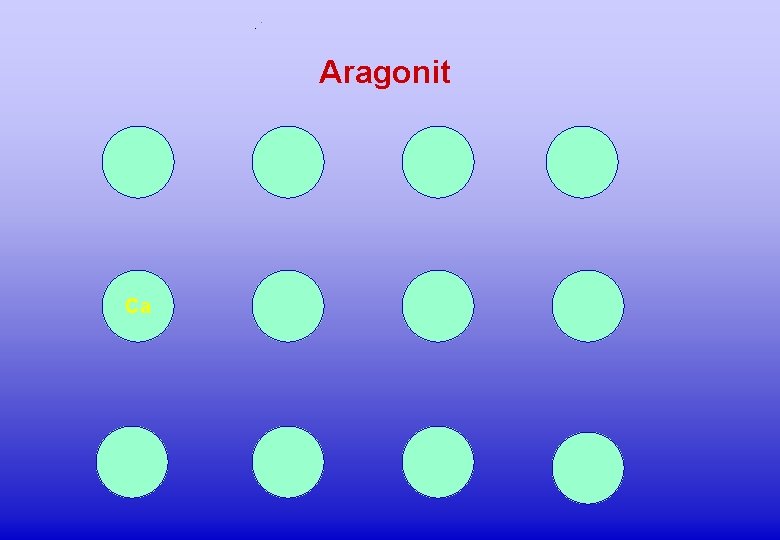
Aragonit Mg

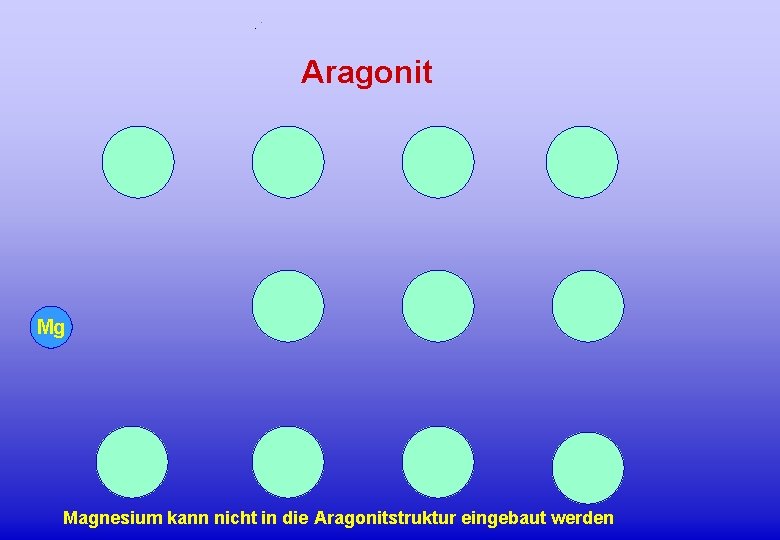
Aragonit Mg Magnesium kann nicht in die Aragonitstruktur eingebaut werden

g Aragonit

Aragonit Ca

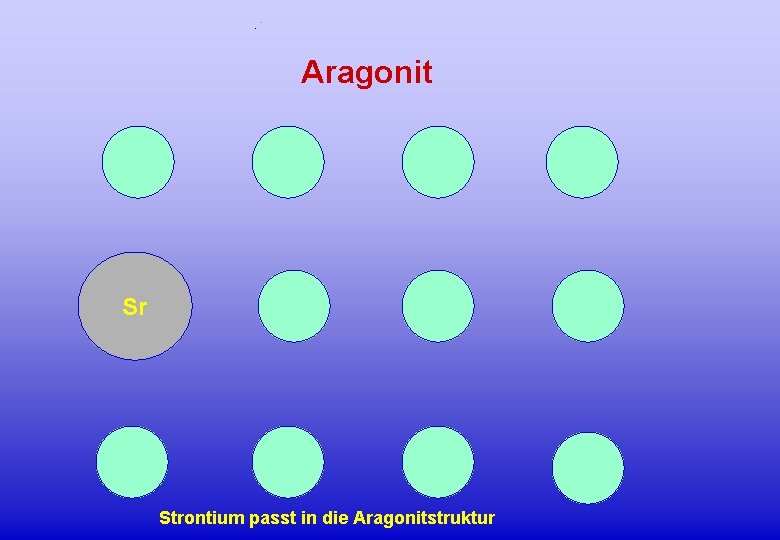
Aragonit Sr Strontium passt in die Aragonitstruktur

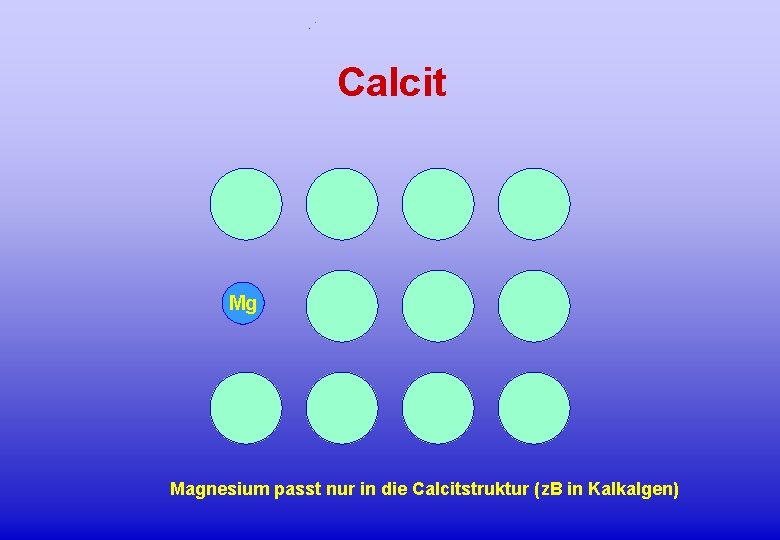
Calcit Mg Magnesium passt nur in die Calcitstruktur (z. B in Kalkalgen)

Wer verbraucht Magnesium ?

Wer verbraucht Magnesium ?

Wer verbraucht Magnesium ? Stein aus einem Becken, in das viel Magnesium gegeben wurde

Überschüssiges Magnesium lagert sich auf dem Gestein ab ! • Hoch Mg-Calcit Ca 0, 87 Mg 0, 13 Ca. CO 3 • Dolomit Mg. Ca(CO 3)2 • Huntit Mg 3 Ca(CO 3)4 • Magnesit Mg. CO 3 • Magnesiumhydroxidcarbonat Mg 5(CO 3)4(OH)2*5 H 2 O • Artinit Mg 2 CO 3(OH)2*3 H 2 O • Brucit Mg(OH)2

Überschüssiges Magnesium lagert sich auf dem Gestein ab ! • Silicatgesteine • Aragonit • Calcit • Dolomit • Magnesit zunehmend

Überschüssiges Magnesium lagert sich auf dem Gestein ab ! abhängig von : • p. H • CO 2 -Gehalt • k. H

Starke Magnesium-Zugabe ist nicht notwendig !

Wenn Mg zugegeben wird. . . wie ?

Übliche Mg-Zugabe : 1000 -Liter-Becken 100 mg/L Mg-Anhebung 758 g Mg. Cl 2 * 6 H 2 O + 95 g Mg. SO 4 * 7 H 2 O

Übliche Mg-Zugabe : Herleitung : 1 kg Meerwasser enthält 19, 35 g Chlorid und 2, 71 g Sulfat

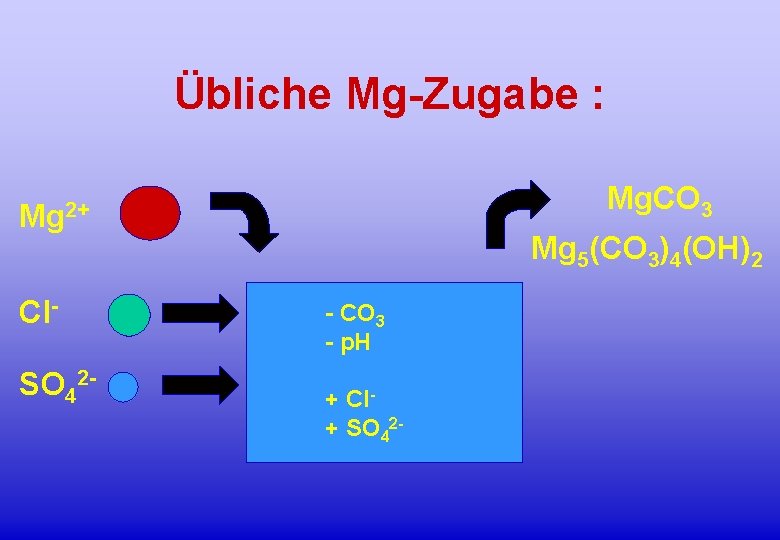
Übliche Mg-Zugabe : Mg. CO 3 Mg 2+ Cl. SO 42 - Mg 5(CO 3)4(OH)2 - CO 3 - p. H + Cl+ SO 42 -

Die Zugabe von Magnesium mit Hilfe von Magnesiumchlorid und Magnesiumsulfat bewirkt : - Überschuss an Chlorid und Sulfat Mangel an Carbonathärte Senkung des p. H

Gegenmaßnahmen : • Sulfat- und Chloridüberschuss unbedingt durch häufigen Wasserwechsel begrenzen • KH und p. H-Verringerung durch Zugabe von Natron (Na. HCO 3) und/oder Soda (Na 2 CO 3) ausgleichen

Bessere Vorgehensweise : • Magnesium nur als Magnesiumchlorid zugeben • KH als Soda (Na 2 CO 3) zugeben • mit Na. Cl-freiem Salz ausgleichen

Rechenbeispiel : • 1000 Liter-Becken soll um 100 mg/L Mg erhöht werden = 100 g Mg • Zugabe 836 g Mg. Cl 2 * 6 H 2 O • + 436 g Na 2 CO 3 (Soda) • + 120 g Na. Cl-freies Salz

VORSICHT. . . denn jedes Becken ist anders ! • KH + p. H kontrollieren • zu niedrige KH mit Natron ausgleichen • bei zu hoher KH weniger Soda zugeben • bei zu niedrigem p. H mehr Kalkwasser anwenden • bei zu hohem p. H Soda tlw. durch Natron ersetzen (je g Soda 1, 6 g Natron)