MADDENN YAPI TALARI MADDE Uzayda yer kaplayan ktlesi











- Slides: 23

MADDENİN YAPI TAŞLARI MADDE : Uzayda yer kaplayan kütlesi, hacmi ve eylemsizliği olan her şey Örnek: Demir, bakır, kurşun, altın, Tüm maddeleri bölerek küçük tanecikler elde edebiliriz. Bir maddeyi sonsuza kadar bölme işlemini devam ettirirsek, bir yapı birimi elde ederiz.

MADDENİN YAPI TAŞLARI Bir maddenin bütün özelliğini taşıyan en küçük taneciğine, o maddenin YAPI TAŞI denir. Maddeyi oluşturan en küçük yapı taşına ATOM denir. Aynı cins atomlardan oluşan maddelere ELEMENT denir. Örnek: bakır, demir, kükürt, hidrojen, oksijen Şu halde atom, bir elementin bütün özelliğini taşıyan en küçük yapı birimidir.

MADDENİN YAPI TAŞLARI Ayrıca, iki yada daha çok atomdan oluşan ve maddelerin bütün özelliklerini taşıyan küçük taneciklere MOLEKÜL adı verilir. Moleküller aynı cins atomlardan oluşabileceği gibi, farklı cins atomlardan da oluşabilirler. Örnek; Hidrojen molekülü ( H 2 ) , Hidrojen atomlarından, Oksijen molekülü (O 2 ) Oksijen atomlarından oluşmuştur.

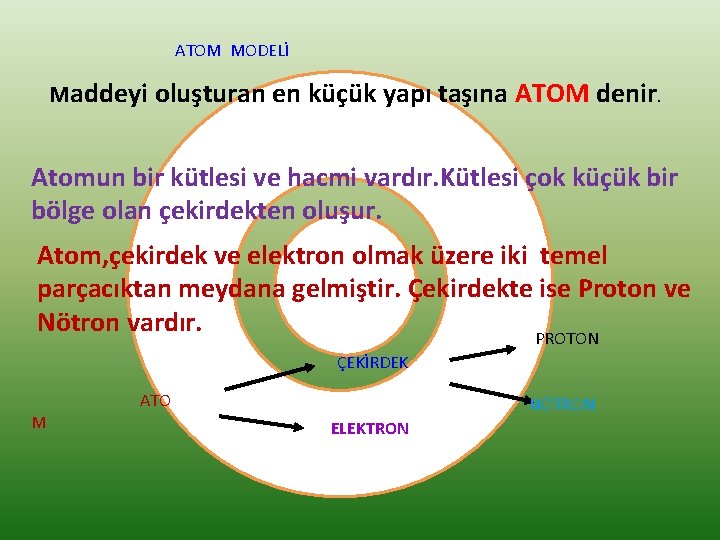
ATOM MODELİ Maddeyi oluşturan en küçük yapı taşına ATOM denir. Atomun bir kütlesi ve hacmi vardır. Kütlesi çok küçük bir bölge olan çekirdekten oluşur. Atom, çekirdek ve elektron olmak üzere iki temel parçacıktan meydana gelmiştir. Çekirdekte ise Proton ve Nötron vardır. PROTON ÇEKİRDEK ATO M NÖTRON ELEKTRON

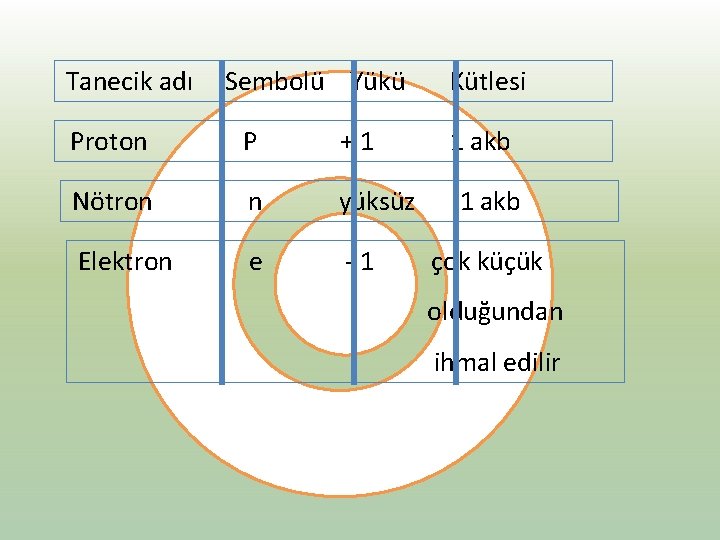
Tanecik adı Sembolü Yükü Proton P +1 Nötron n yüksüz Elektron e -1 Kütlesi 1 akb çok küçük olduğundan ihmal edilir

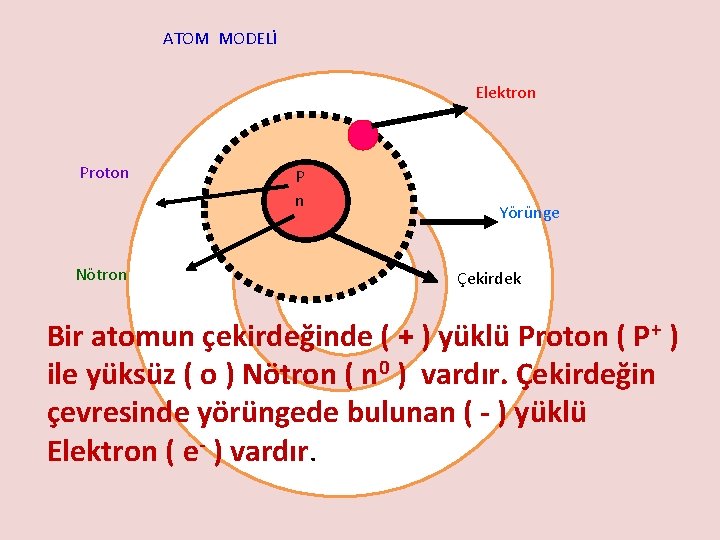
ATOM MODELİ Elektron Proton Nötron P n Yörünge Çekirdek Bir atomun çekirdeğinde ( + ) yüklü Proton ( P+ ) ile yüksüz ( o ) Nötron ( n 0 ) vardır. Çekirdeğin çevresinde yörüngede bulunan ( - ) yüklü Elektron ( e- ) vardır.

NOT: Elektron ve proton sayıları birine eşit olan atomlara NÖTR ( yüksüz ) atom denir.

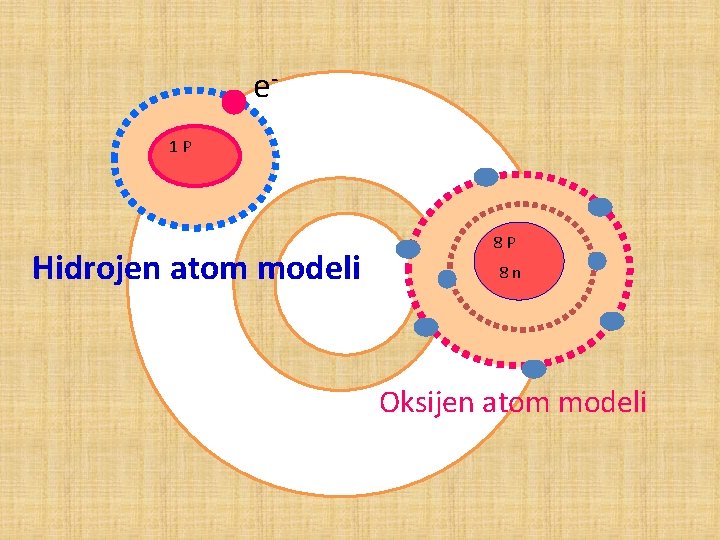
e 1 P Hidrojen atom modeli 8 P 8 n Oksijen atom modeli

ATOM NUMARASI - KÜTLE NUMARASI ATOM NUMARASI : Bir atomun proton sayısına, ATOM NUMARASI denir. Atom numarası ( A No ) ile gösterilir. ATOM NUMARASI = PROTON SAYISI A No = P sayısı

KÜTLE NUMARASI : Bir atomun çekirdeğinde bulunan proton ve nötronların toplamına KÜTLE NUMARASI denir. K No = P + n

Örnek : Çekirdeğinde 17 proton ve 18 nötron bulunan nötr bir atomun kütle numarasını bulunuz. P = 17 KN = P + n n = 18 KN = 17 + 18 KN = ? KN = 35 olur .

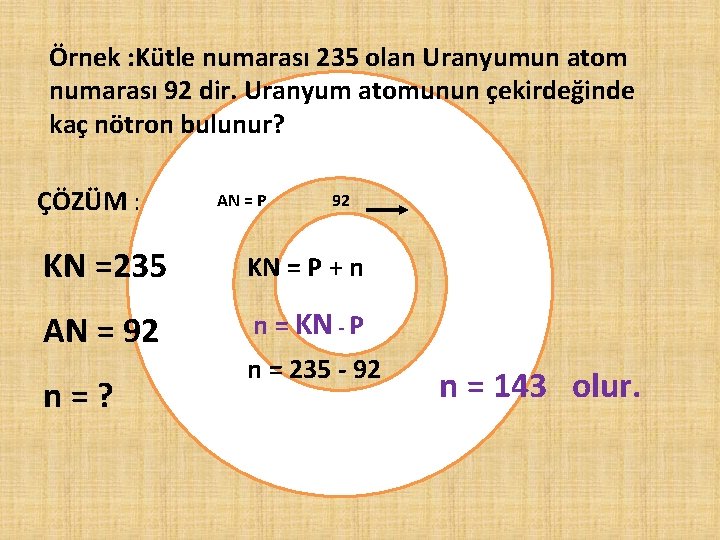
Örnek : Kütle numarası 235 olan Uranyumun atom numarası 92 dir. Uranyum atomunun çekirdeğinde kaç nötron bulunur? ÇÖZÜM : AN = P 92 KN =235 KN = P + n AN = 92 n = KN - P n=? n = 235 - 92 n = 143 olur.

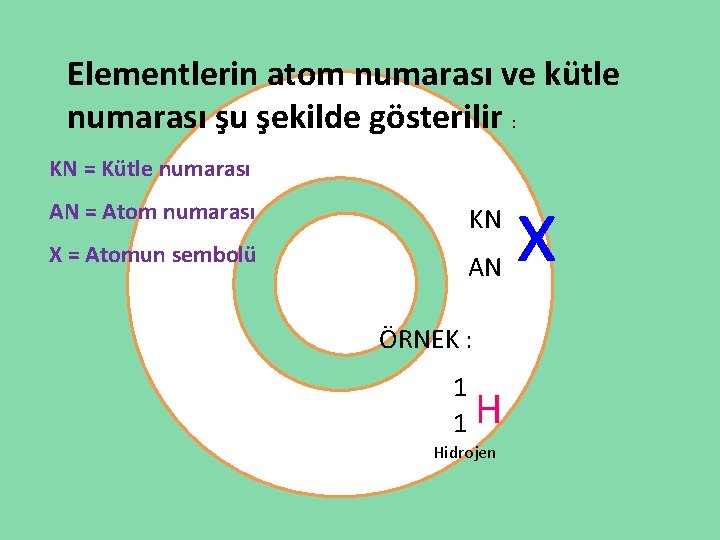
Elementlerin atom numarası ve kütle numarası şu şekilde gösterilir : KN = Kütle numarası AN = Atom numarası KN X = Atomun sembolü AN ÖRNEK : 1 1 H Hidrojen x

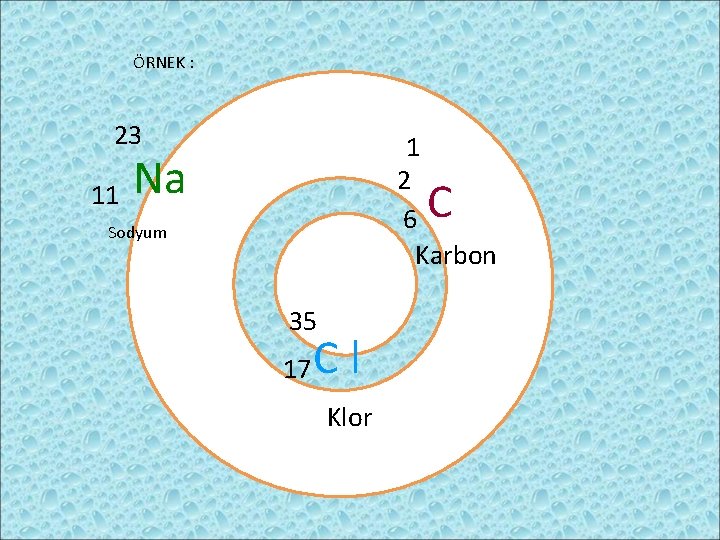
ÖRNEK : 23 11 1 2 6 Karbon Na C Sodyum 35 17 Cl Klor

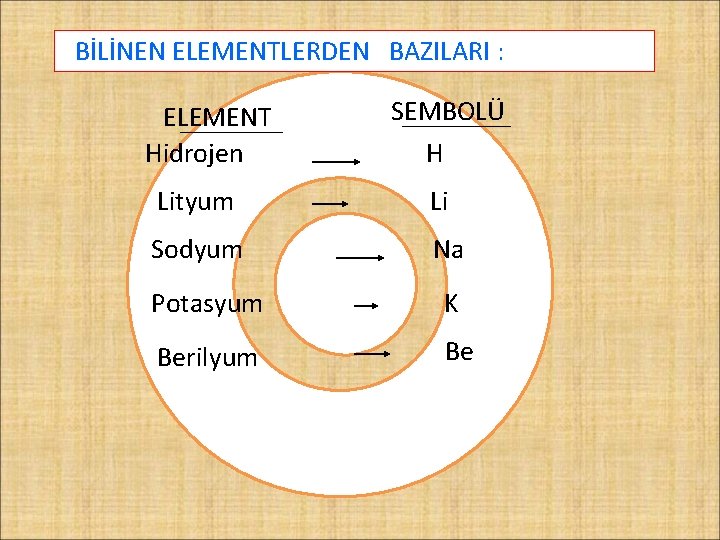
BİLİNEN ELEMENTLERDEN BAZILARI : ELEMENT Hidrojen SEMBOLÜ H Lityum Li Sodyum Na Potasyum K Berilyum Be

Mağnezyum Mg Kalsiyum Ca Bor Alüminyum Karbon B Al C

BİLİNEN ELEMENTLERDEN BAZILARI : ELEMENT SEMBOLÜ Silisyum Si Fosfor P Oksijen O Klor Cl Brom Br Flor İyot Demir F Bakır Gümüş I Fe Cu Ag

İZOTOP ELEMENTLER Bir elementin bütün atomlarındaki proton sayıları aynıdır. Bir elementi bu değer karakterize der. Fakat bir elementin atomlarında farklı sayıda nötron bulunabilir.

İZOTOP ELEMENTLER Bir elementin bütün atomlarındaki proton sayıları aynıdır. Bir elementi bu değer karakterize der. Fakat bir elementin atomlarında farklı sayıda nötron bulunabilir. Aynı elementin değişik kütlede olan atomlarına o elementin İZOTOPLARI denir. Ya da eşit sayıda protona, farklı sayıda nötrona sahip ve kütleleri farklı atom çekirdeklerine o elementin İzotopları denir.

İZOTOP ELEMENTLER Kısaca, atom numaraları ( AN ) aynı, kütle numaraları ( KN ) farklı atomlara İzotop denir. AN = AN KN = KN e- = e n=n

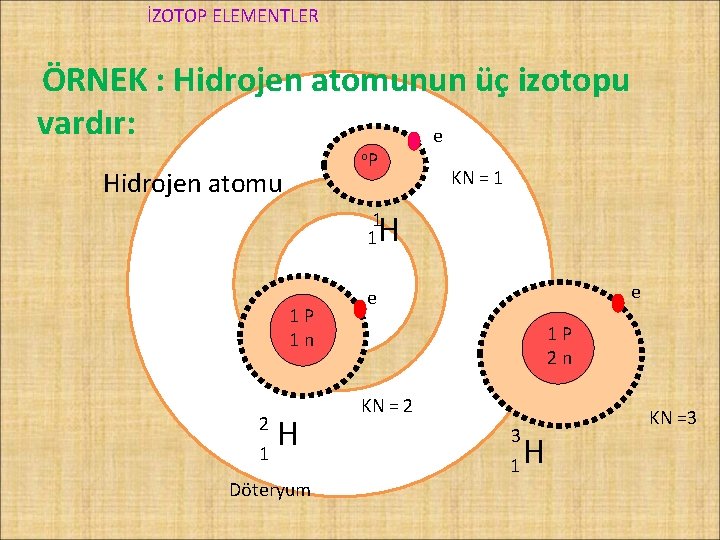
İZOTOP ELEMENTLER ÖRNEK : Hidrojen atomunun üç izotopu vardır: e o. P Hidrojen atomu KN = 1 H 1 1 1 P 1 n 2 1 H Döteryum e e 1 P 2 n KN = 2 3 1 H KN =3

NOT I : İzotop elementlerin, kimyasal özelliklei aynı, fiziksel özellikleri ise farklıdır. Çünkü kimyasal özellikler çekirdekteki proton sayısının tuttuğu elektronlara bağlıdır. Elektronların alınıp verilmesi ile kimyasal değişmeler olur.

SORU : Bir elementin izotop atomlarında aşağıdakilerden hangilerinin sayısı farklıdır? I. Elektron II. Proton III. Nötron IV. Proton ve Elektron A. Yalnız I B. Yalnız III C. I - II D. II - IV İzotop atomların nötron sayıları farklıdır.