MADDENN TANECKL YAPISI NTE Maddenin Tanecikli Yaps niteye



















- Slides: 20

MADDENİN TANECİKLİ YAPISI

ÜNİTE : Maddenin Tanecikli Yapısı Üniteye Giriş • Evrendeki tüm maddeler, tüm cisimler kendilerinden çok küçük parçacıklardan oluşmuşlardır. • Örneğin; çok fırtınalı bir günde arabaların camlarının tozdan adeta görünmediği zamanlar olur. İşte arabanın camını örten toz uzaktan sanki arabanın camını örten bir bez parçası gibi görünür. • Halbuki görünen toz ve kir topluluğu çok daha küçük toz parçalarından oluşur.

• Maddelerde toz parçacıkarı gibi çok küçük, gözle göremeyeceğimiz parçalardan oluşur. • Buna göre bir elmanın gözle görünmeyen daha küçük elma parçacıklarından oluştuğunu düşünebiliriz. • İşte taşı, toprağı, kalemi, defteri kısacası tüm madde ve cisimleri oluşturan parçacıklara ” atom “ denir.

Maddeyi Oluşturan Tanecikler • Günlük hayatta kullandığımız tüm malzemeler, eşya gibi kütlesi ve hacmi olan her şeye madde denir. Maddenin belirli bir şekil verilmiş haline ise cisim denir. Ağaç bir madde iken, ağaçtan yapılan sandalye bir cisimdir. Maddenin belirli bir hacmi ve kütlesi vardır. Maddeler katı, sıvı ve gaz olmak üzere üç farklı şekilde bulunabilirler.

Maddenin özelliklerini aşağıdaki gibi özetleyebiliriz: • Bazı maddelerin belirli biçimi ve hacmi vardır. • Bazı maddeler bulunduğu kabın şeklini alır. Bazıları ise doldurdukları kısmın şeklini alırlar. • Bazı maddeler ısıtıldıklarında erirken bazıları buharlaşırlar. • Aynı koşullarda maddenin miktarı değiştirildiğinde tütlesi ve hacmi değişir. • Bazı maddeler şıkıştırabilirken bazı maddeler sıkıştırılamazlar. • Maddeler küçük taneciklerden oluşurlar.

• 1. Maddenin Sıkışabilme Özelliği • Doğadaki maddeler katı, sıvı ve gaz hâllerde bulunur. • Maddenin katı hâline demir çubuk, alüminyum tencere, kalem, masa, taş örnek verilebilir. • Maddenin sıvı hâline su, alkol, kolonya örnek verilebilir. • Gaz hâline ise hava, bulut, sigara dumanı örnek verilebilir.

• Bu maddelerin sertliklerinin farklı olduğunu hepimiz biliriz. • Havaya yumruk atmak, suda kulaç çekmek, masaya yumruk vurmak birbirinden çok farklıdır ve farklı tepkiler verir. • Burada olduğu gibi maddelerin sıkışabilme özellikleri de farklıdır. • Bir koltuğa oturduğumuzda minderin küçülmesi süngerden kaynaklanır. Süngere kuvvet uygulannca sünger küçülmüştür. İşte buna sıkışma denir. .

• Basit bir örnek vermek gerekirse araba lastiklerinin içerisinde hava vardır. Lastikler hava ile şişirilerek taşıtı taşıması sağlanır. • Lastiğin havası kaçarsa “teker patlamış “ denir ve lastik söner. • Tersi olayda ise lastiğe hava verildikçe içerideki dışa doğru olan itme kuvveti artar ve lastiğin içerisindeki gaz oranı arttıkça gaz sıkışmış olur.

• Şimdi de iki adet şırınga alalım. Şırıngalardan birisine su çekelim. Diğer şırınganın da pistonunu boş iken çekelim. • Boş olarak çekilen şırınganın içerisine hava dolmuştur. Her iki şırınganın da uçlarını tamamen kapatıp pistonlardan bastıralım. • Su dolu olan şırıngada piston ilerlemez iken, hava dolu olan şırıngada piston bir miktar ileri doğru ilerleyebilmektedir. • Yani hava daha önce büyük bir hacim kaplarken, şimdi daha küçük hacim kaplamaktadır. Hava dolu şırınga sıkıştırılabilir.

• Katılar sıkıştırılamazlar, sıvılar sıkıştırılamalar ama gazlar sıkıştırılabilir. • 2. Genleşme • Yaz aylarında telefon tellerinin sıkıştığını, kış aylarında ise normalleştiğini görmüşüzdür. • Yine yaz aylarında tren raylarında şekildeki gibi bozulma olmaması için demir çubuklar arasına boşluklar bırakılır.

• Kullandığımız termometrelerde genleşme prensibinden yararlanılarak yapılmıştır. • Bulunduğu ortamın sıcaklığı değiştirildiğinde termometrenin içinde bulunan sıvının yüksekliği değişir. Maddeler sıcaklık ile genleşirler. 3. Maddenin Boşluklu Yapısı • Süngeri elimizle bastırdığımızda sıkışması, futbol topunun sıcak suda şişmesi gibi olaylara göre maddeler kuvvet etkisi ile ya da sıcaklık etkisi ile hacim değişimine uğrarlar.

• Miktarı değişmeyen maddenin hacminde oluşan bu değişimler, maddenin tanecikleri arasında boşluklar olduğu • ve bu boşlukların büyüklüğünün sıcaklık ya da kuvvet etkisi ile değiştiği sonucunu ortaya çıkarır. • Gazlar hem kolayca sıkışabilirler, hem de kolayca genleşirler. Katı ve sıvı hâldeki maddeler kuvvet etkisi ile sıkışmaya ve sıcaklık etkisi ile genleşmeye karşı , gazlara göre daha dirençlidirler • Yani çok az sıkışırlar ya da az genleşirler. Buna göre, gazlardaki tanecikler arasındaki boşluklar katı ve sıvılara göre oldukça fazladır.

4. Maddeyi Oluşturan Yapıtaşları : ( ATOM ) • Bilim insanları maddeyi sürekli incelemişlerdir ve en küçük parçalara ayırmaya çalışmışlardır. Atom ve Atomun Tarihçesi • Maddenin küçük, bölünemez parçacıklardan oluştuğu düşüncesini ilk olarak Yunanlı filozof Demokritos ( M. Ö. yaklaşık 460 – 370 ) ortaya atarak bu parçacıklara eski Yunanca ” bölünemez “ karşılığı olan ” Atom “ adını vermiştir. • Yeni Zelanda ‘lı fizikçi Ernest Rutherford ( 1871 – 1937 ) da atomu parçalayarak bölünebilir olduğunu • ve atomun yapısında da büyük boşluklar olduğunu ispatlayan ilk bilim insanlarından biriydi.

• Danimarka ‘lı bilim insanı Niels Bohr da 1913 ‘de kendinden önceki araştırmacıların fikirlerini geliştirerek ; • Atomun daha da küçük parçacıklardan oluştuğunu gösteren bir model tasarlamıştır. • Maddenin en küçük yapı birimi olan atom bölünemez değildir. Değişik yöntemlerle bölünebilir. Ancak böyle bir durumda kimliği değişir ve yeni bir madde oluşur.

B. ELEMENTLER ve BİLEŞİKLER 1. Elementenler • Aynı çeşit atomların bir araya gelerek oluşturdukları maddelere element denir. • Hidrojen, oksijen, karbon ve iyot maddelerinin herbiri ayrı bir elementi temsil etmektedir. • Şu anda 100 den fazla sayıda element türü yani 100 den farklı atom türü vardır.

Elementlerin Özellikleri ; • Yapılarında tek cins atom vardır. • Saf maddelerdir. • Erime ve kaynama sıcaklıkları bellidir. • Belirli bir öz kütle değerleri vardır. • Farklı elementlerin atomları farklıdır. • Fiziksel ve kimyasal yollarla daha basit maddelere bölünemezler.

2. Bileşikler • Birden fazla atom bir araya gelerek molekülleri oluşturur. • Moleküller 2 ‘şerli atomlardan oluştuğu gibi 3 ‘ erli, 4 ‘erli hatta onbinlerce atom içerebilir. • İki ya da daha fazla çeşit element atomlarının oluşturdukları yeni, saf maddeye bileşik denir.

• H 2 O molekülünde de iki farklı atom bir araya gelerek 3 atomlu molekülü oluşturmuştur. • H 2 O bir bileşiktir. CO 2 molkülünde iki farklı atom bir araya gelerek 3 atomlu molekülü oluşturmuştur. CO 2 de bir bileşiktir.

• Tuzlarda olduğu gibi bazı bileşikler kristal adı verilen yapılardan oluşur. Bileşiklerin Özellikleri ; Yapılarında en az iki cins atom vardır. Erime va kaynama noktaları bellidir. Belirli bir öz kütle değerleri vardır. Bileşiği oluşturan atomların sayıları arasındaki oran değişirse farklı bir bileşik oluşur. • Bir bileşiği oluşturan atomlar birbirine bağlıdır. • •

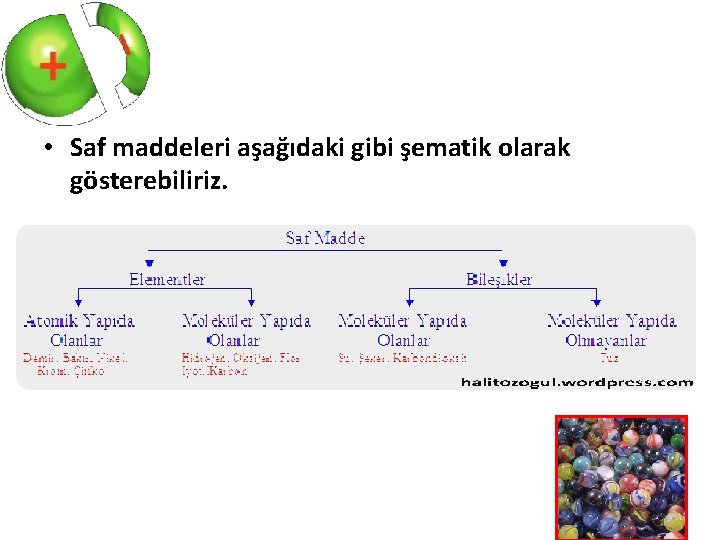
• Saf maddeleri aşağıdaki gibi şematik olarak gösterebiliriz.