MADDENN HALLER VE ISI HLAL AKPOLAT FEN BLGS

MADDENİN HALLERİ VE ISI HİLAL AKPOLAT FEN BİLGİSİ ÖĞRETMENLİĞİ AKDENİZ ÜNİVERSİTESİ 3. SINIF 2. ŞUBE 20130905012 1

ÖZ ISI �Öz ısı bir maddenin bir gramının sıcaklığını 1°C arttırmak için gerekli ısı miktarıdır. c ile gösterilir. �Her saf maddenin aynı şartlardaki öz ısısı farklıdır. Dolayısıyla öz ısı maddeler için ayırt edici bir özelliktir. � Ayırt edici özellikler madde miktarına bağlı değildir. 2
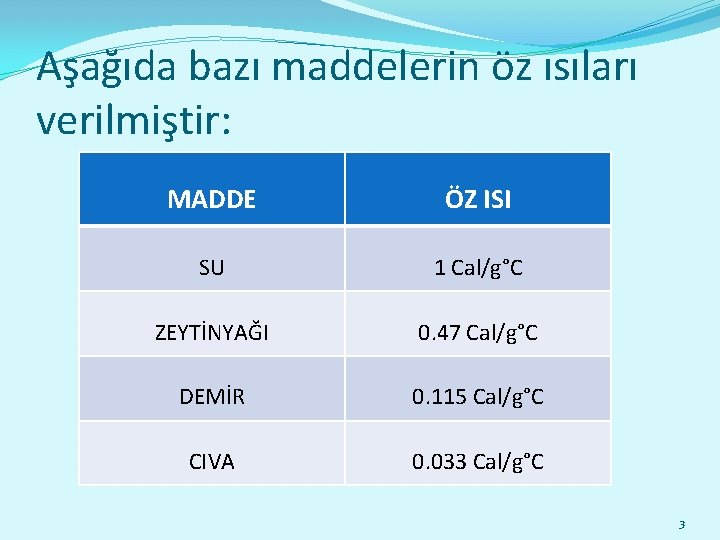
Aşağıda bazı maddelerin öz ısıları verilmiştir: MADDE ÖZ ISI SU 1 Cal/g°C ZEYTİNYAĞI 0. 47 Cal/g°C DEMİR 0. 115 Cal/g°C CIVA 0. 033 Cal/g°C 3

4, 18 J’dür. 1 cal = 4, 18 J’dür. 1 J = 0, 24 cal’dir. Örnek: 200 cal kaç Joule eder? Cevap: 1 cal = 4, 18 Joule 200 cal = 200. 4, 18 Joule = 386 Joule eder. 4
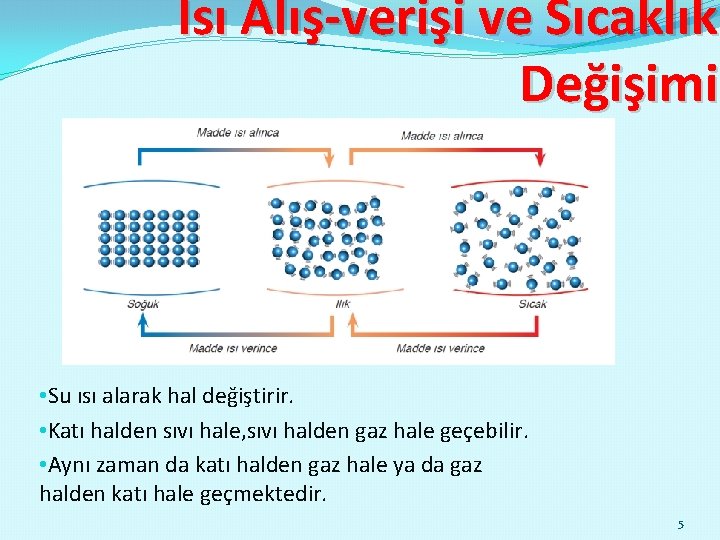
Isı Alış-verişi ve Sıcaklık Değişimi • Su ısı alarak hal değiştirir. • Katı halden sıvı hale, sıvı halden gaz hale geçebilir. • Aynı zaman da katı halden gaz hale ya da gaz halden katı hale geçmektedir. 5
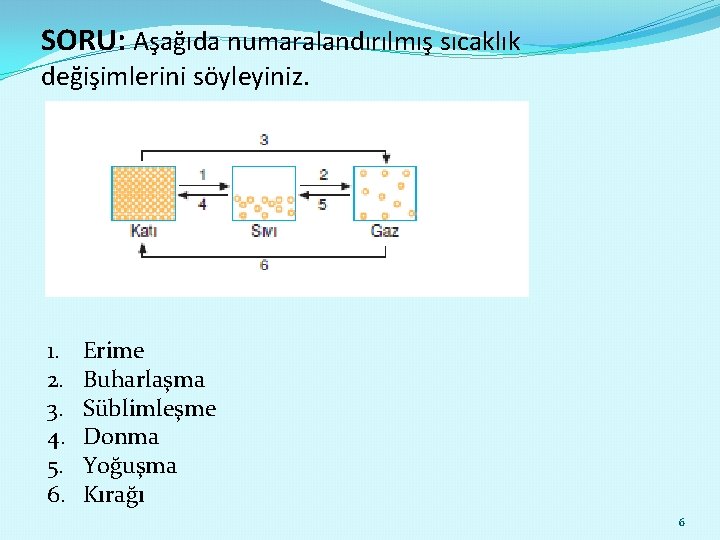
SORU: Aşağıda numaralandırılmış sıcaklık değişimlerini söyleyiniz. 1. 2. 3. 4. 5. 6. Erime Buharlaşma Süblimleşme Donma Yoğuşma Kırağı 6
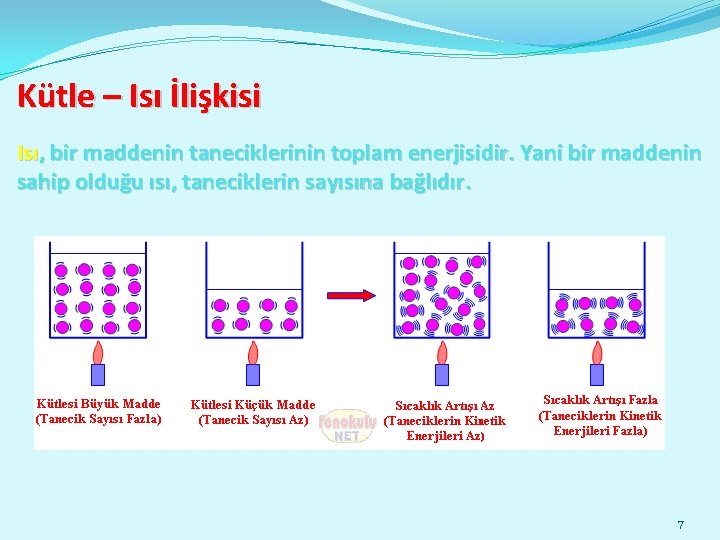
Kütle – Isı İlişkisi Isı, bir maddenin taneciklerinin toplam enerjisidir. Yani bir maddenin sahip olduğu ısı, taneciklerin sayısına bağlıdır. 7

Sıcaklıkları aynı olan farklı hacimlerdeki iki demir bilyenin sahip oldukları ısı enerjileri farklıdır: Demir bilyelerin taneciklerinin ortalama hareket enerjileri aynıdır. Ancak bilyelerin taneciklerinin sayısı farklı olduğu için ısıları farklıdır. Büyük bilyenin tanecik sayısı fazla olduğu için ısısı daha fazladır. 8
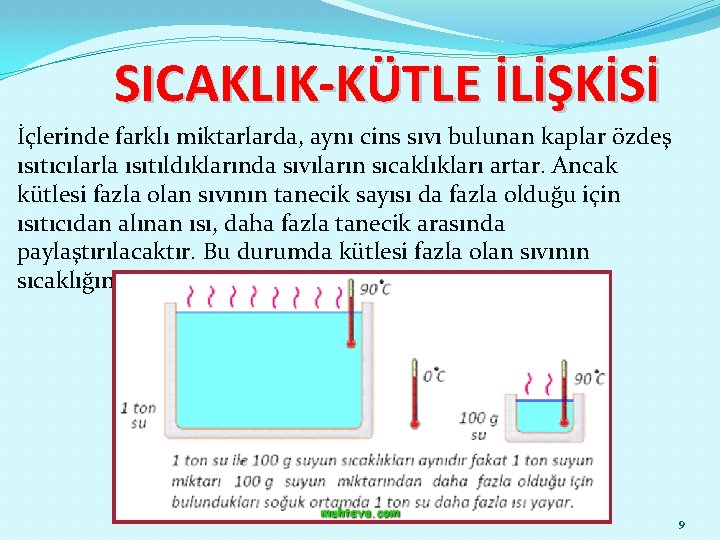
SICAKLIK-KÜTLE İLİŞKİSİ İçlerinde farklı miktarlarda, aynı cins sıvı bulunan kaplar özdeş ısıtıcılarla ısıtıldıklarında sıvıların sıcaklıkları artar. Ancak kütlesi fazla olan sıvının tanecik sayısı da fazla olduğu için ısıtıcıdan alınan ısı, daha fazla tanecik arasında paylaştırılacaktır. Bu durumda kütlesi fazla olan sıvının sıcaklığındaki artış daha az olur. 9

MADDENİN HALLERİ VE ISI-ALIŞ-VERİŞİ • Erime/Donma Isısı • Buharlaşma/Yoğunlaşma Isısı • Isınma-Soğuma Eğrileri 10

ERİME ISISI • Erime sıcaklığına ulaşmış 1 gram saf katı maddenin tamamen erimesi için gerekli ısı miktarına erime ısısı denir. • Hal değiştiren bir maddenin aldığı ısı enerjisi, maddenin tanecikleri arasındaki mesafeyi artırarak moleküller arasındaki çekim kuvvetinin azalmasını sağlar. • Her maddenin tanecikleri arasındaki çekim kuvveti aynı değildir. 11

• Erime ısısı Le ile gösterilir. Birimi J/g’dır. • Erime ısısı sadece erime sıcaklığındaki maddeler için söz konusudur. Örneğin buzun erime ısısı 334, 4 J/g’dır. Bu ısı -20 ºC’deki bir buza verildiğinde buzun sıcaklığı artar ama buz erimez. Ancak aynı ise 0 ºC’deki buza verildiğinde buzun sıcaklığı artmaz ama erir. 12

Bir miktar maddenin erimesi için gerekli ısıyı şu bağıntı ile hesaplayabiliriz: Q= m x L Q= Erime için gerekli ısı enerjisi m =kütle Le =erime ısısı 13
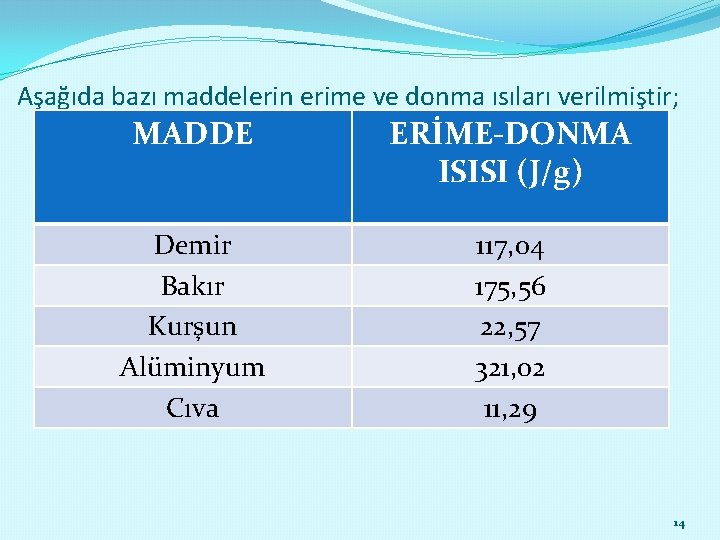
Aşağıda bazı maddelerin erime ve donma ısıları verilmiştir; MADDE ERİME-DONMA ISISI (J/g) Demir Bakır Kurşun Alüminyum Cıva 117, 04 175, 56 22, 57 321, 02 11, 29 14

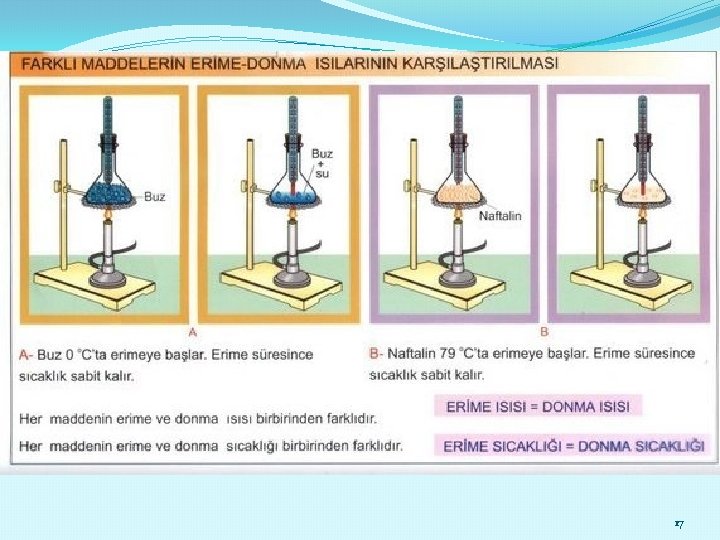
DONMA ISISI �Donma sıcaklığında bulunan 1 gram saf sıvı maddenin tamamen katı hale geçmesi için gerekli ısı miktarına donma ısısı denir. �Donan maddenin çevresine verdiği ısı miktarı, erirken aldığı ısı miktarına eşittir. Yani bir maddenin donma ve erime ısıları birbirine eşittir. Ld şeklinde gösterilir. (Bir madde için Le = Ld) 15

Not: Farklı maddelerin erime ve donma ısıları birbirlerinden farklıdır. Örneğin: suyun erime ve donma ısısı birbirine eşittir ancak demir ve suyun erime(donma) ısıları birbirinden farklıdır. �Bir miktar maddenin donması için gerekli ısıyı şu bağıntı ile hesaplayabiliriz: Q= m x Ld 16
17

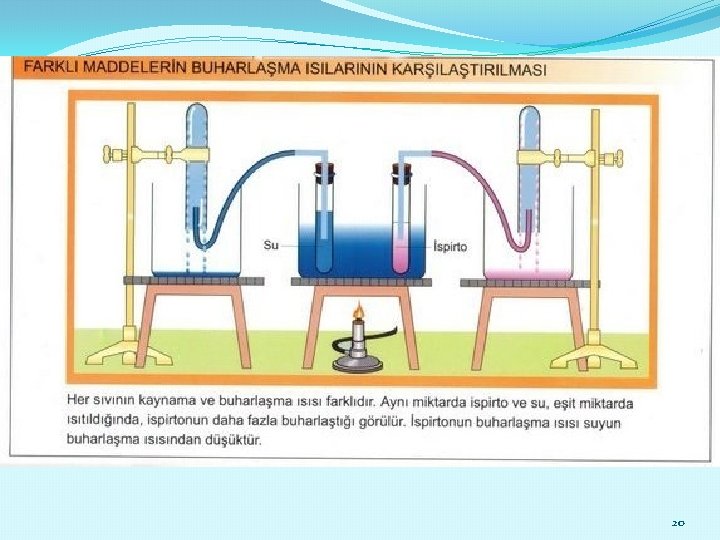
BUHARLAŞMA ISISI �Sıvı halde bulunan bir maddenin gaz haline geçmesi olayına buharlaşma denir. �Kaynama sıcaklığındaki 1 gram saf sıvıyı aynı sıcaklıktaki 1 gram buhar haline getirmek için gerekli ısıya buharlaşma ısısı denir. 18

�Buharlaşma olayının gerçekleşmesi için maddenin ısıya ihtiyaç vardır. �Maddenin aldığı bu ısı, tanecikler arasındaki bağların yok olacak kadar zayıflamasına neden olur ve tanecikler birbirinden bağımsız hale gelir. �Q = m x Lb �Lb ile gösterilir. 19
20

YOĞUNLAŞMA ISISI �Gaz halindeki maddenin sıvı hale geçmesine yoğunlaşma denir. �Kaynama sıcaklığında ve gaz halinde bulunan 1 gram maddenin, aynı sıcaklıkta tamamen sıvı hale geçerken çevresine verdiği ısıya yoğunlaşma ısısı denir. �Ly ile gösterilir. �Buharlaşma ve yoğunlaşma ısıları maddeler için ayırt edici özelliktir. 21

�Not: Sıvılar buharlaşırken aldıkları ısıyı yoğunlaşırken geri verirler. Kaynama sıcaklığındaki buhar yoğunlaşma ısısı kadar ısı kaybettiğinde sıvı haline geçer. Bu yüzden buharlaşma ısısı yoğunlaşma ısısına eşittir. Bir madde için Lb = Ly dir. 22

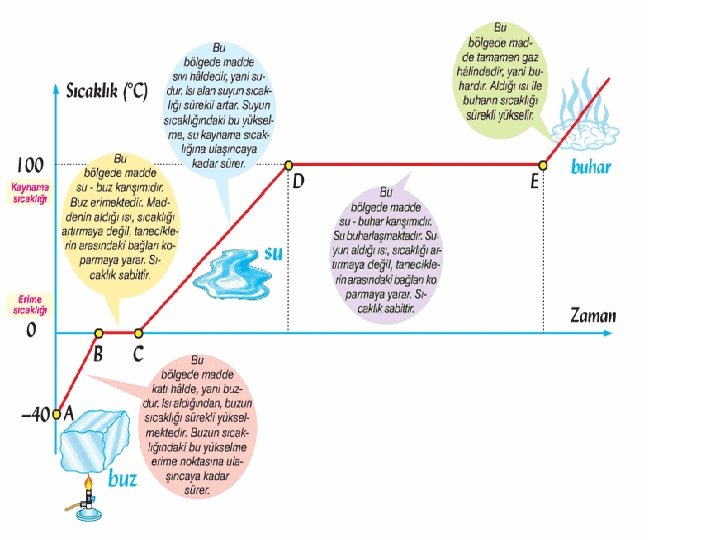
ISINMA-SOĞUMA EĞRİLERİ • 0 C"ta su donar, buz erir; 100 C"ta su kaynar, su buharı yoğuşur. • Suyun miktarı değişse bile bu değerler değişmez. • Aşağıda, buzun hal değiştirerek sıvı hale ve sıvı halden gaz haline geçiş grafiğini görüyoruz. 23
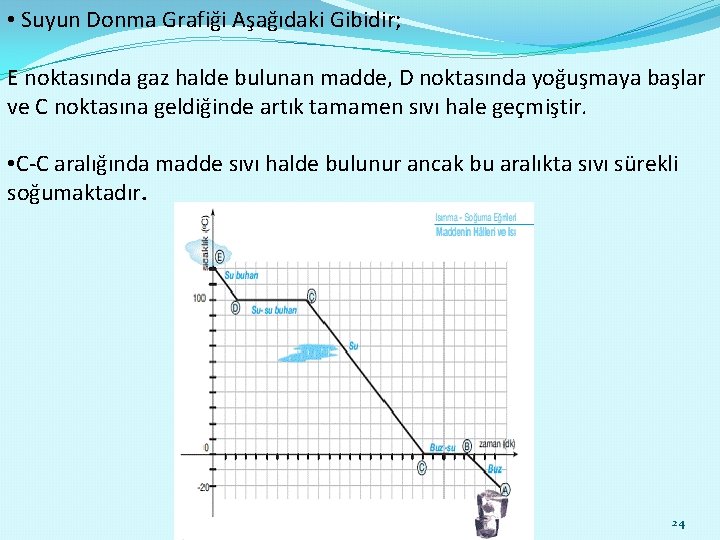
• Suyun Donma Grafiği Aşağıdaki Gibidir; E noktasında gaz halde bulunan madde, D noktasında yoğuşmaya başlar ve C noktasına geldiğinde artık tamamen sıvı hale geçmiştir. • C-C aralığında madde sıvı halde bulunur ancak bu aralıkta sıvı sürekli soğumaktadır. 24
25

�Saf bir maddeye başka bir madde karışınca maddenin erime ve donma sıcaklığı değişmez. (D) �Suya tuz ilave edilince donma noktası yükselir. (Y) �Isı enerjisi kütlenin yoğuşma ısısına bölümüne eşittir. (Y) �Suyun donarken hacmi büyür. (D) �Kışın kar yağmaya başladığında hava sıcaklığı artar. (Y) 26

Kaynakça �İlköğretim Fen Ve Teknoloji Ders Kitabı (8. Sınıf) �www. fenokulu. net �http: //www. bilgicik. com/yazi/maddenin-fizikselozellikleri/ �http: //www. muhteva. com/isinma-ve-soguma-egrilerit 262219. html 27
- Slides: 27