MADDE VE ISI Periyodik Sistem Periyodik Tablonun Tarihsel
MADDE VE ISI

Periyodik Sistem Periyodik Tablonun Tarihsel Gelişimi 1. Johan Döbereiner �Döbereiner elementleri benzer kimyasal özelliğine göre 3’erli gruplar halinde sıralamıştır. �Hatırlatıcı: Döb-e-r-e-in-e-r �e e e isim içindeki 3 tane ‘’e’’ harfinden 3’erli gruplar �Diğer bilim insanlarının isimlerinin hiçbirinde 3 tane ‘’e’’ harfi bulunmuyor.

Periyodik Sistem Periyodik Tablonun Tarihsel Gelişimi 2. Alexandre Beguyer de Chancourtois � Beguyer benzer özellik gösteren elementleri dikey ve sarmal olarak sıralamıştır. �Hatırlatıcı: Beguyer ismindeki ‘’g’’ harfinin altı dikey ve sarmal olarak uzatılabilir.

Periyodik Sistem Periyodik Tablonun Tarihsel Gelişimi 3. John Newlands �Newlands, ilk 8 elementten sonra gelen elementlerin özelliklerinin periyodik olarak devam ettiğini görmüş ve 8’erli gruplar halinde sıralamıştır. �Bu 8’li grupları müzikteki notalara benzetmiş ve ‘’oktav kanunu’’ olarak adlandırmıştır. �Hatırlatıcı: Newlands isminin içindeki ‘’W’’ harfi yatay 8 sayısına benzetilebilir.

Periyodik Sistem Periyodik Tablonun Tarihsel Gelişimi 4. Dimitri Mendeleyev �Mendeleyev elementleri artan atom ağırlığına göre sıralamış ve yaptığı periyodik tablo ile periyodik tablonun temelini attığı için periyodik tablonun babası unvanını almıştır. �Yaptığı periyodik tabloda bazı boşluklar kalmıştır. Bu boşluklar ile bulunmayan bazı elementlerin varlığını tahmin etmiştir. �Hatırlatıcı: Mendeleyev Baba

Periyodik Sistem Periyodik Tablonun Tarihsel Gelişimi 5 - Lothar Meyer �Meyer , elementleri fiziksel özelliklerine göre sıralamıştır. �Mendeleyev ile aynı zamanda birbirine benzer çalışma yapmıştır. �Hatırlatıcı: M-eyer ve M-endeleyev

Periyodik Sistem Periyodik Tablonun Tarihsel Gelişimi 6. Henry Moseley �Moseley, elementleri, artan atom numaralarına(proton sayısı) göre sıralamıştır. �Hatırlatıcı: Atom No su ile Moseley ismindeki Mo kelimesi çağrışım yapılabilir. (MO-NO)

Periyodik Sistem Periyodik Tablonun Tarihsel Gelişimi 7 - Glenn Seaborg �Glenn Seaborg, periyodik tablonun altına iki sıra daha ekleyerek, periyodik tabloya son halini vermiştir. �Hatırlatıcı: Glenn � Seaborg

Periyot ve Gruplar �Periyodik tabloda elementler proton sayısına göre sırlanmıştır. Elementlerin atom numarası yapısındaki proton sayısına göre verilmiştir. �Dolayısı ile ‘’atom numarası’’ , ‘’proton sayısına’’ eşittir. (Atom numarası =Proton sayısı)
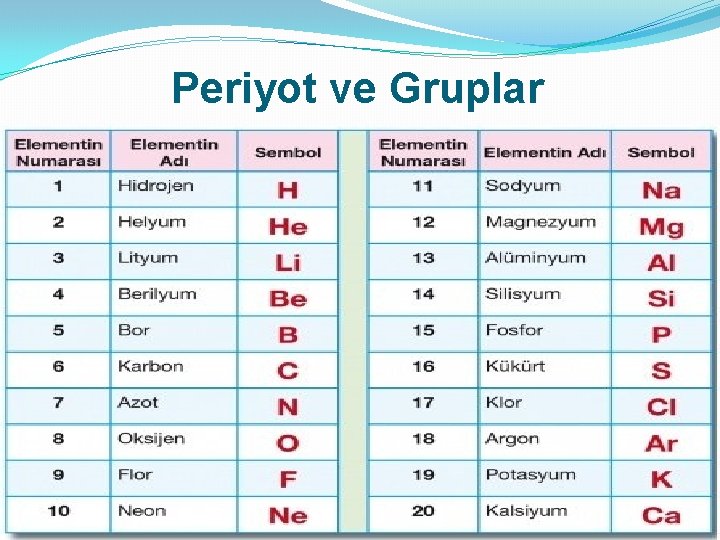
Periyot ve Gruplar
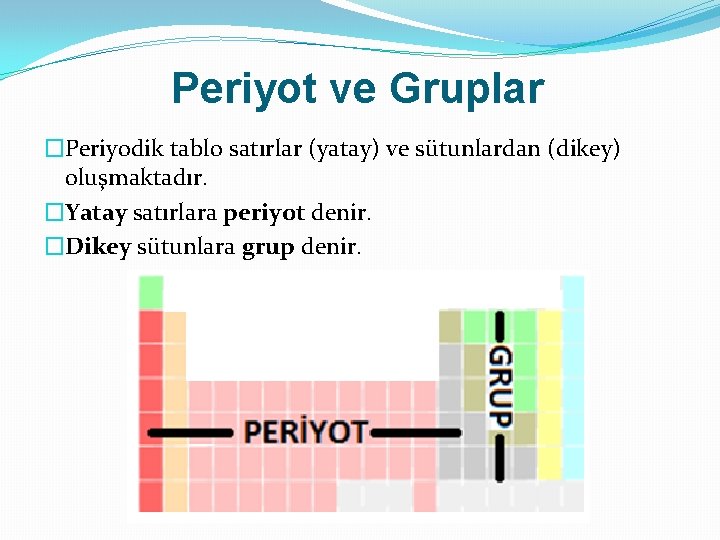
Periyot ve Gruplar �Periyodik tablo satırlar (yatay) ve sütunlardan (dikey) oluşmaktadır. �Yatay satırlara periyot denir. �Dikey sütunlara grup denir.
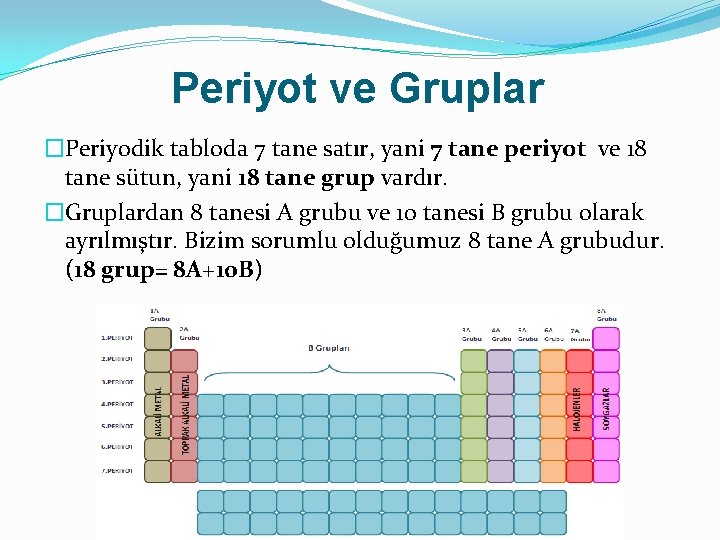
Periyot ve Gruplar �Periyodik tabloda 7 tane satır, yani 7 tane periyot ve 18 tane sütun, yani 18 tane grup vardır. �Gruplardan 8 tanesi A grubu ve 10 tanesi B grubu olarak ayrılmıştır. Bizim sorumlu olduğumuz 8 tane A grubudur. (18 grup= 8 A+10 B)

Periyot ve Gruplar Bir Elementin Periyodik Tabloda Yeri Nasıl Bulunur? �Elementin elektronlarını katmanlara yerleştiririz. �Elde ettiğimiz elektron-katman düzeninde katman sayısı periyot numarasını verir. �Son katmandaki elektron sayısı grup numarasını verir.
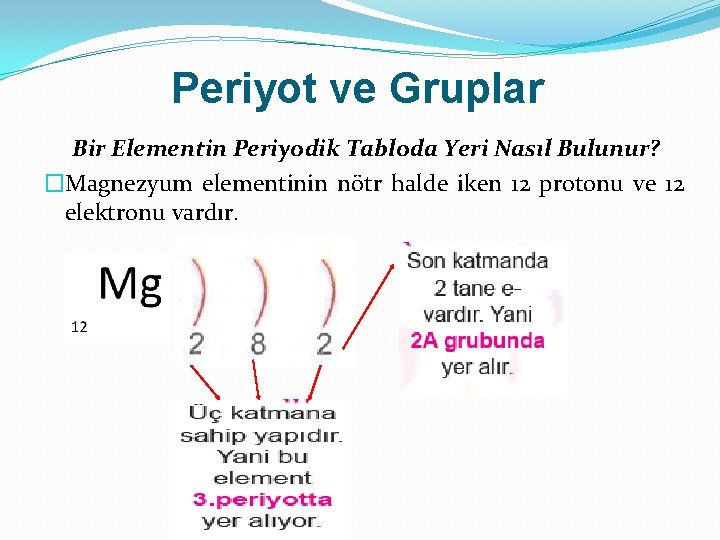
Periyot ve Gruplar Bir Elementin Periyodik Tabloda Yeri Nasıl Bulunur? �Magnezyum elementinin nötr halde iken 12 protonu ve 12 elektronu vardır.

Periyot ve Gruplar �Aynı grupta olan tüm elementlerin son katmanlarında aynı sayıda elektron bulunur. �Örnek; 1 A grubu elementleri; �Yukarıda görüldüğü gibi 1 A grubu elementlerinin son katmanlarında aynı sayıda elektron bulunur.

Periyot ve Gruplar � 2 A grubundaki tüm elementlerin son katmanlarında 2 elektron(e-) bulunur. � 3 A grubundaki tüm elementlerin son katmanlarında 3 elektron(e-) bulunur. � 4 A grubundaki tüm elementlerin son katmanlarında 4 elektron(e-) bulunur. � 5 A grubundaki tüm elementlerin son katmanlarında 5 elektron(e-) bulunur. � 6 A grubundaki tüm elementlerin son katmanlarında 6 elektron(e-) bulunur. � 7 A grubundaki tüm elementlerin son katmanlarında 7 elektron(e-) bulunur. � 8 A grubundaki tüm elementlerin son katmanlarında 8 elektron(e-) bulunur.

Periyot ve Gruplar �İSTİSNA: Helyum (He) elementi 8 A grubunda olmasına rağmen sadece 2 elektrona sahip olduğu için son katmanında 2 elektron(e-) bulunur.

Periyot ve Gruplar �Aynı periyotta olan tüm elementlerin yapısında aynı sayıda katman bulunur. �Örnek; 3. periyot elementleri; �Yukarıda görüldüğü gibi 3. periyot elementlerinin katman sayıları birbirine eşittir.

Periyot ve Gruplar � 1. periyottaki tüm elementler 1 katmana sahip � 2. periyottaki tüm elementler 2 katmana sahip � 3. periyottaki tüm elementler 3 katmana sahip � 4. periyottaki tüm elementler 4 katmana sahip � 5. periyottaki tüm elementler 5 katmana sahip � 6. periyottaki tüm elementler 6 katmana sahip � 7. periyottaki tüm elementler 7 katmana sahip

Periyot ve Gruplar �Aynı gruptaki elementlerin kimyasal özellikleri birbirine benzerdir. (aynı değil) �İSTİSNA: 1 A grubundaki Hidrojen elementi Ametal olduğu için 1 A grubundaki diğer elementlere benzemez. �Ek Bilgi: Bazı gruptaki elementlerin özel adları;
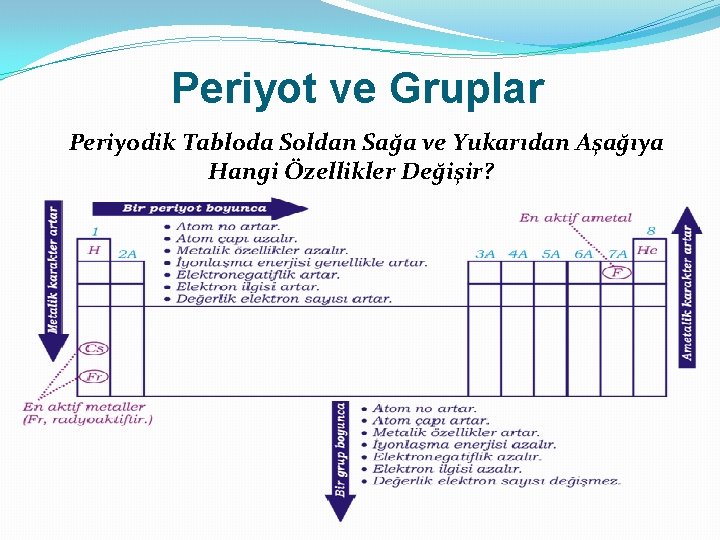
Periyot ve Gruplar Periyodik Tabloda Soldan Sağa ve Yukarıdan Aşağıya Hangi Özellikler Değişir?
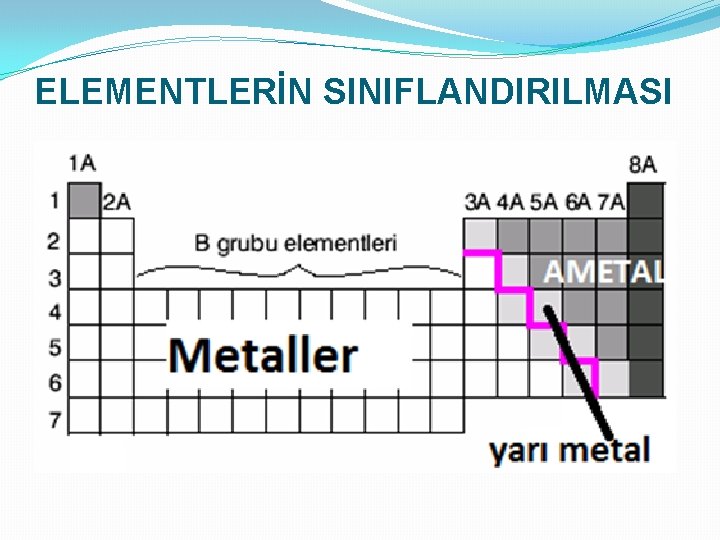
ELEMENTLERİN SINIFLANDIRILMASI

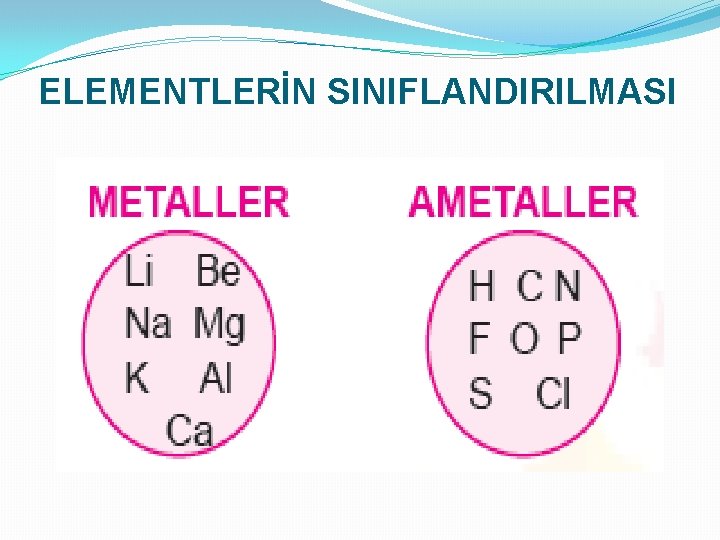
ELEMENTLERİN SINIFLANDIRILMASI �METALLER: Son katmanında 1, 2, 3 elektronu olan elementlerdir. Yani 1 A, 2 A, ve 3 A grupları. �AMETALLER: Son katmanında 5, 6, 7 elektronu olan elementlerdir. Yani 5 A, 6 A, ve 7 A grupları. �Soygazlar: Ametallerin özel bir alt grubudur. Son katmanında 8 elektronu olan elementlerdir. Yani 8 A grubu. �YARIMETALLER: Özellikleri hem metallere hem de ametallere benzerlik gösterir.

ELEMENTLERİN SINIFLANDIRILMASI İLK 20 ELEMENT İÇERİSİNDEKİ METAL, AMETAL (SOYGAZ) VE YARIMETALLER � 1 H (Hidrojen)--Ametal � 2 He (Helyum)--Soygaz � 3 Li (Lityum) )--Metal � 4 Be (Berilyum)--Metal � 5 B (Bor)— Yarımetal � 6 C (Karbon)—Ametal � 7 N (Azot) –Ametal � 8 O (Oksijen)—Ametal � 9 F (Flor) –Ametal � 10 Ne (Neon)--Soygaz � 11 Na (Sodyum)--Metal � 12 Mg (Magnezyum)--Metal � 13 Al (Alüminyum)--Metal � 14 Sİ (Silisyum) -- Yarımetal � 15 P (Fosfor) --Ametal � 16 S (Kükürt) --Ametal � 17 Cl (Klor) --Ametal � 18 Ar (Argon)--Soygaz � 19 K (Potasyum)--Metal � 20 Ca (Kalsiyum)--Metal
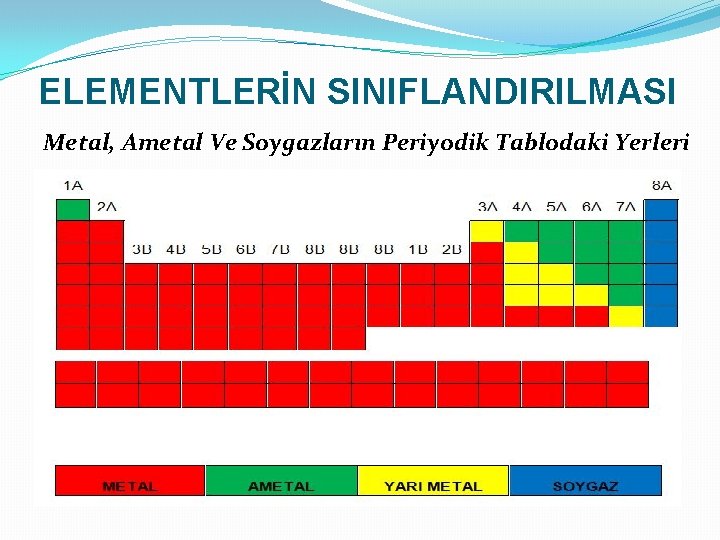
ELEMENTLERİN SINIFLANDIRILMASI Metal, Ametal Ve Soygazların Periyodik Tablodaki Yerleri

ELEMENTLERİN SINIFLANDIRILMASI METALLERİN ÖZELLİKLERİ �Periyodik tablonun sol tarafında yer alırlar ve periyodik tablonun büyük bir bölümünü oluştururlar. �Son katmanlarında 1, 2, 3 elektron bulundururlar. �Bileşik oluştururken elektron (e-) VERMEYE yatkınlardır.

ELEMENTLERİN SINIFLANDIRILMASI METALLERİN ÖZELLİKLERİ �Elektron verdikleri için (+) yüklü Ka(t) yon oluştururlar. �İşlenebilir, tel ve levha haline getirilebilirler. �Isı ve elektriği iyi iletirler. �Parlak görünürler.

ELEMENTLERİN SINIFLANDIRILMASI METALLERİN ÖZELLİKLERİ �Vurulduğunda çınlama sesi çıkarırlar. �Doğada katı halde bulunur. (Cıva hariç) �Kendi aralarında bileşik oluşturmazlar.

ELEMENTLERİN SINIFLANDIRILMASI AMETALLERİN ÖZELLİKLERİ �Periyodik tablonun sağ tarafında yer alırlar. (Hidrojen hariç. ) �Son katmanlarında 5, 6, 7 elektron bulundururular. �Elektron (e-) ALMAYA yatkınlardır. Klor

ELEMENTLERİN SINIFLANDIRILMASI AMETALLERİN ÖZELLİKLERİ �Elektron aldıkları için (-) yüklü Anyon oluştururlar. �Kırılgan oldukları için işlenemezler. �Isı ve elektriği iyi iletmezler.

ELEMENTLERİN SINIFLANDIRILMASI AMETALLERİN ÖZELLİKLERİ �Soluk (mat) renklilerdir. �Doğada katı, sıvı ve gaz halde bulunabilirler. �Kendi aralarında kovalent bağlı bileşikleri oluşturabilirler. Karbon
ELEMENTLERİN SINIFLANDIRILMASI

ELEMENTLERİN SINIFLANDIRILMASI Soygazların Özellikleri �Periyodik tablonun en sağ tarafında yer alırlar. �Son katmanlarında 8 elektron (Helyum hariç) bulundururlar. �Bileşik oluşturma eğilimleri yoktur. �Doğada gaz halde bulunurlar.

ELEMENTLERİN SINIFLANDIRILMASI

ELEMENTLERİN SINIFLANDIRILMASI YARI METALLERİN ÖZELLİKLERİ �Periyodik tabloda metaller ile ametallerin arasında bulunurlar. �Oda koşullarında katı halde bulunurlar. �Parlak veya mat olabilirler.

ELEMENTLERİN SINIFLANDIRILMASI YARI METALLERİN ÖZELLİKLERİ �Elektrik ve ısı iletkenlikleri ametallerden iyi, metallerden kötüdür. �Tel, levha ve toz hâline getirilebilirler. �Yüksek sıcaklıkta iletkenlikleri de artar.

FİZİKSEL VE KİMYASAL DEĞİŞİMLER Fiziksel Değişimler Kimyasal Değişimler �Maddenin sadece dış görünüşünde meydana gelen değişimlerdir. �Genellikle ufalanma, yırtılma, çözünme, rendelenme, kırılma, parçalanma, dövülme şeklinde gerçekleşir. �Sonucunda yeni bir madde oluşmaz. �Maddenin dış görünüşü ile birlikte iç yapısında da meydana gelen değişimlerdir. �Genellikle yanma, çürüme, kızartma, paslanma, mayalanma, ekşime, solunum, elektroliz şeklinde gerçekleşir. �Sonucunda yeni maddeler oluşur.

FİZİKSEL VE KİMYASAL DEĞİŞİMLER Fiziksel Değişim Örnekleri �Kağıdın yırtılması �Havucun rendelenmesi �Cevizin havanda dövülmesi �Camın kırılması �Odunların kırılması �Şekerin suda çözünmesi �Küp şekerin toz şeker haline getirilmesi

FİZİKSEL VE KİMYASAL DEĞİŞİMLER �NOT: Tüm hal değişim olayları, fiziksel değişimdir. �Bir madde hal değiştirirken tanecikler arası mesafe değişirken, taneciklerin yapısında herhangi bir değişiklik olmaz.

FİZİKSEL VE KİMYASAL DEĞİŞİMLER Kimyasal Değişim Örnekleri �Kağıdın yanması �Elmanın çürümesi �Demirin paslanması �Sütün ekşimesi �Sütün yoğurda dönüşmesi �Ekmeğin küflenmesi �Besinlerin sindirilmesi �Suyun elektrolizi

FİZİKSEL VE KİMYASAL DEĞİŞİMLER �NOT: Bir maddenin kimyasal değişim geçirdiğinin bazı ipuçları vardır. Bunlar; alev çıkması, renk değişimi, duman çıkışı, ışık çıkışı, gaz çıkışı, koku çıkışı vb.

FİZİKSEL VE KİMYASAL DEĞİŞİMLER Karşılaştırmalı Fiziksel ve Kimyasal Değişim Örnekleri �Mumun erimesi fiziksel bir değişim iken, mumun yanması kimyasal bir değişimdir.

FİZİKSEL VE KİMYASAL DEĞİŞİMLER Karşılaştırmalı Fiziksel ve Kimyasal Değişim Örnekleri �Suyun elektrolizi kimyasal bir değişim iken, suyun buharlaşması fiziksel bir değişimdir.

FİZİKSEL VE KİMYASAL DEĞİŞİMLER Karşılaştırmalı Fiziksel ve Kimyasal Değişim Örnekleri �Yumurtanın haşlanması kimyasal değişim iken, yumurtanın kırılması fiziksel değişimdir.

KİMYASAL TEPKİMELER �Kimyasal olaylar, kimyasal tepkimeler sayesinde gerçekleşir. �Kimyasal tepkimelerin sembol ve formüllerle ifade edilmesine ise kimyasal denklem denir. �Örneğin, bir kimyasal değişim olan kâğıdın yanması için kağıt ve havadaki oksijenin kimyasal olarak tepkimeye girmesi gerekir. �Bu kimyasal tepkimede kâğıt içindeki maddelerin ve oksijenin sembol ve formüllerle gösterilmesine ise kimyasal denklem denir.
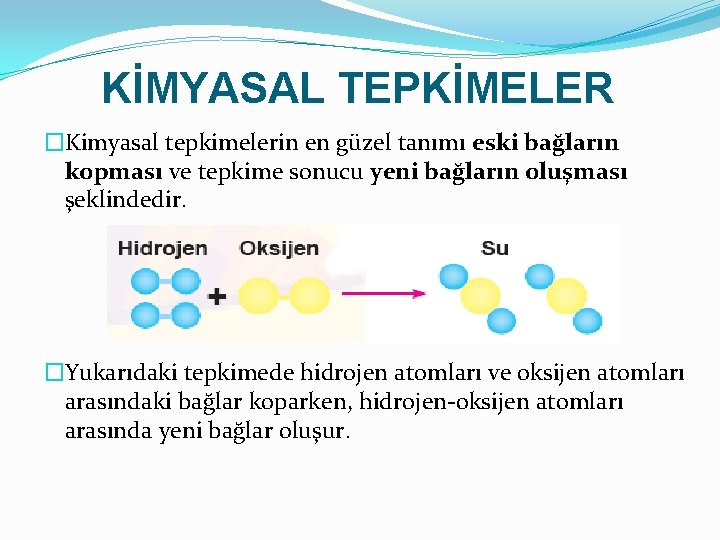
KİMYASAL TEPKİMELER �Kimyasal tepkimelerin en güzel tanımı eski bağların kopması ve tepkime sonucu yeni bağların oluşması şeklindedir. �Yukarıdaki tepkimede hidrojen atomları ve oksijen atomları arasındaki bağlar koparken, hidrojen-oksijen atomları arasında yeni bağlar oluşur.

KİMYASAL TEPKİMELER �Kimyasal tepkimede bazı maddeler tepkimeye girerek azalır, bazı maddeler ise tepkime sonunda oluşur. �Tepkimeye girerek azalan maddelere GİRENLER, tepkime sonunda oluşan maddelere ise ÜRÜNLER denir. �Bu tepkime ‘’+’’ işareti, yazılan maddelerin tepkimeye girdiğini, işareti ise tepkimenin gerçekleşme yönünü göstermektedir.
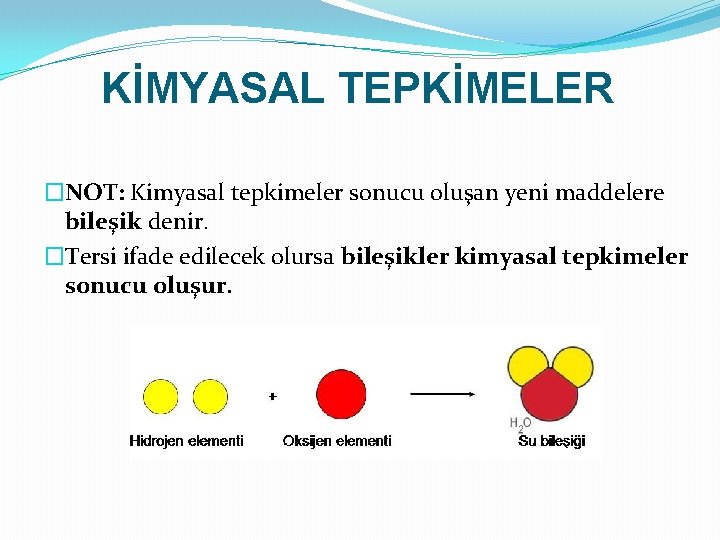
KİMYASAL TEPKİMELER �NOT: Kimyasal tepkimeler sonucu oluşan yeni maddelere bileşik denir. �Tersi ifade edilecek olursa bileşikler kimyasal tepkimeler sonucu oluşur.
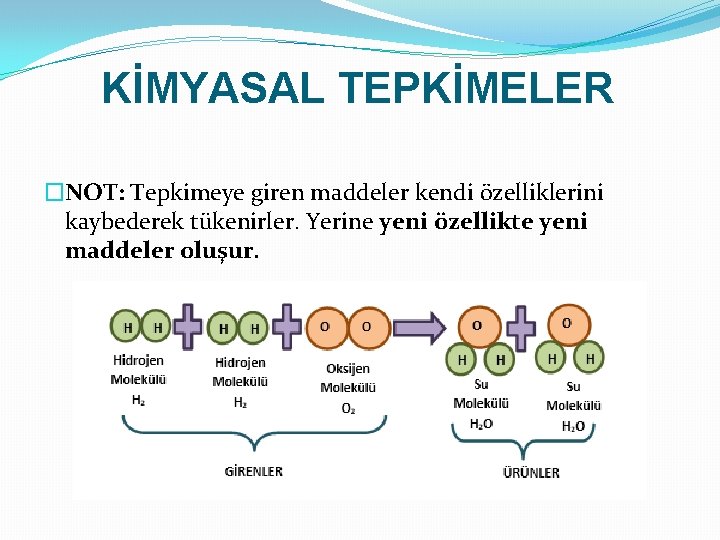
KİMYASAL TEPKİMELER �NOT: Tepkimeye giren maddeler kendi özelliklerini kaybederek tükenirler. Yerine yeni özellikte yeni maddeler oluşur.

KİMYASAL TEPKİMELER �UYARI: Kimyasal tepkimelerde bazı değerler hiçbir zaman değişmez. �Bunlar: Toplam kütle Toplam atom Sayısı Atom Türü

KİMYASAL TEPKİMELER TOPLAM KÜTLE �Bir kimyasal tepkimede giren maddelerin kütleleri toplamı, oluşan ürünlerin kütleleri toplamına eşittir. Bu kanuna ‘’Kütlenin Korunumu Kanunu’’ denir. �Örneğin; Karbon + Oksijen Karbondioksit 12 gr. 32 gr. 44 gr. �Girenlerin kütlesinin toplamı, ürünlerin kütlesine EŞİTTİR. Yani kütle korunur. (Değişmez)
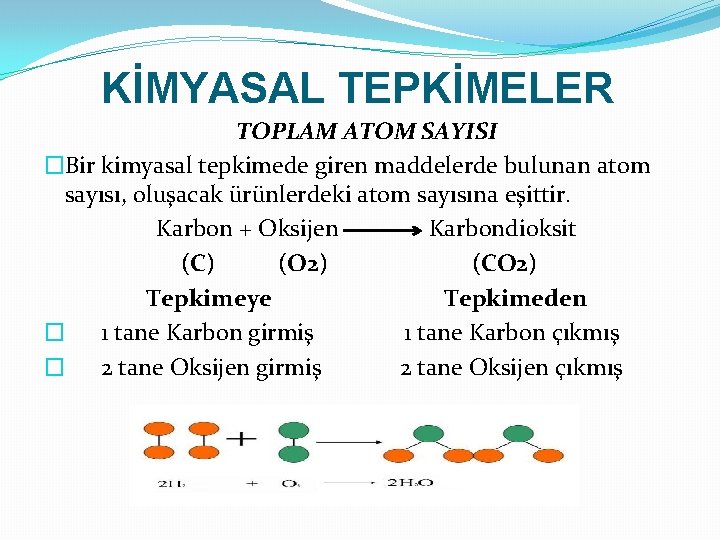
KİMYASAL TEPKİMELER TOPLAM ATOM SAYISI �Bir kimyasal tepkimede giren maddelerde bulunan atom sayısı, oluşacak ürünlerdeki atom sayısına eşittir. Karbon + Oksijen Karbondioksit (C) (O 2) (CO 2) Tepkimeye Tepkimeden � 1 tane Karbon girmiş 1 tane Karbon çıkmış � 2 tane Oksijen girmiş 2 tane Oksijen çıkmış
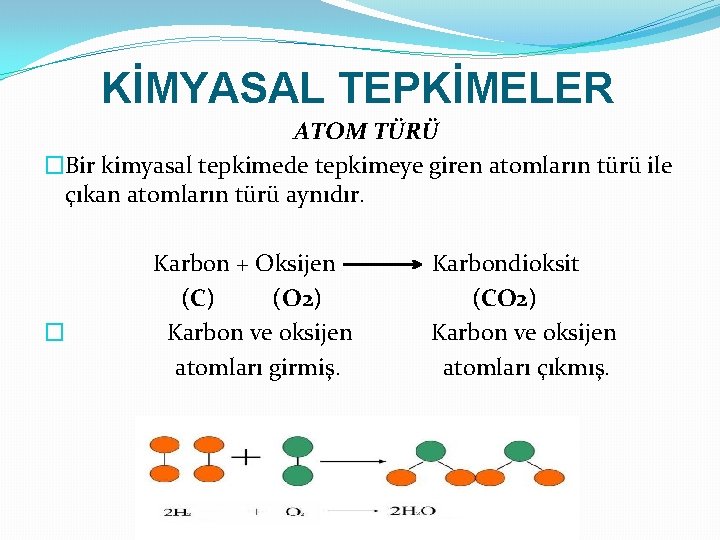
KİMYASAL TEPKİMELER ATOM TÜRÜ �Bir kimyasal tepkimede tepkimeye giren atomların türü ile çıkan atomların türü aynıdır. � Karbon + Oksijen (C) (O 2) Karbon ve oksijen atomları girmiş. Karbondioksit (CO 2) Karbon ve oksijen atomları çıkmış.
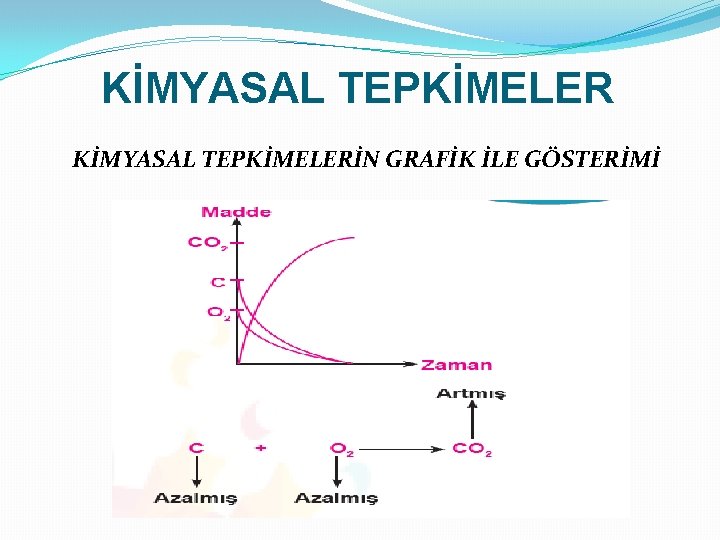
KİMYASAL TEPKİMELERİN GRAFİK İLE GÖSTERİMİ

ASİTLER VE BAZLAR ASİTLERİN GENEL ÖZELLİKLERİ �Sulu çözeltilerine H+ (Hidrojen)iyonu verirler.

ASİTLER VE BAZLAR ASİTLERİN GENEL ÖZELLİKLERİ �Tatları ekşidir. �Eli tahriş ederler. Yakıcıdırlar. �Sulu çözeltileri elektrik akımını iletir.

ASİTLER VE BAZLAR ASİTLERİN GENEL ÖZELLİKLERİ �Mavi turnusol kâğıdını kırmızıya çevirirler.
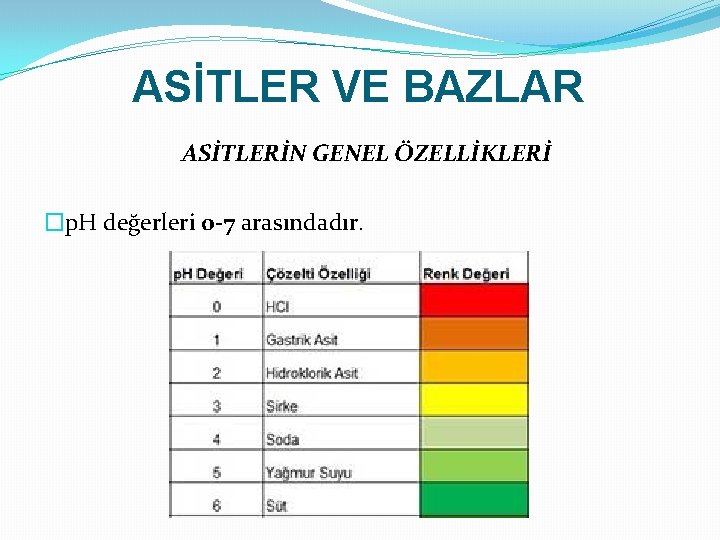
ASİTLER VE BAZLAR ASİTLERİN GENEL ÖZELLİKLERİ �p. H değerleri 0 -7 arasındadır.

ASİTLER VE BAZLAR ASİTLERİN GENEL ÖZELLİKLERİ �Metallerle tepkimeye girerek H 2 gazı çıkarırlar.

ASİTLER VE BAZLAR Günlük Hayattan Asit Örnekleri �Portakal, limon, çilek, süt, yoğurt, sirke gibi birçok yiyecek ile akü sıvısı, mide özsuyu …

ASİTLER VE BAZLARIN GENEL ÖZELLİKLERİ �Sulu çözeltilerine OH- (Hidroksit) iyonu verirler.

ASİTLER VE BAZLARIN GENEL ÖZELLİKLERİ �Tatları acıdır. �Ele kayganlık hissi verirler. Genellikle temizlik malzemelerinde bulunurlar. �Sulu çözeltileri elektrik akımını iletir.

ASİTLER VE BAZLARIN GENEL ÖZELLİKLERİ �Kırmızı turnusol kâğıdını maviye çevirirler.
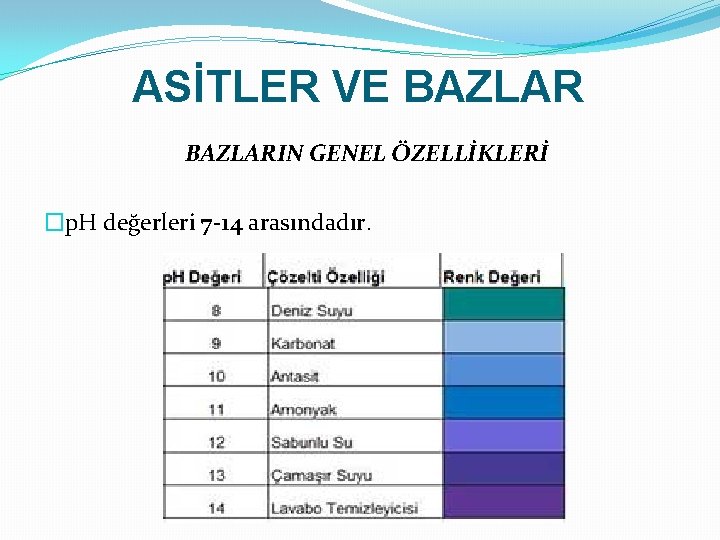
ASİTLER VE BAZLARIN GENEL ÖZELLİKLERİ �p. H değerleri 7 -14 arasındadır.

ASİTLER VE BAZLAR Günlük Hayattan Baz Örnekleri �Sabun, şampuan, çamaşır suyu, amonyak (NH 3), diş macunu, kabartma tozu, mide ilacı …

BELİRTEÇ (AYIRAÇ) �Bir maddenin asit mi yoksa baz mı olduğunu gösteren maddelere belirteç denir.

BELİRTEÇ (AYIRAÇ) �Günlük hayatta yiyeceklerde bulabileceğimiz bazı belirteçler; nar suyu, lahana suyu, kuşburnu, kırmızı turp suyu, kırmızı havuç suyu. . .
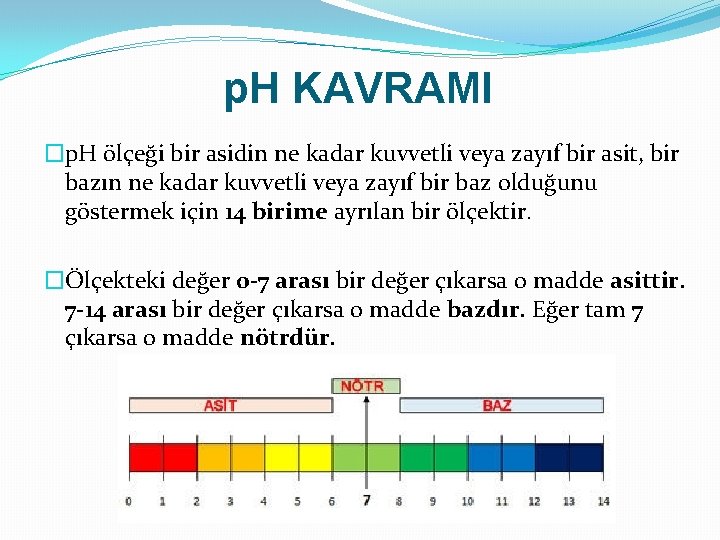
p. H KAVRAMI �p. H ölçeği bir asidin ne kadar kuvvetli veya zayıf bir asit, bir bazın ne kadar kuvvetli veya zayıf bir baz olduğunu göstermek için 14 birime ayrılan bir ölçektir. �Ölçekteki değer 0 -7 arası bir değer çıkarsa o madde asittir. 7 -14 arası bir değer çıkarsa o madde bazdır. Eğer tam 7 çıkarsa o madde nötrdür.

p. H KAVRAMI �Bir maddenin p. H değeri 7’den 0’a doğru yaklaştıkça o maddenin asitlik gücü artar. Yani daha kuvvetli bir asit olur. �Bir maddenin p. H değeri 7’den 14’e doğru yaklaştıkça o maddenin bazlık gücü artar. Yani daha kuvvetli bir baz olur.

ASİT VE BAZLARIN ETKİLERİ �Asitler, metal ve mermerin düşmanıdır.

ASİT VE BAZLARIN ETKİLERİ �Bazlar, cam, porselen ve kristal eşyaların düşmanıdır.
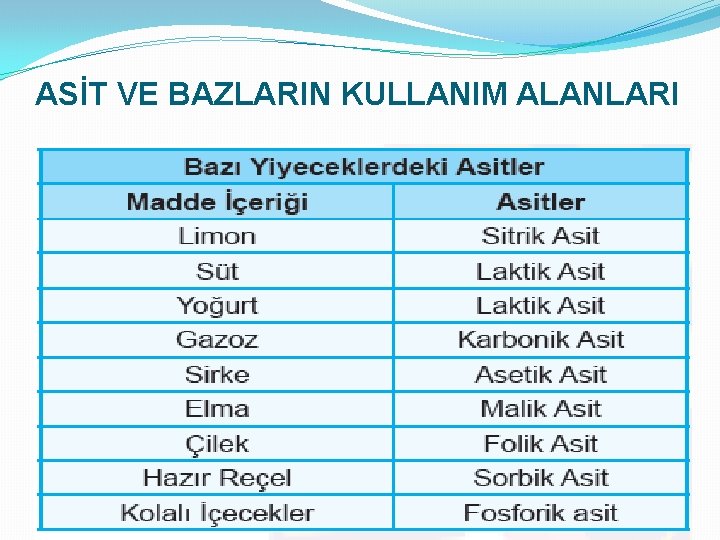
ASİT VE BAZLARIN KULLANIM ALANLARI
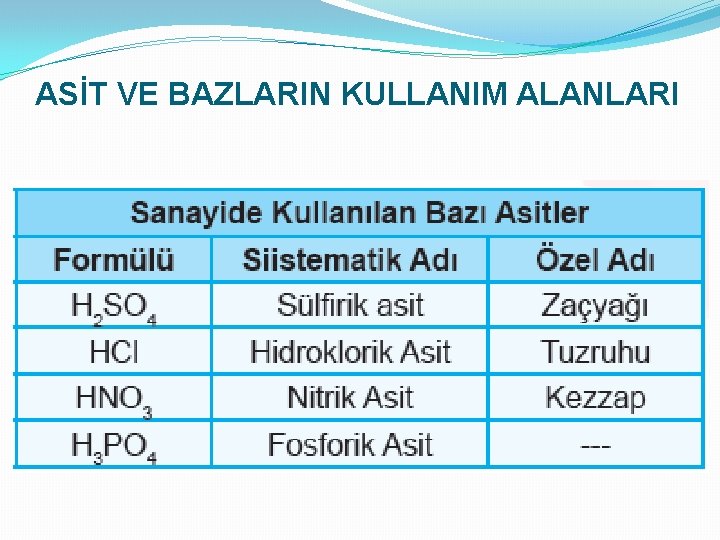
ASİT VE BAZLARIN KULLANIM ALANLARI
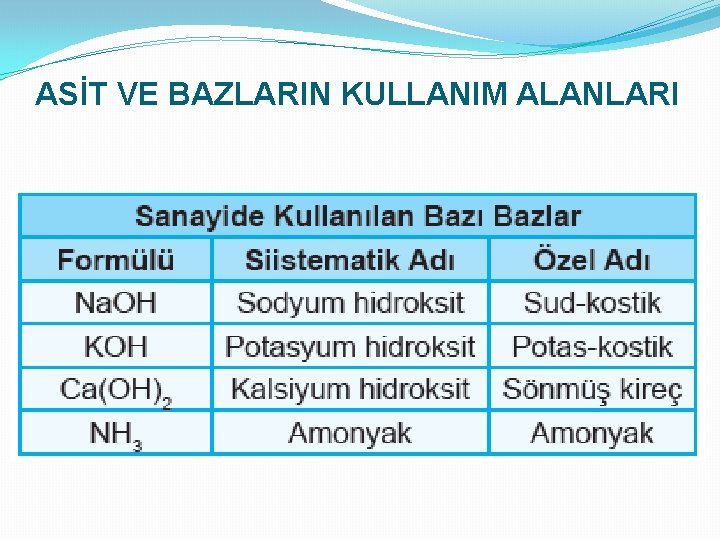
ASİT VE BAZLARIN KULLANIM ALANLARI

ASİT YAĞMURLARI �Petrol, kömür gibi fosil yakıtların yakılması sonucu açığa çıkan CO 2, NO 2 ve SO 2 gazları havada su buharı ile birleşerek asit yağmurlarına dönüşürler. �Yağan asit yağmuru toprağa, denizdeki balıklara, ormanlık alanlara, arabalara, tarihi eserlere ve binalara zarar verir.

ASİT YAĞMURLARI CO 2 + H 2 O(su buharı) Karbonik Asit SO 2+ H 2 O (su buharı) Sülfirik Asit NO 2 + H 2 O (su buharı) Nitrik Asit

ASİT YAĞMURLARI Asit yağmurlarının bu zararlarından korunmak için; �Fosil yakıtlar yerine yenilenebilir(rüzgar, güneş, hidroelektrik vs) enerji kaynaklarını kullanabiliriz. �Bacalara filtre takarak zararlı gazların havaya karışmasını önleyebiliriz. �Araba egzozlarına filtre takabiliriz.

ASİT YAĞMURLARI Asit yağmurlarının bu zararlarından korunmak için; �Orman yangınları için önlemler alabiliriz. �Yeşillik alanlarımızı artırabiliriz. �Sonuç olarak havayı kirleten birçok zararlı gaza karşı alacağımız önlem bizi asit yağmurlarının zararlı etkilerinden korumuş olacaktır.

MADDENİN ISI İLE ETKİLEŞİMİ �Bir maddenin taneciklerinin sahip olduğu toplam kinetik (hareket) enerjisine ısı denir. �Isının birimi joule ya da kaloridir. �Maddelerin ısıları doğrudan ölçülemez. Isı aktarılabilen bir enerjidir. �Maddeler ısı alışverişini gerçekleştirirken maddenin artan ya da azalan değeri sıcaklığıdır.

MADDENİN ISI İLE ETKİLEŞİMİ Isı Alışverişi �Sıcaklıkları farklı iki madde arasında alınıp verilen enerjiye ısı denir. �İki maddeden birinin sıcaklığının diğerinden farklı olması halinde, sıcaklığı yüksek olan maddeden sıcaklığı düşük olan maddeye enerji aktarılır.

MADDENİN ISI İLE ETKİLEŞİMİ Isı Alışverişi �Bir maddenin ısı alışverişi esnasında sıcaklık değeri değişir. �Isı alan bir maddenin sıcaklığı artarken, ısı veren bir maddenin sıcaklığı azalır. �Isı akışı sıcaklığı yüksek olan maddeden sıcaklığı düşük olan maddeye doğrudur.

MADDENİN ISI İLE ETKİLEŞİMİ �Bir maddenin sahip olduğu enerji o maddenin; � kütlesine �cinsine �sıcaklığında meydana gelen değişime bağlıdır.

MADDENİN ISI İLE ETKİLEŞİMİ �Yandaki şekilde içerisinde sıcaklıkları eşit 100 m. L ve 200 m. L su olan kaplar bulunmaktadır. �Bu kaplar 5 dakika boyunca ısıtılıyor. 5 dakikanın sonuna 200 ml’lik suyun ısısı 100 ml’lik suyun ısısından daha fazla olur.

MADDENİN ISI İLE ETKİLEŞİMİ �Isı madde taneciklerinin toplam kinetik enerjisi olduğu için madde ne kadar fazla olursa taneciklerin enerjisi o kadar çok olur. Yani ısısı yüksek olur. �Dolayısıyla maddenin kütlesi arttıkça sahip olduğu ısı enerjisi artar. 30 °C 50 ml. Su Daha az ısı 30 °C 100 ml. Su Daha fazla ısı

MADDENİN ISI İLE ETKİLEŞİMİ �Yandaki şekilde verilen kaplarda miktarları ve ilk sıcaklıkları eşit su ve zeytinyağı bulunmaktadır. �Bu kaplar 10 dakika boyunca ısıtılırsa ısıtılma sonucunda suyun ısısı zeytinyağın ısısından daha büyüktür.

MADDENİN ISI İLE ETKİLEŞİMİ �Maddelerin sıcaklığını artırmak için gerekli olan ısı miktarı maddenin cinsine göre değişir. � 1 gram maddenin sıcaklığını 1°C artırmak için gerekli olan ısı miktarına öz ısı denir. �Birimi joule/g. °C ya da cal/g. °C’tur. �Öz ısı ‘c’ harfi ile sembolize edilir. �Bir maddenin öz ısısı ne kadar büyükse sahip olduğu ısı da o kadar artar.
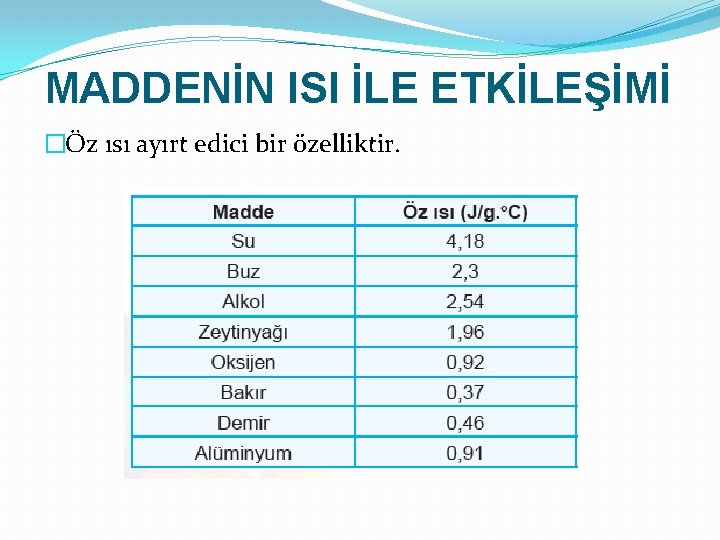
MADDENİN ISI İLE ETKİLEŞİMİ �Öz ısı ayırt edici bir özelliktir.
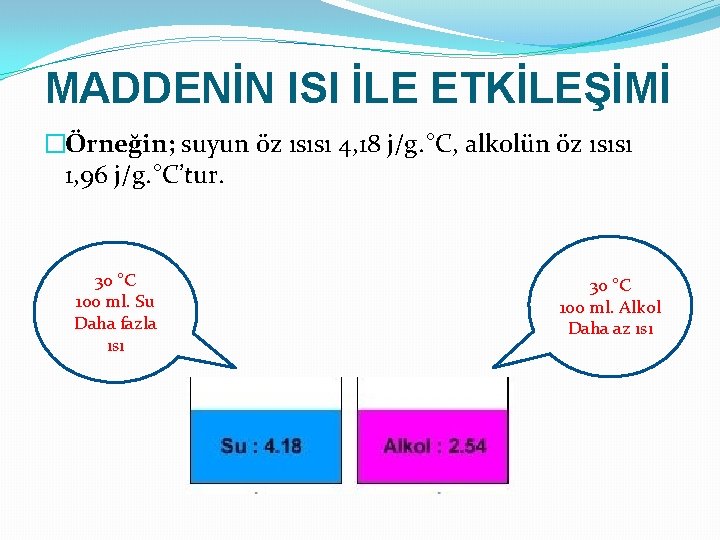
MADDENİN ISI İLE ETKİLEŞİMİ �Örneğin; suyun öz ısısı 4, 18 j/g. °C, alkolün öz ısısı 1, 96 j/g. °C’tur. 30 °C 100 ml. Su Daha fazla ısı 30 °C 100 ml. Alkol Daha az ısı

MADDENİN ISI İLE ETKİLEŞİMİ �Yandaki şekilde verilen kaplarda eşit miktarda ve eşit sıcaklıkta olan sular bulunmaktadır. �Bu kaplardan 1. 5 dakika 2. 20 dakika ısıtılırsa 2. Kabın ısısı daha yüksek olur.

MADDENİN ISI İLE ETKİLEŞİMİ �Aynı kütleye sahip aynı cins maddelerden sıcaklık değişimi büyük olanın ısısı da büyüktür. �Sıcaklık değişimi arttığında maddenin ısısı da artar. 30 °C 100 ml. Su 5 dk ısıtılıyor Daha az ısı 30 °C 100 ml. Su 10 dk ısıtılıyor Daha fazla ısı

MADDENİN ISI İLE ETKİLEŞİMİ �NOT: bu tür deneylere kontrollü deneyler denir. �Bir deneyde kendi elimizle değiştirilen değişkenlere bağımsız değişken denir. �Bağımsız değişkenden etkilenen ve ona bağlı olarak artan ya da azalan değişkene bağımlı değişken denir. �Deneyde değiştirilmeyen değişkenlere ise kontrol edilen değişken denir.

MADDENİN ISI İLE ETKİLEŞİMİ 30 °C 100 ml. Su Daha fazla ısı 30 °C 50 ml. Su Daha az ısı Yukarıdaki deneye göre: �Bağımsız değişken: �Bağımlı değişken: �Kontrol edilen değişken: Su miktarı Isı miktarı Maddenin cinsi ve sıcaklığı
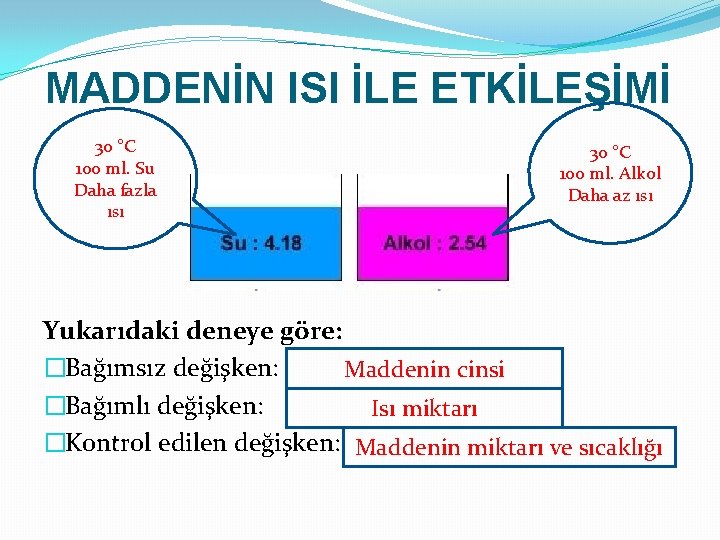
MADDENİN ISI İLE ETKİLEŞİMİ 30 °C 100 ml. Su Daha fazla ısı 30 °C 100 ml. Alkol Daha az ısı Yukarıdaki deneye göre: �Bağımsız değişken: Maddenin cinsi �Bağımlı değişken: Isı miktarı �Kontrol edilen değişken: Maddenin miktarı ve sıcaklığı
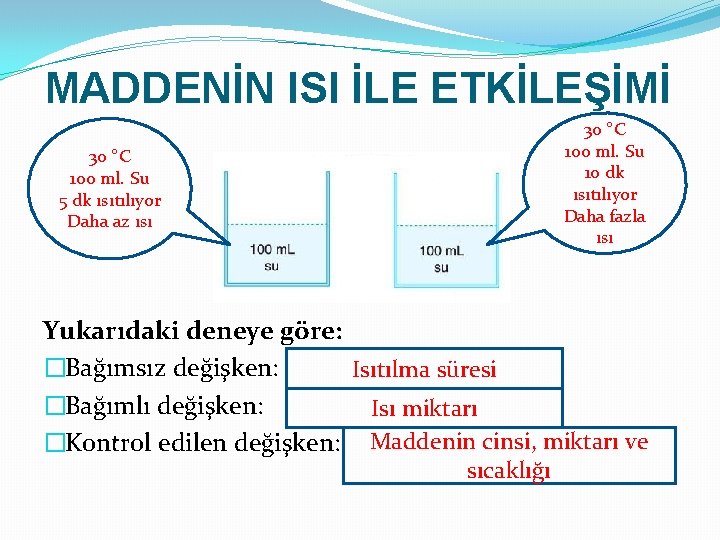
MADDENİN ISI İLE ETKİLEŞİMİ 30 °C 100 ml. Su 10 dk ısıtılıyor Daha fazla ısı 30 °C 100 ml. Su 5 dk ısıtılıyor Daha az ısı Yukarıdaki deneye göre: �Bağımsız değişken: Isıtılma süresi �Bağımlı değişken: Isı miktarı �Kontrol edilen değişken: Maddenin cinsi, miktarı ve sıcaklığı

HAL DEĞİŞİMLERİ �Maddeler ısının etkisiyle hal değiştirebilir. �Maddeler hal değiştirirken belirli miktarda ısıya ihtiyaç duyarlar. �Maddelerin ihtiyaç duydukları ısı maddenin kütlesine ve maddenin cinsine bağlıdır.

HAL DEĞİŞİMLERİ � 1 gram katı maddenin TAMAMEN sıvı hale geçmesi için gerekli olan ısı miktarına erime ısısı denir. �Erime ısısının birimi j/g’dır. �“Le” ile sembolize edilir. �Saf bir maddenin erime ısısı donma ısısına eşittir.
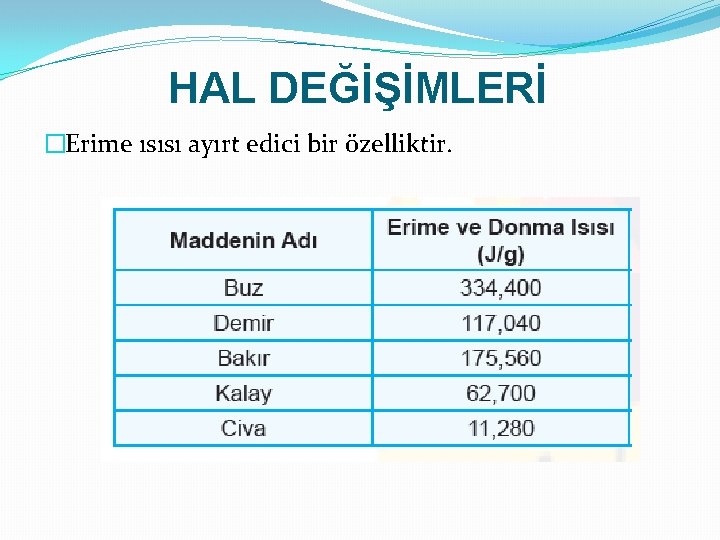
HAL DEĞİŞİMLERİ �Erime ısısı ayırt edici bir özelliktir.
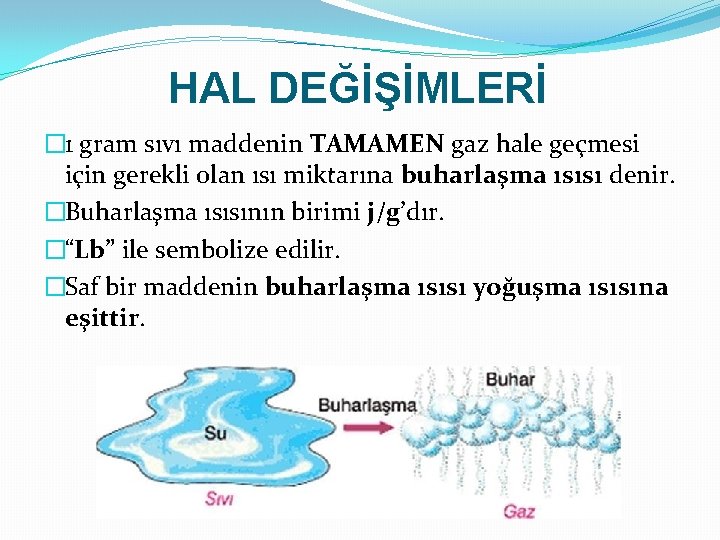
HAL DEĞİŞİMLERİ � 1 gram sıvı maddenin TAMAMEN gaz hale geçmesi için gerekli olan ısı miktarına buharlaşma ısısı denir. �Buharlaşma ısısının birimi j/g’dır. �“Lb” ile sembolize edilir. �Saf bir maddenin buharlaşma ısısı yoğuşma ısısına eşittir.

HAL DEĞİŞİMLERİ �Buharlaşma ısısı ayırt edici bir özelliktir.

HAL DEĞİŞİMLERİ �Saf maddeler hal değiştirirken sıcaklıkları sabit kalır. Maddenin tamamı hal değiştirene kadar sıcaklıkları değişmez.
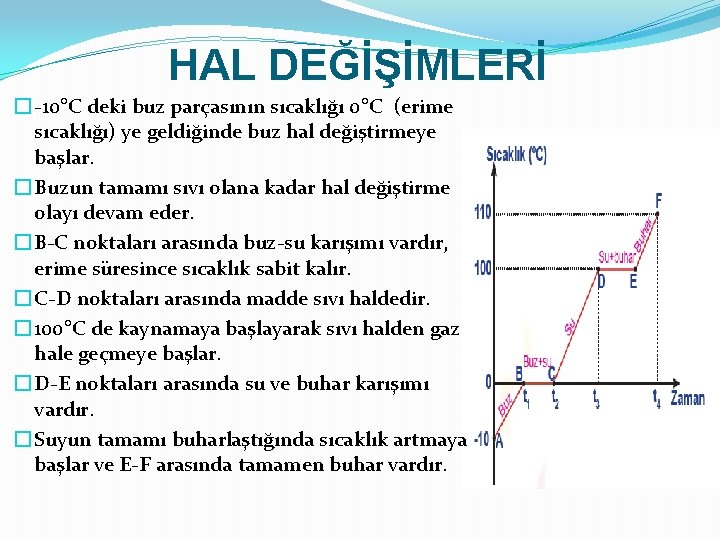
HAL DEĞİŞİMLERİ � -10°C deki buz parçasının sıcaklığı 0°C (erime sıcaklığı) ye geldiğinde buz hal değiştirmeye başlar. � Buzun tamamı sıvı olana kadar hal değiştirme olayı devam eder. � B-C noktaları arasında buz-su karışımı vardır, erime süresince sıcaklık sabit kalır. � C-D noktaları arasında madde sıvı haldedir. � 100°C de kaynamaya başlayarak sıvı halden gaz hale geçmeye başlar. � D-E noktaları arasında su ve buhar karışımı vardır. � Suyun tamamı buharlaştığında sıcaklık artmaya başlar ve E-F arasında tamamen buhar vardır.

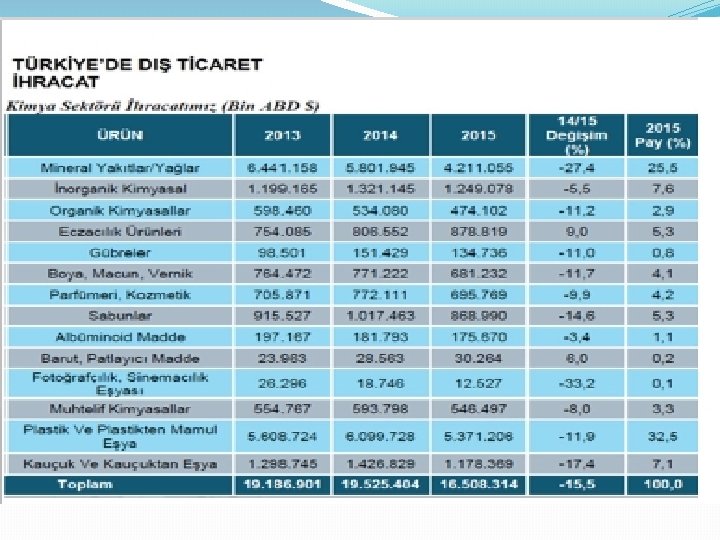
TÜRKİYE’DE KİMYA ENDÜSTRİSİ �Kimya sektörü; mineral yakıtlar/yağlar, inorganik kimyasallar, eczacılık, gübre, boya, macun, vernik, parfümeri ve kozmetik, sabun, barut, patlayıcı madde, plastik ve plastikten mamul eşya ve kauçuktan eşya ürünlerini kapsamaktadır.

TÜRKİYE’DE KİMYA ENDÜSTRİSİ �Kimya sanayi, pek çok sektöre ara mal ve hammadde temin eden bir sanayi dalı olarak gerek üretim gerekse de dış ticarette önemli bir role sahiptir.

TÜRKİYE’DE KİMYA ENDÜSTRİSİ �Kimya sektörü tarım ilaçları, sentetik gübreler, veteriner ilaçları, sentetik elyaflar, sabun, deterjan, temizleyiciler, plastik ham maddeleri, beşerî ilaç sanayi, kozmetik sanayi, boya, yardımcı maddeler, deri, tekstil, inşaat, yapıştırıcı, izolasyon malzemeleri, fotoğraf malzemeleri, barut ve patlayıcılar gibi birçok sanayi alanına nihai ve ara ürün sağlamaktadır.

TÜRKİYE’DE KİMYA ENDÜSTRİSİ �Türk kimya endüstrisi, ağırlıklı olarak petrokimya, sabun, deterjan, gübre, ilaç, boya-vernik, sentetik elyaf, soda gibi çeşitli kimyasal hammadde ve tüketim ürünlerinin üretiminin gerçekleştirildiği tesislerden oluşur. �Sektörde faaliyet gösteren firmaların önemli bir kısmı küçük ve orta ölçekli işletmelerdir ve aynı zamanda büyük ölçekli firmalar ile çok uluslu şirketler de faaliyet göstermektedir.

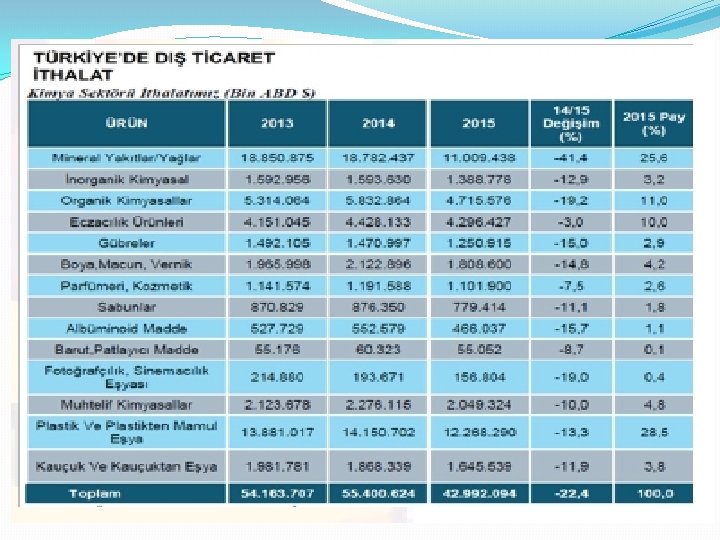
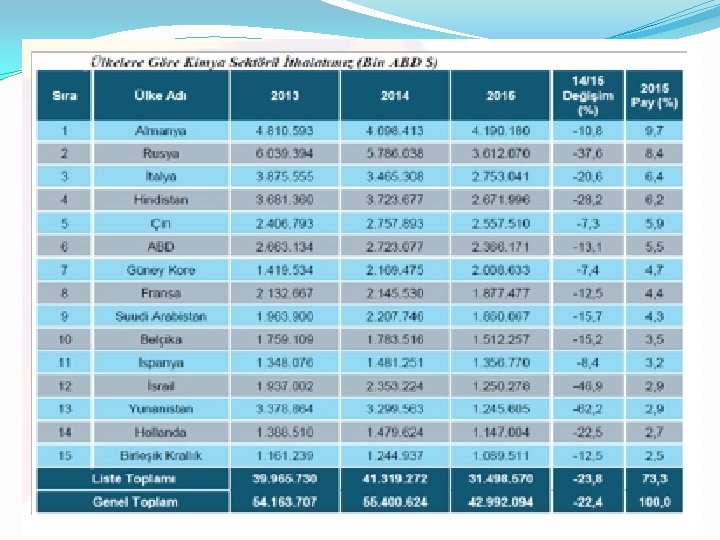
TÜRKİYE’DE KİMYA ENDÜSTRİSİ �Türkiye’de kimya sektörü ithalata bağımlıdır. �Kullanılan hammaddenin yüzde 70`i ithal edilmekte, %30`u ise yerli üretimle karşılanmaktadır. �Plastik üretiminin %90’ı petrokimya sektöründen sağlanmaktadır. �Plastik ve kauçuk sektörü %90`ın üzerinde ithalata bağımlı bir sektördür.

TÜRKİYE’DE KİMYA ENDÜSTRİSİ �Petrol ve petrol ürünleri, deterjan, sabun, ilaç kimyasalları, boya gibi ürünleri üreten kimya firmalarının çoğu Marmara Bölgesinin üç büyük sanayi ili olan İstanbul, Kocaeli ve Sakarya`da, �Ege Bölgesinde İzmir`de yerleşim gösterirken, �Gübre ve petrol ürünleri firmalarının çoğu Akdeniz Bölgesinde toplanmıştır. �Ayrıca Akdeniz bölgesinde ana ham maddelerden olan soda üretim merkezleri de bulunmaktadır. �Karadeniz Bölgesi`nde ise gübre fabrikaları çoğunluktadır.

TÜRKİYE’DE KİMYA ENDÜSTRİSİ �Türkiye`deki en büyük petrokimya şirketi eskiden bir kamu kuruluşu olan ve 2007 yılında özelleştirilen PETKİM’ dir. �PETKİM’in ürettiği ürünler içinde LDPE, HDPE, PVC ve PP ürünleri, elyaf ve aromatikler yer almaktadır. �Bu ürünler inşaat, elektrik, elektronik, ambalaj, tekstil ve ayrıca tıp, boya, deterjan ve kozmetik sektörleri için önemli ham maddeleri sağlamaktadır.

TÜRKİYE’DE KİMYA ENDÜSTRİSİ Türkiye’de Kimya Sektörüne Katkı Sağlayan Kuruluşlar Makine Ve Kimya Endüstrisi Kurumu �Her çeşit silah, mühimmat, patlayıcı madde, makine, teçhizat ve malzeme imalat kapasitelerini karlılık ve verimlilik esasları göz önüne alarak, savunma ve sivil savunma ihtiyaçlarına göre planlama ve ekonomik bir şekilde üretmek ve pazarlamak amacıyla kurulmuştur.

TÜRKİYE’DE KİMYA ENDÜSTRİSİ Türkiye’de Kimya Sektörüne Katkı Sağlayan Kuruluşlar ADCO Petrol Katkıları San ve Tic. A. Ş. �Ürettiği ürünler: Sanayi Yağı Katkıları, Otomotiv Yağı Katkıları, Rafineri Kimyasalları, Sondaj Kimyasalları, Antifriz Paket Katkıları, Sentetik Baz Yağlar, Yakıt ve Biyodizel Katkıları, Yakıt ve Madeni Yağ Boyası, Hidrolik Fren Sıvıları (DOT 3 -DOT 4), Isı Transfer Sıvıları, Savunma Sanayi Yağları gibi ürünlerdir.

TÜRKİYE’DE KİMYA ENDÜSTRİSİ Kimya Endüstrisi Meslek Dalları �Petrokimya ve diğer rezervlerin keşfedilip çıkarılması ve işlenmesi sürecinde maden mühendisliği, petrol mühendisliği, kimya mühendisliği gibi yüksek öğrenim gerektiren mesleklerin yanında bu alanda birçok teknik eleman da görev yapmaktadır.

TÜRKİYE’DE KİMYA ENDÜSTRİSİ Kimya Endüstrisi Meslek Dalları �Hazır gıdalarda kullanılan kimyasal maddeler için gıda mühendisliği, tıbbi ilaç ve kozmetik ürünlerin üretiminde biyo-kimya alanında uzman tıp doktorluğu, zirai ilaç ve gübre üretiminde görev alan ziraat mühendisliği gibi daha birçok meslek dalını, kimya endüstrisinde görev alan meslek dalları arasında yer alır.

Ünite Bitti
- Slides: 116