m K DASAR REKAYASA BIOPROSES TIN 221 22

m. K DASAR REKAYASA BIOPROSES (TIN 221 /2(2 -0) IMOBILISASI ENZIM Departemen Teknologi Industri Pertanian FATETA - IPB 2012

ENZIM 1. Larut dan tidak stabil Hanya dapat digunakan satu kali dalam larutan bebas 2. Enzim sangat mahal dan merupakan bahan yang sulit diperoleh dalam jumlah memadai (isolasi & purifikasi) Harus digunakan cara yang ekonomis dan dapat memperpanjang aktivitas biologisnya Imobilisasi (membuat konformasi aktif enzim tahan terhadap lingkungan) Terbentuk struktur granula enzim padat yang stabil dan tidak larut air.

TEKNIK IMOBILISASI ENZIM DEFINISI (Chibata, 1978) Enzim yang secara fisik ditempatkan di dalam suatu daerah/ruang tertentu, sehingga kestabilannya meningkat dan dapat mempertahankan aktivitas katalitiknya serta dapat digunakan secara berulang-ulang dan kontinyu. “Imobilisasi = biokatalis terbatas pergerakannya diakibatkan oleh perlakuan fisik atau kimia, sehingga konformasi enzim tahan thd lingkungan Enzim menjadi bersifat tak larut (Insoluble enzyme) – mempunyai keuntungan seperti katalis heterogen klasik (yang biasa digunakan)

Keuntungan Imobilisasi : 1. Dapat digunakan berulang biaya << 2. Pemisahan produk lebih mudah 3. Penghentian proses cepat (diambil dengan filtrasi; laju alir <<) 4. Kestabilan lebih baik dengan adanya proses imobilisasi. 5. Produkl tidak terkontaminasi enzim cocok untuk pangan dan farmasi 6. Dapat digunakan untuk proses sinambung ”low residence time” (high volumetric activity) & Pengontrolan lebih baik Kelemahan Imobilisasi : 1. Biaya carrier/penyangga dan proses imobilisasi cukup besar 2. Terjadi perubahan karakteristik enzim 3. Pembatasan transfer massa - problem dengan kofaktor & regenerasi - problem dengan sistem multienzim 4. Aktivitas enzim hilang selama imobilisasi
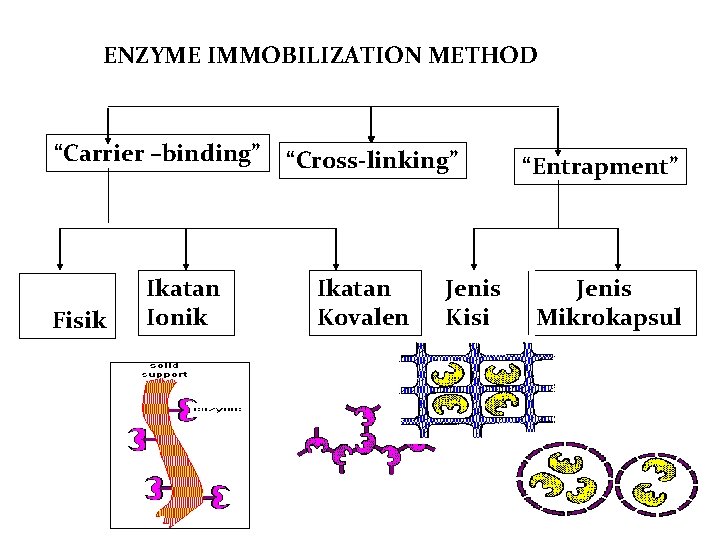
ENZYME IMMOBILIZATION METHOD “Carrier –binding” Adsorp si Fisik Ikatan Ionik “Cross-linking” Ikatan Kovalen Jenis Kisi “Entrapment” Jenis Mikrokapsul

Metode Imobilisasi : 1. “Carrier Binding” (Pengikatan/Pelekatan pada Carrier) • Enzim diikat pada “carrier” (matriks) yang tidak larut air luas permukaan & diameter pori→ muatan enzim E Jenis : a. Adsorbsi fisik - Mudah dilakukan dan ekonomis - Enzim diadsorbsi pada permukaan “carrier” Kelebihan : - Kondisi lunak → aktivitas enzim tetap tinggi - Dapat diregenerasi Kelemahan : - Kekuatan ikatan lemah p. H atau kekuatan ion berubah → bocor! - Enzim dirusak oleh mikroba/enzim proteolitik
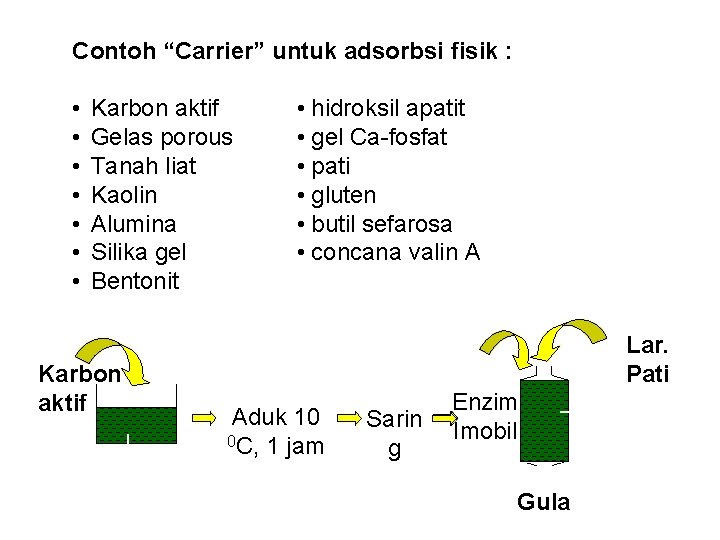
Contoh “Carrier” untuk adsorbsi fisik : • • Karbon aktif Gelas porous Tanah liat Kaolin Alumina Silika gel Bentonit Karbon aktif -amilase • hidroksil apatit • gel Ca-fosfat • pati • gluten • butil sefarosa • concana valin A Lar. Pati Aduk 10 0 C, 1 jam Sarin g Enzim Imobil Gula Amilas e imobil
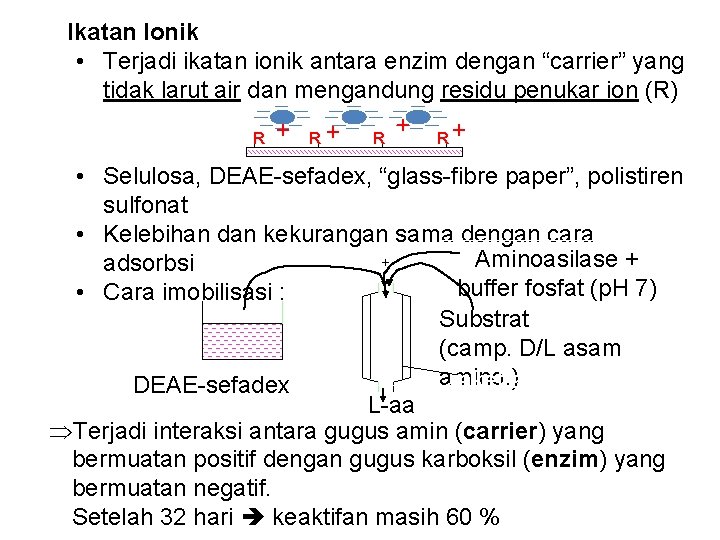
Ikatan Ionik • Terjadi ikatan ionik antara enzim dengan “carrier” yang tidak larut air dan mengandung residu penukar ion (R) E + R+ R • Selulosa, DEAE-sefadex, “glass-fibre paper”, polistiren sulfonat • Kelebihan dan kekurangan sama dengan cara Aminoasilase + + adsorbsi buffer fosfat (p. H 7) • Cara imobilisasi : Substrat (camp. D/L asam amino. ) Jaket air DEAE-sefadex + L-aa air Terjadi interaksi antara gugus amin (carrier) yang bermuatan positif dengan gugus karboksil (enzim) yang bermuatan negatif. Setelah 32 hari keaktifan masih 60 %
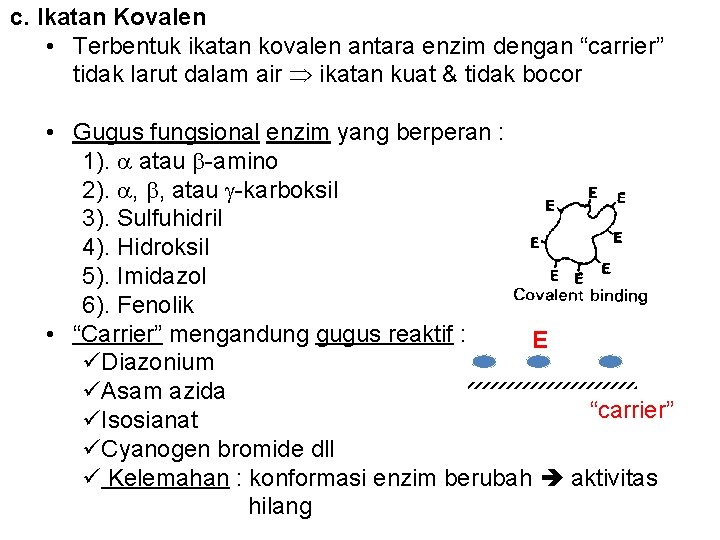
c. Ikatan Kovalen • Terbentuk ikatan kovalen antara enzim dengan “carrier” tidak larut dalam air ikatan kuat & tidak bocor • Gugus fungsional enzim yang berperan : 1). atau -amino 2). , , atau -karboksil 3). Sulfuhidril 4). Hidroksil 5). Imidazol 6). Fenolik • “Carrier” mengandung gugus reaktif : E üDiazonium üAsam azida “carrier” üIsosianat üCyanogen bromide dll ü Kelemahan : konformasi enzim berubah aktivitas hilang
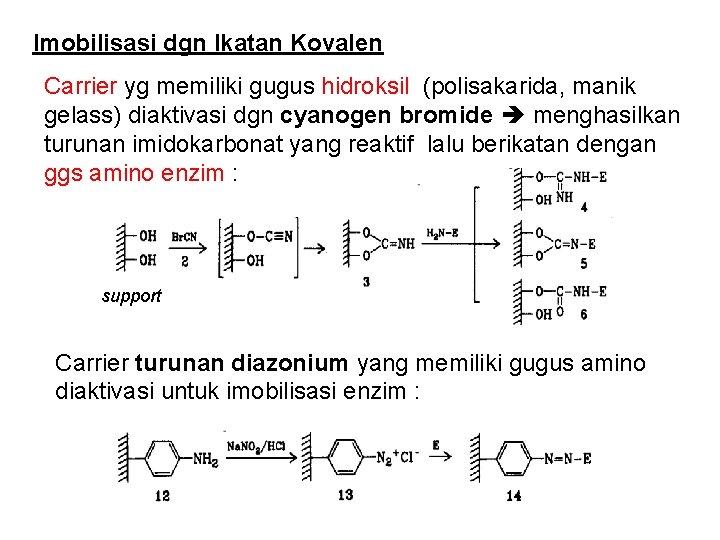
Imobilisasi dgn Ikatan Kovalen Carrier yg memiliki gugus hidroksil (polisakarida, manik gelass) diaktivasi dgn cyanogen bromide menghasilkan turunan imidokarbonat yang reaktif lalu berikatan dengan ggs amino enzim : support Carrier turunan diazonium yang memiliki gugus amino diaktivasi untuk imobilisasi enzim :
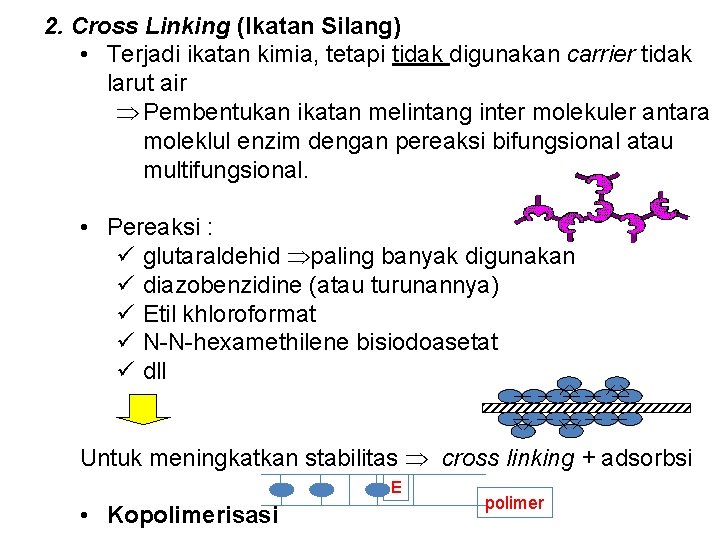
2. Cross Linking (Ikatan Silang) • Terjadi ikatan kimia, tetapi tidak digunakan carrier tidak larut air Pembentukan ikatan melintang inter molekuler antara moleklul enzim dengan pereaksi bifungsional atau multifungsional. • Pereaksi : ü glutaraldehid paling banyak digunakan ü diazobenzidine (atau turunannya) ü Etil khloroformat ü N-N-hexamethilene bisiodoasetat ü dll Untuk meningkatkan stabilitas cross linking + adsorbsi E • Kopolimerisasi polimer
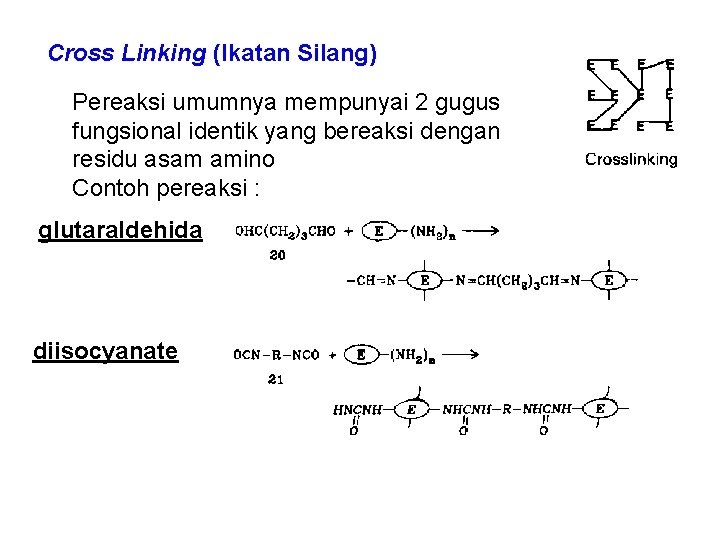
Imobilisasi dg Ikatan (Crosslinking) Cross Linking (Ikatan. Silang) Pereaksi umumnya mempunyai 2 gugus fungsional identik yang bereaksi dengan residu asam amino Contoh pereaksi : glutaraldehida diisocyanate
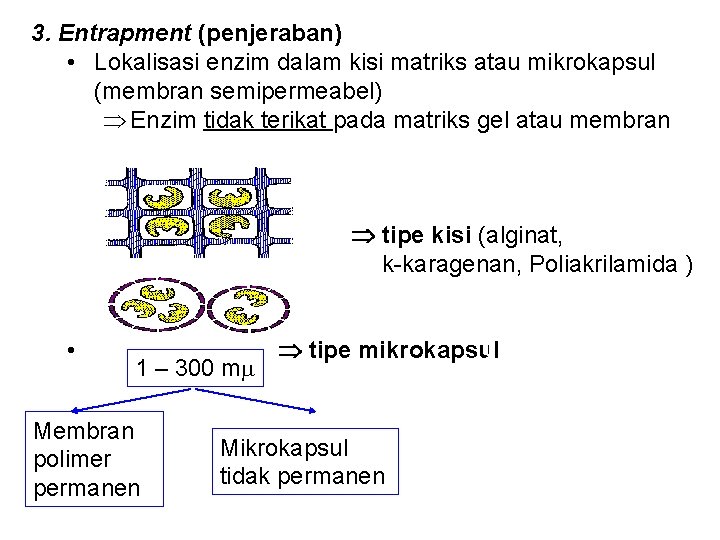
3. Entrapment (penjeraban) • Lokalisasi enzim dalam kisi matriks atau mikrokapsul (membran semipermeabel) Enzim tidak terikat pada matriks gel atau membran tipe kisi (alginat, k-karagenan, Poliakrilamida ) tipe mikrokapsul 1 – 300 m Bahan : Nilon, poliurea, etil selulosa, polistiren, Membran Kolodion, nitroselulosa, Mikrokapsul polimer butil asetat selulosa dll tidak permanen •

Immobilization by Entrapment Gel Poliakrilamida
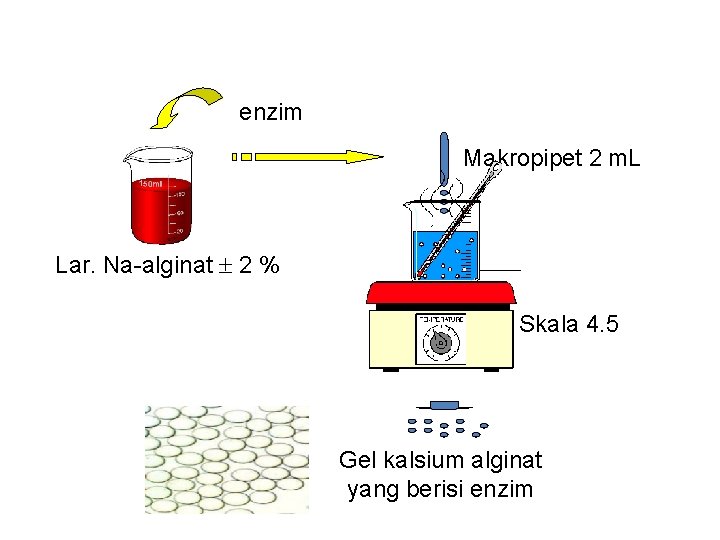
Cara Penjeraban Tipe Kisi enzim Makropipet 2 m. L Lar. Na-alginat 2 % Ca. Cl 2 0. 1 M Skala 4. 5 Gel kalsium alginat yang berisi enzim

Perubahan Sifat Enzim Terimobilisasi 1. Aktivitas V 1(aktivitas relatif) Perbandingan aktivitas enzim imobil vs enzim larut dalam jumlah sama V 2 (aktivitas spesifik absolut) Kecepatan reaksi per unit berat atau unit volume seluruh katalis V 1 tidak deaktivasi enzim akibat prosesimobilisasi V 2 kemungkinan untuk mengimobilisasi enzim lebih banyak/sedikit per unit berat/volume katalis Penyebab penurunan aktivitas : • Konfigurasi menghalangi substrat • Gugus reaktif pada sisi aktif ikut terikat pada matriks • Terbentuk konfigurasi tidak aktif • Kondisi reaksi ekstrim denaturasi

2. p. H optimum enzim imobil Penyebab perubahan p. H : distribusi yang tidak seragam ion H+, ion OH- dan substrat bermuatan Aktivitas Relatif (%) Carrier bermuatan negatif p. H optimum bersifat basa CMC, Asam galakturonat, Asam poliaspartat, anhidrida etilen Carrier bermuatan positif p. H lebih asam DEAE-selulosa, Polimer poliornithil c 4 a 7 b a : enzim chymotripsin larut b : kopolimer chym – anhidrida etilen (-) c : chym – poliornithil (+) → p. H

3. Stabilitas operasi = t 1/2 (half-life) = waktu dimana terjadi kehilangan 50 % dari aktivitas enzim semula k = konstanta kerusakan enzim t = waktu operasi E 0 = aktivitas enzim mula-mula E = aktivitas enzim pada wktu t Stabilitas operasi ditentukan oleh : • Jenis enzim • Cara imobilisasi • Jenis bioreaktor
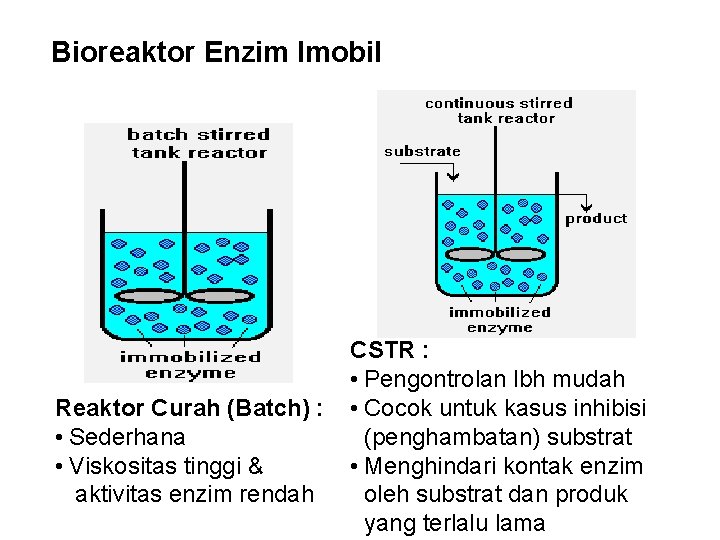
Bioreaktor Enzim Imobil Reaktor Curah (Batch) : • Sederhana • Viskositas tinggi & aktivitas enzim rendah CSTR : • Pengontrolan lbh mudah • Cocok untuk kasus inhibisi (penghambatan) substrat • Menghindari kontak enzim oleh substrat dan produk yang terlalu lama
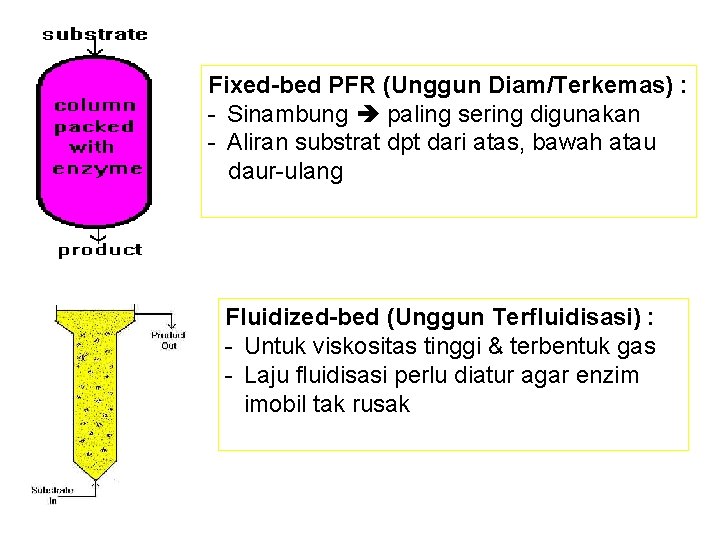
Fixed-bed PFR (Unggun Diam/Terkemas) : - Sinambung paling sering digunakan - Aliran substrat dpt dari atas, bawah atau daur-ulang Fluidized-bed (Unggun Terfluidisasi) : - Untuk viskositas tinggi & terbentuk gas - Laju fluidisasi perlu diatur agar enzim imobil tak rusak
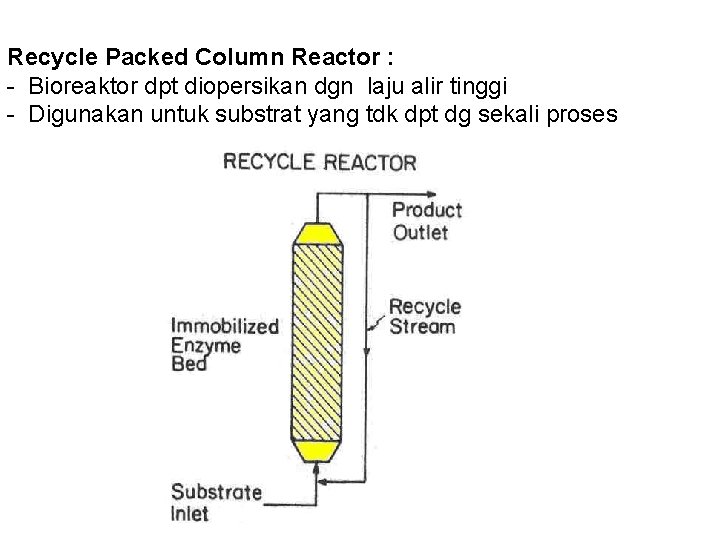
Recycle Packed Column Reactor : - Bioreaktor dpt diopersikan dgn laju alir tinggi - Digunakan untuk substrat yang tdk dpt dg sekali proses

Pengukuran Efisiensi Imobilisasi (Aktifitas enzim yang teradsorbsi pada penyangga) • Larutan enzim : - aktifitas : 591 U/m. L - volume larutan : 40 m. L Total aktifitas : 40 x 591 = 23600 U • Bobot Penyangga (carrier) : 11 gram Setelah mobilisasi Aktifitas enzim terimobilisasi : 381 U/g penyangga Total aktifitas enzim yang teradsorbsi pada penyangga = 11 x 381 U = 4191 U Persentase aktifitas enzim teradsorbsi = 4191/23600 x 100% = 17, 8 %

Imobilisasi Sel : • Meningkatkan konsentrasi biomassa produktivitas > • Konsentrasi sel menentukan waktu tinggal dlm bioreaktor • Operasi sinambung dg laju alir > (waktu tinggal pendek), tidak terjadi wash out • Biomassa dapat digunakan kembali • Pemisahan biomassa lebih mudah Metode : 1. Carrier biding : E. coli A. oryzae, dll 2. Entraping paling banyak diteliti Matriks yang digunakan : • Kolagen, Selulosa triasetat tipe membran • Alginat, Agar, Karagenan, Poliakrilamida tipe kisi 3. Cross linking : E. coli
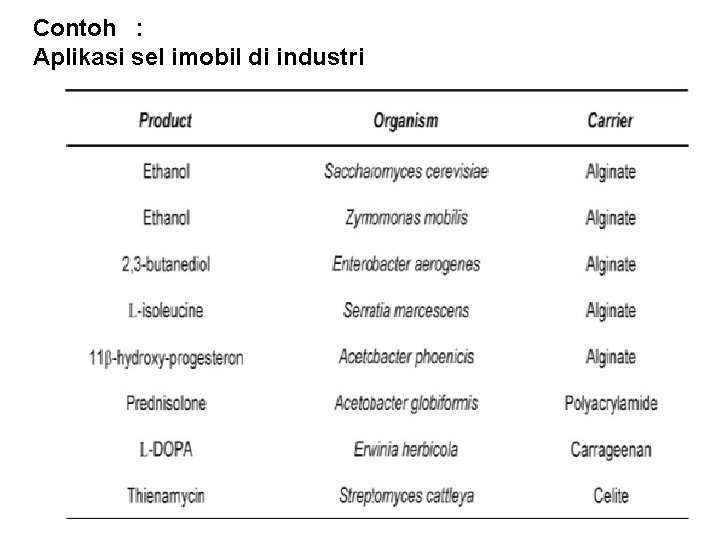
Contoh : Aplikasi sel imobil di industri

Aplikasi Enzim Imobil di Industri 1. Produksi Fruktosa dari Glukosa (HFS) Glukosa Fruktosa Glukoisomerase : Intraseluler & Mahal (diimobilisasi dg ikatan ionik - DEAE-Selulosa) 2. Produksi L-asam amino (e. g L-Metionin) bentuk yg dapat diserap tubuh Hasil reaksi kimia campuran asam amino : asetil D&L asam amino (rasemat) + aminoasilase imobil (DEAESephadex) terjadi deasilasi hanya pada asam amino yg bentuk L 3. Produksi Antibiotika APA (6 -amino penicillanic acid) - Benzil Penisilin (hasil fermentasi) + penisilin amidase(diimobilisasi ikatan ionik dg selulosa asetat) APA - APA + gugus metil α-metil benzil penisilin (=Ampisilin, antibiotika spektrum luas)

BIOSENSOR Prinsip pengukuran : perubahan oksigen, kofaktor NADH (menyerap cahaya pd λ 340 nm) atau senyawa lain (amonia dll) Contoh (lar glukosa) Kolom kapile Sistem Monitoring Glukosa O 2 Glukosidase Glukonolakton + H 2 O 2 Elektroda O 2 Glu. oks imobil O 2 diukur dengan elektroda Recording electrometer Penentuan Asam Askorbat Asam L-Askorbat + ½ O 2 asam dehidroaskorbat + H 2 O Askorbat oksidase O 2 diukur dengan elektroda
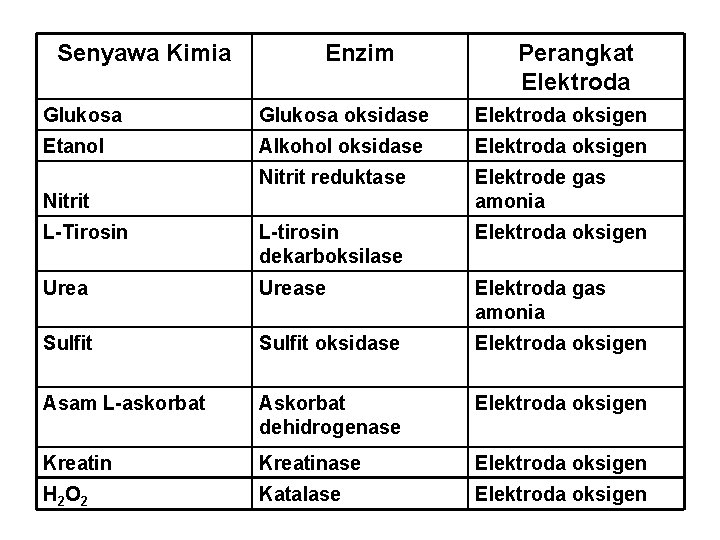
Senyawa Kimia Enzim Perangkat Elektroda Glukosa oksidase Elektroda oksigen Etanol Alkohol oksidase Elektroda oksigen Nitrit reduktase Elektrode gas amonia L-Tirosin L-tirosin dekarboksilase Elektroda oksigen Urease Elektroda gas amonia Sulfit oksidase Elektroda oksigen Asam L-askorbat Askorbat dehidrogenase Elektroda oksigen Kreatinase Elektroda oksigen H 2 O 2 Katalase Elektroda oksigen Nitrit

Contoh Aplikasi • Produksi sirup Fruktosa dari Inulin Umbi Dahlia Dalam Reaktor Sinambung Unggun Terkemas (Fixedbed) Menggunakan Enzim Inulinase Imobil ( Skripsi Sujatmono , T. S, 1992)
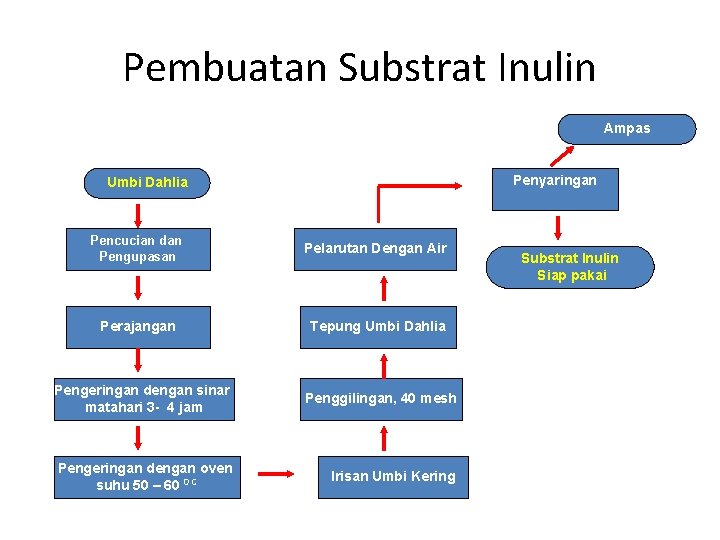
Pembuatan Substrat Inulin Ampas Penyaringan Umbi Dahlia Pencucian dan Pengupasan Pelarutan Dengan Air Perajangan Tepung Umbi Dahlia Pengeringan dengan sinar matahari 3 - 4 jam Penggilingan, 40 mesh Pengeringan dengan oven suhu 50 – 60 0 C Irisan Umbi Kering Substrat Inulin Siap pakai
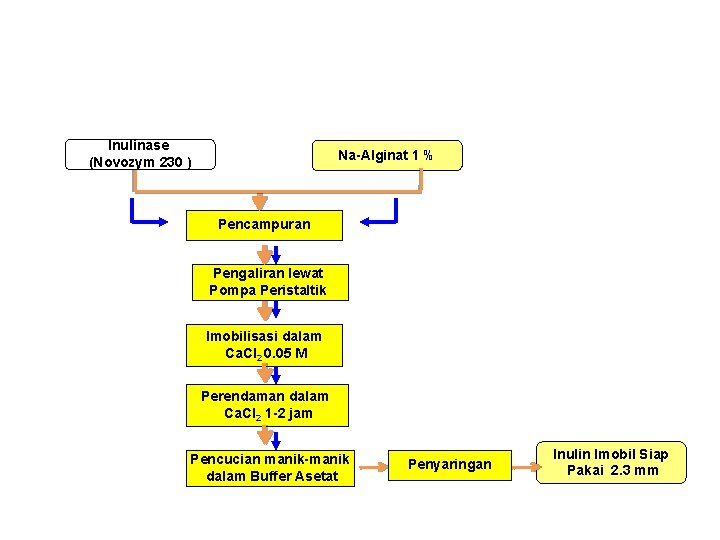
Pembuatan Enzim Inulinase Imobil Inulinase (Novozym 230 ) Na-Alginat 1 % Pencampuran Pengaliran lewat Pompa Peristaltik Imobilisasi dalam Ca. Cl 2 0. 05 M Perendaman dalam Ca. Cl 2 1 -2 jam Pencucian manik-manik dalam Buffer Asetat Penyaringan Inulin Imobil Siap Pakai 2. 3 mm
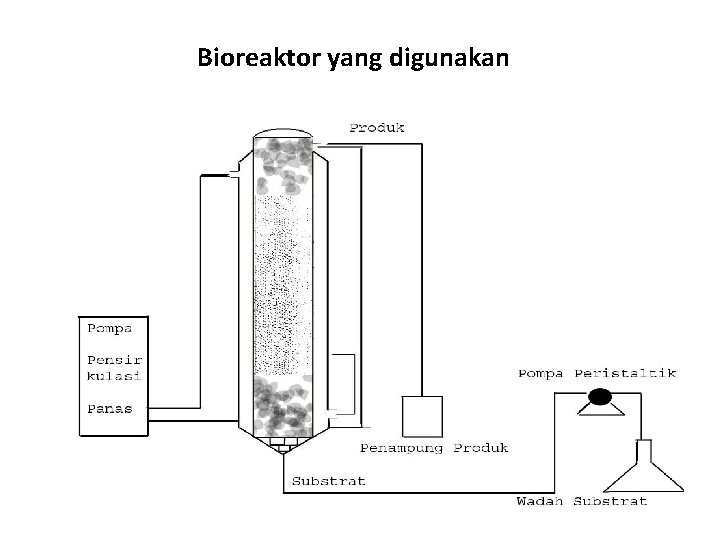
Bioreaktor yang digunakan
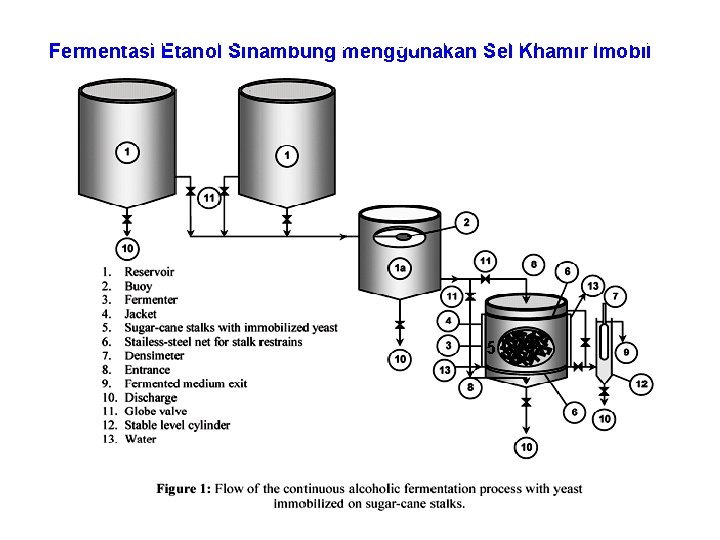
Fermentasi Etanol Sinambung menggunakan Sel Khamir Imobil 5
- Slides: 32