LUYN TP CACBON SILIC V HP CHT CA

LUYỆN TẬP: CACBON- SILIC VÀ HỢP CHẤT CỦA CHÚNG
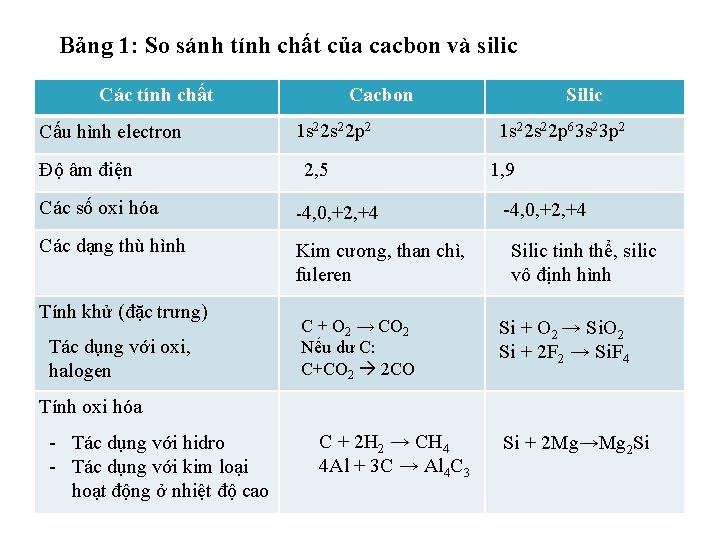
Bảng 1: So sánh tính chất của cacbon và silic Các tính chất Cấu hình electron Độ âm điện Cacbon 1 s 22 p 2 2, 5 Các số oxi hóa -4, 0, +2, +4 Các dạng thù hình Kim cương, than chì, fuleren Tính khử (đặc trưng) Tác dụng với oxi, halogen C + O 2 → CO 2 Nếu dư C: C+CO 2 2 CO Silic 1 s 22 p 63 s 23 p 2 1, 9 -4, 0, +2, +4 Silic tinh thể, silic vô định hình Si + O 2 → Si. O 2 Si + 2 F 2 → Si. F 4 Tính oxi hóa - Tác dụng với hidro - Tác dụng với kim loại hoạt động ở nhiệt độ cao C + 2 H 2 → CH 4 4 Al + 3 C → Al 4 C 3 Si + 2 Mg→Mg 2 Si
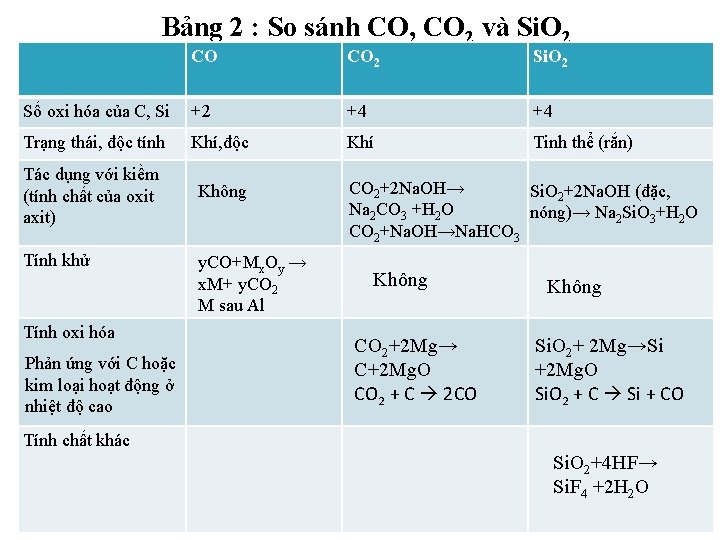
Bảng 2 : So sánh CO, CO 2 và Si. O 2 CO CO 2 Si. O 2 Số oxi hóa của C, Si +2 +4 +4 Trạng thái, độc tính Khí, độc Khí Tinh thể (rắn) Tác dụng với kiềm (tính chất của oxit axit) Không Tính khử Tính oxi hóa Phản ứng với C hoặc kim loại hoạt động ở nhiệt độ cao y. CO+Mx. Oy → x. M+ y. CO 2 M sau Al CO 2+2 Na. OH→ Si. O 2+2 Na. OH (đặc, Na 2 CO 3 +H 2 O nóng)→ Na 2 Si. O 3+H 2 O CO 2+Na. OH→Na. HCO 3 Không CO 2+2 Mg→ C+2 Mg. O CO 2 + C 2 CO Không Si. O 2+ 2 Mg→Si +2 Mg. O Si. O 2 + C Si + CO Tính chất khác Si. O 2+4 HF→ Si. F 4 +2 H 2 O
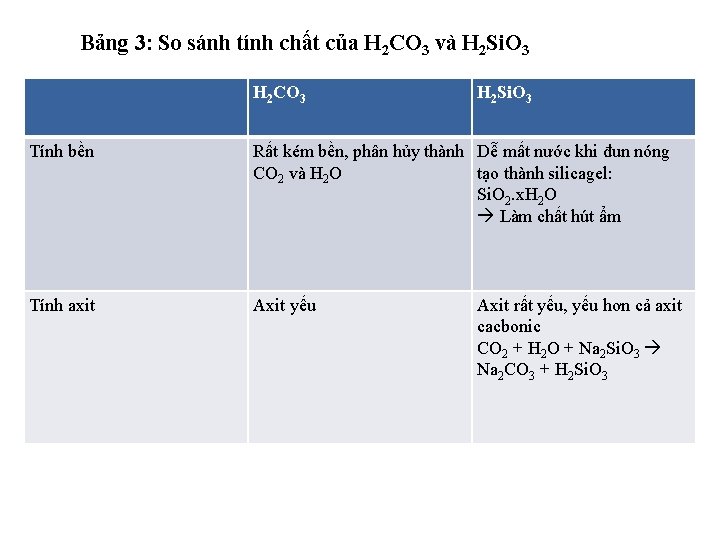
Bảng 3: So sánh tính chất của H 2 CO 3 và H 2 Si. O 3 H 2 CO 3 H 2 Si. O 3 Tính bền Rất kém bền, phân hủy thành Dễ mất nước khi đun nóng CO 2 và H 2 O tạo thành silicagel: Si. O 2. x. H 2 O Làm chất hút ẩm Tính axit Axit yếu Axit rất yếu, yếu hơn cả axit cacbonic CO 2 + H 2 O + Na 2 Si. O 3 Na 2 CO 3 + H 2 Si. O 3

BÀI TẬP LÝ THUYẾT Câu 1: Chất khí nào sau đây không cháy trong oxi? A. C 2 H 2. B. CH 4 C. CO 2 D. NH 3 Câu 2: Dẫn khí CO 2 đến dư vào dung dịch Na. OH, dung dịch sau phản ứng chứachất nào? A. Na 2 CO 3 và Na. OH B. Na. HCO 3 C. Na 2 CO 3 D. Na. HCO 3 và Na 2 CO 3 Câu 3: Hiện tượng xảy ra khi nhỏ từ từ tới dư dung dịch Na. OH vào dung dịch Ba(HCO 3)2 là: A. Có kết tủa trắng không tan trong dung dịch Na. OH B. Có sủi bọt khí không màu thoát ra C. Không có hiện tượng gì D. Có kết tủa trắng xuất hiện và tan trong Na. OH Câu 4: Chất nào sau đây là chất lưỡng tính : A. Na 2 CO 3 B. Al. Cl 3 C. KHSO 4 D. Ca(HCO 3)2

BÀI TẬP LÝ THUYẾT Câu 5: Trong các phản ứng hoá học sau, phản ứng nào sai? A. 3 CO + Fe 2 O 3 3 CO 2 + 2 Fe. B. CO + Cu. O CO 2 + Cu. C. 3 CO + Al 2 O 3 2 Al + 3 CO 2. D. 2 CO + O 2 2 CO 2. Câu 6: Để loại bỏ khí CO 2 có lẫn trong hỗn hợp CO và CO 2, ta dẫn hỗn hợp khí qua A. dung dịch Ca(OH)2. B. dung dịch HCl. C. dung dịch Na. Cl. D. dung dịch H 2 O. Câu 7: Phát biểu nào sau đây không đúng A. Dung dịch đậm đặc của Na 2 Si. O 3 và K 2 Si. O 3 được gọi là thủy tinh lỏng B. Đám cháy magie có thể dập tắt bằng cát khô C. Khí CO 2 là chất khí gây ra hiệu ứng nhà kính D. Có thể phòng độc khí CO bằng cách sử dụng mặt nạ chứa than hoạt tính

BÀI TẬP LÝ THUYẾT Câu 8: Số Oxi hóa cao nhất của silic thể hiện ở hợp chất nào sau đây : A. Si. H 4 B. Si. O C. Si. O 2 D. Mg 2 Si Câu 9: Hai dung dịch phản ứng với nhau tạo khí CO 2 và không tạo kết tủa. Hai dung dịch đó là: A. Ca. CO 3 và HCl B. Na 2 CO 3 và Ba. Cl 2 C. Fe. Cl 3 và K 2 CO 3 D. Na. HCO 3 và HCl Câu 10: Chất X có một số tính chất sau: - Tan trong nước tạo thành dung dịch có khả năng làm quỳ tím chuyển màu xanh. - Tạo kết tủa với dung dịch Ba(OH)2. Vậy X là: A. Na 2 SO 4 B. Na. HSO 4 C. Na 2 CO 3 D. Na. OH
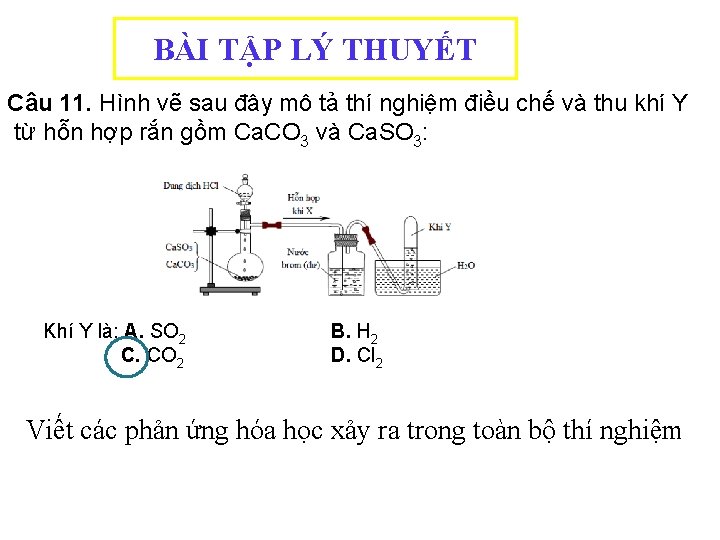
BÀI TẬP LÝ THUYẾT Câu 11. Hình vẽ sau đây mô tả thí nghiệm điều chế và thu khí Y từ hỗn hợp rắn gồm Ca. CO 3 và Ca. SO 3: Khí Y là: A. SO 2 C. CO 2 B. H 2 D. Cl 2 Viết các phản ứng hóa học xảy ra trong toàn bộ thí nghiệm

BÀI TẬP LÝ THUYẾT Câu 12. Chỉ dùng thêm cách đun nóng, nhận biết các dung dịch: Na 2 CO 3, Ba(HCO 3)2, Na. HCO 3, Na 2 SO 4, HCl. - Đun nóng các dung dịch: Mẫu có khí và tủa là Ba(HCO 3)2 Mẫu có sủi bọt khí: Na. HCO 3 Các mẫu còn lại không hiện tượng. - Cho Na. HCO 3 vào 3 mẫu thử còn lại, mẫu có sủi bọt khí là HCl. - Cho HCl vào 2 mẫu còn lại, mẫu sủi bọt khí là Na 2 CO 3. - Mẫu không ht là Na 2 SO 4.

BÀI TẬP LÝ THUYẾT Câu 13. Cho khí CO dư đi vào ống sứ nung nóng đựng hỗn hợp gồm Al 2 O 3, Fe 3 O 4 và Cu. O. Sau khi phản ứng hoàn toàn, thu được chất rắn X và khí Y. - Dẫn Y vào nước vôi trong thu được kết tủa trắng sau đó tủa tan. - Chất rắn X tác dụng với dung dịch HNO 3 đặc, nguội, dư. Viết các phương trình hóa học và xác định các chất trong X và Y. Chất rắn X: Al 2 O 3, Fe, Cu Khí Y: CO 2, CO Khí Y + Ca(OH)2: CO 2 + Ca(OH)2 Ca. CO 3 + H 2 O CO 2 + Ca. CO 3 + H 2 O Ca(HCO 3)2 X + HNO 3 đặc nguội: Al 2 O 3 + 6 HNO 3 2 Al(NO 3)3 + 3 H 2 O Cu + HNO 3 Cu(NO 3)2 + NO 2 + H 2 O

BÀI TẬP LÝ THUYẾT Câu 14: Thực hiện dãy chuyển hoá sau (ghi rõ đk nếu có) (2) (3) (4) (5) (6) CO 2 �Ca. CO 3 �Ca(HCO 3)2�CO 2 �C �CO �Fe (1) (8) Na. NO 3 (9) (10) H 2 Si. O 3 → Si. O 2 → Si. F 4 (7)

BÀI TẬP TOÁN Bài 1. Cho 6, 72 lít khí CO 2 (ở đktc) hấp thụ hết vào V lít dung dịch Ba(OH)2 0, 4 M. Sau phản ứng hoàn thu được 29, 55 g kết tủa. Giá trị của ? Bài 2. Sục V lít CO 2 (đktc) vào 200 ml dung dịch hỗn hợp KOH 0, 5 M và Ba(OH)2 0, 375 M thu được 11, 82 gam kết tủa. Giá trị của V là A. 1, 344 l lít. B. 4, 256 lít. C. 8, 512 lít. D. 1, 344 l lít hoặc 4, 256 lít

BÀI TẬP TOÁN Bài 3: Sục 4, 48(lít) CO 2 (đktc) vào 500 ml dd Ba(OH)2 0, 3 M, sau phản ứng thu được bao nhiêu gam kết tủa. Bài 4. Để khử hoàn toàn 21, 6 gam hỗn hợp gồm Fe. O, Fe 2 O 3, Fe 3 O 4 và Cu. O cần vừa đủ 2, 24 lít khí CO (đktc). Tính khối lượng kim loại thu được sau phản ứng.
- Slides: 13