LOS SUBTIPOS TUMORALES DE LAUREN PREDICEN SUPERVIVENCIA Y

LOS SUBTIPOS TUMORALES DE LAUREN PREDICEN SUPERVIVENCIA Y RESPUESTA A QUIMIOTERAPIA EN EL CÁNCER GÁSTRICO AVANZADO: ESTUDIO MULTICÉNTRICO CON 1303 PACIENTES. • • Presentado por: Dra. Raquel Hernández. Complejo Hospitalario Universitario de Canarias, Tenerife. Coautores: § Dr. Alberto Carmona-Bayonas. § Dra. Elvira Buxo. § Dra. Aitziber Gil-Negrete. § Dr. Aitor Azcarate. § Dra. Ana Custodio. § Dra. Asunción Diaz. § Dr. José Enrique Lorenzo. § Dr. Carlos López. § Dr. Javier Gallego. 1 #SEOM 2017

INTRODUCCIÓN Y OBJETIVOS • El cáncer gástrico constituye la 5ª neoplasia más frecuente a nivel mundial y la 3ª causa de muerte por cáncer en ambos sexos. 1 • La elección del tratamiento con quimioterapia en el cáncer gástrico avanzado (CGA), Her 2 negativo, se basa en las preferencias del centro, pérfil de efectos adversos y las comorbilidades del paciente, sin que exista un esquema aceptado como estándar 2. A excepción del Her 2, no existen otros factores predictivos de respuesta. • La clasificación histológica de Lauren (1965) divide al cáncer gástrico en tipo intestinal (IT) y difuso (DT)3, 4, 5 Esta clasificación histológica es relevante desde el punto de vista pronóstico, epidemiológico y patogénico. • Estos dos tipos histológicos difieren en sus características clínicas y moleculares, representando dos entidades molecularmente diferentes. 1: Ferlay et al, 2015. 2: Duo-Ji M-M 2017. 3: Tan et al, 2011. 4: Ma et al, 2016. 5: Yong; et al, 2017. 2 #SEOM 2017

INTRODUCCIÓN Y OBJETIVOS • El efecto predictivo de cada subtipo histológico en relación a la eficacia de la quimioterapia no ha sido esclarecido definitivamente. En la actualidad, ambos se tratan de manera similar. 6, 7 v Ensayos pivotales en población occidental no reportan análisis de subgrupos pre-planeados en función de estos criterios. v La ACRG (mayoría de datos asiáticos) sugiere que la heterogeneidad histológica se corresponde con sensibilidad específica a fármacos, abriendo la puerta a terapias personalizadas. 8, 9, 10 o Evidencia aún débil, con test de interacción a menudo no significativos o no comunicados y series con tamaño muestral limitado. • El objetivo de estudio es evaluar si la clasificación de Lauren influye en la eficacia de los distintos esquemas de tratamiento y en la supervivencia. 6: Van Cutsem et al, 2006. 7: Cunningham et al, 2008. 8: Koizumi et al, 2008, 2014. 9: Boku et al, 2009. 10: Narahara et al, 2011. 3 #SEOM 2017
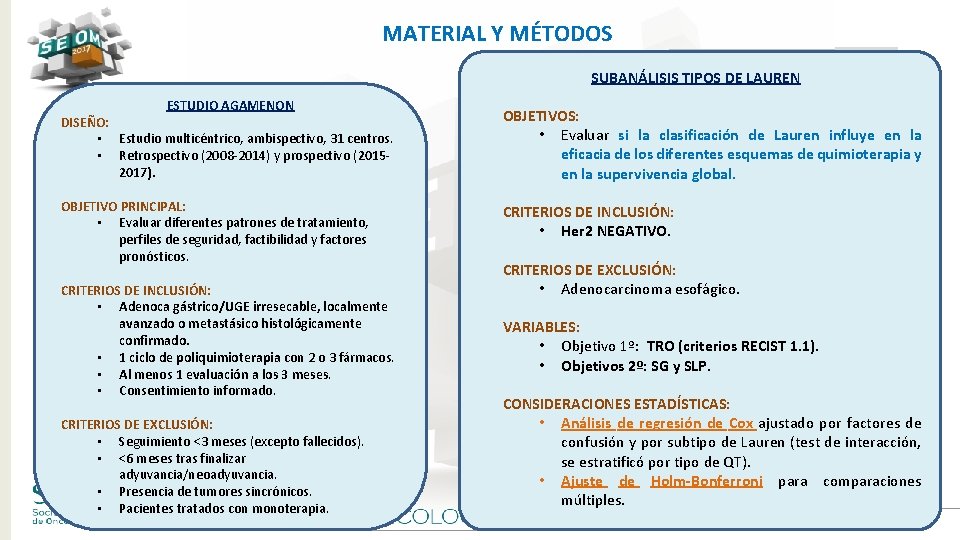
MATERIAL Y MÉTODOS SUBANÁLISIS TIPOS DE LAUREN ESTUDIO AGAMENON DISEÑO: • Estudio multicéntrico, ambispectivo, 31 centros. • Retrospectivo (2008 -2014) y prospectivo (20152017). OBJETIVO PRINCIPAL: • Evaluar diferentes patrones de tratamiento, perfiles de seguridad, factibilidad y factores pronósticos. CRITERIOS DE INCLUSIÓN: • Adenoca gástrico/UGE irresecable, localmente avanzado o metastásico histológicamente confirmado. • 1 ciclo de poliquimioterapia con 2 o 3 fármacos. • Al menos 1 evaluación a los 3 meses. • Consentimiento informado. CRITERIOS DE EXCLUSIÓN: • Seguimiento <3 meses (excepto fallecidos). • <6 meses tras finalizar adyuvancia/neoadyuvancia. • Presencia de tumores sincrónicos. • Pacientes tratados con monoterapia. OBJETIVOS: • Evaluar si la clasificación de Lauren influye en la eficacia de los diferentes esquemas de quimioterapia y en la supervivencia global. CRITERIOS DE INCLUSIÓN: • Her 2 NEGATIVO. CRITERIOS DE EXCLUSIÓN: • Adenocarcinoma esofágico. VARIABLES: • Objetivo 1º: TRO (criterios RECIST 1. 1). • Objetivos 2º: SG y SLP. CONSIDERACIONES ESTADÍSTICAS: • Análisis de regresión de Cox ajustado por factores de confusión y por subtipo de Lauren (test de interacción, se estratificó por tipo de QT). • Ajuste de Holm-Bonferroni para comparaciones múltiples. #SEOM 2017
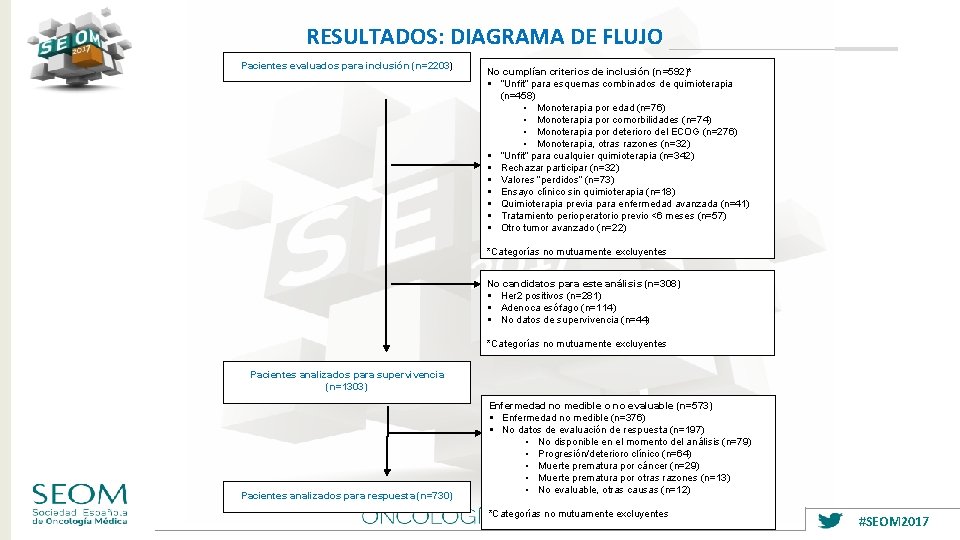
RESULTADOS: DIAGRAMA DE FLUJO Pacientes evaluados para inclusión (n=2203) No cumplían criterios de inclusión (n=592)* § “Unfit” para esquemas combinados de quimioterapia (n=458) • Monoterapia por edad (n=76) • Monoterapia por comorbilidades (n=74) • Monoterapia por deterioro del ECOG (n=276) • Monoterapia, otras razones (n=32) § “Unfit” para cualquier quimioterapia (n=342) § Rechazar participar (n=32) § Valores “perdidos” (n=73) § Ensayo clínico sin quimioterapia (n=18) § Quimioterapia previa para enfermedad avanzada (n=41) § Tratamiento perioperatorio previo <6 meses (n=57) § Otro tumor avanzado (n=22) *Categorías no mutuamente excluyentes No candidatos para este análisis (n=308) § Her 2 positivos (n=281) § Adenoca esófago (n=114) § No datos de supervivencia (n=44) *Categorías no mutuamente excluyentes Pacientes analizados para supervivencia (n=1303) Pacientes analizados para respuesta (n=730) Enfermedad no medible o no evaluable (n=573) § Enfermedad no medible (n=376) § No datos de evaluación de respuesta (n=197) • No disponible en el momento del análisis (n=79) • Progresión/deterioro clínico (n=64) • Muerte prematura por cáncer (n=29) • Muerte prematura por otras razones (n=13) • No evaluable, otras causas (n=12) *Categorías no mutuamente excluyentes #SEOM 2017
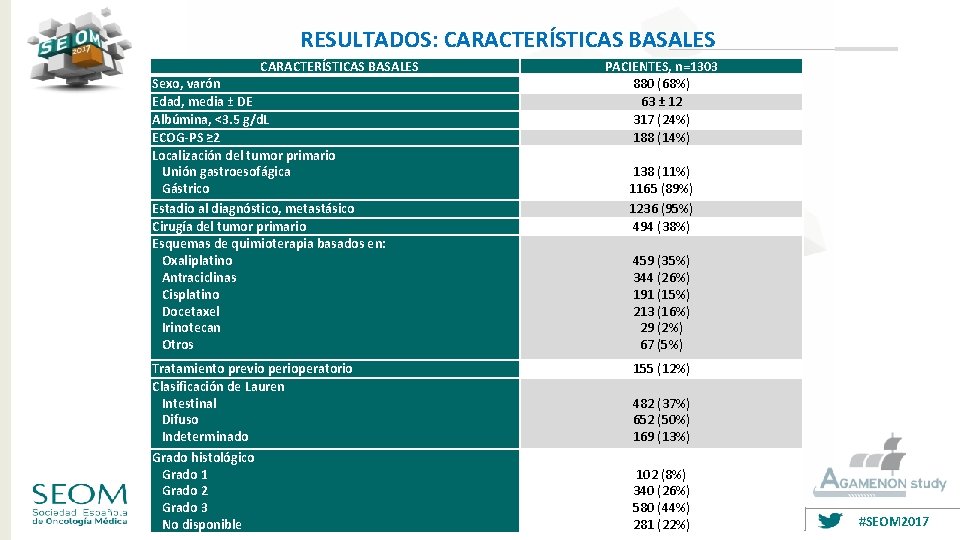
RESULTADOS: CARACTERÍSTICAS BASALES Sexo, varón Edad, media ± DE Albúmina, <3. 5 g/d. L ECOG-PS ≥ 2 Localización del tumor primario Unión gastroesofágica Gástrico Estadio al diagnóstico, metastásico Cirugía del tumor primario Esquemas de quimioterapia basados en: Oxaliplatino Antraciclinas Cisplatino Docetaxel Irinotecan Otros Tratamiento previo perioperatorio Clasificación de Lauren Intestinal Difuso Indeterminado Grado histológico Grado 1 Grado 2 Grado 3 No disponible PACIENTES, n=1303 880 (68%) 63 ± 12 317 (24%) 188 (14%) 138 (11%) 1165 (89%) 1236 (95%) 494 (38%) 459 (35%) 344 (26%) 191 (15%) 213 (16%) 29 (2%) 67 (5%) 155 (12%) 482 (37%) 652 (50%) 169 (13%) 102 (8%) 340 (26%) 580 (44%) 281 (22%) #SEOM 2017
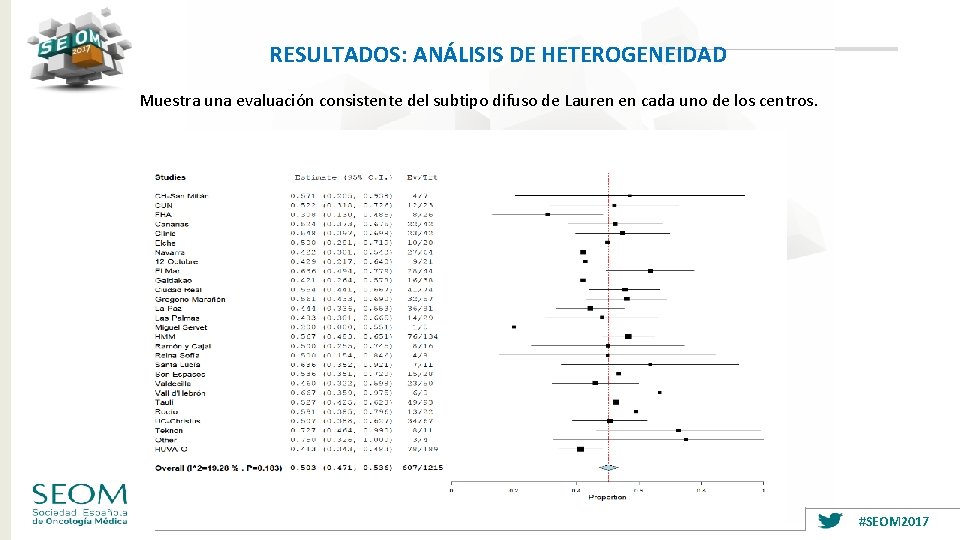
RESULTADOS: ANÁLISIS DE HETEROGENEIDAD Muestra una evaluación consistente del subtipo difuso de Lauren en cada uno de los centros. #SEOM 2017

RESULTADOS PACIENTES: Ø 2203 pacientes (corte en junio 2017) tratados con quimioterapia de 1ª línea (1/2008 y 3/2017). ØPacientes evaluables: 1303 (supervivencia) y 730 (respuestas). PRONÓSTICO: ØPronóstico diferente según el subtipo histológico; (log-rank test of X 2=7. 7, df=2, p=0. 021). ØIT: m. OS 11. 0 meses (95% CI, 10. 3– 12. 1). ØDT: 9. 3 meses (95% CI, 8. 3– 10. 3). ØTumores “no clasificados”: 10. 1 meses (95% CI, 8. 5– 11. 1). Ø El subtipo difuso presenta mayor mortalidad; HR: 1. 201 (95% CI, 1. 054– 1. 368), p=0. 0056, respecto al IT. #SEOM 2017
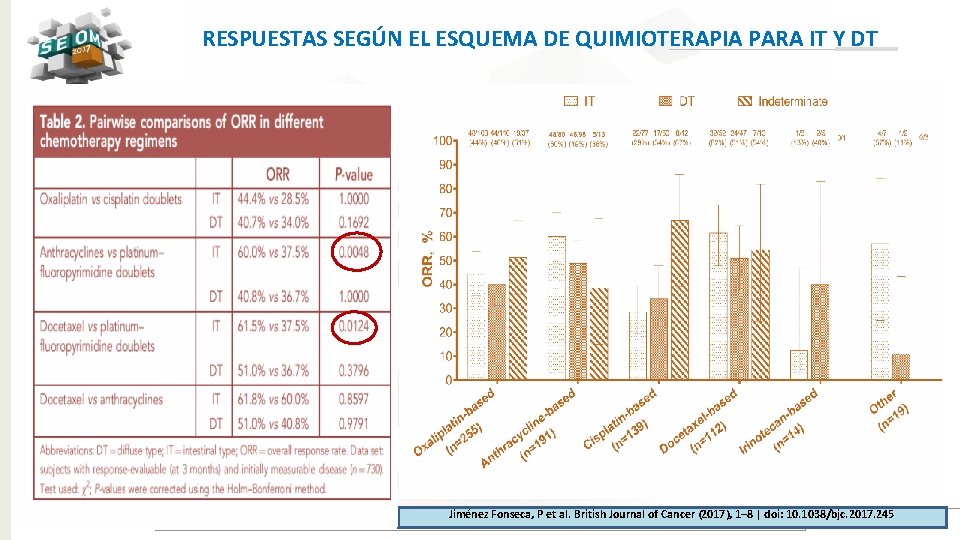
RESPUESTAS SEGÚN EL ESQUEMA DE QUIMIOTERAPIA PARA IT Y DT Jiménez Fonseca, P et al. British Journal of Cancer (2017), 1– 8 | doi: 10. 1038/bjc. 2017. 245 #SEOM 2017
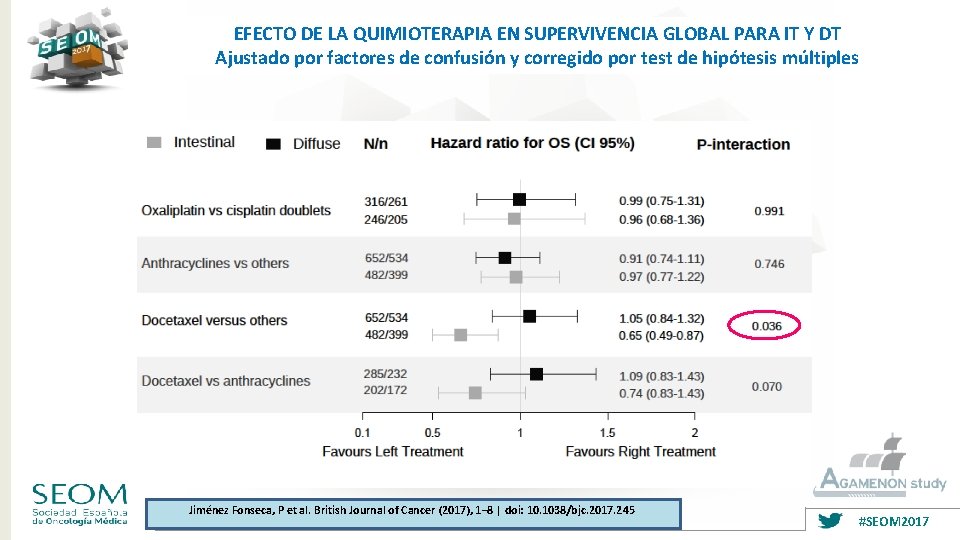
EFECTO DE LA QUIMIOTERAPIA EN SUPERVIVENCIA GLOBAL PARA IT Y DT Ajustado por factores de confusión y corregido por test de hipótesis múltiples Jiménez Fonseca, P et al. British Journal of Cancer (2017), 1– 8 | doi: 10. 1038/bjc. 2017. 245 #SEOM 2017
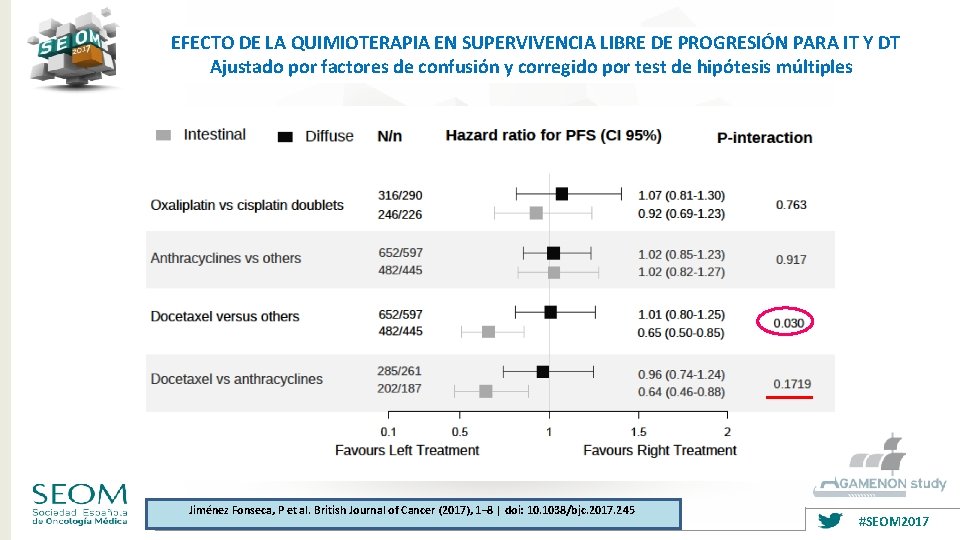
EFECTO DE LA QUIMIOTERAPIA EN SUPERVIVENCIA LIBRE DE PROGRESIÓN PARA IT Y DT Ajustado por factores de confusión y corregido por test de hipótesis múltiples Jiménez Fonseca, P et al. British Journal of Cancer (2017), 1– 8 | doi: 10. 1038/bjc. 2017. 245 #SEOM 2017

CONCLUSIONES • En nuestro estudio Agamenon, la clasificación según los subtipos de Lauren, predice supervivencia y respuesta a diferentes esquemas de quimioterapia. • Nuestros datos apoyan la hipótesis de que la heterogeneidad histopatológica se traduce en una sensibilidad específica a diversos citotóxicos. • Resulta necesario validar el efecto de variables como la histología que podrían modificar la respuesta a los fármacos. • Futuras investigaciones clínicas deberían considerar estratificar por el tipo de Lauren el efecto del tratamiento en el cancer gástrico avanzado. • Importancia de la confirmación de estos resultados extraídos de “real world data” mediante estudios prospectivos diseñados a tal efecto. 13 #SEOM 2017

AGRADECIMIENTOS • A todos los pacientes. • Equipo coordinador (Dr Alberto Carmona) del estudio AGAMENON y al resto de investigadores. 14 #SEOM 2017
- Slides: 13