Los niveles contienen SUBNIVELES N 1 N 2

Los niveles contienen SUBNIVELES N 1 N 2 N 3 N 4 1 subnivel 2 subniveles 3 subniveles 4 subniveles etc. . .

Los subniveles se identifican de acuerdo a la forma de los orbitales del átomo con las letras s, p, d y f
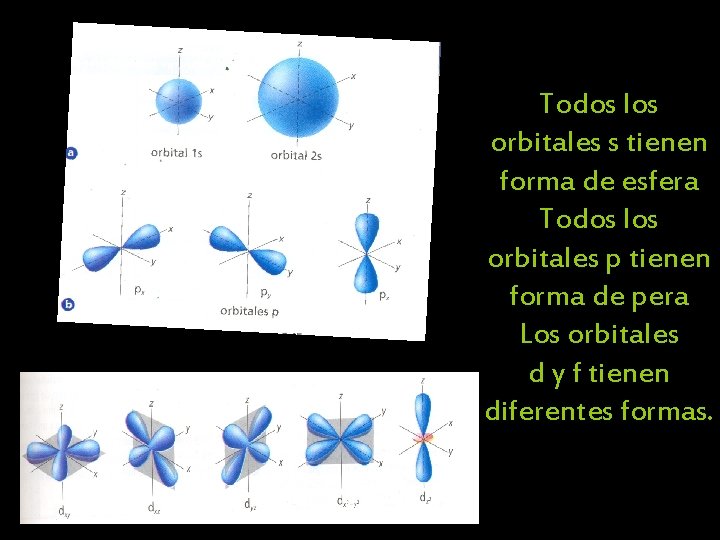
Todos los orbitales s tienen forma de esfera Todos los orbitales p tienen forma de pera Los orbitales d y f tienen diferentes formas.

El nivel principal de energía 1 contiene 1 subnivel = 1 s El nivel principal de energía 2 contiene 2 subniveles= 2 s y 2 p El nivel principal de energía 3 contiene 3 subniveles= 3 s 3 p y 3 d El nivel principal de energía 4 contiene 4 subniveles= 4 s 4 p 4 d y 4 f
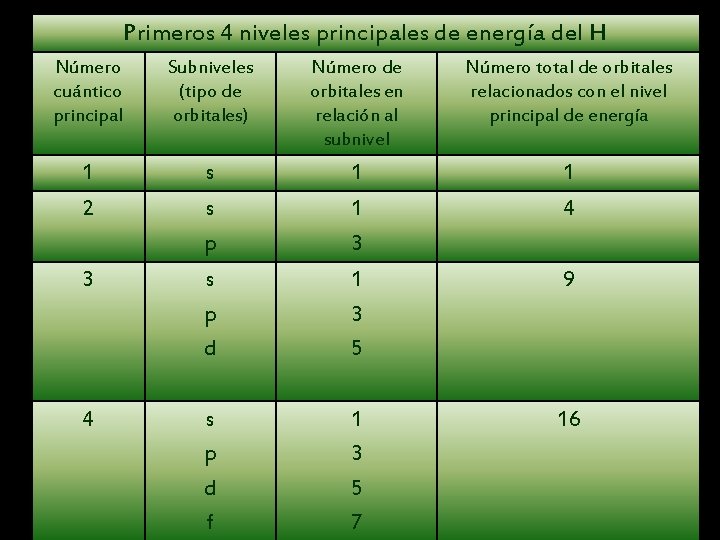
Primeros 4 niveles principales de energía del H Número cuántico principal Subniveles (tipo de orbitales) Número de orbitales en relación al subnivel Número total de orbitales relacionados con el nivel principal de energía 1 2 s s p d 1 1 3 5 1 4 s p d f 1 3 5 7 16 3 4 9

Número de orbitales posibles= n 2 Cada orbital puede tener 2 electrones Número máximo de electrones por orbital= 2 n 2

CONFIGURACIONES ELECTRÓNICAS El ordenamiento de los electrones en los átomos se denomina configuración electrónica

Los sistemas de baja energía son más estables. . . . Los electrones en un átomo tienden a asumir el ordenamiento que le confiera al átomo la menor energía posible y la mayor estabilidad.

Reglas para las Configuraciones electrónicas 1 Principio de Aufbau (distribución electrónica o construcción progresiva) Cada electrón ocupa el orbital disponible con energía más baja.
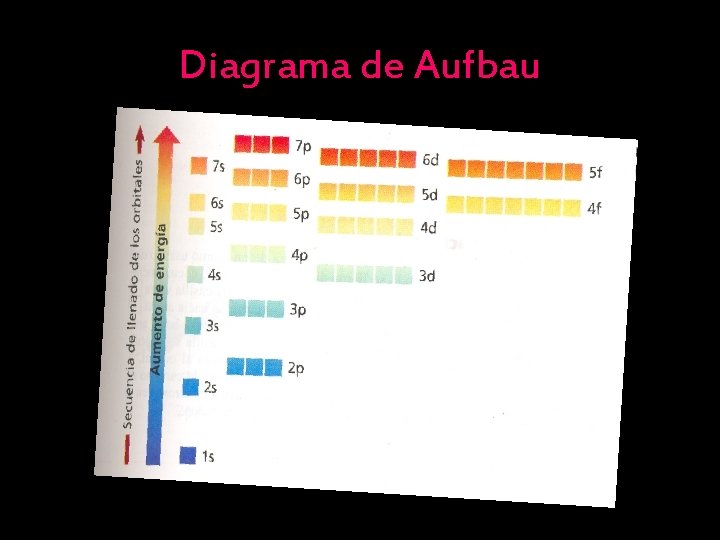
Diagrama de Aufbau

a) Todos los orbitales relacionados con un subnivel de energía son de igual energía = los tres orbitales 2 p tienen la misma energía. b) En átomos con múltiples electrones, los subniveles de energía dentro de un nivel principal tienen energía diferentes = los orbitales 2 p tienen energía más alta que el orbital 2 s.

c) Según la cantidad de energía, la secuencia de los subniveles en un nivel principal es s, p, d y f. d) Los orbitales relacionados con subniveles de energía de un nivel principal pueden superponerse a los orbitales relacionados con los subniveles de energía de otro nivel principal = 4 s tiene menor energía que los cinco orbitales relacionados con el subnivel 3 d

2 Principio de exclusión de Pauli Un máximo de dos electrones pueden ocupar un mismo orbital atómico pero solamente si los electrones tienes spin opuesto.

3 Regla de Hund Los electrones cuyo giro es igual deben ocupar todos los orbitales que tienen igual energía antes que los electrones con giro opuesto puedan ocupar los mismo orbitales. Orbitales 2 p
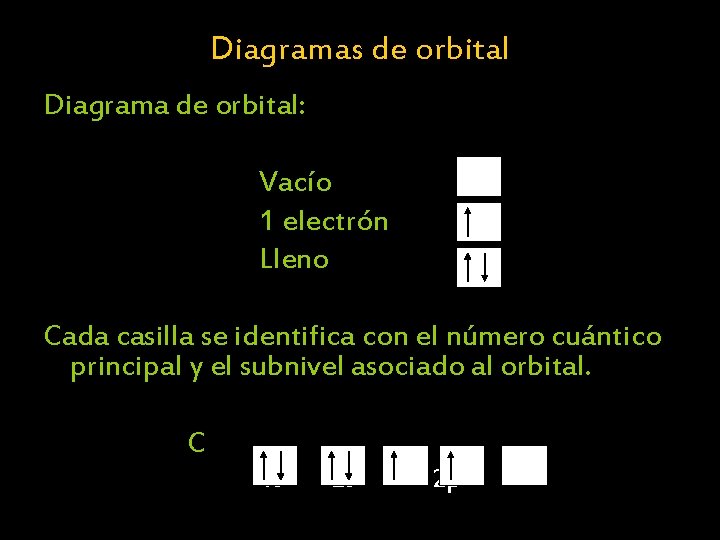
Diagramas de orbital Diagrama de orbital: Vacío 1 electrón Lleno Cada casilla se identifica con el número cuántico principal y el subnivel asociado al orbital. C 1 s 2 s 2 p

Configuración electrónica Señala el nivel principal, el subnivel asociado a cada orbital y el número de electrones de cada orbital como un superíndice. C 1 s 22 p 2
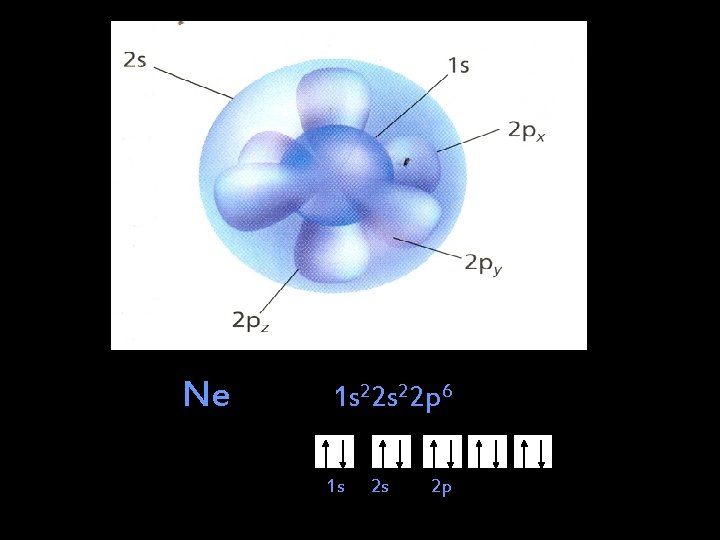
Ne 1 s 22 p 6 1 s 2 s 2 p
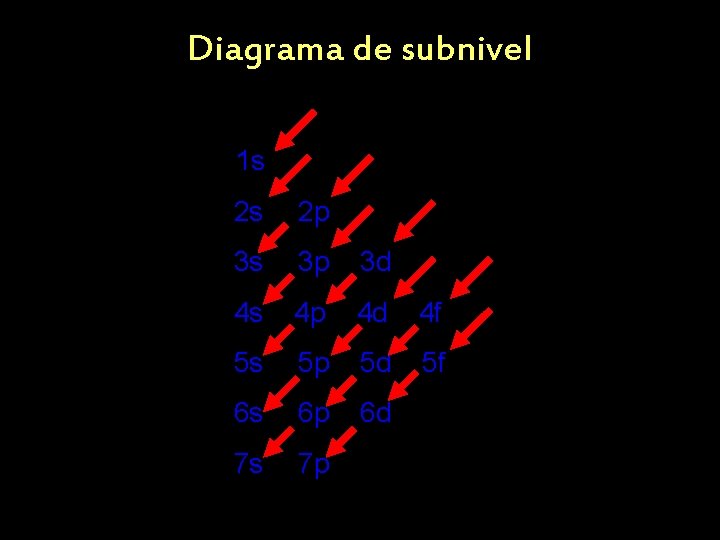
Diagrama de subnivel 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 5 s 5 p 5 d 5 f 6 s 6 p 6 d 7 s 7 p
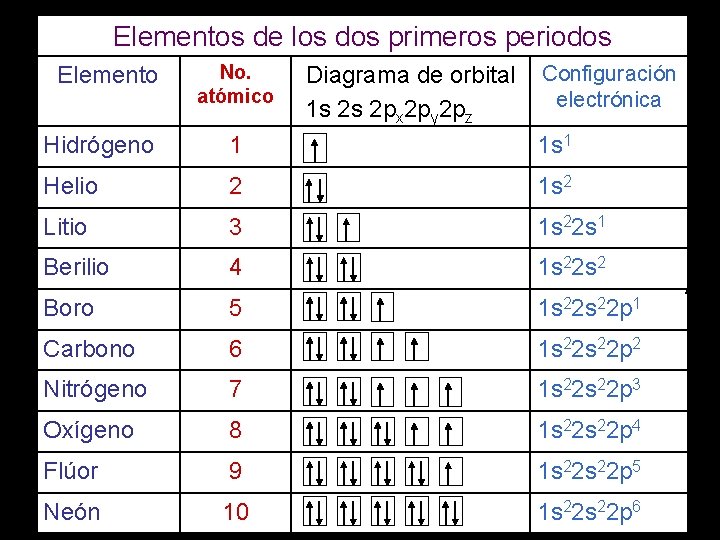
Elementos de los dos primeros periodos Elemento No. atómico Diagrama de orbital 1 s 2 s 2 px 2 py 2 pz Configuración electrónica Hidrógeno 1 1 s 1 Helio 2 1 s 2 Litio 3 1 s 22 s 1 Berilio 4 1 s 22 s 2 Boro 5 1 s 22 p 1 Carbono 6 1 s 22 p 2 Nitrógeno 7 1 s 22 p 3 Oxígeno 8 1 s 22 p 4 Flúor 9 1 s 22 p 5 Neón 10 1 s 22 p 6

Notación del núcleo de gas noble Es un método para abreviar configuraciones electrónicas. Se usa entre paréntesis la configuración electrónica del gas noble del periodo anterior al elemento representado y se completa con el nivel de energía que éste llena. Na 1 s 22 p 63 s 1 1 s 2 s 2 p 3 s Ne 1 s 22 p 6 1 s 2 s Na [Ne]3 s 1 2 p

Ejercicios Escribe las configuraciones del estado raso para los siguientes elementos utilizando el diagrama orbital, la configuración electrónica completa y la configuración electrónica utilizando la notación del núcleo de gases nobles: BROMO ESTRONCIO ANTIMONIO TITANIO AZUFRE CLORO CROMO COBRE
![Excepciones a las configuraciones Cromo [Ar] 4 s 13 d 4 Cobre [Ar] 4 Excepciones a las configuraciones Cromo [Ar] 4 s 13 d 4 Cobre [Ar] 4](http://slidetodoc.com/presentation_image_h/22cc872fa81fa341ba55ca8b9e57939d/image-22.jpg)
Excepciones a las configuraciones Cromo [Ar] 4 s 13 d 4 Cobre [Ar] 4 s 13 d 10

Electrones de valencia Son aquellos situados en los orbitales atómicos más externos del átomo, generalmente asociados al nivel principal de energía más alto del átomo. S [Ne]3 s 23 p 4 6 electrones de valencia Cs [Xe]6 s 1 1 electrón de valencia

Estructuras de símbolos electrónicos (estructuras de Lewis) Es una forma de representación de los electrones de valencia de los átomos que fue diseñada por un químico catedrático estadounidense llamado G. N. Lewis. Símbolo = representa el núcleo atómico y los electrones de niveles internos Puntos= representan los electrones de valencia
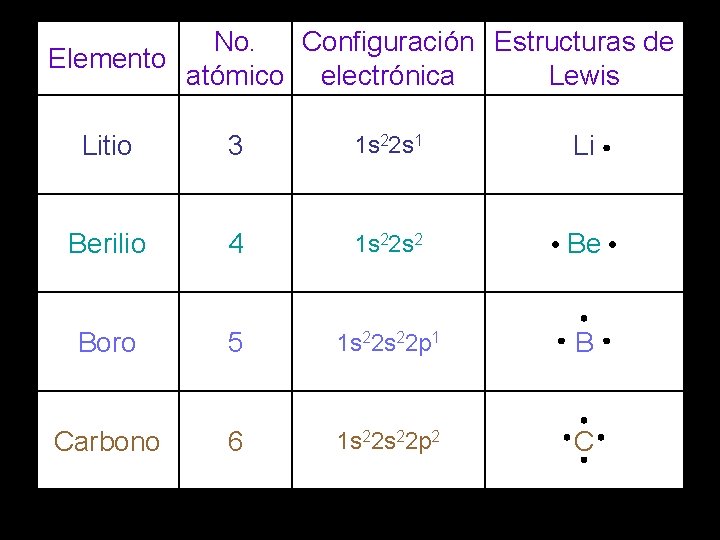
No. Configuración Estructuras de Elemento atómico electrónica Lewis Litio 3 1 s 22 s 1 Li Berilio 4 1 s 22 s 2 Be Boro 5 1 s 22 p 1 B Carbono 6 1 s 22 p 2 C
- Slides: 25