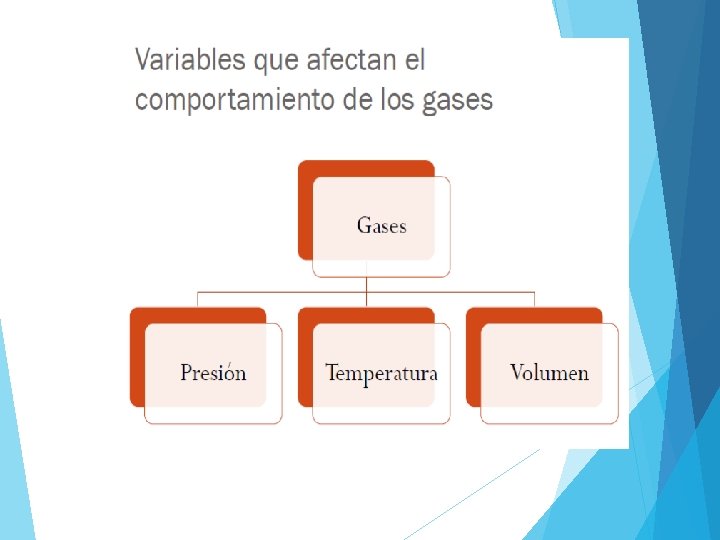
Los gases y comportamiento su Objetivos Comprender el

Los gases y comportamiento su Objetivos: Comprender el comportamiento y las propiedades de los gases. Convertir escalas termométricas Conocer las leyes de los gases ideales.

Gas: Estado de la materia en que las sustancias no tienen cuerpo ni volumen propio.

Cinética molecular de los gases. Los gases están formados por partículas. Entre las partículas, la fuerza de atracción son mínimas, y se encuentran en constante movimiento. Ocupan todo el volumen disponible. El aumento de la temperatura, aumenta la velocidad de las partículas.

Propiedades de los gases. 1. - Fluidez: ocupan todo el espacio disponible… ¿por qué? Porque prácticamente no poseen fuerzas de unión entre sus moléculas. 2. - Difusión: un gas se mezcla con otro debido al movimiento de las moléculas. ¿alguien puede dar un ejemplo de esto?
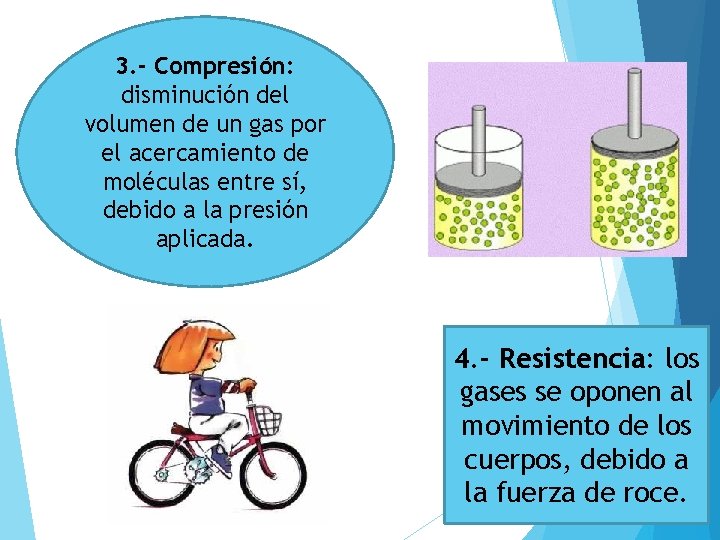
3. - Compresión: disminución del volumen de un gas por el acercamiento de moléculas entre sí, debido a la presión aplicada. 4. - Resistencia: los gases se oponen al movimiento de los cuerpos, debido a la fuerza de roce.
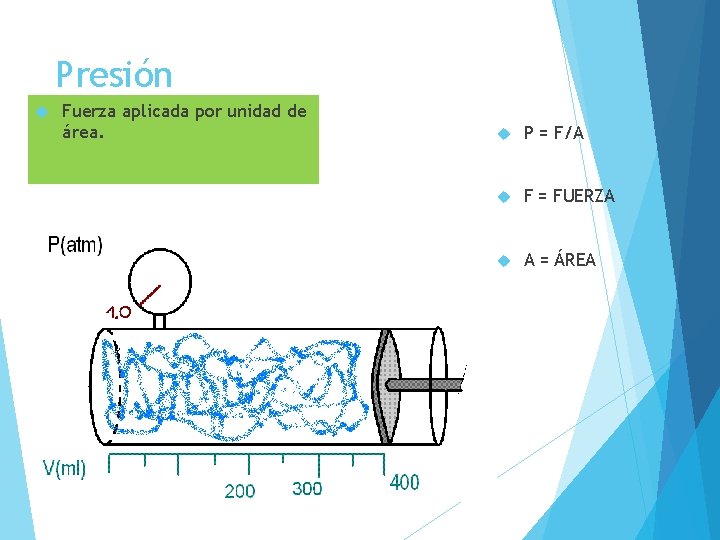
Presión Fuerza aplicada por unidad de área. P = F/A F = FUERZA A = ÁREA


Presión atmosférica. Es la presión que ejerce el aire sobre la Tierra. Se ejerce en todas las direcciones. Según lo que podemos observar en la imagen, Carolina… ¿dónde es mayor la presión atmosférica?

Diferencias de calor y temperatura. TEMPERATURA CALOR • Energía producida por la vibración acelerada de las partículas, que se manifiesta elevando la temperatura. • Medida del grado de calor, o sea del movimiento de las partículas.



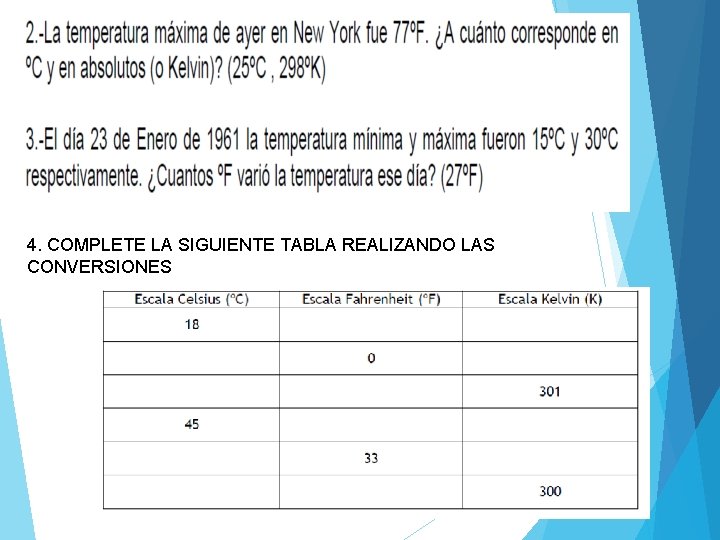
4. COMPLETE LA SIGUIENTE TABLA REALIZANDO LAS CONVERSIONES

LEYES DE LOS GASES
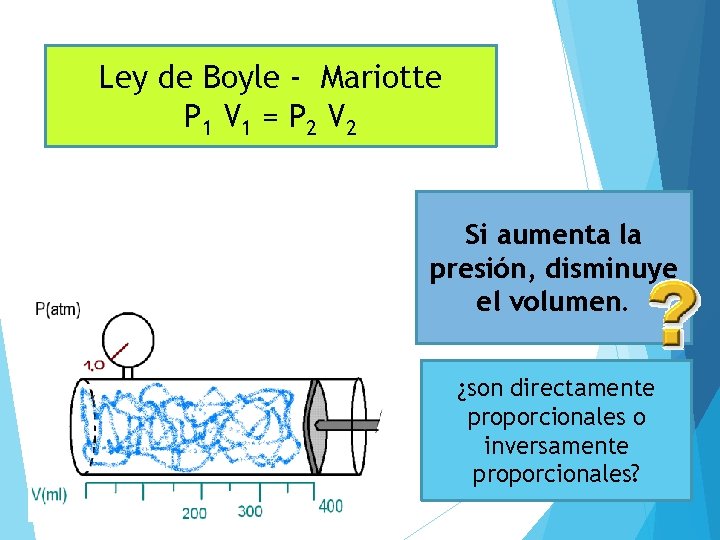
Ley de Boyle - Mariotte P 1 V 1 = P 2 V 2 Si aumenta la presión, disminuye el volumen. ¿son directamente proporcionales o inversamente proporcionales?

LEY DE BOYLE – MARIOTTE A temperatura constante, el volumen de un gas es inversamente proporcional con la presión que soporta - Transformación Isotérmica: temperatura constante. Varía presión y volumen
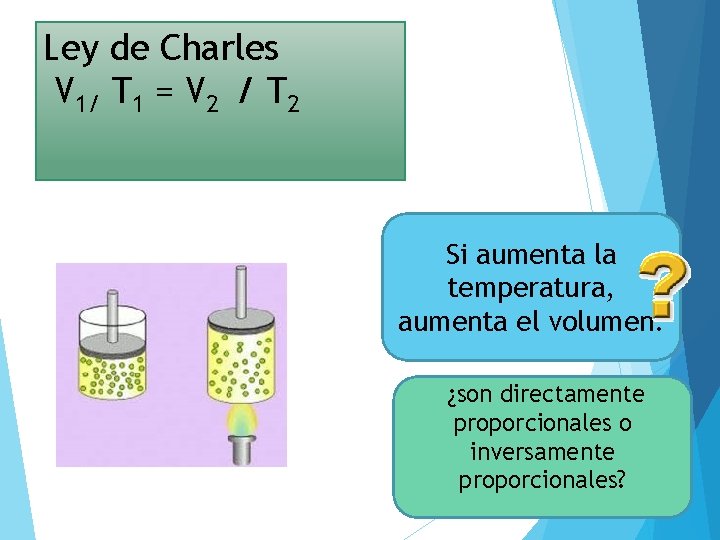
Ley de Charles V 1/ T 1 = V 2 / T 2 Si aumenta la temperatura, aumenta el volumen. ¿son directamente proporcionales o inversamente proporcionales?

LEY DE CHARLES A presión constante, el volumen de un gas aumenta proporcionalmente con el incremento de temperatura - Transformación Isobárica: presión constante. Varía volumen y temperatura Volumen (m. L) Temperatura (K) V 1 T 1 = V 2 T 2
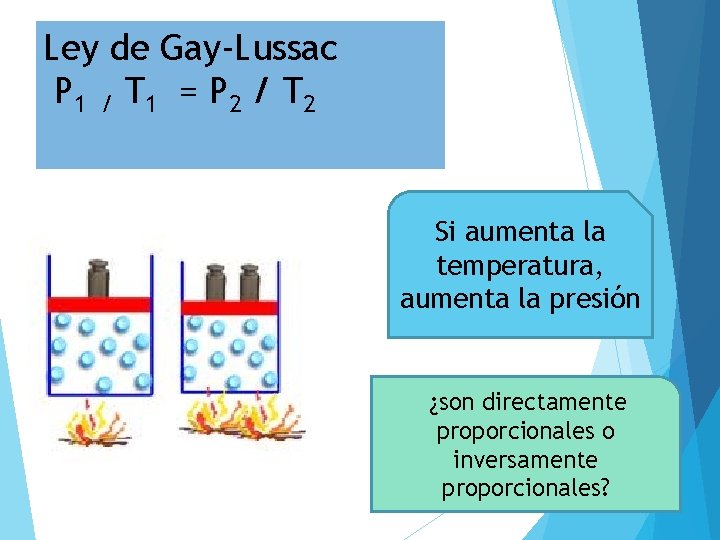
Ley de Gay-Lussac P 1 / T 1 = P 2 / T 2 Si aumenta la temperatura, aumenta la presión ¿son directamente proporcionales o inversamente proporcionales?

LEY DE GAY-LUSSAC A volumen constante, la presión de un gas aumenta proporcionalmente con el incremento de temperatura - Transformación Isocórica: volumen constante. Varía presión y temperatura 750 K 1028 K P 1 T 1 = P 2 T 2

LEY COMBINADA DE LOS GASES P 1 · V 1 = P 2 · V 2 T 1 T 2
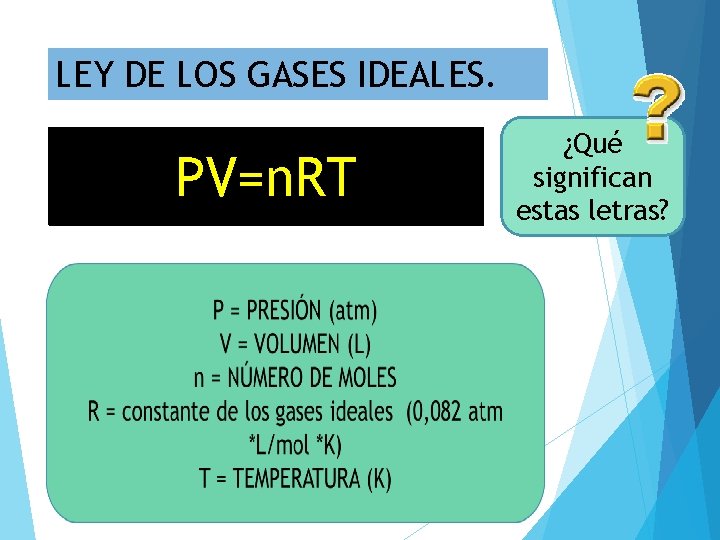
LEY DE LOS GASES IDEALES. PV=n. RT ¿Qué significan estas letras?

LEY DE AVOGADRO El volumen de un gas aumenta proporcionalmente con el incremento del número de moles CONDICIONES NORMALES DE PRESIÓN Y TEMPERATURA (CNPT) § Presión : 1 atm (760 mm. Hg) § Temperatura : 273 K (0°C)
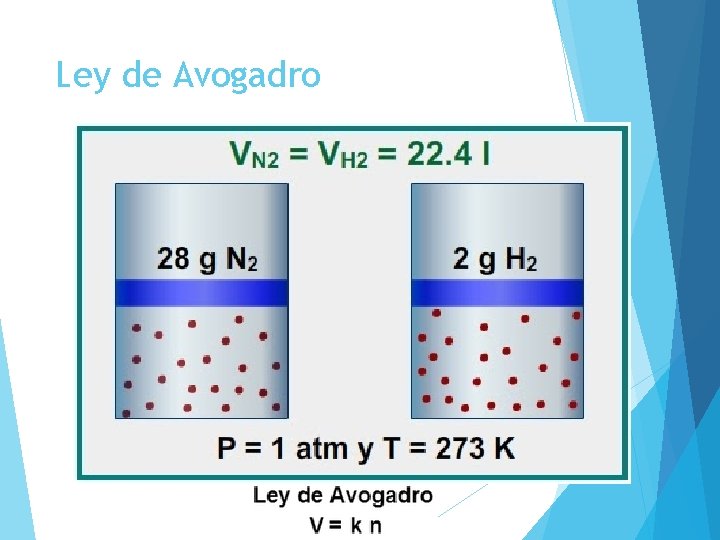
Ley de Avogadro

CONCEPTOS ESTEQUIOMÉTRICOS VOLUMEN MOLAR: 22, 4 L Volumen que ocupa un mol de cualquier gas en C. N. P. T. : Condiciones Normales de Presión y Temperatura Presión : 1 atm (760 mm. Hg) Temperatura : 273 K (0°C) He 22, 4 L 1 mol 1 atm 273 K O 2 22, 4 L 1 mol 1 atm 273 K CO 2 22, 4 L 1 mol 1 atm 273 K

EJERCICIO Calcula la cantidad de mol de un gas ideal, si: P = 2 (atm), V = 1 (L) y T= 20 (K). Calcula la presión de un gas ideal si: V= 5 (L), n = 10 mol, T = 10 (K).
- Slides: 27