Los compuestos que contienen al grupo carboxilo son

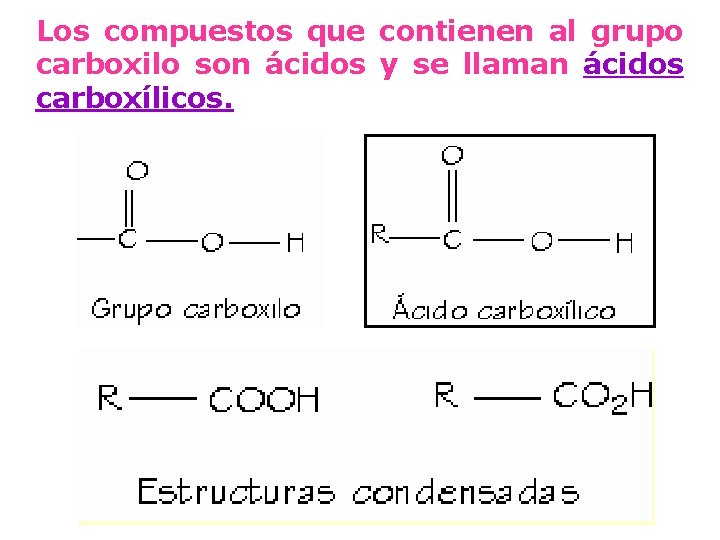
Los compuestos que contienen al grupo carboxilo son ácidos y se llaman ácidos carboxílicos.
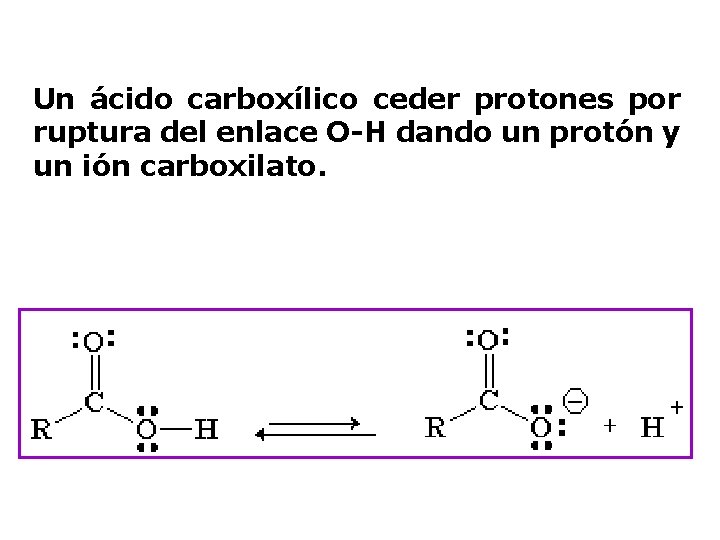
Un ácido carboxílico ceder protones por ruptura del enlace O-H dando un protón y un ión carboxilato.

Los ácidos carboxílicos presentan reacciones de sustitución en las que se sustituye el grupo –OH, produciendose un derivado de ácido. Algunos derivados son los siguientes grupos: ester, amida, cloruro de ácido.
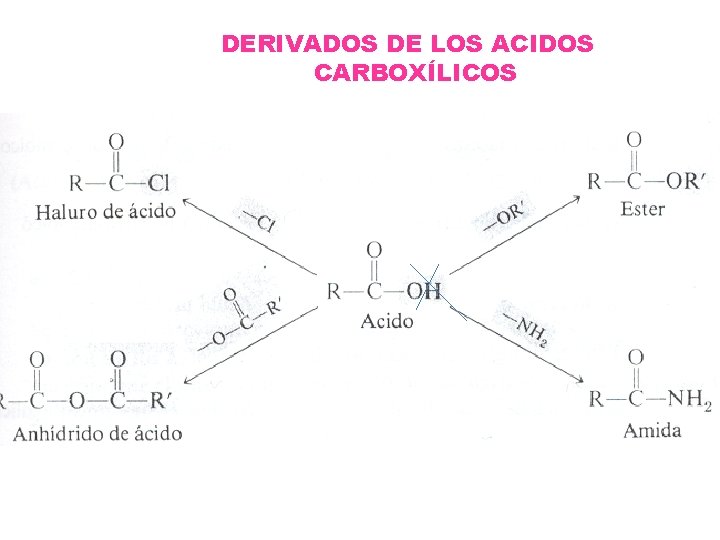
DERIVADOS DE LOS ACIDOS CARBOXÍLICOS

CLASIFICACIÓN DE ACIDOS CARBOXÍLICOS: 1. Por tipo de radical • Aromaticos • Alifáticos (R- o Ar-) 2. Por número de grupos carboxílicos: • Monocarboxílicos • Dicarboxílicos • Tricarboxílicos.
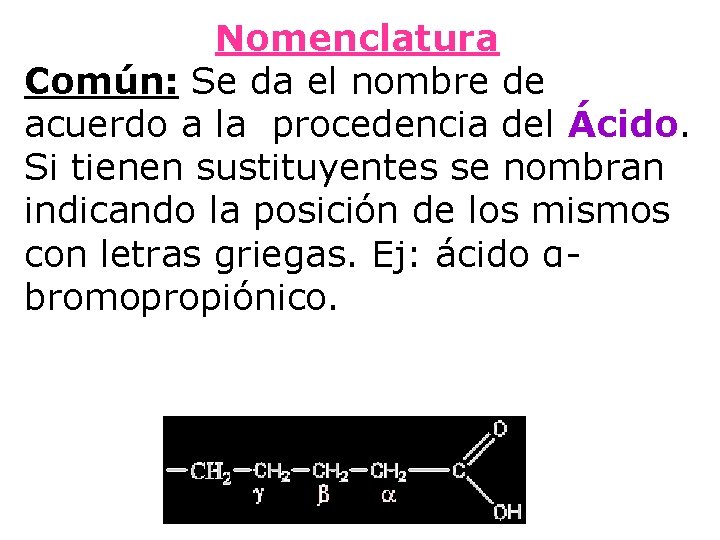
Nomenclatura Común: Se da el nombre de acuerdo a la procedencia del Ácido. Si tienen sustituyentes se nombran indicando la posición de los mismos con letras griegas. Ej: ácido αbromopropiónico.
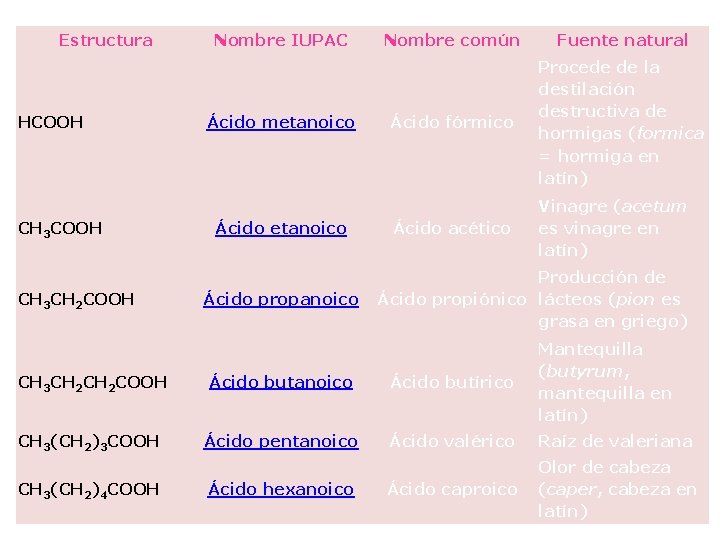
Estructura HCOOH CH 3 CH 2 COOH Nombre IUPAC Ácido metanoico Ácido propanoico Nombre común Fuente natural Ácido fórmico Procede de la destilación destructiva de hormigas (formica = hormiga en latín) Ácido acético Vinagre (acetum es vinagre en latín) Producción de Ácido propiónico lácteos (pion es grasa en griego) CH 3 CH 2 COOH Ácido butanoico Ácido butírico Mantequilla (butyrum, mantequilla en latín) CH 3(CH 2)3 COOH Ácido pentanoico Ácido valérico Raíz de valeriana Ácido caproico Olor de cabeza (caper, cabeza en latín) CH 3(CH 2)4 COOH Ácido hexanoico

UIQPA: Se inicia con la palabra ACIDO seguida por el nombre del alcano básico sustituyendo la “O” por el sufijo “OICO” CH 3 COOH Acido etanoico

A. Carboxílicos sustituídos: 1. Se numera la cadena más larga que contenga al grupo COOH. El carbono No. 1, corresponde al carbono del grupo carboxilo. 2. Se inicia el nombre con la palabra ACIDO.

3. Se nombran sustituyentes en alfabético. los orden 4. Se da el nombre del hidrocarburo de la cadena principal con la terminación OICO.
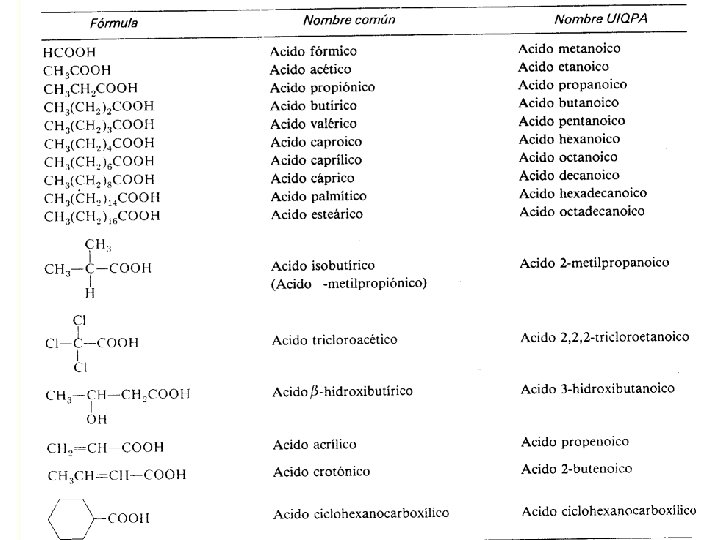

ACIDOS DICARBOXÍLICOS Se pueden encontrar moléculas con más de un grupo carboxilo. La presencia de dos grupos carboxilo unidos a una cadena o a un anillo carbonado, clasifica a la molécula como un ácido dicarboxílico. Se les puede nombrar por las dos nomenclaturas.

Algunos ácidos dicarboxílicos y sus derivados son importantes en el metabolismo celular. El ácido oxálico (COMUN) es el primero de la serie, está formado por dos grupos carboxílicos unidos entre sí. En la nomenclatura UIQPA, se da el nombre del alcano precursor y se agrega la terminación dioico antecedido por la palabra ácido.
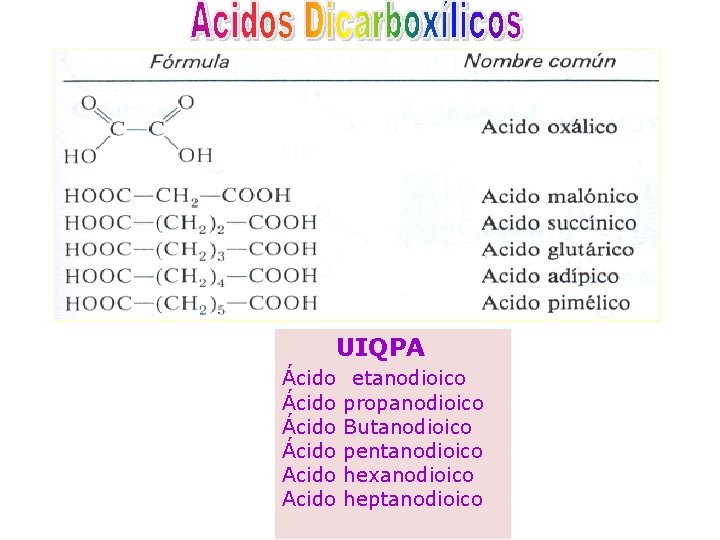
UIQPA Ácido Acido etanodioico propanodioico Butanodioico pentanodioico hexanodioico heptanodioico
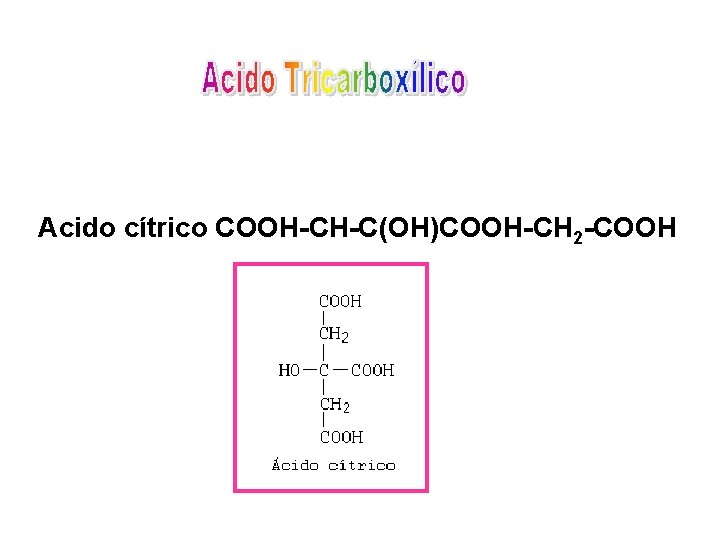
Acido cítrico COOH-CH-C(OH)COOH-CH 2 -COOH

Se conocen comunes. por sus nombres También se les nombra como derivados del ácido básico (ácido benzoico). Cuando el grupo arilo no está enlazado directamente al grupo carboxilo, el aromático se menciona como sustituyente.
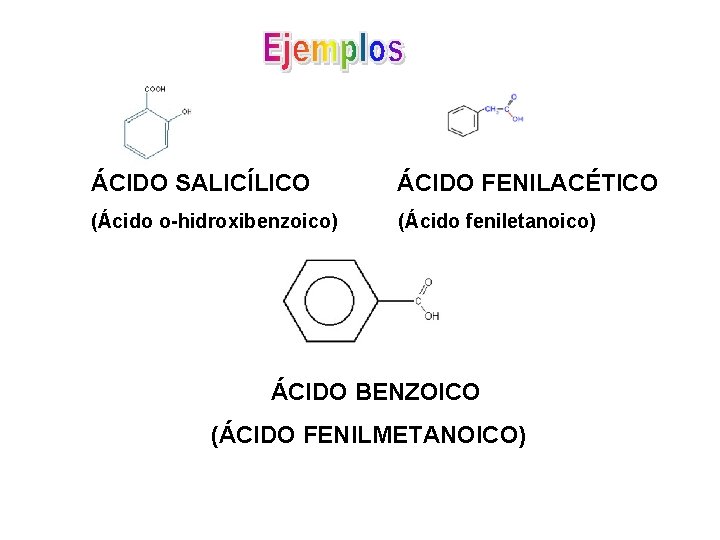
ÁCIDO SALICÍLICO ÁCIDO FENILACÉTICO (Ácido o-hidroxibenzoico) (Ácido feniletanoico) ÁCIDO BENZOICO (ÁCIDO FENILMETANOICO)

PROPIEDADES FÍSICAS Los menores de 10 átomos de Carbono son líquidos, incoloros y de olor muy desagradable. Los mayores de 10 átomos de Carbono son sólidos, cerosos e inodoros. Los de bajo peso molecular (hasta 3 C) son solubles en agua, y disminuye su solubilidad conforme aumenta su peso. Todos son solubles en solventes orgánicos.
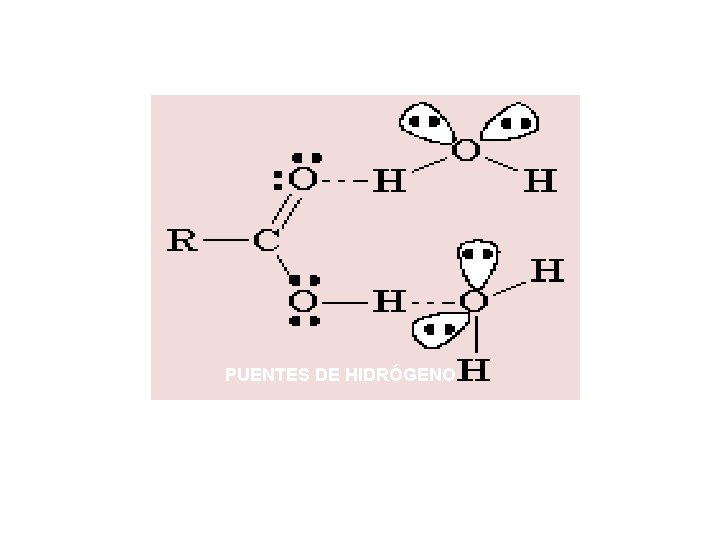
PUENTES DE HIDRÓGENO

Puntos de ebullición: Los ácidos carboxílicos hierven a temperaturas superiores que los alcoholes, cetonas o aldehídos de pesos moleculares semejantes. Además forman puentes de hidrógeno.
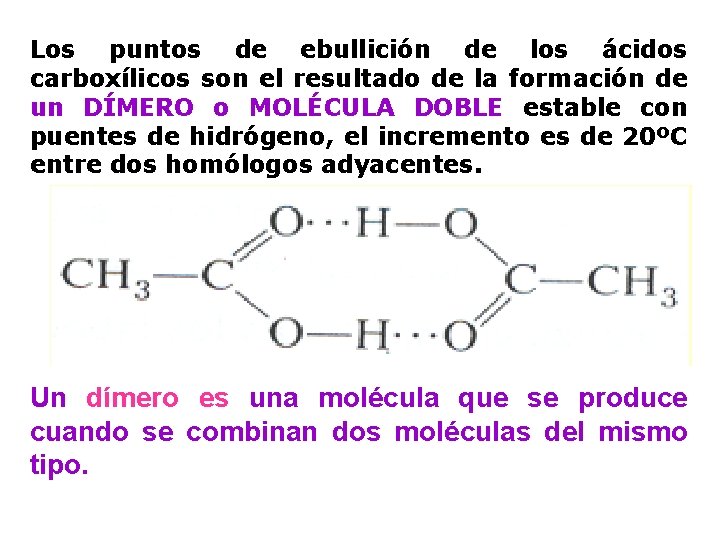
Los puntos de ebullición de los ácidos carboxílicos son el resultado de la formación de un DÍMERO o MOLÉCULA DOBLE estable con puentes de hidrógeno, el incremento es de 20ºC entre dos homólogos adyacentes. Un dímero es una molécula que se produce cuando se combinan dos moléculas del mismo tipo.

Puntos de fusión: Los ácidos dicarboxílicos tienen puntos de fusión muy altos. Al tener dos grupos carboxilos por molécula , las fuerzas de los puentes de hidrógeno son especialmente fuertes por lo que en estos diácidos se necesita una alta temperatura para romper la red de puentes de hidrógeno en el cristal y fundir el diácido.

Propiedades Químicas Las sustancias que liberan iones hidrógeno en agua, se clasifican como ácidos. Los ácidos carboxílicos son los más ácidos de los compuestos orgánicos, pero si se comparan con los ácidos inorgánicos, los carboxílicos son ácidos mucho más débiles.
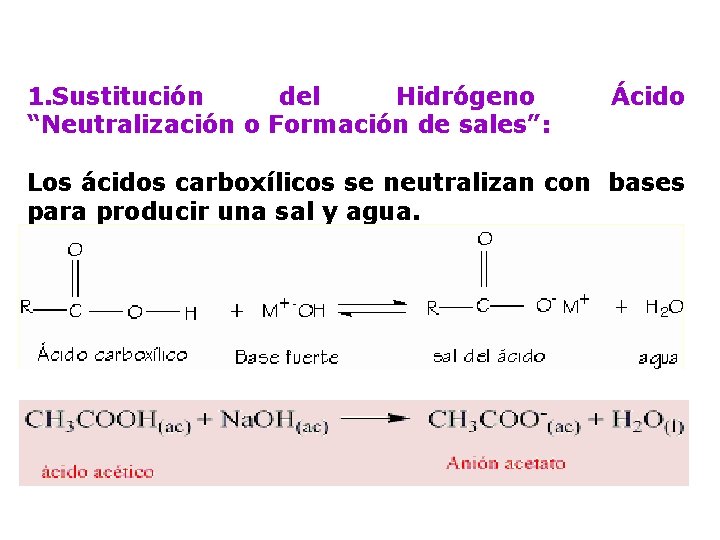
1. Sustitución del Hidrógeno “Neutralización o Formación de sales”: Ácido Los ácidos carboxílicos se neutralizan con bases para producir una sal y agua.
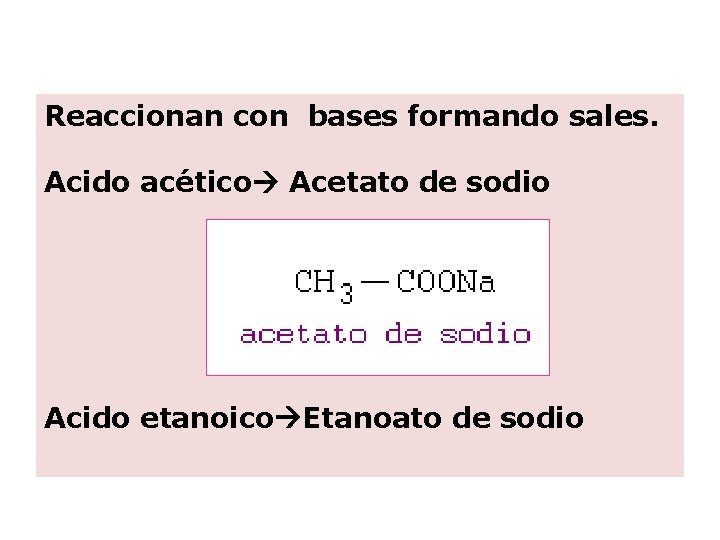
Reaccionan con bases formando sales. Acido acético Acetato de sodio Acido etanoico Etanoato de sodio
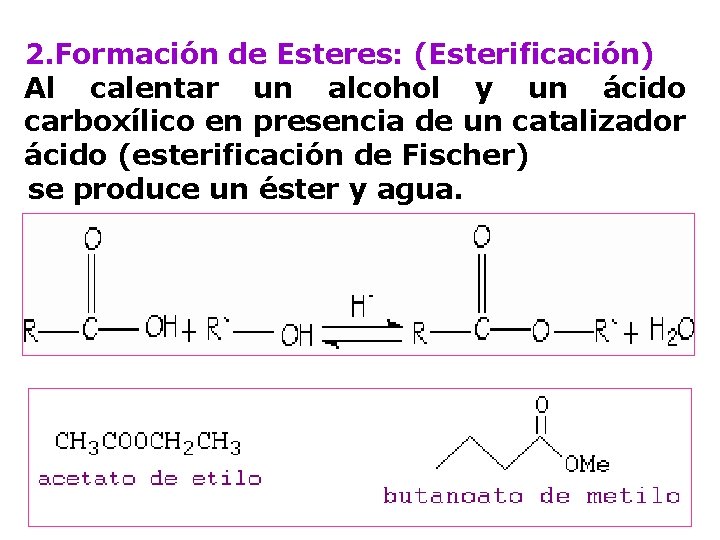
2. Formación de Esteres: (Esterificación) Al calentar un alcohol y un ácido carboxílico en presencia de un catalizador ácido (esterificación de Fischer) se produce un éster y agua.

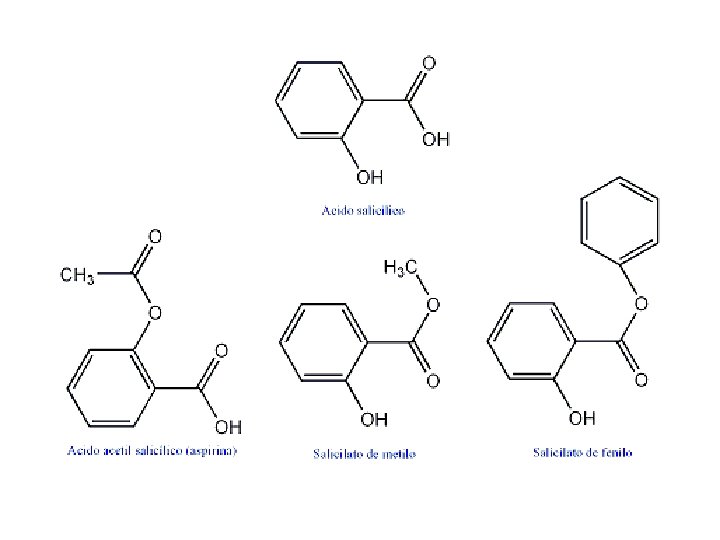
Importancia Los ACIDOS CARBOXÍLICOS contienen el grupo carboxilo que es uno de los grupos más importantes en química y bioquímica, ya que permite la síntesis de otros compuestos. Los ácidos son compuestos que confieren olor y sabor a muchos productos. Algunos de los derivados tienen importancia como analgésicos como el ácido salicílico y el ácido acetilsalicílico.
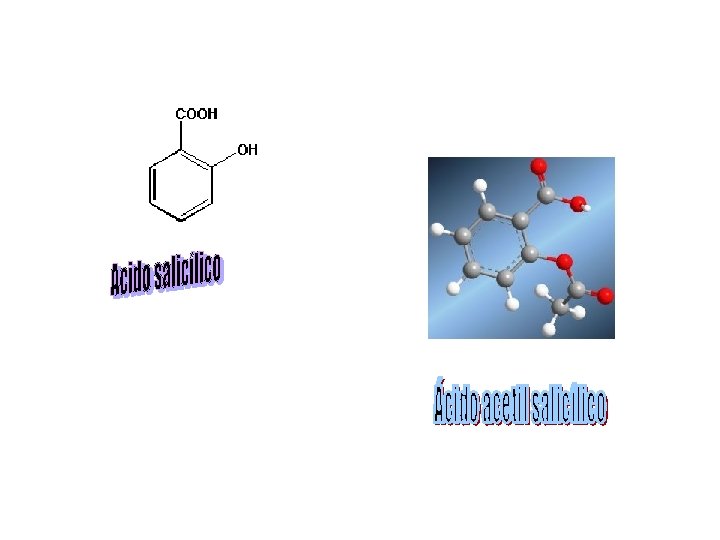
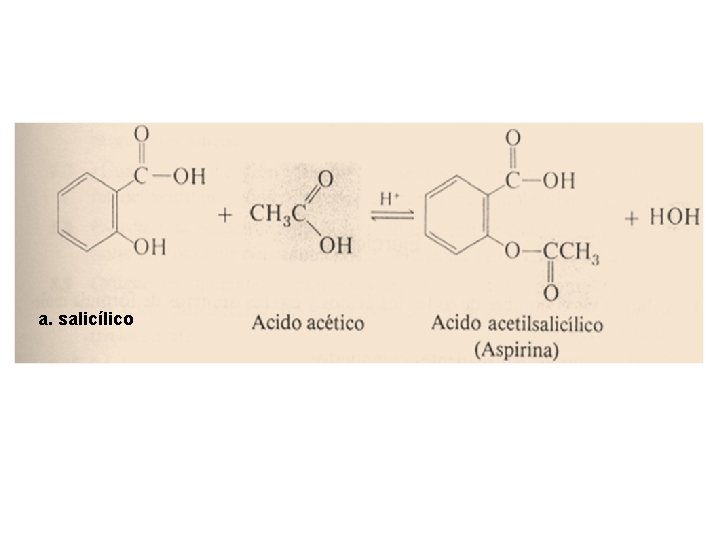
a. salicílico

ÉSTERES Los ésteres son los derivados más importantes de los ácidos carboxílicos. Están ampliamente distribuidos en la naturaleza, las grasas y aceites vegetales son ésteres de ácidos grasos de cadena larga y glicerol. Contienen en su molécula un grupo carbonilo unido a un grupo –OR.

Su fórmula general es: RCOOR’ donde R puede ser un hidrógeno, un grupo alquilo o arilo y R’ puede ser arilo o alquilo pero NO hidrógeno. Los ésteres están compuestos de dos partes: el ácido y el alcohol que les dió orígen.

NOMENCLATURA Común: Se escribe el nombre común de la porción ácida, sustituyendo “ico” por “ato. ”. Después la preposición de y luego la porción alquílica o arílica, UIQPA: Primero se nombra la porción ácida, sustituyendo “ico” por “ato”, inmediatamente la porción alquílica o arílica antecedida por la preposición de.
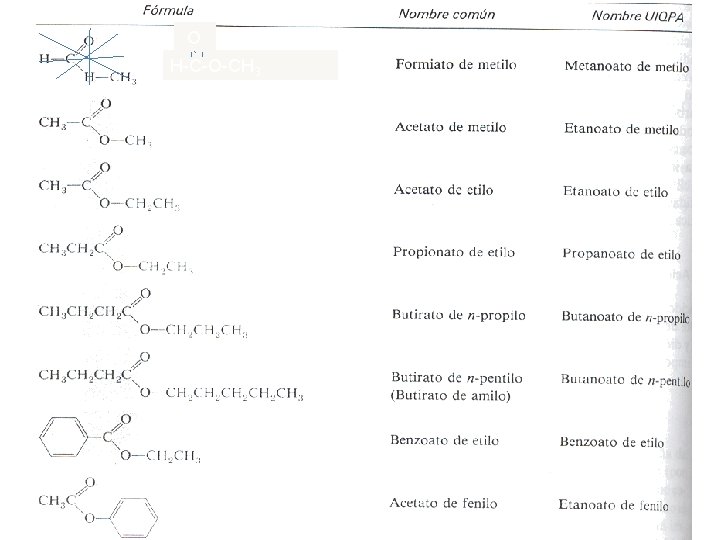
O H-C-O-CH 3
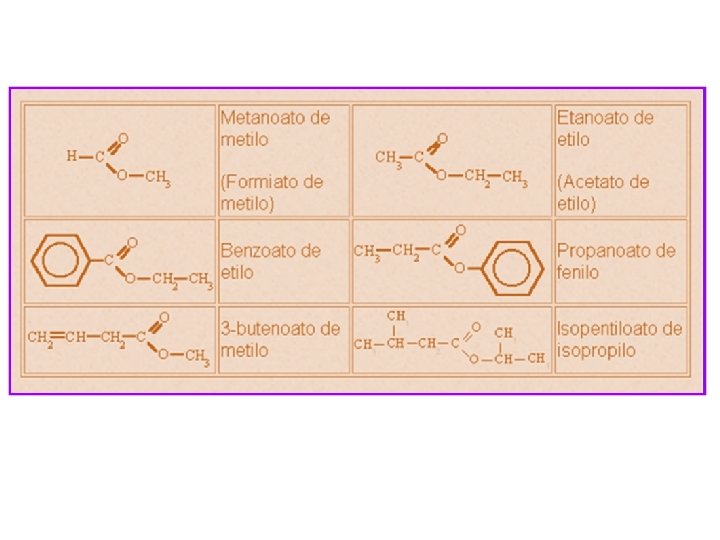

PROPIEDADES FÍSICAS Poseen olores agradables, los aromas de muchas flores y frutos se deben a presencia de ésteres. Se emplean en la fabricación de perfumes y como agentes saborizantes en las industrias de confitería y bebidas no alcohólicas. Son líquidos incoloros, insolubles y menos densos que el agua, no forman enlaces de hidrógeno.
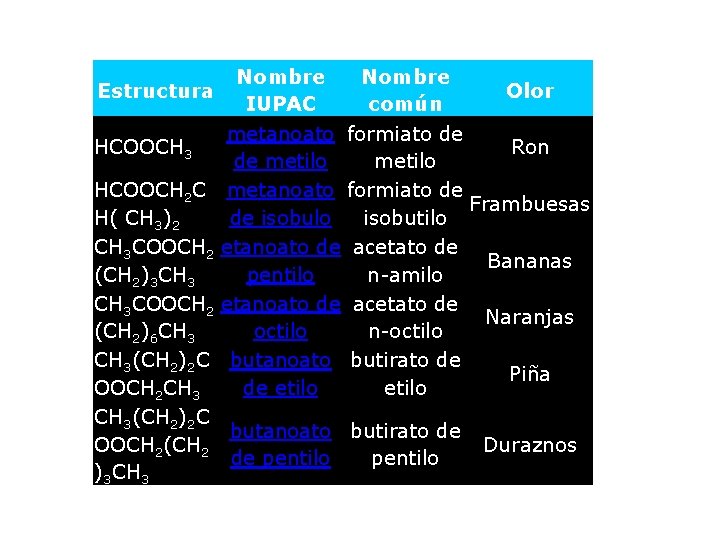
Estructura HCOOCH 3 Nombre IUPAC metanoato de metilo metanoato de isobulo etanoato de pentilo etanoato de octilo butanoato de etilo Nombre Olor común formiato de Ron metilo formiato de Frambuesas isobutilo acetato de Bananas n-amilo acetato de Naranjas n-octilo butirato de Piña etilo HCOOCH 2 C H( CH 3)2 CH 3 COOCH 2 (CH 2)3 CH 3 COOCH 2 (CH 2)6 CH 3(CH 2)2 C OOCH 2 CH 3(CH 2)2 C butanoato butirato de OOCH 2(CH 2 de pentilo )3 CH 3 Duraznos


AMIDAS Las amidas son derivados de los ácidos carboxílicos, contienen un átomo de nitrógeno unido a un grupo carbonilo. La fórmula general de una amida es: RCONH 2
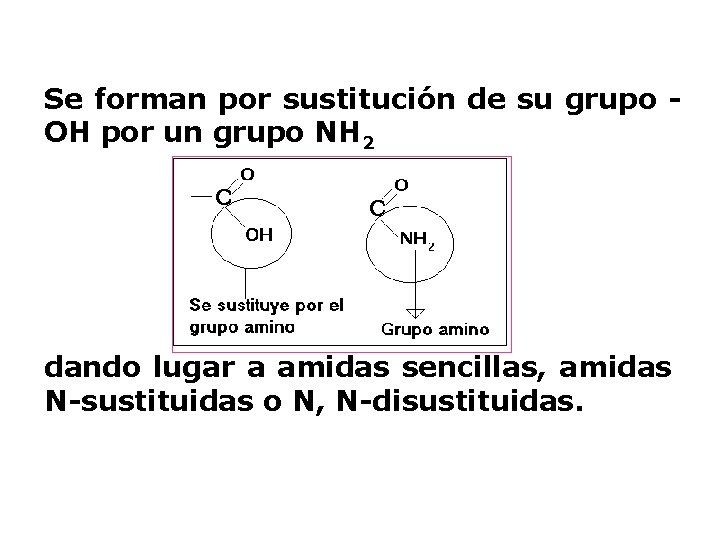
Se forman por sustitución de su grupo OH por un grupo NH 2 dando lugar a amidas sencillas, amidas N-sustituidas o N, N-disustituidas.
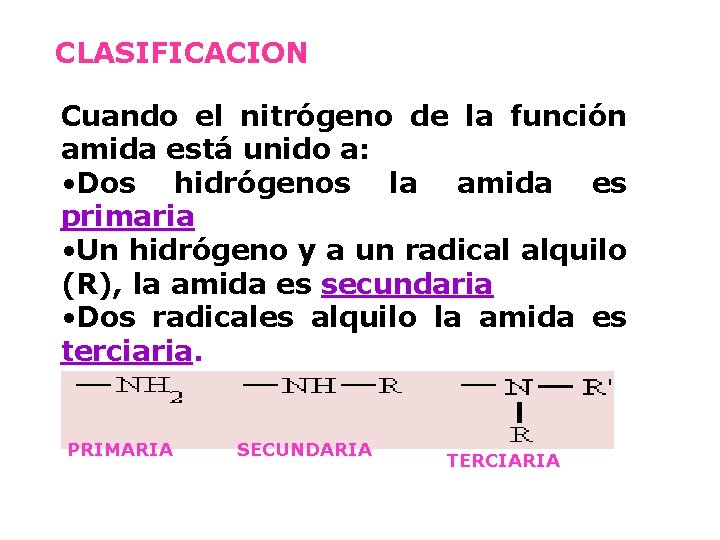
CLASIFICACION Cuando el nitrógeno de la función amida está unido a: • Dos hidrógenos la amida es primaria • Un hidrógeno y a un radical alquilo (R), la amida es secundaria • Dos radicales alquilo la amida es terciaria PRIMARIA SECUNDARIA TERCIARIA
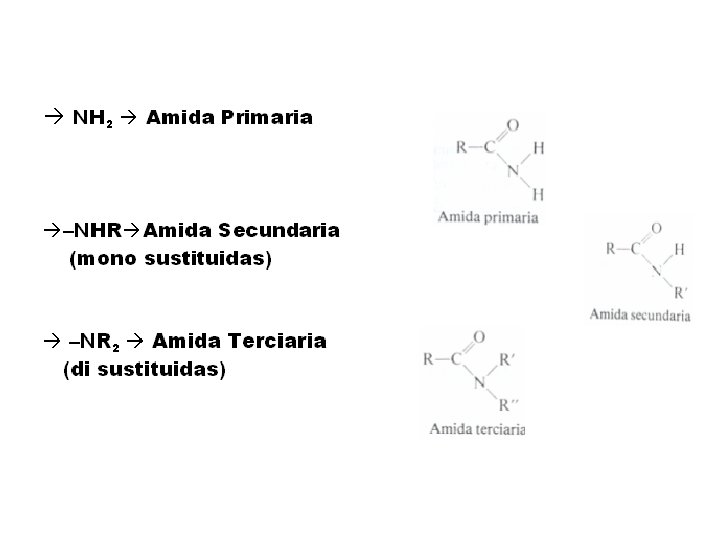

NOMENCLATURA Común: Se nombran como el ácido del que provienen y la terminación “ico” se reemplaza por el sufijo o terminación – amida. Si se trata de amidas sustituidas hay que especificar los radicales unidos al nitrógeno anteponiendo la letra N.
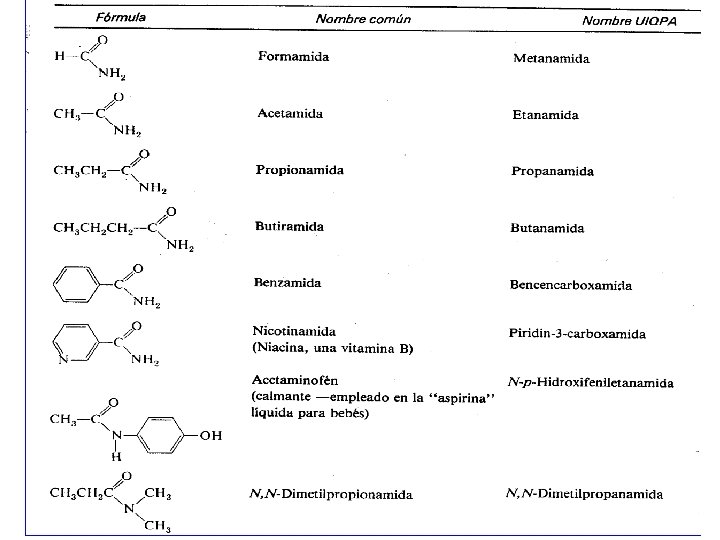

UIQPA: Se les da el nombre UIQPA del ácido del que provienen reemplazando la terminación “oico” por el sufijo o terminación –amida. Si se trata de amidas sustituidas hay que especificar los radicales unidos al nitrógeno anteponiendo la letra N.

El enlace C-N se denomina enlace amida Este enlace es muy estable y se encuentra en las unidades repetitivas del nylon y otros polímeros industriales y principalmente en las proteínas donde también se denomina enlace peptídico NYLON
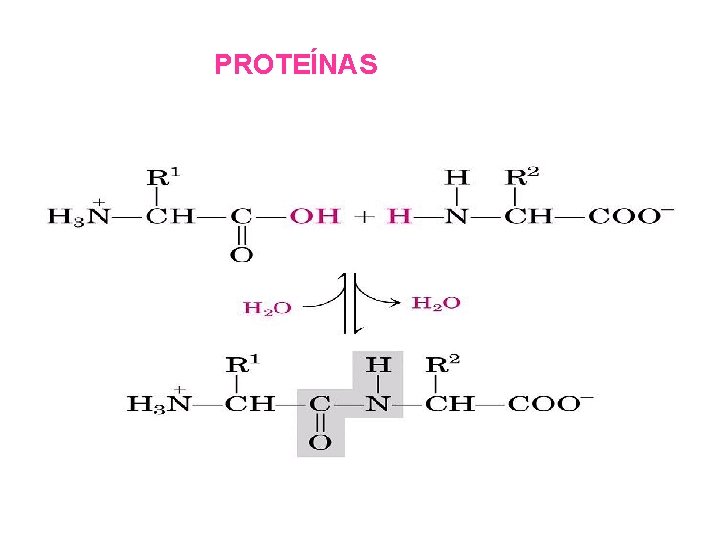
PROTEÍNAS
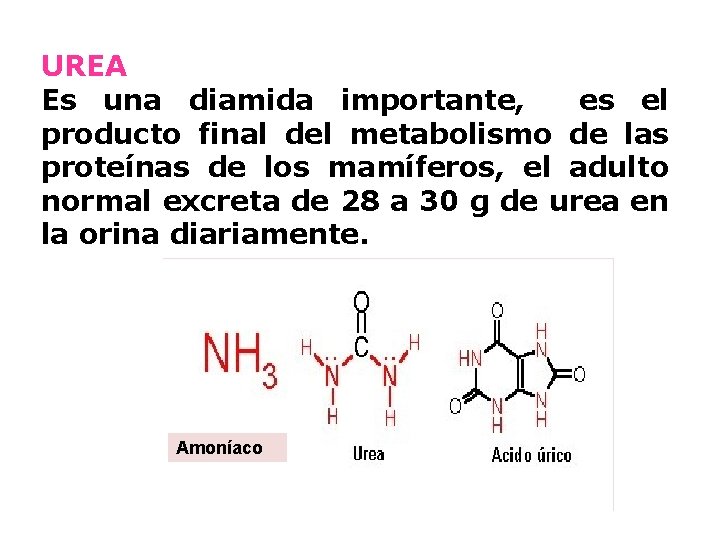
UREA Es una diamida importante, es el producto final del metabolismo de las proteínas de los mamíferos, el adulto normal excreta de 28 a 30 g de urea en la orina diariamente. Amoníaco

PROPIEDADES FÍSICAS • Todas las amidas primarias son excepción de la formamida. sólidas, a • Son incoloras e inodoras. • Las amidas inferiores son solubles en agua (formamida butiramida) y alcohol. • Son moléculas neutras. • Poseen puntos de fusión y ebullición anormalmente altos (debido a la naturaleza polar del grupo amida y formación de puentes de H).

- Slides: 51