Los compuestos que contienen al grupo carboxilo son

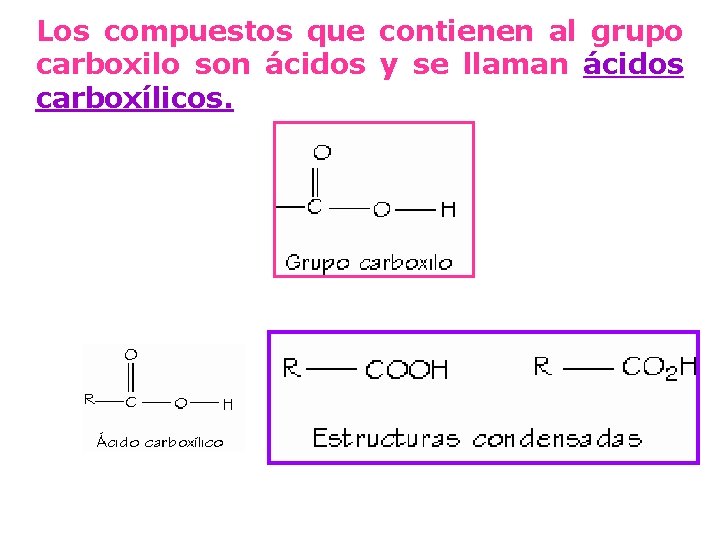
Los compuestos que contienen al grupo carboxilo son ácidos y se llaman ácidos carboxílicos.

Los ácidos carboxílicos presentan reacciones de sustitución en las que se sustituye el grupo –OH, produciéndose un derivado de ácido. Algunos derivados son: ester, amida, cloruro de ácido.
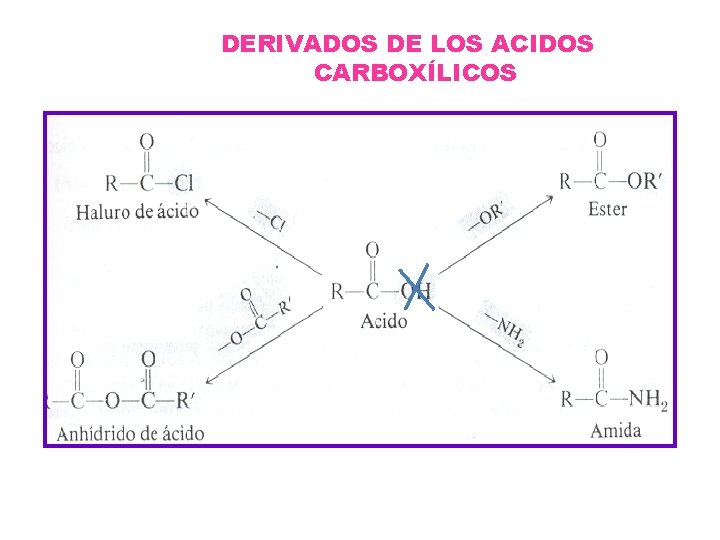
DERIVADOS DE LOS ACIDOS CARBOXÍLICOS

CLASIFICACIÓN DE ACIDOS CARBOXÍLICOS: 1. Por tipo de radical (“R-” , “ Ar-”) • Aromaticos • Alifáticos 2. Por número de grupos carboxílicos: • Monocarboxílicos • Dicarboxílicos • Tricarboxílicos

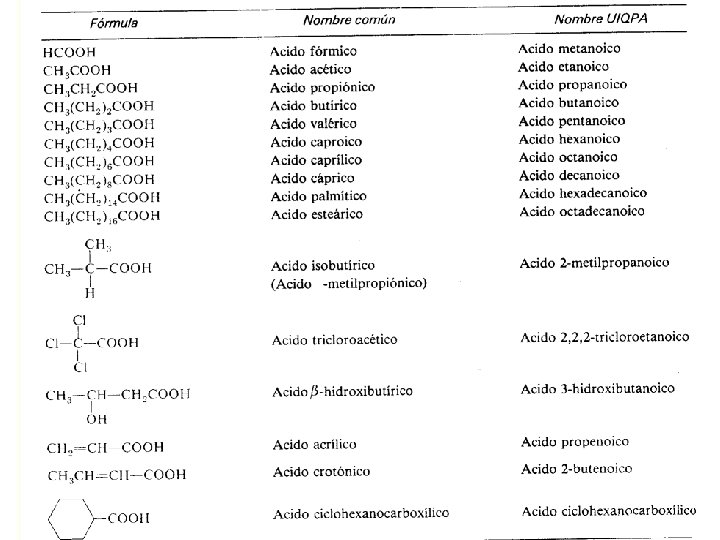
Nomenclatura Común: Para los ácidos de cadena normal se da el nombre de acuerdo a la procedencia del Ácido. Ejemplos: ESTRUCTURA NOMBRE DEL ÁCIDO ORÍGEN DEL NOMBRE HCOOH ÁCIDO FÓRMICA: hormiga en latín. CH 3 COOH ÁCIDO ACÉTICO ACETUM: vinagre en latín.
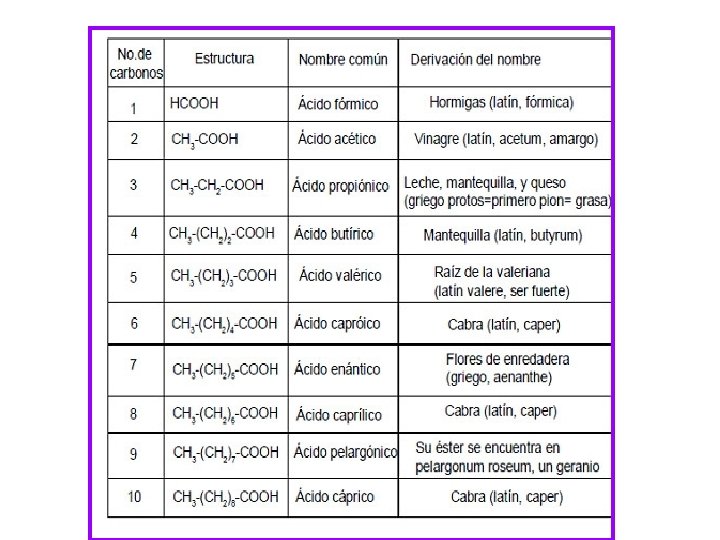
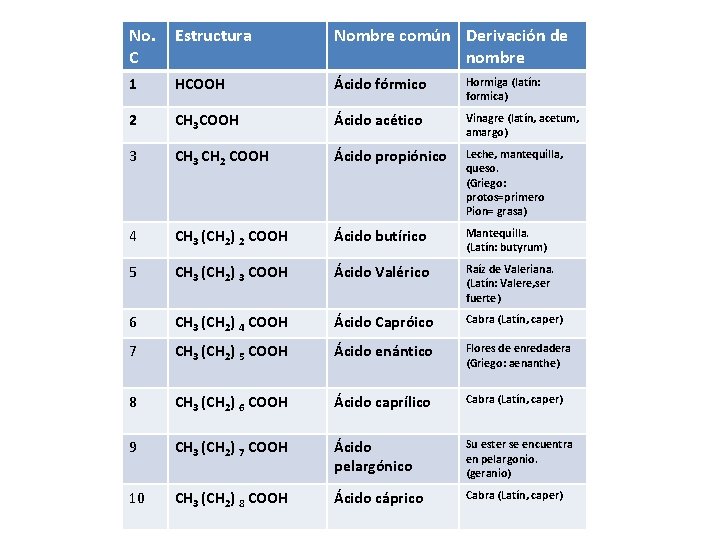
No. C Estructura Nombre común Derivación de nombre 1 HCOOH Ácido fórmico Hormiga (latín: formica) 2 CH 3 COOH Ácido acético Vinagre (latín, acetum, amargo) 3 CH 2 COOH Ácido propiónico Leche, mantequilla, queso. (Griego: protos=primero Pion= grasa) 4 CH 3 (CH 2) 2 COOH Ácido butírico Mantequilla. (Latín: butyrum) 5 CH 3 (CH 2) 3 COOH Ácido Valérico Raíz de Valeriana. (Latín: Valere, ser fuerte) 6 CH 3 (CH 2) 4 COOH Ácido Capróico Cabra (Latín, caper) 7 CH 3 (CH 2) 5 COOH Ácido enántico Flores de enredadera (Griego: aenanthe) 8 CH 3 (CH 2) 6 COOH Ácido caprílico Cabra (Latín, caper) 9 CH 3 (CH 2) 7 COOH Ácido pelargónico Su ester se encuentra en pelargonio. (geranio) 10 CH 3 (CH 2) 8 COOH Ácido cáprico Cabra (Latín, caper)
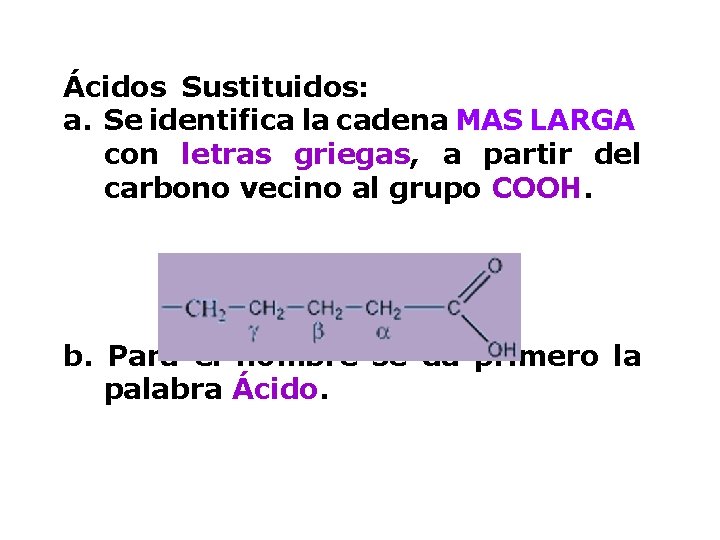
Ácidos Sustituidos: a. Se identifica la cadena MAS LARGA con letras griegas, a partir del carbono vecino al grupo COOH. b. Para el nombre se da primero la palabra Ácido.

3 c. Se indica la posición de los sustituyentes en òrden alfabètico. (Ácido α-etil- β-metil) d. Se agrega inmediatamente el nombre del ácido de acuerdo a su procedencia Ácido α-metil- β-etilbutirico Ácido α- bromopropiónico β α CH 3 CH Br COOH
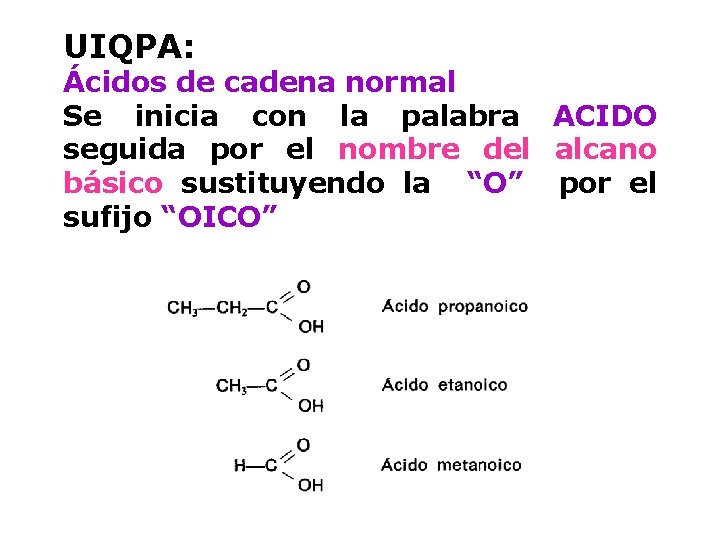
UIQPA: Ácidos de cadena normal Se inicia con la palabra ACIDO seguida por el nombre del alcano básico sustituyendo la “O” por el sufijo “OICO”
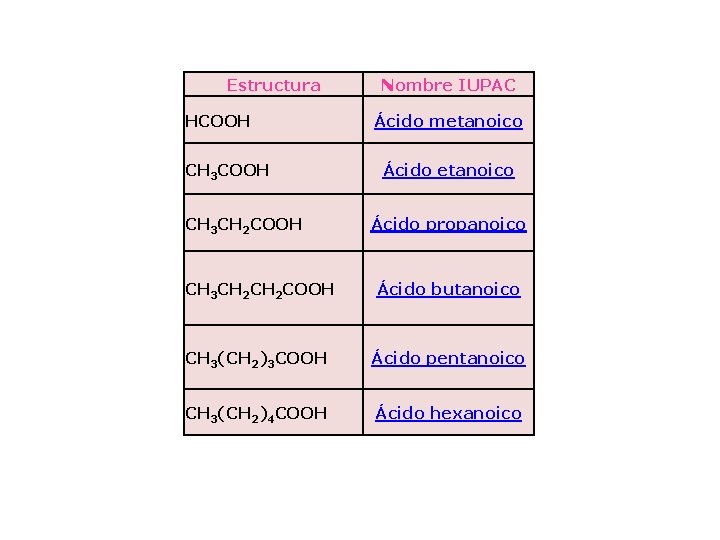
Estructura HCOOH CH 3 CH 2 COOH Nombre IUPAC Ácido metanoico Ácido propanoico CH 3 CH 2 COOH Ácido butanoico CH 3(CH 2)3 COOH Ácido pentanoico CH 3(CH 2)4 COOH Ácido hexanoico

Ácidos Carboxílicos Sustituídos: 1. Se numera la cadena más larga que contenga al grupo COOH. El carbono No. 1, corresponde al carbono del grupo carboxilo. 2. Se inicia el nombre con la palabra ACIDO. 3. Se nombran los sustituyentes en orden alfabético.
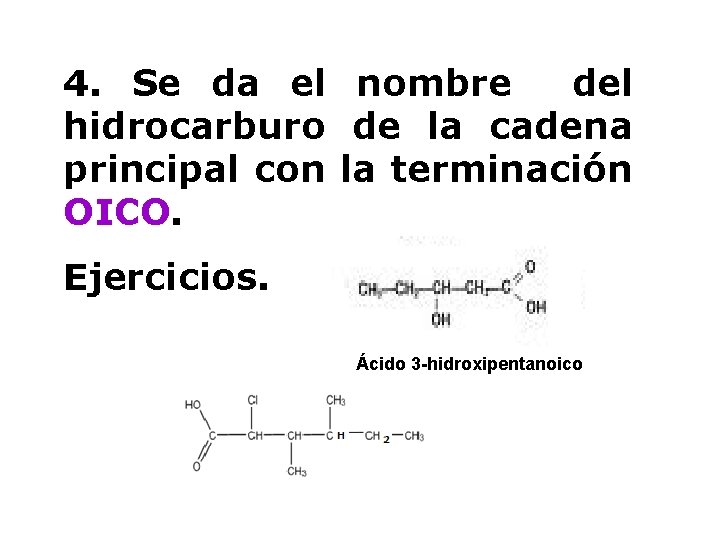
4. Se da el nombre del hidrocarburo de la cadena principal con la terminación OICO. Ejercicios. Ácido 3 -hidroxipentanoico

ACIDOS DICARBOXÍLICOS Se pueden encontrar moléculas con más de un grupo carboxilo. La presencia de dos grupos carboxilo unidos a una cadena o a un anillo carbonado, clasifica a la molécula como un ácido dicarboxílico. Se les puede nombrar por las dos nomenclaturas.

Algunos ácidos dicarboxílicos y sus derivados son importantes en el metabolismo celular. El ácido oxálico (COMUN) es el primero de la serie, está formado por dos grupos carboxílicos unidos entre sí. En la nomenclatura UIQPA, se da el nombre del alcano precursor y se agrega la terminación dioico antecedido por la palabra ácido.
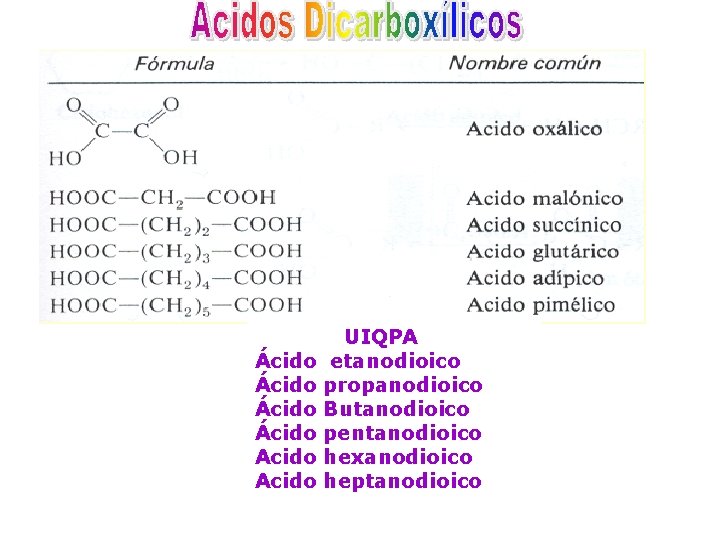
UIQPA Ácido etanodioico Ácido propanodioico Ácido Butanodioico Ácido pentanodioico Acido hexanodioico Acido heptanodioico
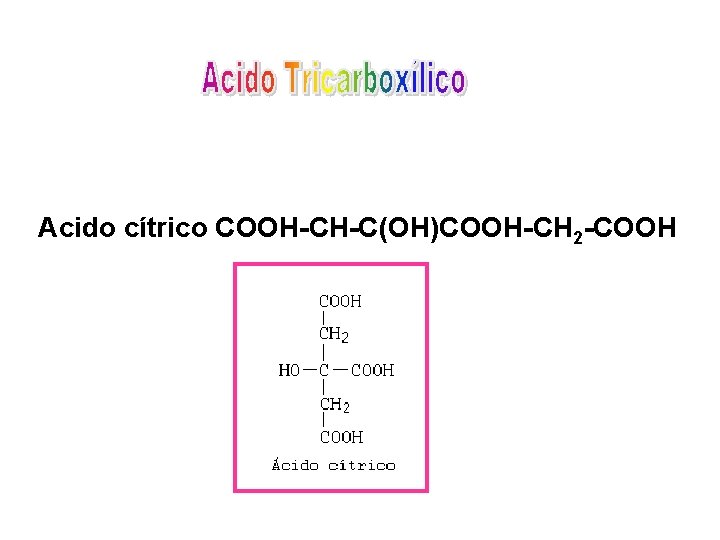
Acido cítrico COOH-CH-C(OH)COOH-CH 2 -COOH

Se conocen comunes. por sus nombres También se les nombra como derivados del ácido básico (ácido benzoico). Cuando el grupo arilo no está enlazado directamente al grupo carboxilo, el aromático se menciona como sustituyente.
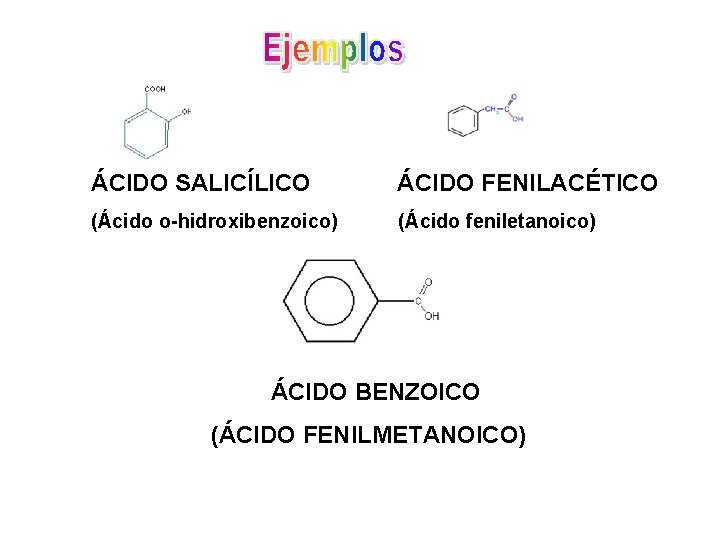
ÁCIDO SALICÍLICO ÁCIDO FENILACÉTICO (Ácido o-hidroxibenzoico) (Ácido feniletanoico) ÁCIDO BENZOICO (ÁCIDO FENILMETANOICO)

PROPIEDADES FÍSICAS • Los menores de 10 átomos de Carbono son líquidos, incoloros y de olor muy desagradable. • Los mayores de 10 átomos de Carbono son sólidos, cerosos e inodoros. Los dicarboxìlicos y aromàticos son sòlidos y cristalinos. • Los de bajo peso molecular (hasta 5 C) son solubles en agua, y disminuye su solubilidad conforme aumenta su peso. • Todos son solubles en solventes orgánicos.
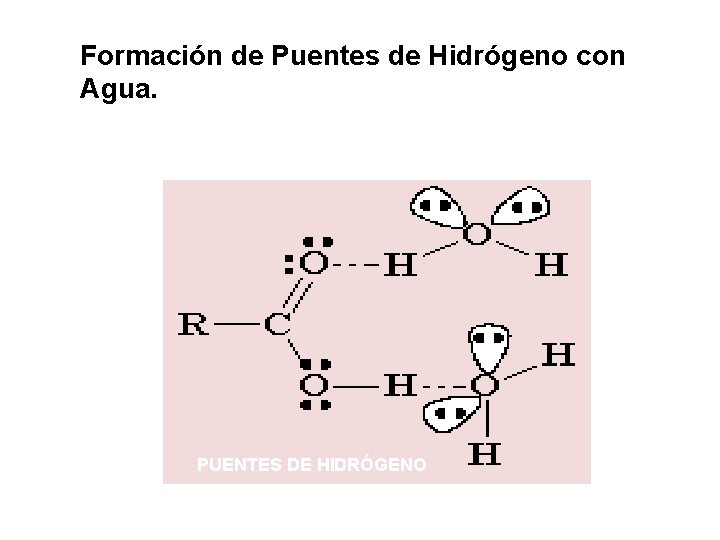
Formación de Puentes de Hidrógeno con Agua. PUENTES DE HIDRÓGENO

Puntos de ebullición: Los ácidos carboxílicos hierven a temperaturas superiores que los alcoholes, cetonas o aldehídos de pesos moleculares semejantes. Además forman puentes de hidrógeno entre ellos.
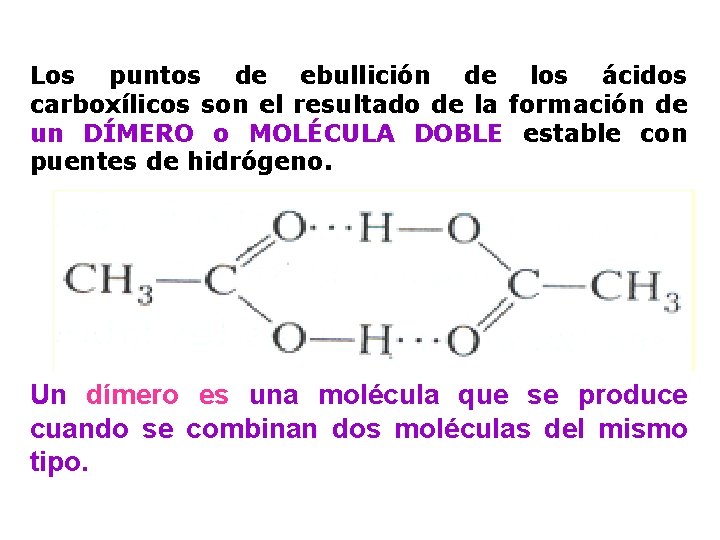
Los puntos de ebullición de los ácidos carboxílicos son el resultado de la formación de un DÍMERO o MOLÉCULA DOBLE estable con puentes de hidrógeno. Un dímero es una molécula que se produce cuando se combinan dos moléculas del mismo tipo.

Puntos de fusión: El punto de fusión varía según el número de carbonos, siendo más elevado el de los ácidos fórmico y acético, al compararlos con los ácidos propiónico, butírico y valérico de 3, 4 y 5 carbonos, respectivamente. Después de 6 carbonos el punto de fusión se eleva de manera irregular.
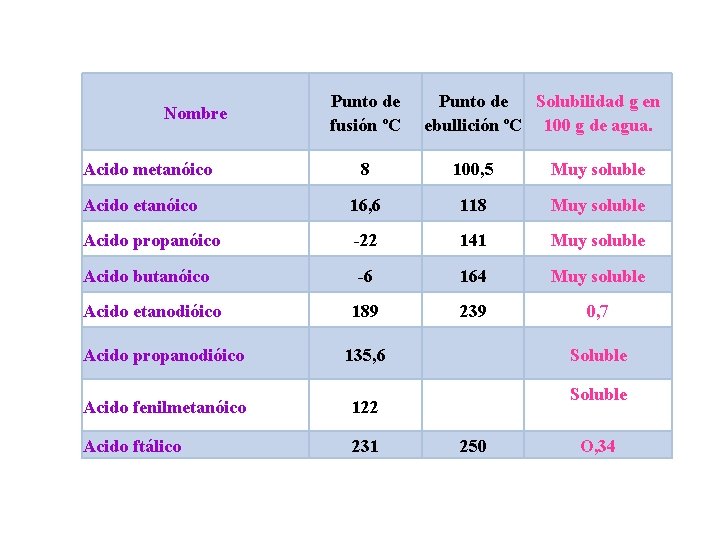
Nombre Acido metanóico Punto de fusión ºC Punto de Solubilidad g en ebullición ºC 100 g de agua. 8 100, 5 Muy soluble Acido etanóico 16, 6 118 Muy soluble Acido propanóico -22 141 Muy soluble Acido butanóico -6 164 Muy soluble 189 239 0, 7 Acido propanodióico 135, 6 Soluble Acido fenilmetanóico 122 Soluble Acido ftálico 231 250 O, 34 Acido etanodióico

Los ácidos dicarboxílicos tienen puntos de fusión muy altos. Al tener dos grupos carboxilos por molécula , las fuerzas de los puentes de hidrógeno son especialmente fuertes por lo que se necesita una alta temperatura para romper la red de puentes de hidrógeno.

Propiedades Químicas Las sustancias que liberan iones hidrógeno en agua, se clasifican como ácidos. Los ácidos carboxílicos son los más ácidos de los compuestos orgánicos, pero si se comparan con los ácidos inorgánicos, los carboxílicos son ácidos mucho más débiles.
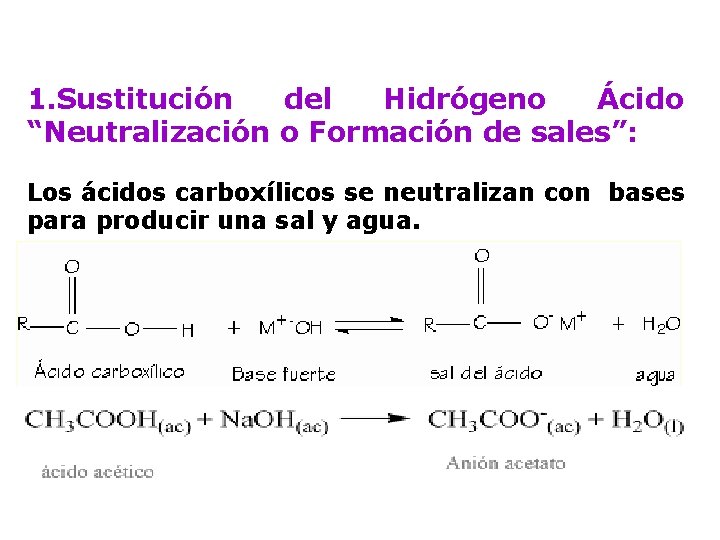
1. Sustitución del Hidrógeno Ácido “Neutralización o Formación de sales”: Los ácidos carboxílicos se neutralizan con bases para producir una sal y agua.
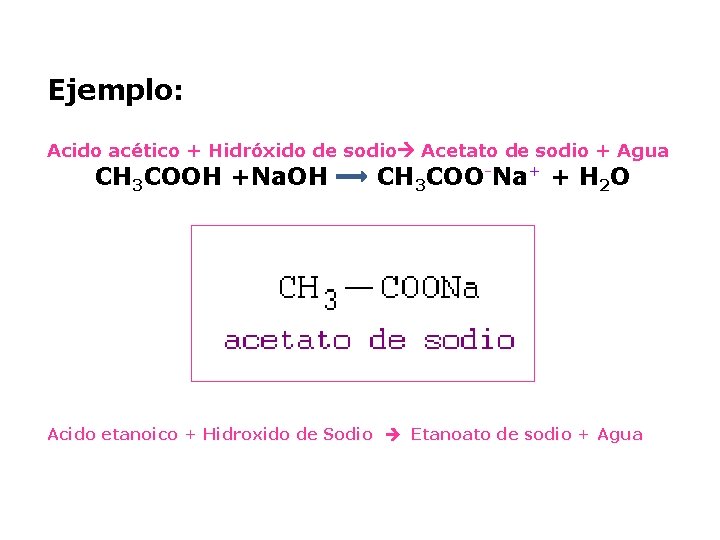
Ejemplo: Acido acético + Hidróxido de sodio Acetato de sodio + Agua CH 3 COOH +Na. OH CH 3 COO-Na+ + H 2 O Acido etanoico + Hidroxido de Sodio Etanoato de sodio + Agua

Importancia de los Ácidos Carboxílicos • Forman parte de una gran cantidad de células corporales, constituyendo los fosfolípidos y triacilglicéridos, que son ácidos grasos que se encuentran en las membranas celulares, neuronas, músculo cardíaco y tejido nervioso. • Están presentes en procesos fundamentales como el ciclo metabólico de las células en el organismo, llamado Ciclo de Krebs. • La biotina como ácido carboxílico interviene en el metabolismo de hidratos de carbono y algunos aminoácidos como factor de crecimiento.
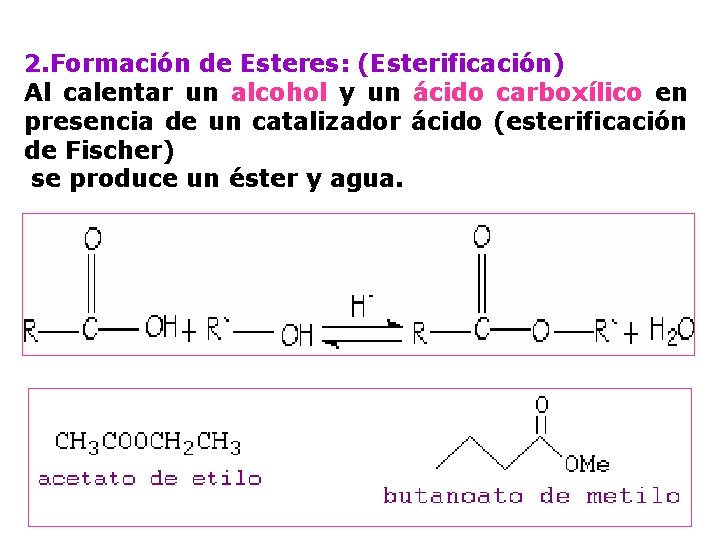
2. Formación de Esteres: (Esterificación) Al calentar un alcohol y un ácido carboxílico en presencia de un catalizador ácido (esterificación de Fischer) se produce un éster y agua.
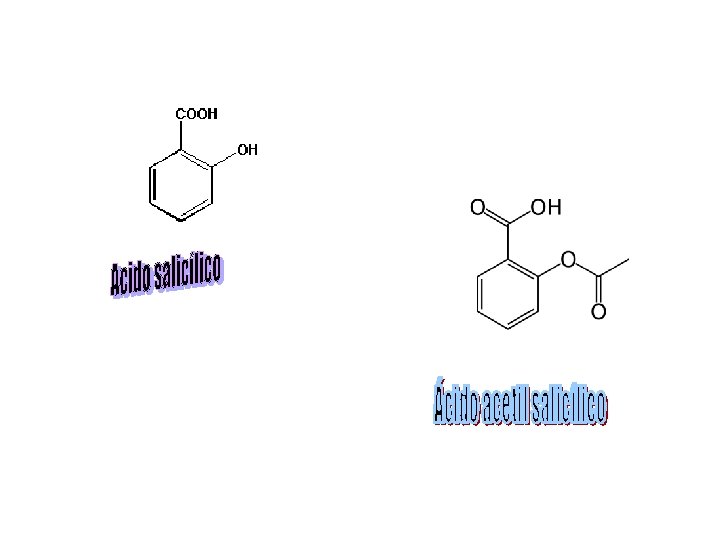

Importancia Los ACIDOS CARBOXÍLICOS contienen el grupo carboxilo que es uno de los grupos más importantes en química y bioquímica, ya que permite la síntesis de otros compuestos. Los ácidos son compuestos que confieren olor y sabor a muchos productos. Algunos de los derivados tienen importancia como analgésicos como el ácido salicílico y el ácido acetilsalicílico.

ÉSTERES Los ésteres son los derivados más importantes de los ácidos carboxílicos. Están ampliamente distribuidos en la naturaleza, las grasas y aceites vegetales son ésteres de ácidos grasos de cadena larga y glicerol. Contienen en su molécula un grupo carbonilo unido a un grupo –OR.
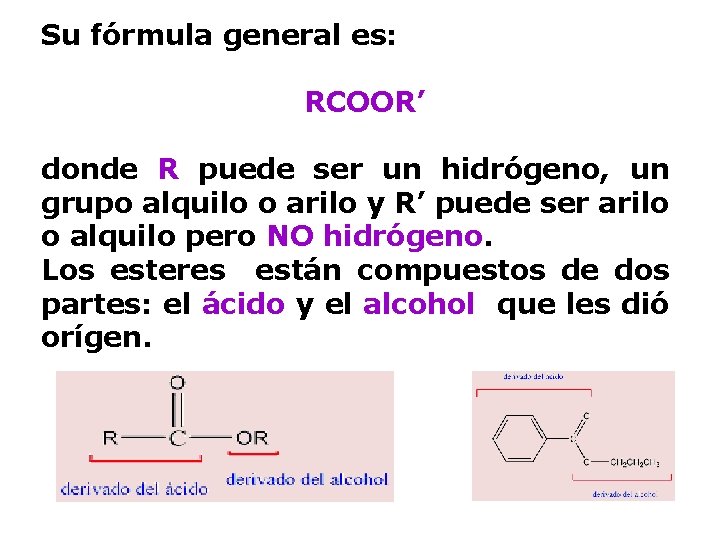
Su fórmula general es: RCOOR’ donde R puede ser un hidrógeno, un grupo alquilo o arilo y R’ puede ser arilo o alquilo pero NO hidrógeno. Los esteres están compuestos de dos partes: el ácido y el alcohol que les dió orígen.
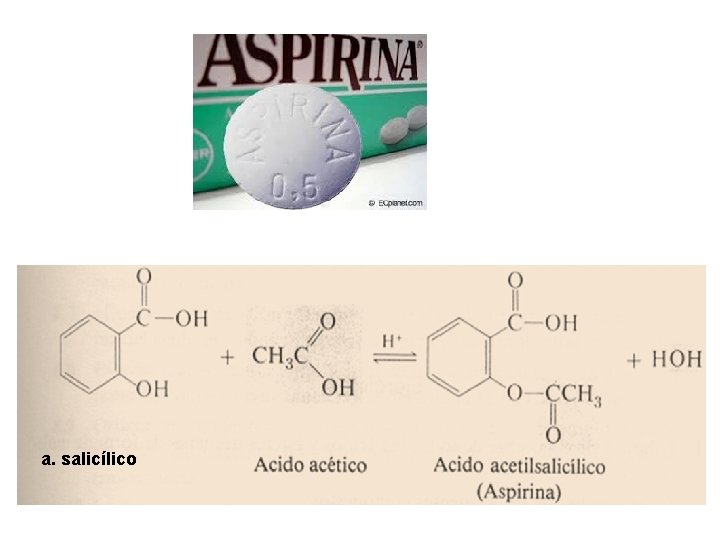
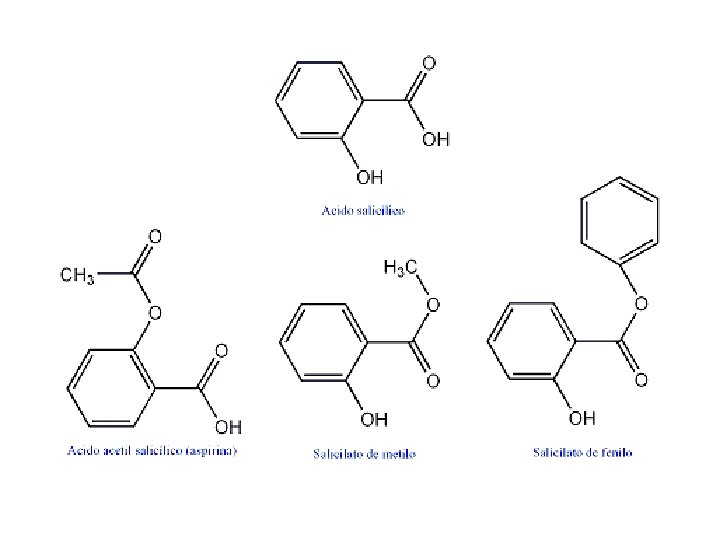
a. salicílico
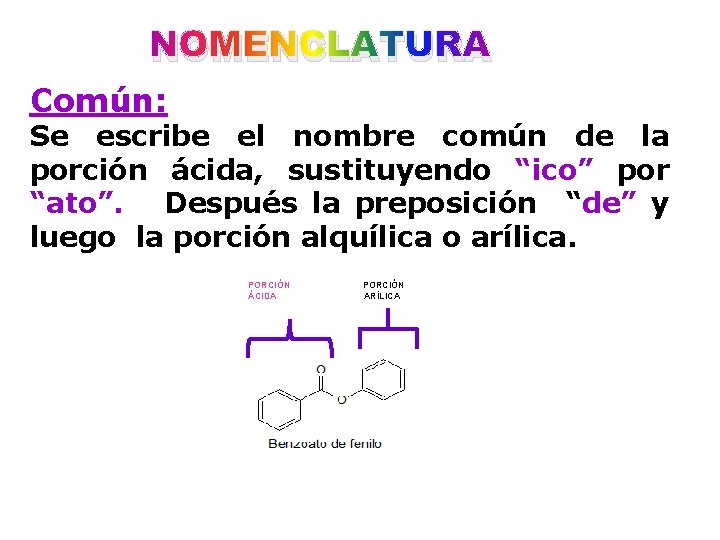
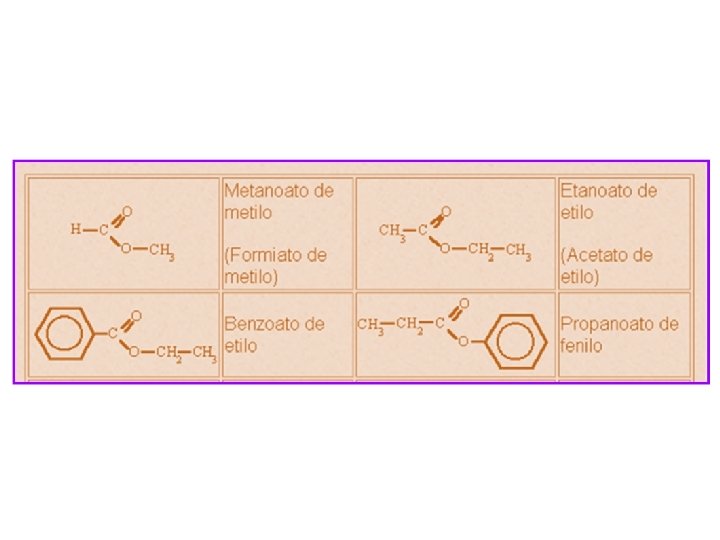
NOMENCLATURA Común: Se escribe el nombre común de la porción ácida, sustituyendo “ico” por “ato”. ”. Después la preposición “de” y luego la porción alquílica o arílica. PORCIÓN PORCIÓN ÁCIDA ARÍLICA
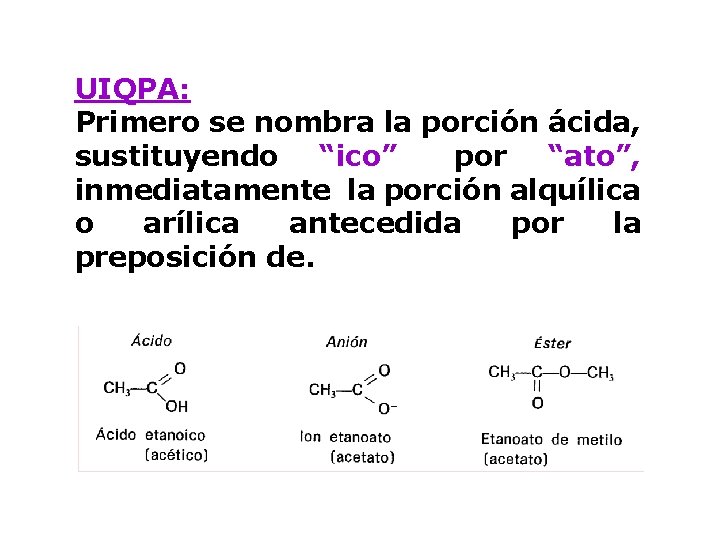
UIQPA: Primero se nombra la porción ácida, sustituyendo “ico”” por “ato”, inmediatamente la porción alquílica o arílica antecedida por la preposición de.
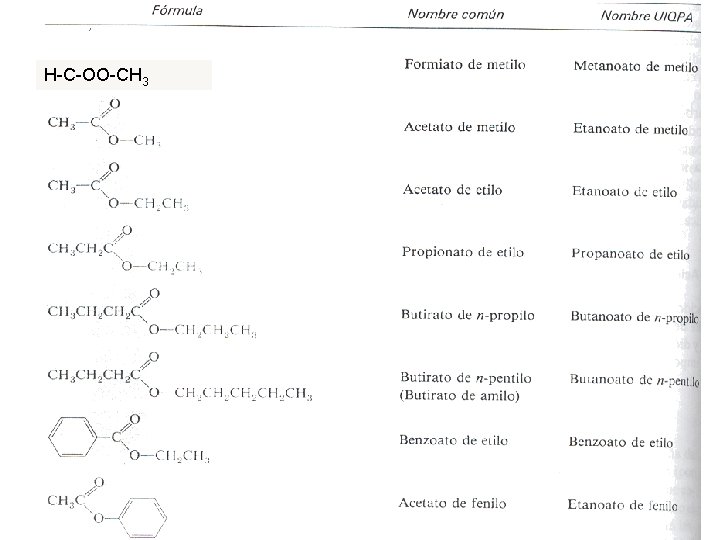
H-C-OO-CH 3
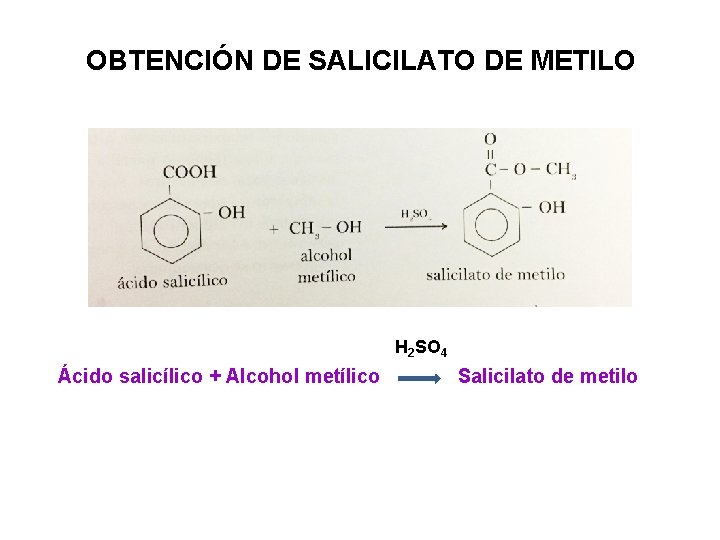
OBTENCIÓN DE SALICILATO DE METILO 3 H 2 SO 4 Ácido salicílico + Alcohol metílico Salicilato de metilo

PROPIEDADES FÍSICAS Poseen olores agradables, los aromas de muchas flores y frutos se deben a presencia de ésteres. Se emplean en la fabricación de perfumes y como agentes saborizantes en las industrias de confitería y bebidas no alcohólicas. Son líquidos incoloros, insolubles y menos densos que el agua, no forman enlaces de hidrógeno.
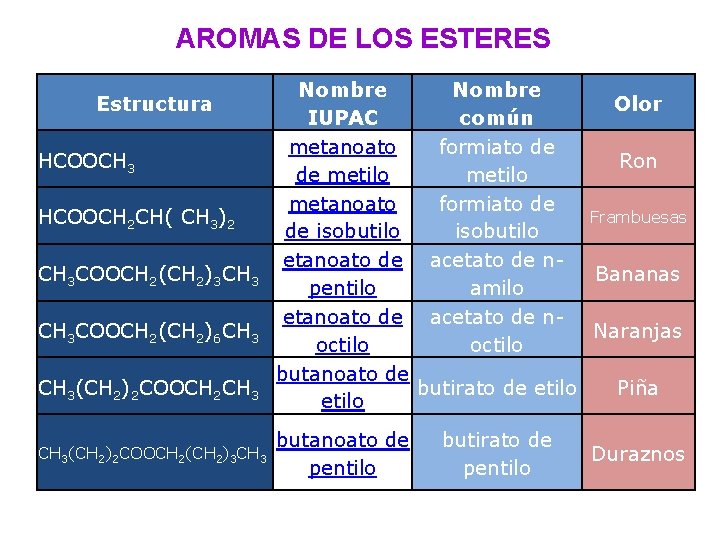
AROMAS DE LOS ESTERES Estructura HCOOCH 3 HCOOCH 2 CH( CH 3)2 CH 3 COOCH 2(CH 2)3 CH 3 COOCH 2(CH 2)6 CH 3(CH 2)2 COOCH 2(CH 2)3 CH 3 Nombre Olor IUPAC común metanoato formiato de Ron de metilo metanoato formiato de Frambuesas de isobutilo etanoato de acetato de n. Bananas pentilo amilo etanoato de acetato de n. Naranjas octilo butanoato de butirato de etilo Piña etilo butanoato de pentilo butirato de pentilo Duraznos


AMIDAS Las amidas son derivados de los ácidos carboxílicos. Presentan un átomo de nitrógeno unido a un grupo carbonilo. La fórmula general de una amida es: RCONH 2
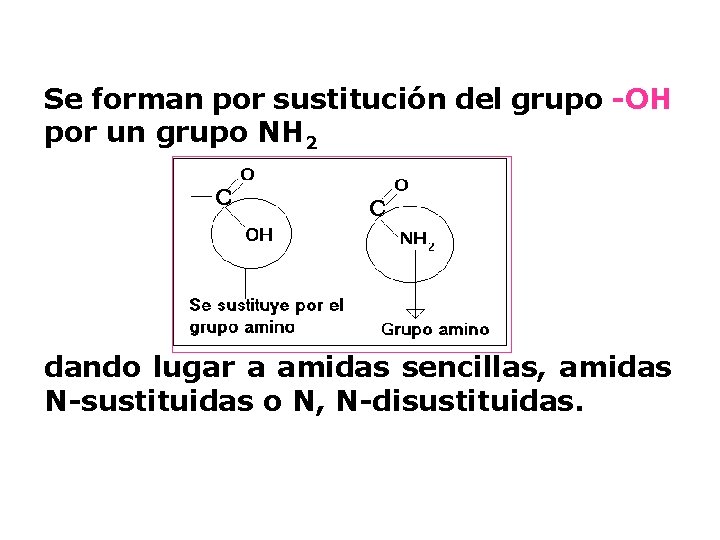
Se forman por sustitución del grupo -OH por un grupo NH 2 dando lugar a amidas sencillas, amidas N-sustituidas o N, N-disustituidas.
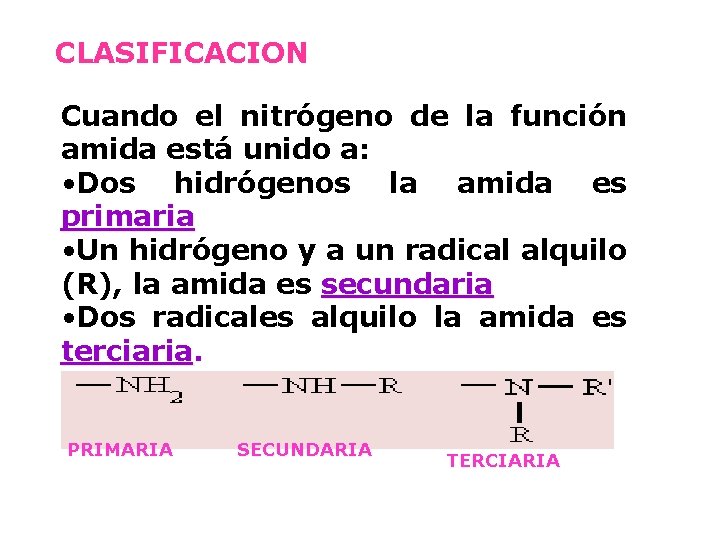
CLASIFICACION Cuando el nitrógeno de la función amida está unido a: • Dos hidrógenos la amida es primaria • Un hidrógeno y a un radical alquilo (R), la amida es secundaria • Dos radicales alquilo la amida es terciaria PRIMARIA SECUNDARIA TERCIARIA
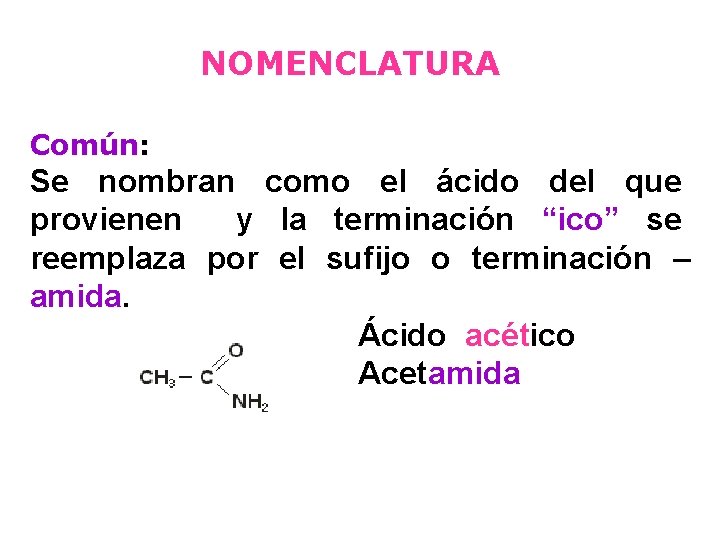
NOMENCLATURA Común: Se nombran como el ácido del que provienen y la terminación “ico” se reemplaza por el sufijo o terminación – amida. Ácido acético Acetamida
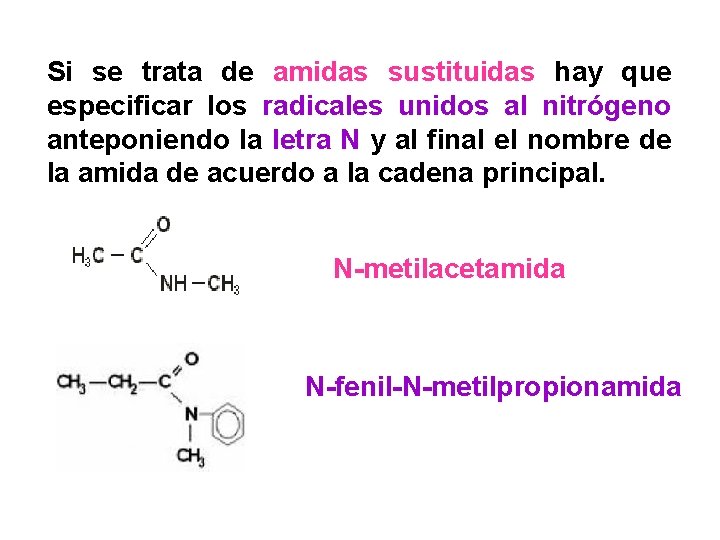
Si se trata de amidas sustituidas hay que especificar los radicales unidos al nitrógeno anteponiendo la letra N y al final el nombre de la amida de acuerdo a la cadena principal. N-metilacetamida N-fenil-N-metilpropionamida
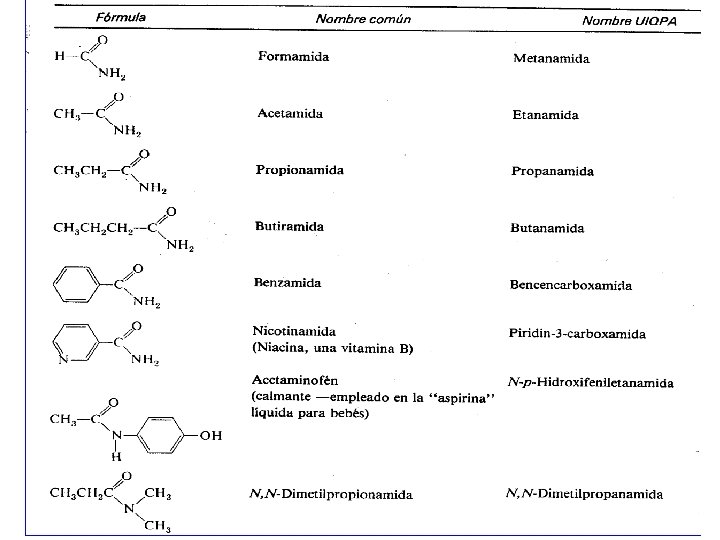

UIQPA: Se les da el nombre UIQPA del ácido del cual provienen reemplazando la terminación “oico” por el sufijo o terminación –amida.
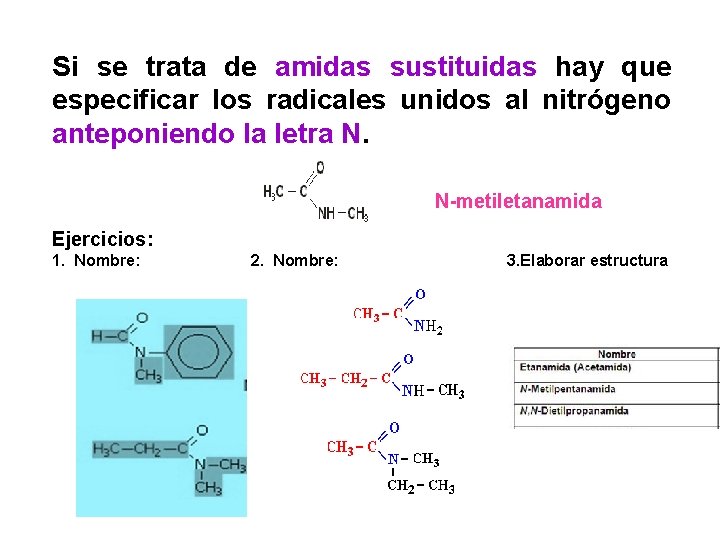
Si se trata de amidas sustituidas hay que especificar los radicales unidos al nitrógeno anteponiendo la letra N. N-metiletanamida Ejercicios: 1. Nombre: 2. Nombre: 3. Elaborar estructura
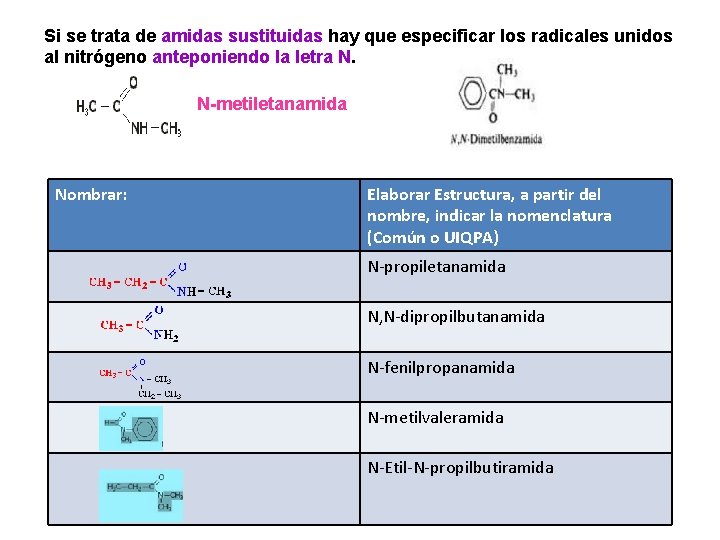
Si se trata de amidas sustituidas hay que especificar los radicales unidos al nitrógeno anteponiendo la letra N. N-metiletanamida Nombrar: Elaborar Estructura, a partir del nombre, indicar la nomenclatura (Común o UIQPA) N-propiletanamida N, N-dipropilbutanamida N-fenilpropanamida N-metilvaleramida N-Etil-N-propilbutiramida

El enlace C-N se denomina enlace amida Este enlace es muy estable y se encuentra en las unidades repetitivas del nylon y otros polímeros industriales y principalmente en las proteínas donde también se denomina enlace peptídico NYLON
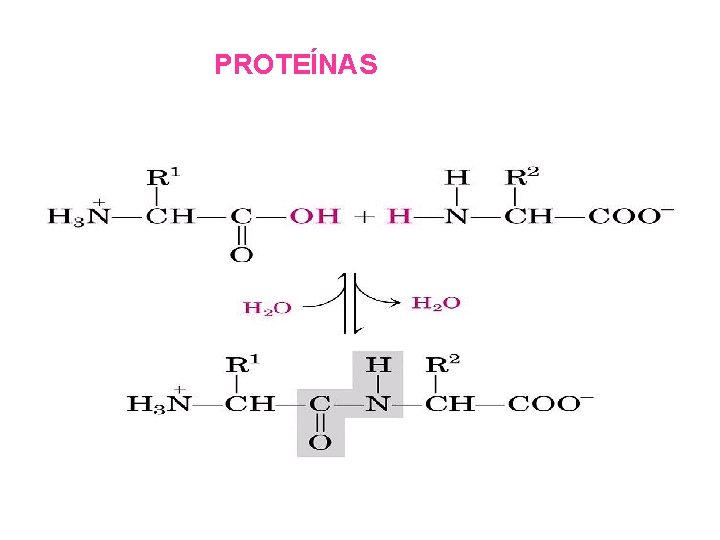
PROTEÍNAS
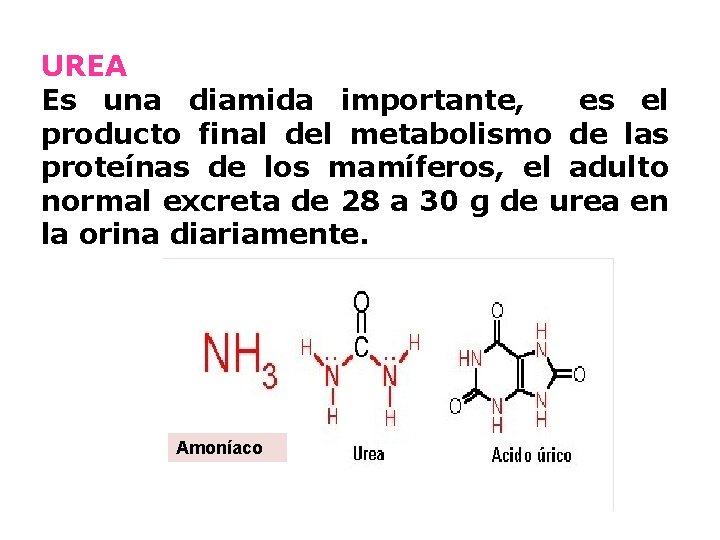
UREA Es una diamida importante, es el producto final del metabolismo de las proteínas de los mamíferos, el adulto normal excreta de 28 a 30 g de urea en la orina diariamente. Amoníaco

PROPIEDADES FÍSICAS • Todas las amidas primarias son excepción de la formamida. sólidas, a • Son incoloras e inodoras. • Las amidas inferiores son solubles en agua (formamida butiramida) y alcohol. • Son moléculas neutras. • Poseen puntos de fusión y ebullición anormalmente altos (debido a la naturaleza polar del grupo amida y formación de puentes de H).
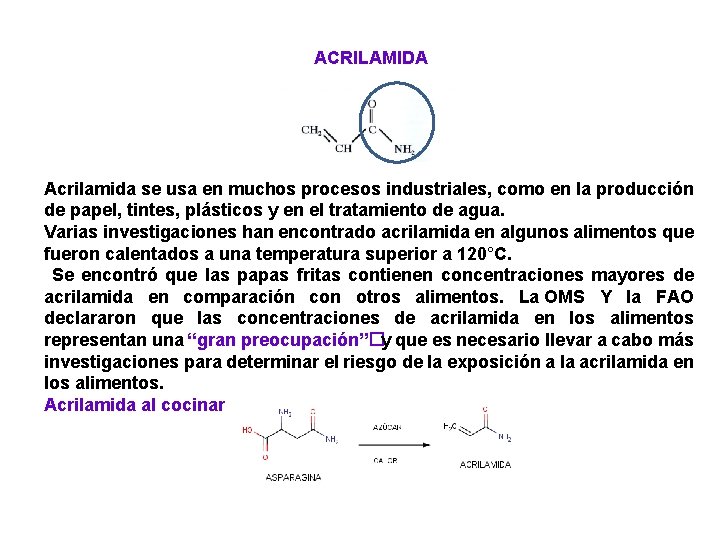
ACRILAMIDA Acrilamida se usa en muchos procesos industriales, como en la producción de papel, tintes, plásticos y en el tratamiento de agua. Varias investigaciones han encontrado acrilamida en algunos alimentos que fueron calentados a una temperatura superior a 120°C. Se encontró que las papas fritas contienen concentraciones mayores de acrilamida en comparación con otros alimentos. La OMS Y la FAO declararon que las concentraciones de acrilamida en los alimentos representan una “gran preocupación”� y que es necesario llevar a cabo más investigaciones para determinar el riesgo de la exposición a la acrilamida en los alimentos. Acrilamida al cocinar

La asparagina es un aminoácido (un componente esencial de las proteínas) que se encuentra en muchas verduras, a concentraciones mayores en algunas variedades de papas. Al calentarlas a altas temperaturas en presencia de determinados azúcares, la asparagina puede formar acrilamida. Se ha determinado que los procedimientos de cocina que utilizan altas temperaturas, tales como freír, hornear o asar, producen acrilamida. Los tiempos más largos de cocinado pueden también aumentar la producción de acrilamida cuando la temperatura de cocción es superior a los 120°C.

Una serie de estudios de casos y controles ha investigado la relación que existe entre el consumo alimentario de acrilamida y el riesgo de presentar cánceres de faringe, esófago, cavidad oral, intestino grueso, riñón, seno y ovario, sin embargo no hay resultados concluyentes. Se ha mostrado que concentraciones altas de acrilamida en el lugar de trabajo causan daño neurológico, por ejemplo, entre los trabajadores que usan polímeros de acrilamida para la clarificación del agua en plantas de preparación de carbón. No hay regulaciones en cuanto a la cantidad de acrilamida que puedan contener los alimentos. http: //www. scielo. cl/scielo. php? pid=s 071775182007000100001&script=sci_arttext

- Slides: 64