LOGO CHIA S KINH NGHIM IU TR VIM


























- Slides: 50

L/O/G/O CHIA SẺ KINH NGHIỆM ĐIỀU TRỊ VIÊM GAN SIÊU VI C BS. CKII HUỲNH THỊ KIM YẾN ĐẠI HỌC Y DƯỢC CẦN THƠ

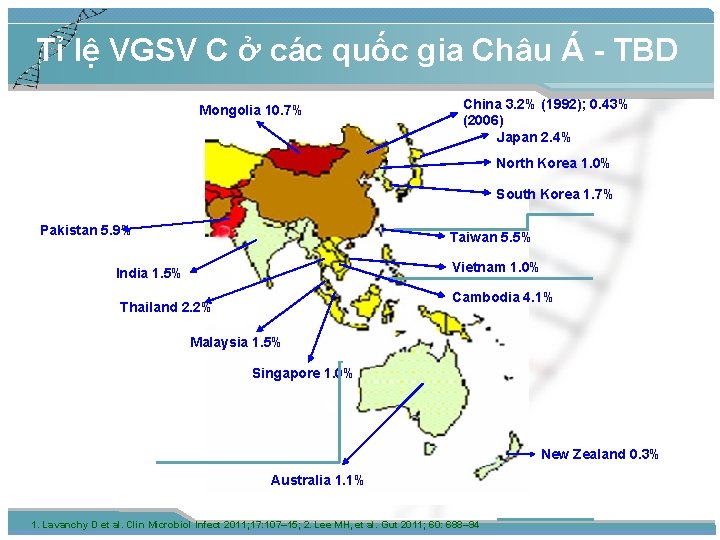
Tỉ lệ VGSV C ở các quốc gia Châu Á - TBD Mongolia 10. 7% China 3. 2% (1992); 0. 43% (2006) Japan 2. 4% North Korea 1. 0% South Korea 1. 7% Pakistan 5. 9% Taiwan 5. 5% Vietnam 1. 0% India 1. 5% Cambodia 4. 1% Thailand 2. 2% Malaysia 1. 5% Singapore 1. 0% New Zealand 0. 3% Australia 1. 1% 1. Lavanchy D et al. Clin Microbiol Infect 2011; 17: 107– 15; 2. Lee MH, et al. Gut 2011; 60: 688– 94

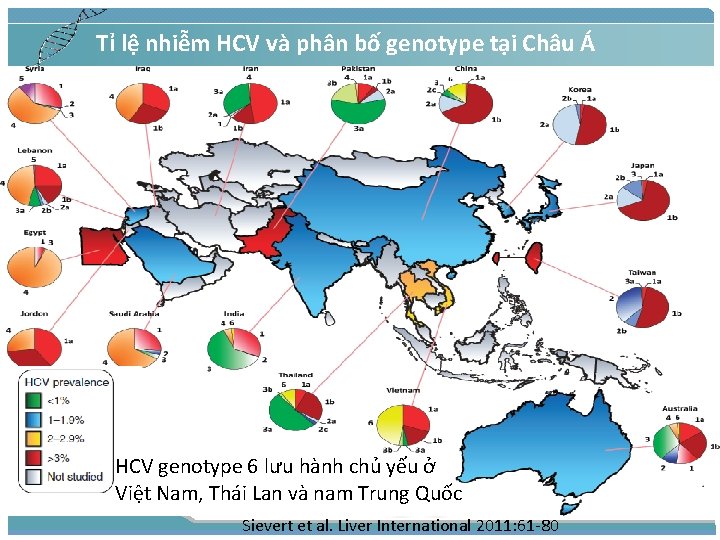
Tỉ lệ nhiễm HCV và phân bố genotype tại Châu Á HCV genotype 6 lưu hành chủ yếu ở Việt Nam, Thái Lan và nam Trung Quốc Sievert et al. Liver International 2011: 61 -80

CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM Độc lập - Tự do - Hạnh phúc HƯỚNG DẪN CHẨN ĐOÁN VÀ ĐIỀU TRỊ BỆNHVIÊM GAN VI RÚT C (Ban hành kèm theo Quyết định số 5012/QĐ-BYT ngày 20/09/2016 Của Bộ trưởng Bộ Y tế) KT. BỘ TRƯỞNG THỨ TRƯỞNG (đã ký) Nguyễn ViếT Tiến

CẬN L M SÀNG • Theo các anh chị chẩn đoán VGSVC cần làm XN nào ý nghĩa của các XN? a. Anti – HCV test nhanh b. Anti – HCV Elisa c. HCV RNA định tính d. HCV RNA định lượng

CẬN L M SÀNG • Anti-HCV • HCV RNA

CẬN L M SÀNG • HCV RNA: Để xác định người bệnh đang nhiễm HCV. Tất cả người có anti – HCV (+) cần được làm xét nghiệm HCV RNA

Hiện nay trong điều trị viêm gan siêu vi C có cần làm xét nghiệm genotype không • 1. Cần làm: Tại sao? • 2. Không cần làm: Tại sao?

XN SÀNG LỌC VGSVC • Định type virus viêm gan C: + Giúp lựa chọn phác đồ phù hợp. + Tiên lượng đáp ứng điều trị.

CHẨN ĐOÁN XÁC ĐỊNH VGSV C CẤP • Thời gian nhiễm < 6 tháng • Có tiền sử phơi nhiễm với nguồn bệnh. • anti-HCV có thể (-) trong vài tuần đầu, hoặc dương tính sau 8 - 12 tuần phơi nhiễm. + HCV RNA (+) 2 tuần sau khi phơi nhiễm + AST, ALT thươ ng tăng • Co thể có biê u hiê n lâm sa ng hoă c không.

CHẨN ĐOÁN NHIỄM HCV CẤP • Có chuyển đảo anti – HCV (-) (+) • Anti HCV (-) nhưng HCV (+)

CHẨN ĐOÁN XÁC ĐỊNH VGSV C MẠN • Anti HCV (+), HCV RNA (+) • Thơ i gian mă c bê nh > 6 tha ng • Không có / hoặc có xơ hóa gan, xơ gan.

• Trong điều kiện thực tế bệnh viện của các anh chị, để chẩn đoán được BN VGSV mạn cần? • a. Tiền sử • b. Fibroscan • c. APRI • d. HCV RNA

Châ n đoa n xa c đi nh VGSV C ma n Bảng điểm Metavir Fibro. Scan F 0 – không xơ hóa F 0: 1 -5 k. Pa F 1 – xơ hóa khoảng cửa F 1: 5 - 7 k. Pa không có vách ngăn F 2 – xơ hóa khoảng cửa F 2: 7, 1 – 9, 5 k. Pa với vài vách ngăn F 3 – Nhiều vách ngăn nhưng chưa xơ gan F 3: 9, 6 – 12, 5 k. Pa F 4 – Xơ gan F 4: > 12, 5 k. Pa

Châ n đoa n xa c đi nh VGSV C ma n • APRI: AST x 100/ASTGHTBT APRI = ……………. Tiểu cầu (109/l) • F 0 - F 1: APRI : < 0, 5 • F 2 : APRI : 0, 5 – 1, 0 • F 3: APRI: 1, 0 – 2 • F 4 : APRI: > 2

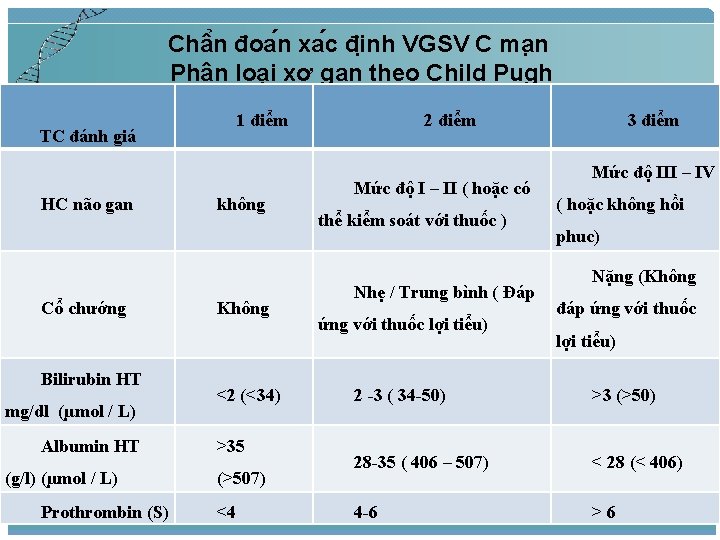
Châ n đoa n xa c đi nh VGSV C ma n Phân loại xơ gan theo Child Pugh 1 điểm TC đánh giá HC não gan Cổ chướng Bilirubin HT mg/dl (µmol / L) Albumin HT (g/l) (µmol / L) Prothrombin (S) không Không <2 (<34) >35 (>507) <4 2 điểm Mức độ I – II ( hoặc có thể kiểm soát với thuốc ) Nhẹ / Trung bình ( Đáp ứng với thuốc lợi tiểu) 3 điểm Mức độ III – IV ( hoặc không hồi phuc) Nặng (Không đáp ứng với thuốc lợi tiểu) 2 -3 ( 34 -50) >3 (>50) 28 -35 ( 406 – 507) < 28 (< 406) 4 -6 >6

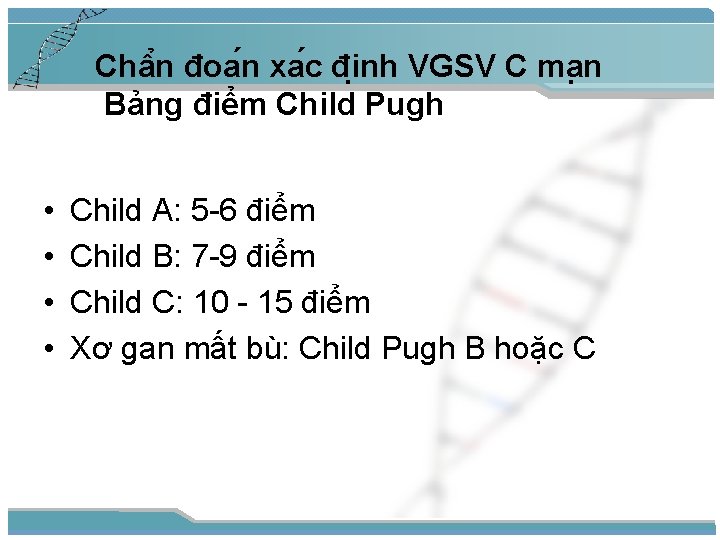
Châ n đoa n xa c đi nh VGSV C ma n Bảng điểm Child Pugh • • Child A: 5 -6 điểm Child B: 7 -9 điểm Child C: 10 - 15 điểm Xơ gan mất bù: Child Pugh B hoặc C

CHẨN ĐOÁN VGSV C Ở TRẺ EM • Trẻ em < 18 tháng tuổi: XN HCV RNA lúc trẻ 6 tháng và 12 tháng • Trẻ được chẩn đoán nhiễm HCV khi có ít nhất 2 lần HCV (+)

CHẨN ĐOÁN VGSV C Ở TRẺ EM • Trẻ ≥ 18 tháng tuổi • Anti – HCV (+) và HCV RNA (+)

XÁC ĐỊNH CÁC BỆNH LÝ ĐI KÈM • • Đồng nhiễm VG A, B, D, E, Viêm gan tự miễn. Viêm gan do rượu. Viêm gan nhiễm mỡ không do rượu. Nhiễm HIV. Đái tháo đường, Bệnh lý tuyến giáp.

ĐIỀU TRỊ VGSV C CẤP • Điều trị hổ trợ • Điều trị đặc hiệu • Không khuyến cáo điều trị người bệnh nhiễm HCV cấp • Xem xét điều trị khi có biểu hiện nặng hơn. Đe dọa tính mạng • TD HCV RNA ít nhất 12 tuần sau chẩn đoán

ĐIỀU TRỊ VGSV C CẤP • Nếu HCV (+) sau 12 tuần theo dõi • Điều trị bằng DAAs như VGSVC mạn

VGSVC ĐIỀU TRỊ NGAY KHÔNG CHỜ Cơ hội thành công cao. Giảm nguy cơ biến chứng Giảm lây lan trong cộng đồng

MỤC TIÊU Loại trừ HCV RNA dưới ngưỡng phát hiện (< 15 IU/ml) W 12 sau khi kết thúc ĐT , gọi là SVR 12

MỤC TIÊU HCV dưới ngưỡng W 24 sau khi kết thúc ĐT SVR 24 phác đồ có Peg - Interfer Cải thiện mô học.

MỤC TIÊU Phòng ngừa các biến chứng và các bệnh liên quan HCV Dự phòng lây nhiễm HCV trong cộng đồng

ĐIỀU TRỊ VGSV C MẠN CHUẨN BỊ ĐIỀU TRỊ • Khám lâm sàng toàn diện

Theo các anh chị trong thực tế khi chọn thuốc điều trị VGSVC mạn điều cần quan tâm a. Giá thành b. Chất lượng thuốc c. Tỉ lệ thành công d. Tác dụng phụ

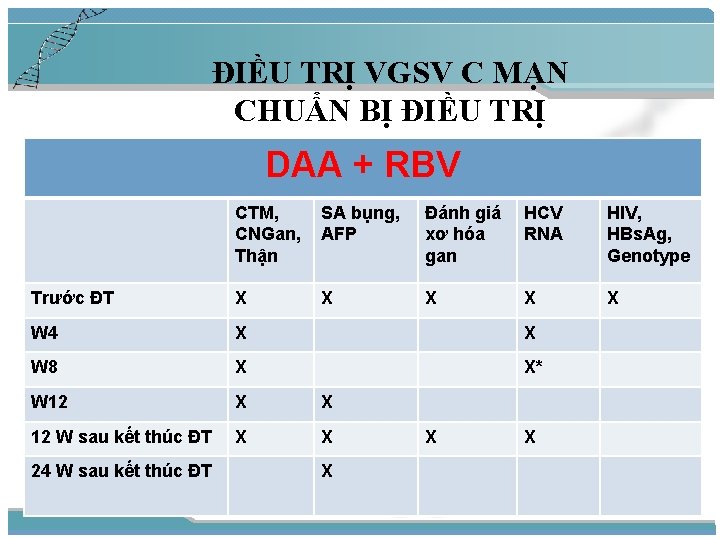
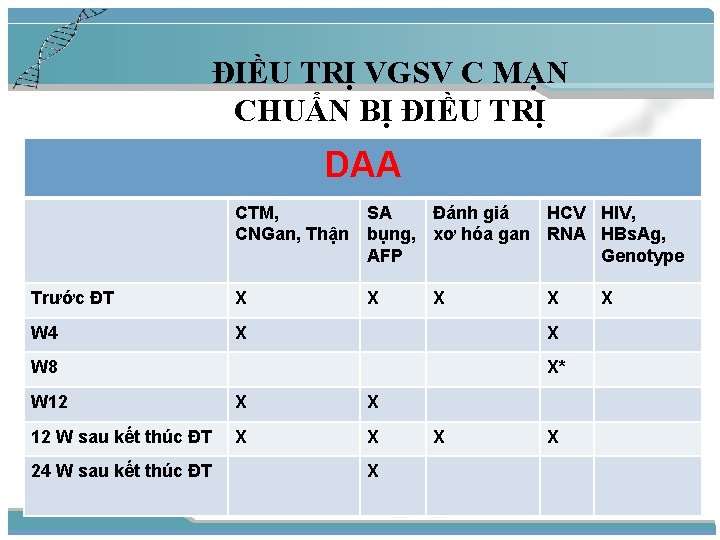
ĐIỀU TRỊ VGSV C MẠN CHUẨN BỊ ĐIỀU TRỊ DAA + RBV CTM, CNGan, Thận SA bụng, AFP Đánh giá xơ hóa gan HCV RNA HIV, HBs. Ag, Genotype Trước ĐT X X X W 4 X X W 8 X X* W 12 X X 12 W sau kết thúc ĐT X X 24 W sau kết thúc ĐT X X X

ĐIỀU TRỊ VGSV C MẠN CHUẨN BỊ ĐIỀU TRỊ DAA CTM, CNGan, Thận SA Đánh giá HCV HIV, bụng, xơ hóa gan RNA HBs. Ag, AFP Genotype Trước ĐT X X W 4 X X X W 8 X* W 12 X X 12 W sau kết thúc ĐT X X 24 W sau kết thúc ĐT X X X

ĐIỀU TRỊ VGSV C MẠN CHUẨN BỊ ĐiỀU TRỊ • Tư vấn cho bệnh nhân + Đường lây nhiễm + Các biến chứng, khả năng tái nhiễm mới + Kiêng rượu bia

ĐIỀU TRỊ VGSV C MẠN CHUẨN BỊ ĐiỀU TRỊ • Phác đồ điều trị + Hiệu quả + Tác dụng không mong muốn + Khả năng sinh quái thai.

ĐIỀU TRỊ VGSVC 2015 2, 3 1, 4, 5, 6 1 Sofosbuvir + RBV Sofosbuvir + ledipasvir (± RBV) Ombitasvir / Paritaprevir / Ritonavir / + Dasabuvir (± RBV) www. themegallery. com

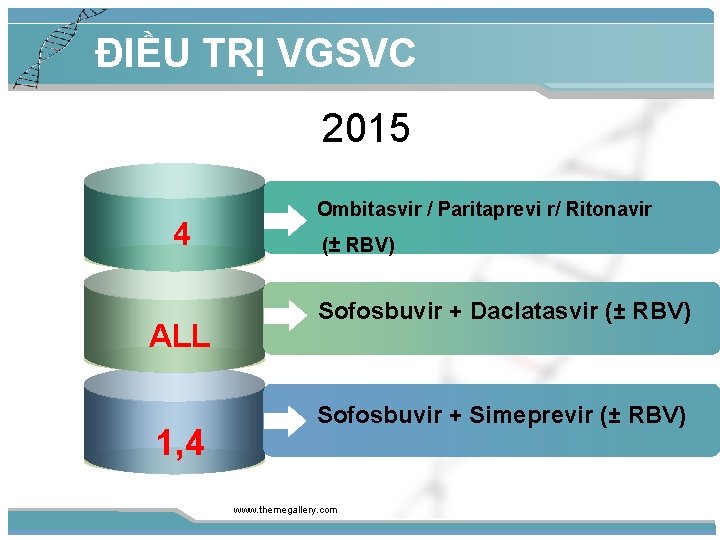
ĐIỀU TRỊ VGSVC 2015 4 ALL 1, 4 Ombitasvir / Paritaprevi r/ Ritonavir (± RBV) Sofosbuvir + Daclatasvir (± RBV) Sofosbuvir + Simeprevir (± RBV) www. themegallery. com

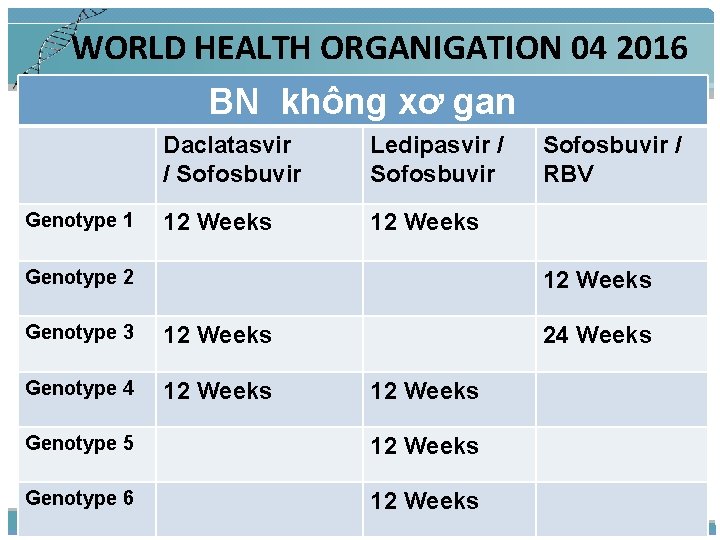
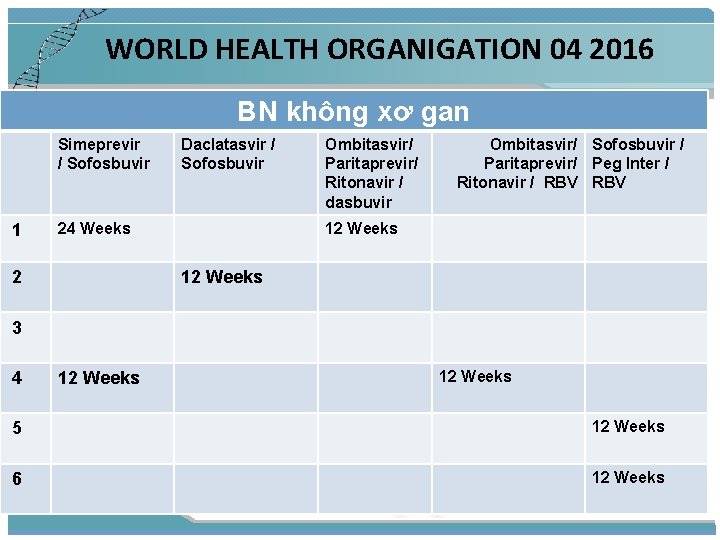
WORLD HEALTH ORGANIGATION 04 2016 BN không xơ gan Genotype 1 Daclatasvir / Sofosbuvir Ledipasvir / Sofosbuvir 12 Weeks Genotype 2 Sofosbuvir / RBV 12 Weeks Genotype 3 12 Weeks Genotype 4 12 Weeks 24 Weeks 12 Weeks Genotype 5 12 Weeks Genotype 6 12 Weeks

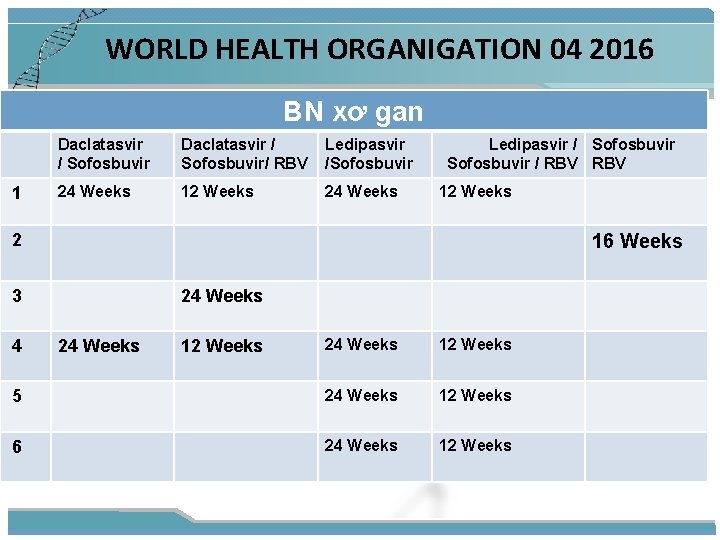
WORLD HEALTH ORGANIGATION 04 2016 BN xơ gan 1 Daclatasvir / Sofosbuvir/ RBV Ledipasvir /Sofosbuvir 24 Weeks 12 Weeks 24 Weeks Ledipasvir / Sofosbuvir / RBV 12 Weeks 2 16 Weeks 3 24 Weeks 12 Weeks 5 24 Weeks 12 Weeks 6 24 Weeks 12 Weeks 4 24 Weeks 12 Weeks

WORLD HEALTH ORGANIGATION 04 2016 BN không xơ gan Simeprevir / Sofosbuvir 1 Daclatasvir / Sofosbuvir 24 Weeks 2 Ombitasvir/ Paritaprevir/ Ritonavir / dasbuvir Ombitasvir/ Sofosbuvir / Paritaprevir/ Peg Inter / Ritonavir / RBV 12 Weeks 3 4 12 Weeks 5 12 Weeks 6 12 Weeks

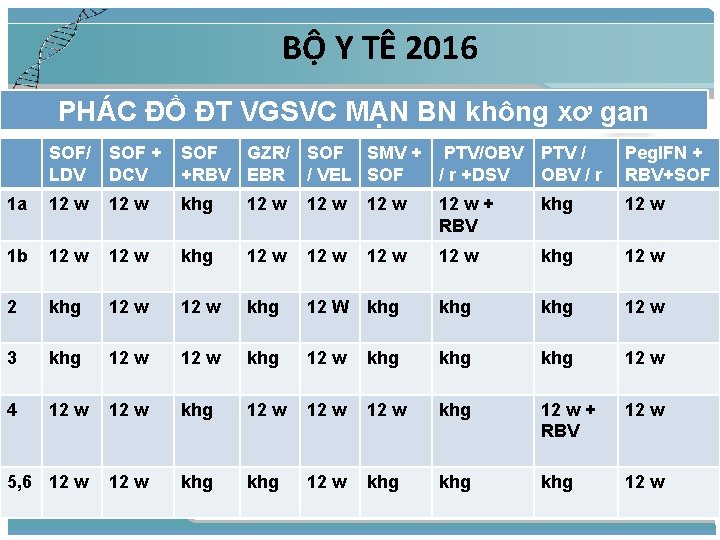
BỘ Y TÊ 2016 PHÁC ĐỒ ĐT VGSVC MẠN BN không xơ gan SOF/ LDV SOF + DCV SOF GZR/ SOF SMV + PTV/OBV +RBV EBR / VEL SOF / r +DSV PTV / OBV / r Peg. IFN + RBV+SOF 1 a 12 w khg 12 w + RBV khg 12 w 1 b 12 w khg 12 w 2 khg 12 w khg 12 W khg khg 12 w 3 khg 12 w khg khg 12 w 4 12 w khg 12 w + RBV 12 w 5, 6 12 w khg khg 12 w

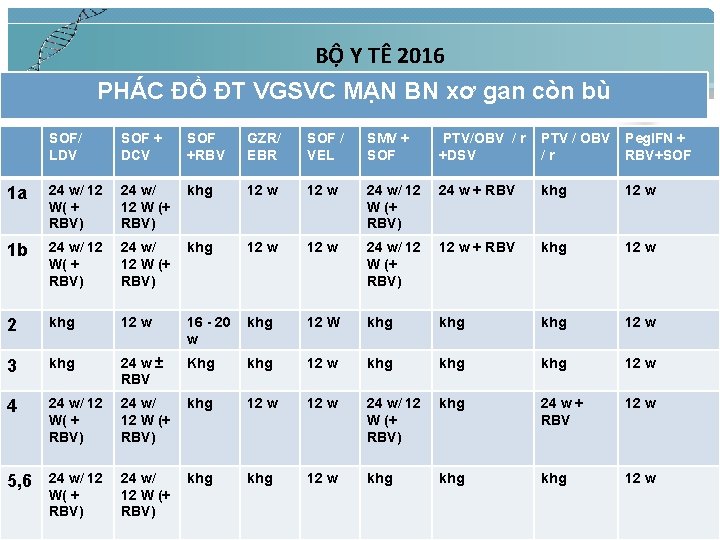
BỘ Y TÊ 2016 PHÁC ĐỒ ĐT VGSVC MẠN BN xơ gan còn bù SOF/ LDV SOF + DCV SOF +RBV GZR/ EBR SOF / VEL SMV + SOF PTV/OBV / r +DSV PTV / OBV /r Peg. IFN + RBV+SOF 1 a 24 w/ 12 W( + RBV) 24 w/ 12 W (+ RBV) khg 12 w 24 w/ 12 W (+ RBV) 24 w + RBV khg 12 w 1 b 24 w/ 12 W( + RBV) 24 w/ 12 W (+ RBV) khg 12 w 24 w/ 12 W (+ RBV) 12 w + RBV khg 12 w 2 khg 12 w 16 - 20 w khg 12 W khg khg 12 w 3 khg 24 w ± RBV Khg khg 12 w khg khg 12 w 4 24 w/ 12 W( + RBV) 24 w/ 12 W (+ RBV) khg 12 w 24 w/ 12 W (+ RBV) khg 24 w + RBV 12 w 5, 6 24 w/ 12 W( + RBV) 24 w/ 12 W (+ RBV) khg 12 w khg khg 12 w

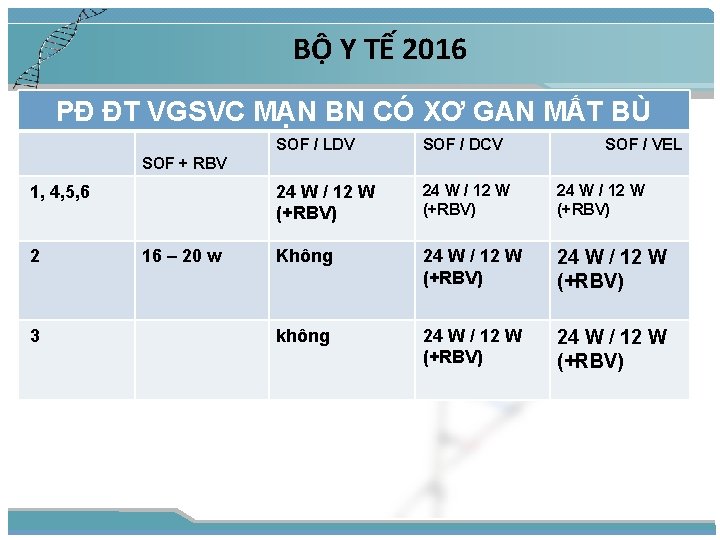
BỘ Y TẾ 2016 PĐ ĐT VGSVC MẠN BN CÓ XƠ GAN MẤT BÙ SOF / LDV SOF / DCV SOF / VEL 24 W / 12 W (+RBV) Không 24 W / 12 W (+RBV) không 24 W / 12 W (+RBV) SOF + RBV 1, 4, 5, 6 2 3 16 – 20 w

BỘ Y TẾ 2016 ĐIỀU TRỊ VGSV C MẠN • Phác đồ có RBV thì khởi đầu với liều 600 mg, tăng dần theo cân nặng nếu BN dung nạp tốt • Điều trị DAAs cho BN xơ gan mất bù cần được theo dõi tại cơ sở chuyên khoa/ Đa khoa tuyến tỉnh hoặc tuyến trung ương

Điều trị VG C khởi đầu trong bảo hiểm y tế như thế nào?

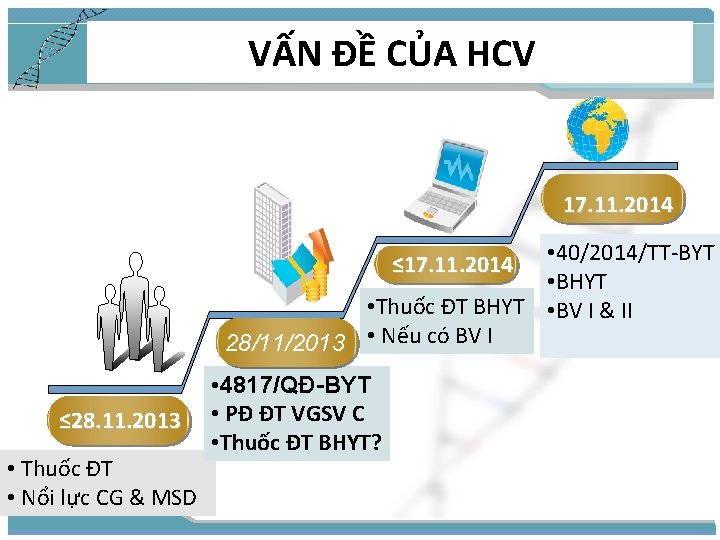
VẤN ĐỀ CỦA HCV 17. 11. 2014 • 40/2014/TT-BYT • BHYT • Thuốc ĐT BHYT • BV I & II 28/11/2013 • Nếu có BV I ≤ 17. 11. 2014 ≤ 28. 11. 2013 • Thuốc ĐT • Nổi lực CG & MSD • 4817/QĐ-BYT • PĐ ĐT VGSV C • Thuốc ĐT BHYT?

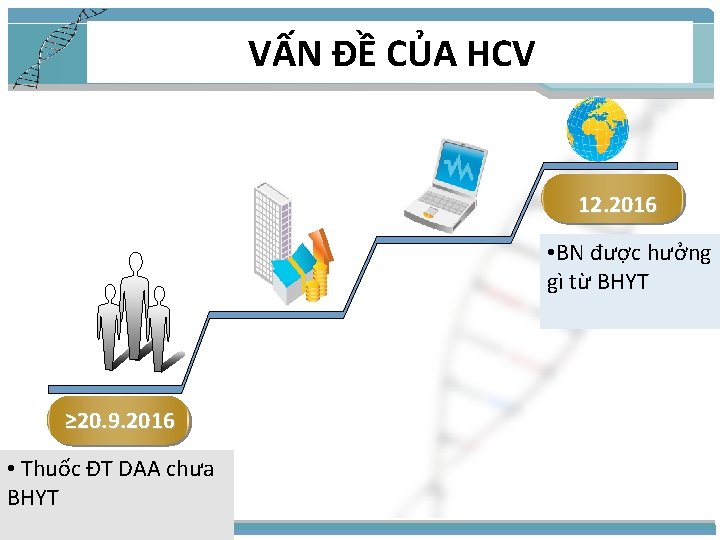
VẤN ĐỀ CỦA HCV 12. 2016 • BN được hưởng gì từ BHYT ≥ 20. 9. 2016 • Thuốc ĐT DAA chưa BHYT

ĐIỀU TRỊ VGSVC HIỆN NAY Nhiều thành tựu: virus, SHPT, Thuốc, TN LS KẾT LUẬN Thay đổi, kế thừa, liên tục, phát triển

ĐIỀU TRỊ VGSVC HIỆN NAY Có nên ĐT cho tất cả các đối tượng BN KẾT LUẬN Phác đồ nào là tối ưu Thời gian ĐT ± RBV

ĐIỀU TRỊ VGSVC HIỆN NAY Vấn đề kháng thuốc KẾT LUẬN Giải quyết như thế nào?



L/O/G/O CH N THÀNH CÁM ƠN