Logam Alkali Tanah Created by Arina Zahidah Ika

Logam Alkali Tanah

Created by: Arina Zahidah Ika Nur Syafitriani Tyas Widya Utami Fauzia Hanum Fadlillah Octa Noviari Zaenab Lubis Dania Clarisa Novarina Darmawan P Fadjar Fauzi R Fajar Rahasmoro

Definisi Logam Alkali Tanah Logam alkali tanah terdiri dari 6 unsur yang terdapat di golongan IIA. Yang termasuk ke dalam golongan II A yaitu : Berilium (Be), Magnesium (Mg), Calcium (Ca), Stronsium (Sr), Barium (Ba), dan Radium (Ra). Di sebut logam karena memiliki sifat seperti logam. Disebut alkali karena mempunyai sifat alkalin jika direaksikan dengan air. Dan istilah tanah karena oksidasinya sukar larut dalam air, dan banyak ditemukan dalam bebatuan di kerak bumi. Oleh sebab itu, istilah “alkali tanah” biasa digunakan untuk menggambarkan kelompok unsur golongan II A. Tiap logam memiliki konfigurasi elektron sama seperti gas mulia atau golongan VIII A, setelah di tambah 2 elektron pada lapisan kulit S paling luar. Contohnya konfigurasi elektron pada Magnesium (Mg) yaitu : 1 s 22 p 63 s 2 atau (Ne) 3 s 2. Ikatan yang dimiliki kebanyakan senyawa logam alkali tanah adalah ikatan ionik. Karena, elektron paling luarnya telah siap untuk di lepaskan, agar mencapai kestabilan. Unsur alkali tanah memiliki reaktifitas tinggi, sehingga tidak ditemukan dalam bentuk monoatomik , unsur ini mudah bereaksi dengan oksigen, dan logam murni yang ada di udara, membentuk lapisan luar pada oksigen.

Keberadaan Alkali Tanah di Alam Logam alkali tanah memilii sifat yang reaktif sehingga di alam hanya ditemukan dalam bentuk senyawanya. Berikut keberadaan senyawa yang mengandung logam alkali: • Berilium tidak begitu banyak terdapat di kerak bumi, bahkan hampir bisa dikatakan tidak ada. Sedangkan di alam berilium dapat bersenyawa menjadi Mineral beril [Be 3 Al 2(Si. O 6)3], dan Krisoberil [Al 2 Be. O 4]. • Magnesium berperingkat nomor 7 terbanyak yang terdapat di kerak bumi, dengan 1, 9% keberadaannya. Di alam magnesium bisa bersenyawa menjadi Magnesium Klorida [Mg. Cl 2], Senyawa Karbonat [Mg. CO 3], Dolomit [Mg. Ca(CO 3)2], dan Senyawa Epsomit [Mg. SO 4. 7 H 2 O] • Kalsium adalah logam alkali yang paling banyak terdapat di kerak bumi. Bahkan kalsium menjadi nomor 5 terbanyak yang terdapat di kerak bumi, dengan 3, 4% keberadaanya. Di alam kalsium dapat membentuk senyawa karbonat [Ca. CO 3], Senyawa Fospat [Ca. PO 4], Senyawa Sulfat [Ca. SO 4], Senyawa Fourida [Ca. F] • Stronsium berada di kerak bumi dengan jumlah 0, 03%. Di alam strontium dapat membuntuk senyawa Mineral Selesit [Sr. SO 4], dan Strontianit • Barium berada di kerak bumi sebanyak 0, 04%. Di alam barium dapat membentuk senyawa : Mineral Baritin [Ba. SO 4], dan Mineral Witerit [Ba. CO 3]

Cara Memperoleh Logam Alkali Tanah 1. Ekstraksi Berilium (Be) a. Metode reduksi Untuk mendapatkan Berilium, bisa didapatkan dengan mereduksi Be. F 2. Sebelum mendapatkan Be. F 2, kita harus memanaskan beril [Be 3 Al 2(Si. O 6)3] dengan Na 2 Si. F 6 hingga 700 0 C. Karena beril adalah sumber utama berilium. Be. F 2 + Mg Mg. F 2 + Be b. Metode Elektrolisis Untuk mendapatkan berilium juga kita dapat mengekstraksi dari lelehan Be. Cl 2 yang telah ditambah Na. Cl. Karena Be. Cl 2 tidak dapat mengahantarkan listrik dengan baik, sehingga ditambahkan Na. Cl. Reaksi yang terjadi adalah : Katoda : Be 2+ + 2 e- Be Anode : 2 Cl- Cl 2 + 2 e-

2. Ekstraksi Magnesium (Mg) a. Metode Reduksi Untuk mendapatkan magnesium kita dapat mengekstraksinya dari dolomit [Mg. Ca(CO 3)2] karena dolomite merupakan salah satu sumber yang dapat menhasilkan magnesium. Dolomite dipanaskan sehingga terbentuk Mg. O. Ca. O. lalu Mg. O. Ca. O. dipanaskan dengan Fe. Si sehingga menghasilkan Mg. 2[ Mg. O. Ca. O] + Fe. Si 2 Mg + Ca 2 Si. O 4 + Fe b. Metode Elektrolisis Selain dengan ekstraksi dolomite magnesium juga bisa didapatkan dengan mereaksikan air alut dengan Ca. O. Reaksi yang terjadi : Ca. O + H 2 O Ca 2+ + 2 OH Mg 2+ + 2 OH- Mg(OH)2 Selanjutnya Mg(OH)2 direaksikan dengan HCl Untuk membentuk Mg. Cl 2 Mg(OH)2 + 2 HCl Mg. Cl 2 + 2 H 2 O Setelah mendapatkan lelehan Mg. Cl 2 kita dapat mengelektrolisisnya untuk mendapatkan magnesium Katode : Mg 2+ + 2 e. Mg Anode : 2 Cl. Cl 2 + 2 e

3. Ekstraksi Kalsium (Ca) a. Metode Elektrolisis Batu kapur (Ca. CO 3) adalah sumber utama untuk mendapatkan kalsium (Ca). Untuk mendapatkan kalsium, kita dapat mereaksikan Ca. CO 3 dengan HCl agar terbentuk senyawa Ca. Cl 2. Reaksi yang terjadi : Ca. CO 3 + 2 HCl Ca. Cl 2 + H 2 O + CO 2 Setelah mendapatkan Ca. Cl 2, kita dapat mengelektrolisisnya agar mendapatkan kalsium (Ca). Reaksi yang terjadi : Katoda ; Ca 2+ + 2 e- Ca Anoda ; 2 Cl- Cl 2 + 2 e- b. Metode Reduksi Logam kalsium (Ca) juga dapat dihasilkan dengan mereduksi Ca. O oleh Al atau dengan mereduksi Ca. Cl 2 oleh Na. Reduksi Ca. O oleh Al 6 Ca. O + 2 Al 3 Ca + Ca 3 Al 2 O 6 Reduksi Ca. Cl 2 oleh Na Ca. Cl 2 + 2 Na Ca + 2 Na. Cl

4. Ekstraksi Strontium (Sr) Metode Elektrolisis Untuk mendapatkan Strontium (Sr), Kita bisa mendapatkannya dengan elektrolisis lelehan Sr. Cl 2. Lelehan Sr. Cl 2 bisa didapatkan dari senyawa selesit [Sr. SO 4]. Karena Senyawa selesit merupakan sumber utama Strontium (Sr). Reaksi yang terjadi ; katode ; Sr 2+ +2 e- Sr anoda ; 2 Cl- Cl 2 + 2 e-

5. Ekstraksi Barium (Ba) a. Metode Elektrolisis Barit (Ba. SO 4) adalah sumber utama untuk memperoleh Barium (Ba). Setelah diproses menjadi Ba. Cl 2 barium bisa diperoleh dari elektrolisis lelehan Ba. Cl 2. Reaksi yang terjadi : katode ; Ba 2+ +2 e- Ba anoda ; 2 Cl- Cl 2 + 2 e- b. Metode Reduksi Selain dengan elektrolisis, barium bisa kita peroleh dengan mereduksi Ba. O oleh Al. Reaksi yang terjadi : 6 Ba. O + 2 Al 3 Ba + Ba 3 Al 2 O 6.
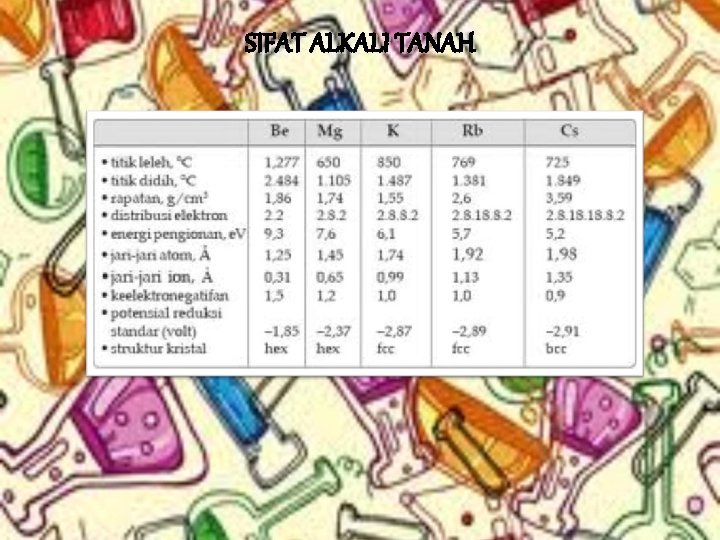
SIFAT ALKALI TANAH

Sifat Kimia Logam Alkali Tanah Sifat Kimia (reaksi-reaksi) unsur Alkali Tanah. 1. Reaksi dengan Air. Sifat reaksi dengan air dalam satu golongan dari atas ke bawah makin reaktif dan eksotermis (spt. gol I-A). Mg (s) + 2 H 2 O (l) → Mg(OH)2 (aq) + H 2 (g) , reaksinya lambat. Ca (s) + 2 H 2 O (l) → Ca(OH)2 (aq) + H 2 (g) , reaksi lebih cepat. Sr (s) + 2 H 2 O (l) → Sr(OH)2 (aq) + H 2 (g) , reaksi cepat. 2. Reaksi dengan Asam. Be (s) + HCl (aq) → Be. Cl 2 (aq) + H 2 (g) Mg (s) + H 2 SO 4 (aq) → Mg. SO 4 (aq) + H 2 (g) Ca (s) + HBr (aq) → Ca. Br 2 (aq) + H 2 (g) 3. Reaksi dengan basa, hanya Be sebagai logam amphoter yaitu : Be (s) + Na. OH (aq) → Na 2 Be. O 2 (aq) + H 2 (g) 4. Reaksi Logam Alkali Tanah ( M = Be s. d Ba ) dengan Udara. 2 M (s) + O 2 (g) → 2 MO (s) 3 M (s) + N 2 (g) → M 3 N 2 (s) 5. Reaksi Logam Alkali Tanah ( M ) dengan Halogen ( X 2 ). M (s) + X 2 (g) → MX 2 (s) Contoh : Mg (s) + Br 2 (g) → Mg. Br 2 (s) 6. Reaksi Logam Alkali Tanah ( M ) dengan Hidrogen ( H 2 ) M (s) + H 2 (g) → MH 2 (s) Contoh : Ca (s) + H 2 (g) → Ca. H 2 (s)

Kegunaan Logam Alkali Tanah

Berilium (Be) 1. Berilium digunakan untuk memadukan logam agar lebih kuat, akan tetapi bermasa lebih ringan. Biasanya paduan ini digunakan pada kemudi pesawat Zet. 2. Berilium digunakan pada kaca dari sinar X. 3. Berilium digunakan untuk mengontrol reaksi fisi pada reaktor nuklir 4. Campuran berilium dan tembaga banyak dipakai pada alat listrik, maka Berilium sangat penting sebagai komponen televisi. Magnesium (Mg) 1. Magnesium digunakan untuk memberi warna putih terang pada kembang api dan pada lampu Blitz. 2. Senyawa Mg. O dapat digunakan untuk melapisi tungku, karena senyawa Mg. O memiliki titik leleh yang tinggi. 3. Senyawa Mg(OH)2 digunakan dalam pasta gigi untuk mengurangi asam yang terdapat di mulut dan mencagah terjadinnya kerusakan gigi, sekaligus sebagai pencegah maag 4. Mirip dengan Berilium yang membuat campuran logam semakin kuat dan ringan sehingga biasa digunakan pada alat rumah tangga.

Kalsium (Ca) 1. Kalsium digunakan pada obatan, bubuk pengembang kue dan plastik. 2. Senyawa Ca. SO 4 digunakan untuk membuat Gips yang berfungsi untuk membalut tulang yang patah. 3. Senyawa Ca. CO 3 biasa digunakan untuk bahan bangunan seperti komponen semen dan cat tembok. Selain itu digunakan untuk membuat kapur tulis dan gelas. 4. Kalsium Oksida (Ca. O) dapat mengikat air pada Etanol karena bersifat dehidrator, dapat juga mengeringkan gas dan mengikat Karbondioksida pada cerobong asap. 5. Ca(OH)2 digunakan sebagai pengatur p. H air limbah dan juga sebagai sumber basa yang harganya relatif murah 6. Kalsium Karbida (Ca. C 2) disaebut juga batu karbit merupakan bahan untuk pembuatan gas asetilena (C 2 H 2) yang digunakan untuk pengelasan. 7. Kalsium banyak terdapat pada susu dan ikan teri yang berfungsi sebagai pembentuk tulang dan gigi. Stronsium (Sr) 1. Stronsium dalam senyawa Sr(NO 3)2 memberikan warna merah apabila digunakan untuk bahan kembang api. 2. Stronsium sebagai senyawa karbonat biasa digunakan dalam pembuatan kaca televisi berwarna dan komputer.

Barium (Ba) 1. Ba. SO 4 digunakan untuk memeriksa saluran pencernaan karena mampu menyerap sinar X 2. Ba. SO 4 digunakan sebagai pewarna pada plastic karena memiliki kerapatan yang tinggi dan warna terang. 3. Ba(NO 3)2 digunakan untuk memberikan warna hijau pada kembang api.

Dampak Pada Kehidupan Dapat menimbulkan terjadinya air sadah ü Kesadahan Air dapat menurunkan efisiensi dari deterjen dan sabun. ü Kesadahan Air dapat menyebabkan noda pada bahan pecah belah dan bahan flat. ü Kesadahan Air dapat menyebabkan bahan linen berubah pucat. ü Mineral Kesadahan Air dapat menyumbat semburan pembilas dan saluran air. ü Residu Kesadahan Air dapat melapisi elemen pemanas dan menurunkan efisiensi panas. ü Kesadahan Air dapat menciptakan biuh logam pada kamar mandi shower dan bathtubs.

Terima Kasih
- Slides: 17