LNERGIE LIBRE Thermochimie chapitre 4 Guy COLLIN 2014

L’ÉNERGIE LIBRE Thermochimie : chapitre 4 Guy COLLIN, 2014 -12 -29

Objectifs n n n G=H-TS n Dans une transformation, une partie seulement de l’énergie d’un système peut être utilisée, le produit T DS mesurant l’énergie inutilisable. On peut donc définir une fonction Énergie libre telle que DG = DH - T DS. Tout comme l’enthalpie, on ne peut connaître la valeur absolue de cette énergie libre. Comment varie cette fonction avec les paramètres habituels que sont la température et la pression.

Rappels n Dans le chapitre précédent, on a introduit brièvement la notion d’entropie S ainsi que celle de l’énergie utilisable G la fraction de la chaleur transformable en énergie. ou mieux : La variance d’un système (voir plus loin) est telle que u = C + 2 - j. Pour un système à un constituant, puisqu’il y a au moins une phase, la variance est de 2 : G=H-TS il faut déterminer deux paramètres pour déterminer le système. Ce sont la température et la pression. n
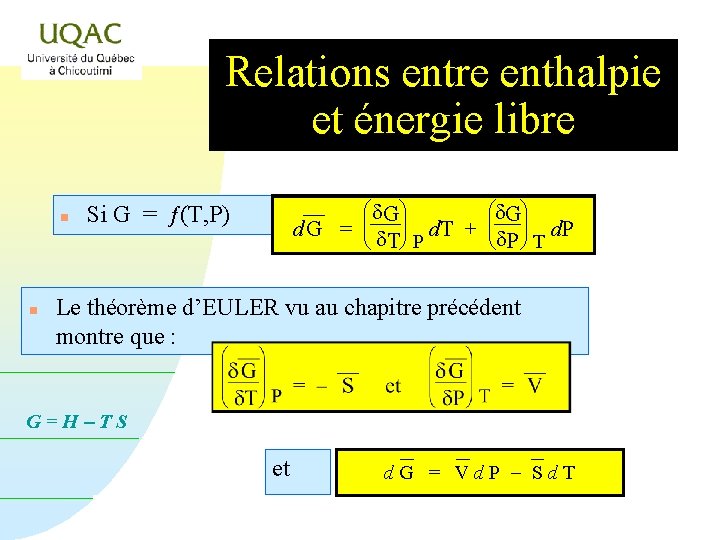
Relations entre enthalpie et énergie libre n n ¾ Si G = ƒ(T, P) d. G = æ d. G ö ç ÷ d è Tø P d. T + æd. Gö ç ÷ è d. P ø T d. P Le théorème d’EULER vu au chapitre précédent montre que : G=H-TS et d. G = Vd. P - Sd. T

Relations entre enthalpie et énergie libre DG = DH - T DS n On peut donc calculer pour une transformation donnée, la variation d’énergie libre si l’on connaît à la fois les variations correspondantes DH, DS et la température à laquelle a lieu cette transformation : d. G = Vd. P - Sd. T G=H-TS n La dernière formule permet d’atteindre le même résultat en connaissant DS et le volume molaire.
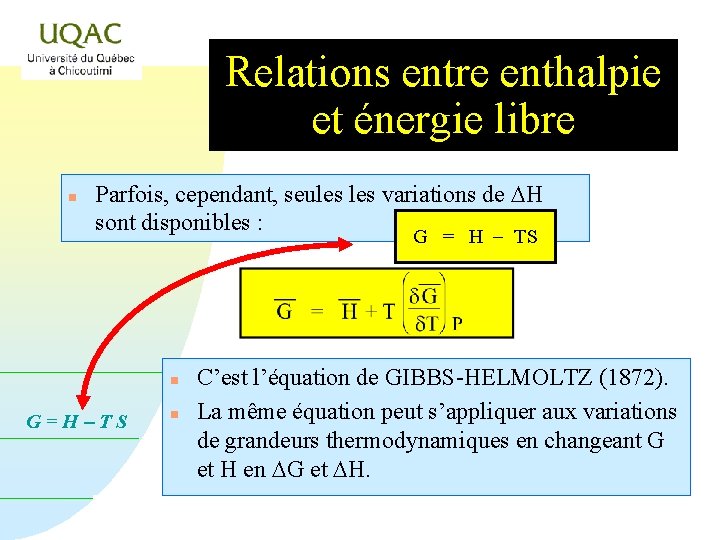
Relations entre enthalpie et énergie libre n Parfois, cependant, seules variations de DH sont disponibles : G = H - TS n G=H-TS n C’est l’équation de GIBBS-HELMOLTZ (1872). La même équation peut s’appliquer aux variations de grandeurs thermodynamiques en changeant G et H en DG et DH.
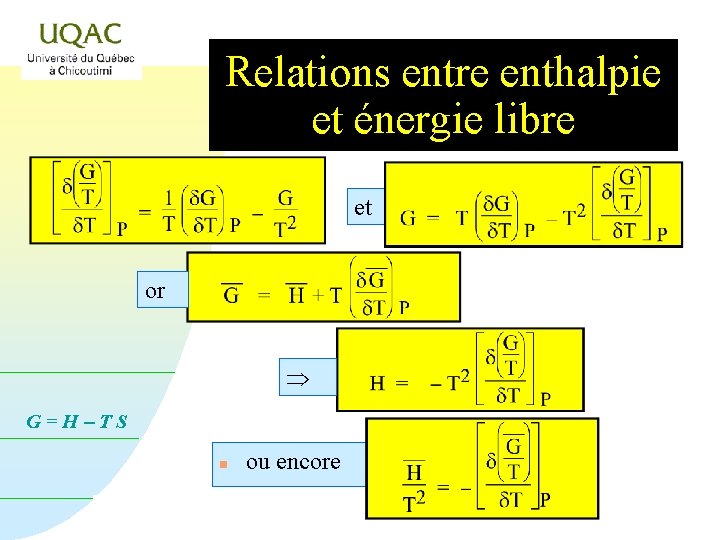
Relations entre enthalpie et énergie libre et or G=H-TS n ou encore
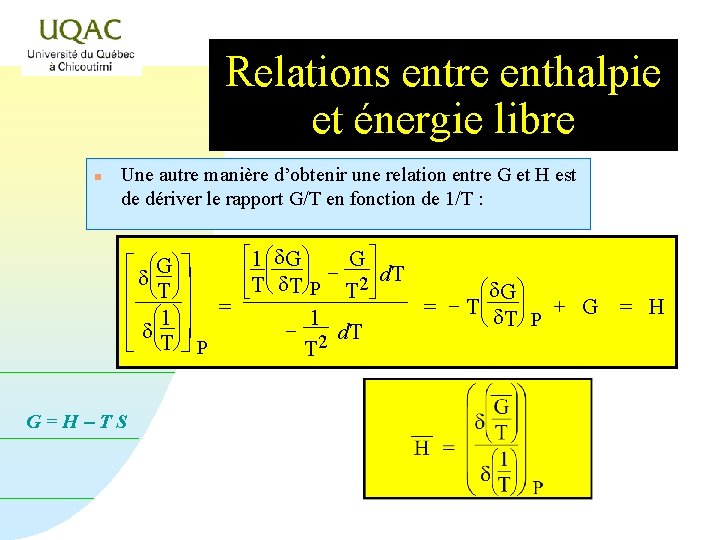
Relations entre enthalpie et énergie libre n Une autre manière d’obtenir une relation entre G et H est de dériver le rapport G/T en fonction de 1/T : é 1 æ d. G ö ù G ê ç ú é dæçG ö÷ ù ÷ êT è d T ø P ú d. T ê èTøú 2 æ d. G ö T û ë ÷ - Tç ê æ öú = = + G = H 1 1 è d. T ø P ê dç ÷ú d. T 2 ë èT ø û P T G=H-TS
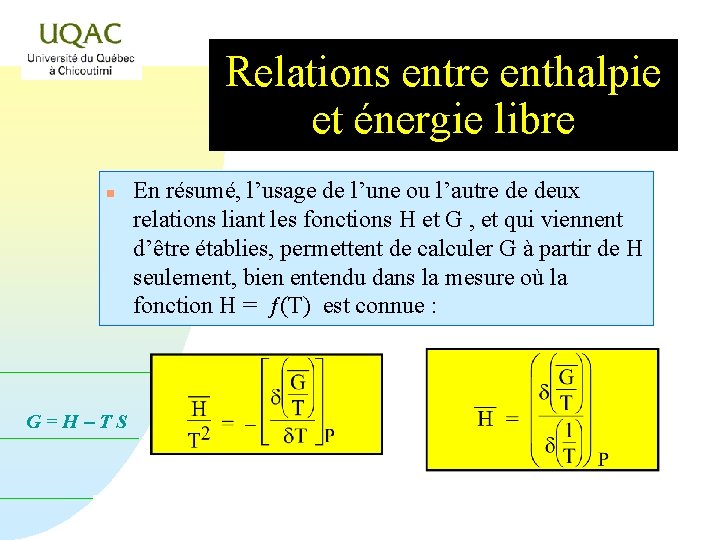
Relations entre enthalpie et énergie libre n G=H-TS En résumé, l’usage de l’une ou l’autre de deux relations liant les fonctions H et G , et qui viennent d’être établies, permettent de calculer G à partir de H seulement, bien entendu dans la mesure où la fonction H = ƒ(T) est connue :

Signification physique de DG n Compte tenu des conventions de signe, la variation de l’énergie libre, DG, permet de prévoir le sens d’une réaction : si DG < 0, la réaction peut avoir lieu dans le sens où elle est écrite. u si DG = 0, la réaction est à l’équilibre et, finalement, u si DG > 0, la réaction va dans le sens inverse où elle est écrite. u Il faut rappeler que si DG < 0, la réaction peut ne pas évoluer naturellement. En effet, si la thermodynamique prédit le sens G =d’une H - T réaction, S elle n’en prédit pas la vitesse. n Un cours de cinétique permet de calculer ces vitesses de réaction. n
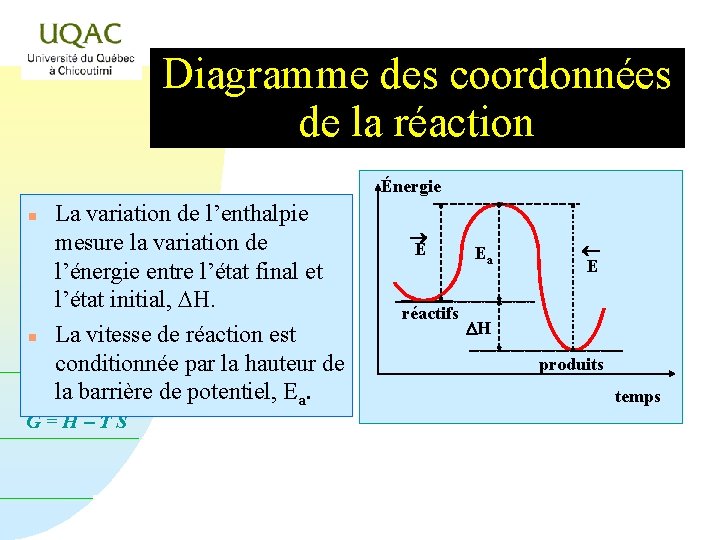
Diagramme des coordonnées de la réaction Énergie n n La variation de l’enthalpie mesure la variation de l’énergie entre l’état final et l’état initial, DH. La vitesse de réaction est conditionnée par la hauteur de la barrière de potentiel, Ea. G=H-TS ® E réactifs Ea ¬ E DH produits temps
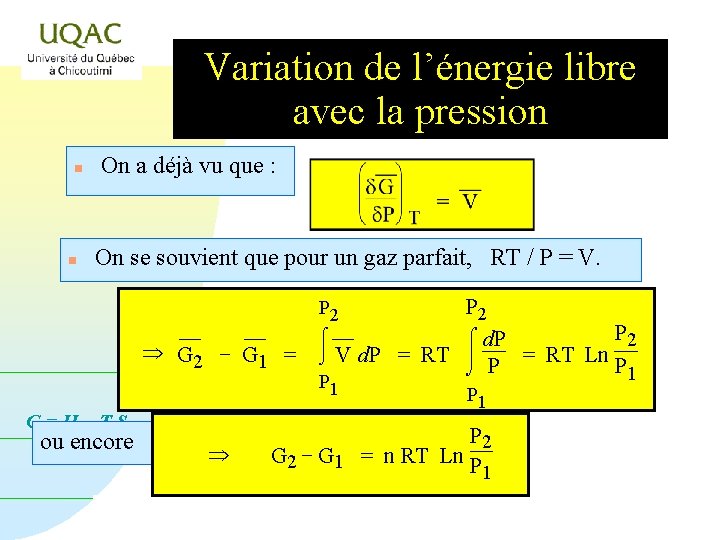
Variation de l’énergie libre avec la pression n n On a déjà vu que : On se souvient que pour un gaz parfait, RT / P = V. P 2 ó d. P ¾ ¾ ô ¾ G 2 - G 1 = ôõ V d. P = RT ô = RT Ln P 1 õ P P P 2 1 G=H-TS ou encore P 1 P 2 G 2 - G 1 = n RT Ln P 1

Tables d’énergie libre Tout comme pour l’enthalpie et l’entropie, on trouvera des tables d’énergie libre standard de formation des différents composés chimiques. n Notons que ces tables ne sont pas indispensables puisque si l’on disposent des tables correspondantes relatives à l’enthalpie et à l’entropie, on saura retrouver les valeurs G=H-TS de l’énergie libre standard de formation. n

Conclusion n Plusieurs relations mathématiques existent entre les fonctions enthalpie et énergie libre. La relation de GIBBS-HELMOLTZ et le théorème d’EULER permettent d’établir plusieurs de ces relations mathématiques. Le signe de la variation de l’énergie libre permet de connaître le sens naturelle d’une transformation : si DG < 0, la réaction peut avoir lieu dans le sens où elle est écrite; u si DG = 0, la réaction est à l’équilibre et, finalement, u si DG > 0, la réaction va dans le sens inverse où elle est écrite. G=H-TS u
- Slides: 14