LIRPOS URAC 30 L ARRIVEE DES BIOSIMILAIRES EN

LIRPOS – URAC 30 L’ ARRIVEE DES BIOSIMILAIRES EN RHUMATOLOGIE Pr Najia HAJJAJ-HASSOUNI Université Mohammed V Souissi –Faculté de Médecine et de Pharmacie- Rabat Hôpital El Ayachi – Salé – CHU Rabat-Salé Réunion Cooper Pharma – Casablanca, 19 juin 2014

Impact sur les enfants Altération de la qualité de vie 84% Retrait de l’école pour −raisons financières (garçons et filles) −s’occuper du parent malade (uniquement les filles) 36% 19% 17% Rkain H, Allali F, Jroundi I, Hajjaj-Hassouni N. Socioeconomic impact of rheumatoid arthritis in Morocco. Joint Bone Spine. 2006 May; 73(3): 278 -83

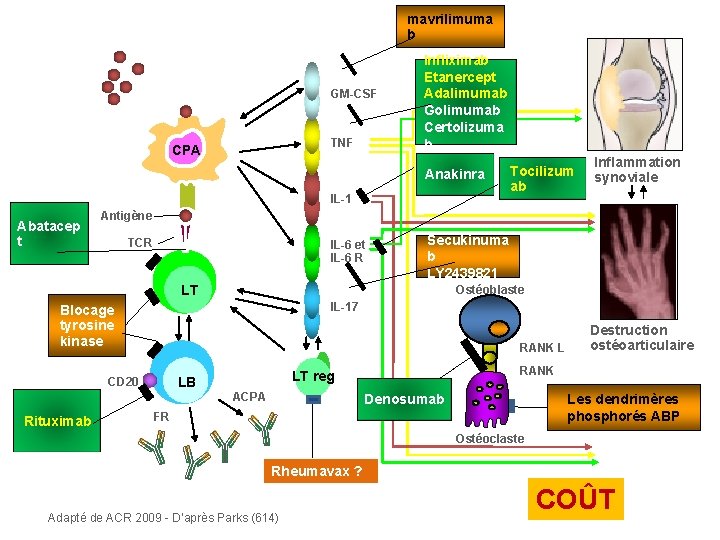
mavrilimuma b GM-CSF TNF CPA Infliximab Etanercept Adalimumab Golimumab Certolizuma b Anakinra IL-1 Abatacep t Inflammation synoviale Antigène TCR IL-6 et IL-6 R Secukinuma b LY 2439821 LT Ostéoblaste IL-17 Blocage tyrosine kinase RANK L ACPA Destruction ostéoarticulaire RANK LT reg LB CD 20 Rituximab Tocilizum ab Denosumab Les dendrimères phosphorés ABP FR Ostéoclaste Rheumavax ? Adapté de ACR 2009 - D’après Parks (614) COÛT

BIOSIMILAIRE ▪ Agence Nationale de Sécurité du Médicament et des Produits de Santé (ANSM) : www. ansm. fr Un médicament bio-similaire = similaire mais non strictement identique à un médicament biologique de référence qui a déjà été autorisé en Europe. ▪ European Medicines Agency (EMA) www. emaeuropa. eu A biosimilar is a biological medicinal product that contains a version of known biological active substance of an already authorized original medicinal product (reference medicinal product).

BIOSIMILARITÉ: LE CONCEPT ▪ “Très faible probabilité de différences cliniquement significatives” ▪ Principe essentiel de la comparaison de deux médicaments issus de la biotechnologie : – 1 er : Référence, commercialisé > 10 ans UE – 2ème : souhaite être déclaré « biosimilaire » au 1 er.

▪ Cette comparaison porte sur une analyse extensive des propriétés: – Physico-chimiques et biologiques (qualité) – Pharmacodynamiques, toxicologiques (sécurité) – Cliniques (efficacité et tolérance) CMC : Chemistry, Manufacturing, Control Les médicaments biosimilaires: Etat des lieux; Alexandre Moreau et al : Rapport de l’ANSM; Septembre 2013

GÉNÉRIQUE vs BIOSIMILAIRE GÉNÉRIQUE ▪ Synthèse chimique BIOSIMILAIRE ▪ Cellule vivante Lignée cellulaire unique provenant de bactérie ou mammaire Protéines recombinantes ▪ Structure définie et facile à caractériser ▪ Structure hétérogène, difficile à caractériser ▪ Relativement stable ▪ Variable ; Sensible aux conditions externes ▪ Habituellement per os ▪ Habituellement injecté ▪ Médecine Générale ▪ Spécialités ▪ Impuretés bien connues ▪ Profil des impuretés complexe ▪ AMM: sur la base de la bioéquivalence ▪ AMM : sur la base d'une équivalence de résultats thérapeutiques

Biosimilaires En théorie: ▪ Mêmes indications que le médicament de référence. Mais : ▪ Peuvent avoir moins d’indications que le médicament de référence ▪ faute d’études probantes d’efficacité et de sécurité dans l’indication concernée

Précautions à prendre ▪ Surveillance post-AMM au long cours par les autorités réglementaires et les cliniciens; Registres ▪ Plan de gestion du risque post-AMM; y compris les tests d'immunogénicité et de suivi de pharmacovigilance post-autorisation ▪ Substitution par le pharmacien non autorisée ▪ Interchangeabilité et switchs multiples non recommandés

▪ L’extrapolation des indications n’est permise qu’avec des résultats d’étude de qualité méthodologique irréprochable ▪ Il est important avant chaque prescription de vérifier le résumé des caractéristiques du produit (RCP) : Dose; Indications…. . ▪ Etiquettage : tout biosimilaire doit être identifiable, c'est à dire un nom de marque doit être utilisé et une DCI distincte doit être attribuée

Biosimilaires : Aspects Réglementaires ▪ EMA (European Medicines Agency) : ▪ 2004: 1ère base juridique établie par les autorités réglementaires UE ▪ 2005 puis 2013: actualisation ▪ 2009: adoptée par le comité d'experts standardisation biologique de l'OMS de la ▪ FDA: 2012 : élaboration des premiers guidelines. ▪ Plusieurs autres pays: des lignes directrices locales pour l'approbation des produits biosimilaires soit déjà adoptées ou en cours de discussion.

Guidelines Ac monoclonaux biosimilaires ▪ Etudes non cliniques ▪ Essais randomisés, double-aveugle versus biothérapie de référence – Démontrer la similarité clinique (non‐infériorité) – Dans la principale indication (population homogène) du médicament de référence – Données d’immunogénicité

• In-vitro analytical studies and in-vivo animal studies • The US Food and Drug Administration (FDA) requires that clinical studies must then show “that there are no clinically meaningful differences » between the biosimilar and the reference biopharmaceutical “ the safety, purity, and potency of the product ” Kay J, et al. Ann Rheum Dis October 2013 Vol 72 No 10
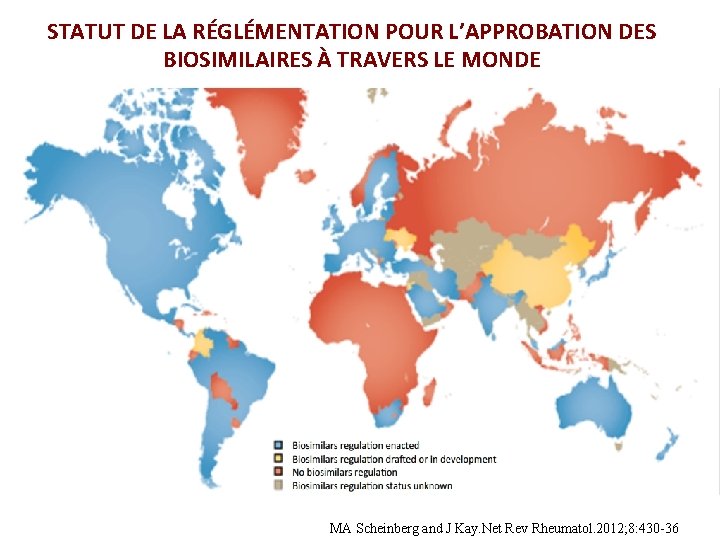
STATUT DE LA RÉGLÉMENTATION POUR L’APPROBATION DES BIOSIMILAIRES À TRAVERS LE MONDE MA Scheinberg and J Kay. Net Rev Rheumatol. 2012; 8: 430 -36

SITUATION AU MAROC ▪AMM: ↑ des dépôts de dossiers issus de la biotechnologie ▪Produits importés qui ont déjà l’AMM dans le pays d’origine ▪Textes d’application en cours d’élaboration (code de la pharmacie 17/04) ▪Article 2 : définit la spécialité générique ▪Article 12 : modalités de constitution de demande AMM Youssef KHAYATI. Chef du Service de l’Assurance Qualité - Laboratoire National de Contrôle des Médicaments Direction du Médicament et de la Pharmacie - 4ème Journée Pharmaceutique de Mohammedia 25/04/2009

Biosimilaires - Etats des lieux en Europe Depuis 2006, 14 biosimilaires autorisés et commercialisés dans l’UE Principalement 3 références: 1. Hormone de croissance : Somatropine : Omnitrope®, Valtropin® 2. Facteurs de croissance: Granulocyte-Colony Stimulating Factor : r-met. Hu. G-CSF: Filgrastim (Biograstim®, Filgrastim Hexal®, Filgrastim ratiopharm®, Nivestim®, Ratiograstim®, Tevagrastim®, Zarzio®…) • Erythropoïétines : Epoïétine (Abseamed®, Binocrit®, Epoetin alfa Hexal®, Retacrit®, Silapo®)
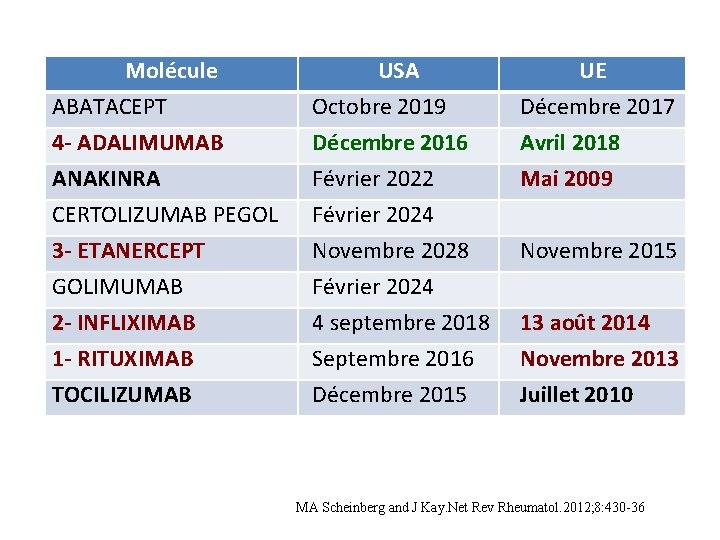
Molécule USA UE ABATACEPT 4 - ADALIMUMAB ANAKINRA CERTOLIZUMAB PEGOL 3 - ETANERCEPT GOLIMUMAB 2 - INFLIXIMAB 1 - RITUXIMAB TOCILIZUMAB Octobre 2019 Décembre 2016 Février 2022 Février 2024 Novembre 2028 Février 2024 4 septembre 2018 Septembre 2016 Décembre 2015 Décembre 2017 Avril 2018 Mai 2009 Novembre 2015 13 août 2014 Novembre 2013 Juillet 2010 MA Scheinberg and J Kay. Net Rev Rheumatol. 2012; 8: 430 -36
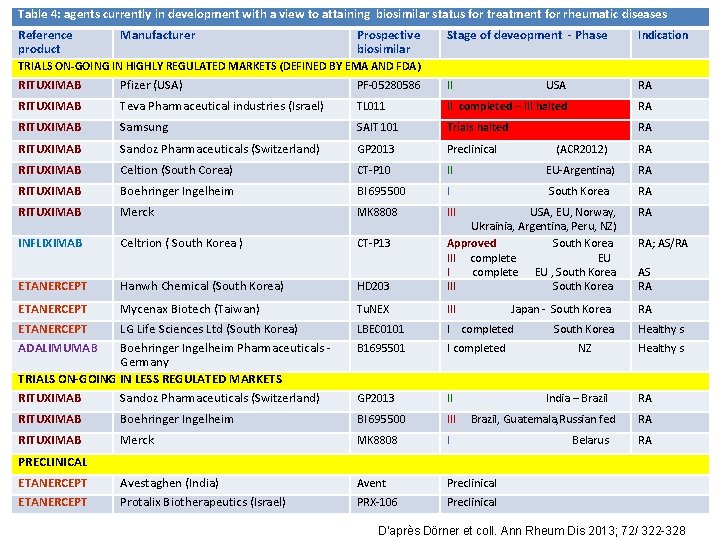
Table 4: agents currently in development with a view to attaining biosimilar status for treatment for rheumatic diseases Reference product Manufacturer Prospective biosimilar Stage of deveopment - Phase Indication TRIALS ON-GOING IN HIGHLY REGULATED MARKETS (DEFINED BY EMA AND FDA) RITUXIMAB Pfizer (USA) PF-05280586 II USA RA RITUXIMAB Teva Pharmaceutical industries (Israel) TL 011 II completed – III halted RA RITUXIMAB Samsung SAIT 101 Trials halted RA RITUXIMAB Sandoz Pharmaceuticals (Switzerland) GP 2013 Preclinical RITUXIMAB Celtion (South Corea) CT-P 10 RITUXIMAB Boehringer Ingelheim RITUXIMAB (ACR 2012) RA II EU-Argentina) RA BI 695500 I South Korea RA Merck MK 8808 III INFLIXIMAB Celtrion ( South Korea ) CT-P 13 ETANERCEPT Hanwh Chemical (South Korea) RA HD 203 USA, EU, Norway, Ukrainia, Argentina, Peru, NZ) Approved South Korea III complete EU , South Korea III South Korea Mycenax Biotech (Taiwan) LG Life Sciences Ltd (South Korea) Boehringer Ingelheim Pharmaceuticals Germany TRIALS ON-GOING IN LESS REGULATED MARKETS RITUXIMAB Sandoz Pharmaceuticals (Switzerland) Tu. NEX III RA LBEC 0101 I completed B 1695501 I completed GP 2013 II RITUXIMAB Boehringer Ingelheim BI 695500 III RITUXIMAB Merck MK 8808 I Avestaghen (India) Protalix Biotherapeutics (Israel) Avent Preclinical PRX-106 Preclinical ETANERCEPT ADALIMUMAB Japan - South Korea RA; AS/RA AS RA South Korea Healthy s NZ Healthy s India – Brazil, Guatemala, Russian fed Belarus RA RA RA PRECLINICAL ETANERCEPT D’après Dörner et coll. Ann Rheum Dis 2013; 72/ 322 -328
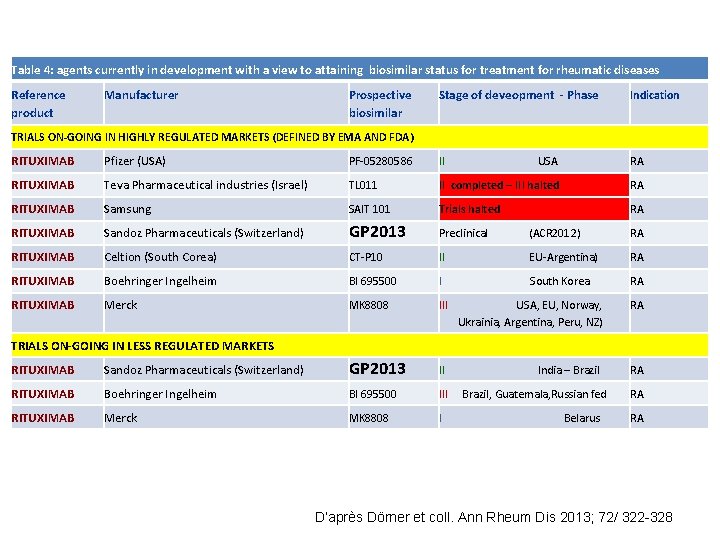
Table 4: agents currently in development with a view to attaining biosimilar status for treatment for rheumatic diseases Reference product Manufacturer Prospective biosimilar Stage of deveopment - Phase Indication TRIALS ON-GOING IN HIGHLY REGULATED MARKETS (DEFINED BY EMA AND FDA) RITUXIMAB Pfizer (USA) PF-05280586 II USA RA RITUXIMAB Teva Pharmaceutical industries (Israel) TL 011 II completed – III halted RA RITUXIMAB Samsung SAIT 101 Trials halted RA RITUXIMAB Sandoz Pharmaceuticals (Switzerland) GP 2013 Preclinical (ACR 2012) RA RITUXIMAB Celtion (South Corea) CT-P 10 II EU-Argentina) RA RITUXIMAB Boehringer Ingelheim BI 695500 I South Korea RA RITUXIMAB Merck MK 8808 III USA, EU, Norway, Ukrainia, Argentina, Peru, NZ) RA India – Brazil RA TRIALS ON-GOING IN LESS REGULATED MARKETS RITUXIMAB Sandoz Pharmaceuticals (Switzerland) GP 2013 II RITUXIMAB Boehringer Ingelheim BI 695500 III RITUXIMAB Merck MK 8808 I Brazil, Guatemala, Russian fed Belarus RA RA D’après Dörner et coll. Ann Rheum Dis 2013; 72/ 322 -328
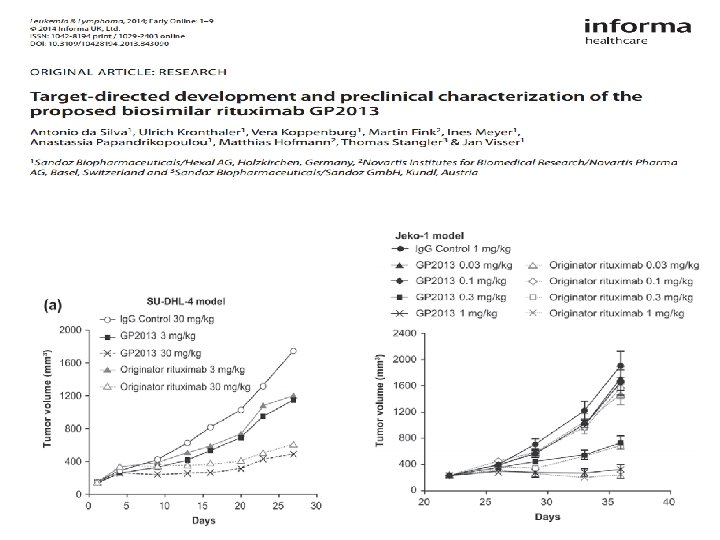
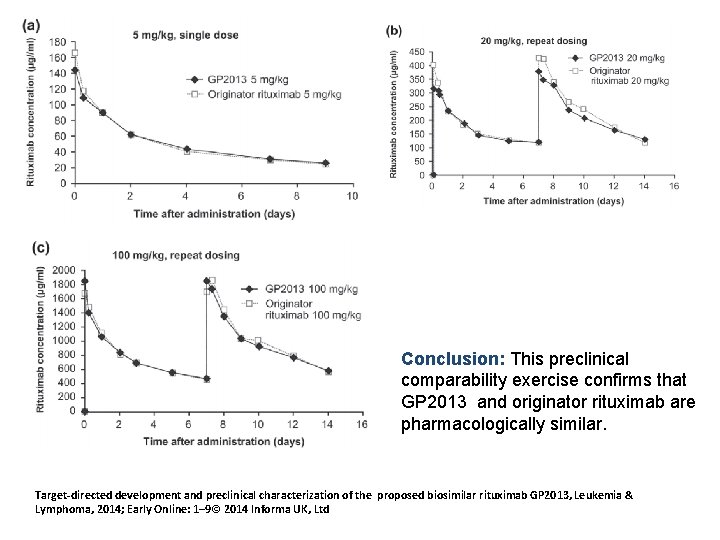
Conclusion: This preclinical comparability exercise confirms that GP 2013 and originator rituximab are pharmacologically similar. Target-directed development and preclinical characterization of the proposed biosimilar rituximab GP 2013, Leukemia & Lymphoma, 2014; Early Online: 1– 9© 2014 Informa UK, Ltd
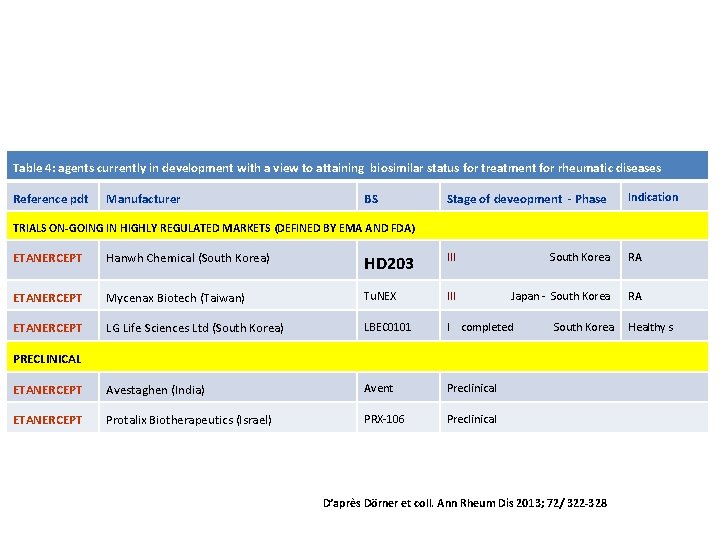
Table 4: agents currently in development with a view to attaining biosimilar status for treatment for rheumatic diseases Reference pdt Manufacturer BS Stage of deveopment - Phase Indication TRIALS ON-GOING IN HIGHLY REGULATED MARKETS (DEFINED BY EMA AND FDA) ETANERCEPT Hanwh Chemical (South Korea) HD 203 III South Korea RA ETANERCEPT Mycenax Biotech (Taiwan) Tu. NEX III Japan - South Korea RA ETANERCEPT LG Life Sciences Ltd (South Korea) LBEC 0101 I completed ETANERCEPT Avestaghen (India) Avent Preclinical ETANERCEPT Protalix Biotherapeutics (Israel) PRX-106 Preclinical South Korea PRECLINICAL D’après Dörner et coll. Ann Rheum Dis 2013; 72/ 322 -328 Healthy s

Bio. Drugs June 2012, Volume 26, Issue 3, pp 177 -184 • Etude Randomisée en double aveugle en 2 périodes et 2 séquences • Phase III • 37 volontaires sains • Objectif : comparaison de la pharmacocinétique de Enbrel et HD 203 • 25 mg : S/C • 48 h de l’injection ; prélèvements sanguins • Concentrations sériques des produits : dosage immuno-enzymatique
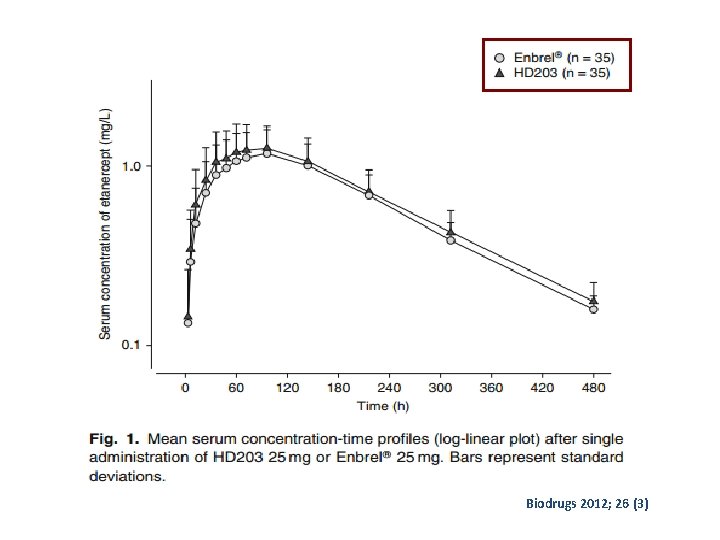
Biodrugs 2012; 26 (3)
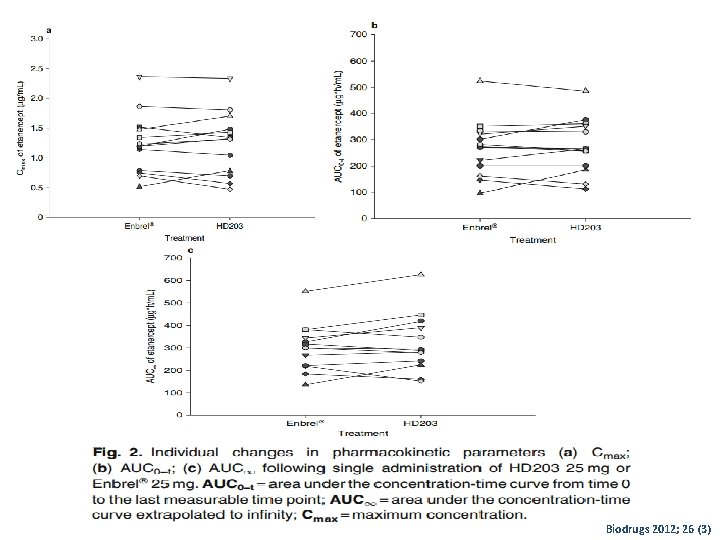
Biodrugs 2012; 26 (3)
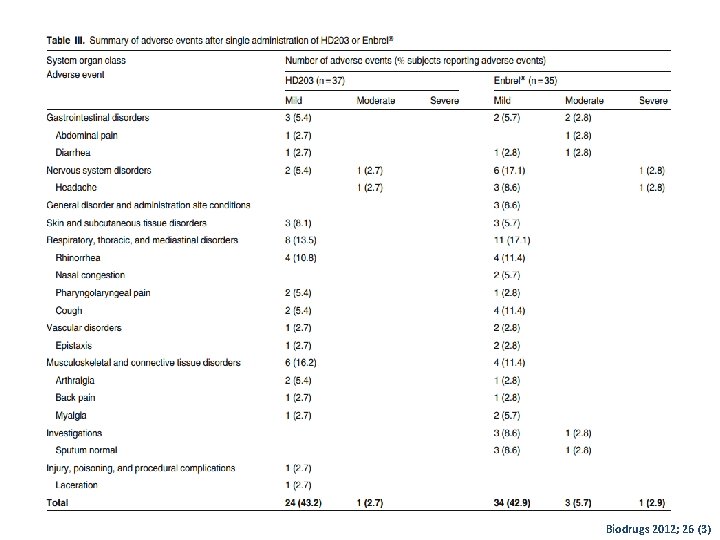
Biodrugs 2012; 26 (3)
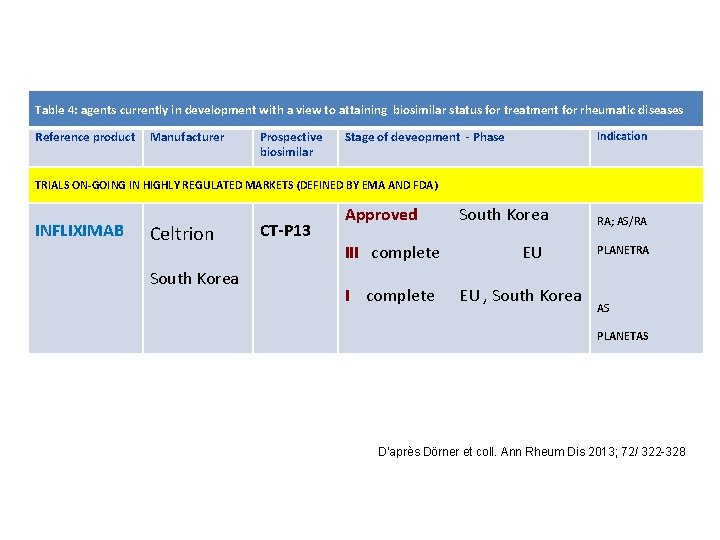
Table 4: agents currently in development with a view to attaining biosimilar status for treatment for rheumatic diseases Reference product Manufacturer Prospective biosimilar Stage of deveopment - Phase Indication TRIALS ON-GOING IN HIGHLY REGULATED MARKETS (DEFINED BY EMA AND FDA) INFLIXIMAB Celtrion South Korea CT-P 13 Approved III complete South Korea EU EU , South Korea RA; AS/RA PLANETRA AS PLANETAS D’après Dörner et coll. Ann Rheum Dis 2013; 72/ 322 -328
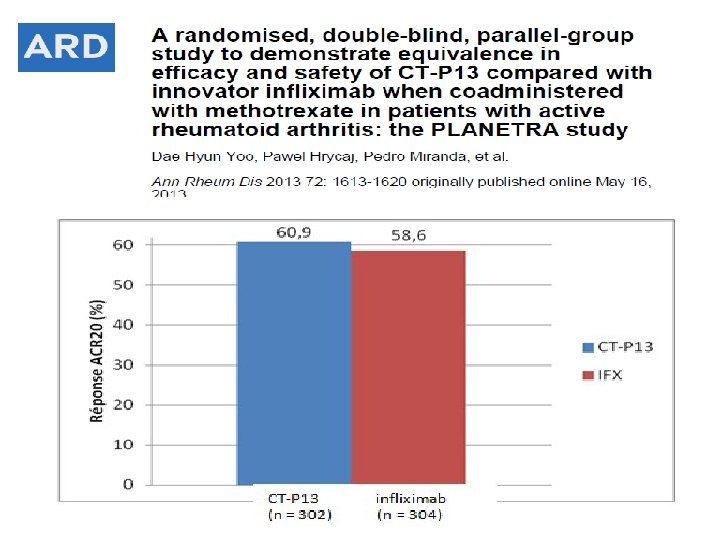
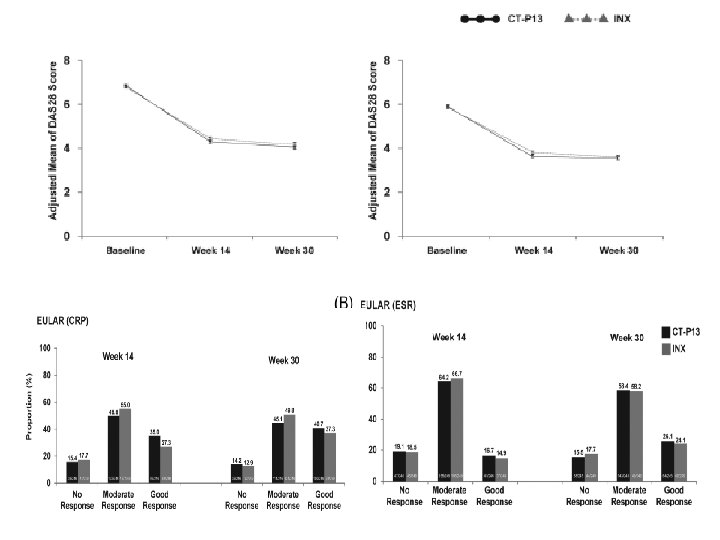

Tolérance apparaît tout à fait comparable: ▪ Les réactions aux perfusions : 5% des patients traités par CT-P 13 Vs 5, 6% des patients traités par IFX. ▪ L’études d’immunogénicité à la semaine 30: 40, 2% de patients sous CT-P 13 ont développé des anticorps antibiomédicament vs 39, 9% sous IFX. Ann Rheum Dis 2013 72: 1613 -1620 originally published online May 16, 2013

HOSPIRA CELTRION

Copies des AC monoclonaux commercialisés non approuvés par l’EMA/ FDA http: //www. biosimilarnews. com/indian-biosimilars-market

Quelle est la perception des rhumatologues? Value in Health, 16, 7, A 388 -A 389, 2013 ▪ But: Evaluer la perception des biosimilaires par 173 rhumatologues et la probabilité d’utilisation de ces produits dans la Polyarthrite Rhumatoïde

Value in Health, 16, 7, A 388 -A 389, 2013 ▪ Résultats − 47% prêts à prescrire …à quelques malades au début − 5 facteurs pouvant empêcher la prescription: • Doute sur la similarité avec la molécule de référence • Manque de données (sécurité , profil d’efficacité) • Manque de données sur le long terme • Défaut de guidelines nationaux sur l’utilisation des biosimilaires • Manque de données par pays

Conclusion ▪ Un biosimilaire est «un produit biothérapeutique qui est similaire en termes de qualité, sécurité et efficacité à un biothérapeutique de référence déjà autorisé » ▪ Le marché des biosimilaires est un marché prometteur: 2018: 40% du marché des biologiques UE ▪ La sécurité des patients doit rester la préoccupation principale lors de l'élaboration, l'évaluation et l'approbation d'un médicament biosimilaire ▪ Les biologiques qu’ils soient princeps ou biosimilaires : difficiles à utiliser et gérer

• Plusieurs questions à poser : − Simplification de l’arsenal thérapeutique ou, au contraire, allonger la liste des médicaments admis ? − Plus grande facilité d’utilisation ? − Prix < médicaments de référence? − Baisse attendue de 30% qui entrainerait également une baisse du biologique de référence ? − Positions des cliniciens, des patients, du comité économique des produits de santé ? Attitude scientifique et sécuritaire

RA national campaign movie. mpg
- Slides: 39