Ligao Qumica RPECV TLV TOM Paula Melo Silva















- Slides: 36

Ligação Química RPECV – TLV - TOM Paula Melo Silva

Ligação Química RPECV – Repulsão dos Pares Eletrónicos da Camada de Valência TLV – Teoria da Ligação de Valência (TEV) TOM – Teoria das orbitais moleculares

Gilbert Newton Lewis (1875 - 1946) Regra do Octeto (válida apenas para elementos do 2º Período) Os átomos tendem a formar ligações até ficarem rodeados de oito eletrões de valência, por forma a adquirirem uma configuração de gás nobre, de particular estabilidade.

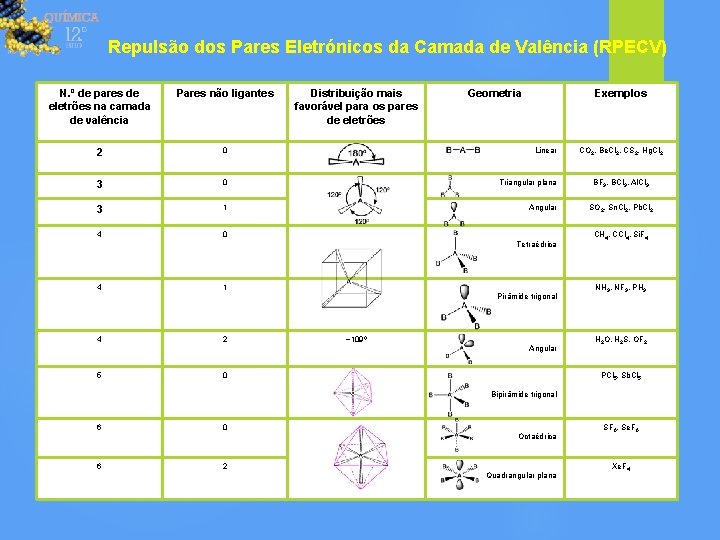
Repulsão dos Pares Eletrónicos da Camada de Valência (RPECV) N. º de pares de eletrões na camada de valência Pares não ligantes Distribuição mais favorável para os pares de eletrões Geometria Exemplos 2 0 Linear 3 0 Triangular plana 3 1 Angular 4 0 Tetraédrica 4 1 Pirâmide trigonal 4 2 ~109º Angular 5 0 CO 2, Be. Cl 2, CS 2, Hg. Cl 2 BF 3, BCl 3, Al. Cl 3 SO 2, Sn. Cl 2, Pb. Cl 2 CH 4, CCl 4, Si. F 4 NH 3, NF 3, PH 3 H 2 O, H 2 S, OF 2 PCl 5, Sb. Cl 5 Bipirâmide trigonal 6 0 Octaédrica 6 2 Quadrangular plana SF 6, Se. F 6 Xe. F 4

Teoria da ligação de valência (TLV) Dois átomos aproximam-se um do outro até que as suas orbitais coalescem (Sobreposição). Orbital 1 s atómica Ligação s (sigma)

Teoria da ligação de valência (TLV) Ligação s (sigma). Da coalescência de duas orbitais s ou px (considerando a aproximação dos dois átomos ao longo do eixo dos xx, estas últimas coalescem de topo), formar -se-á uma nuvem eletrónica de simetria cilíndrica em torno do eixo internuclear, designando-se a ligação formada por ligação s (sigma). Orbital 2 px atómica Ligação s (sigma)

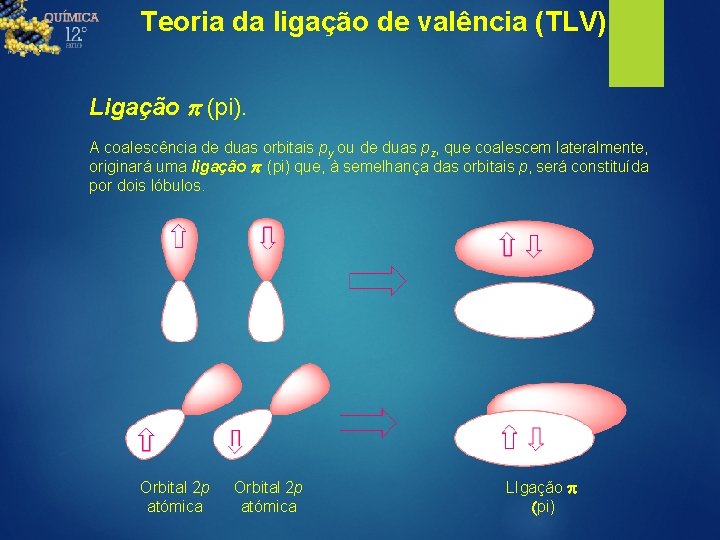
Teoria da ligação de valência (TLV) Ligação p (pi). A coalescência de duas orbitais py ou de duas pz, que coalescem lateralmente, originará uma ligação p (pi) que, à semelhança das orbitais p, será constituída por dois lóbulos. Orbital 2 p atómica LIgação p (pi)

Teoria da ligação de valência (TLV) Uma ligação s é mais forte do que uma p, em virtude de a coalescência de topo ser superior à coalescência lateral – critério da coalescência máxima. Ao somatório das ligações s e p que se estabelecem entre dois átomos, chama-se multiplicidade da ligação.

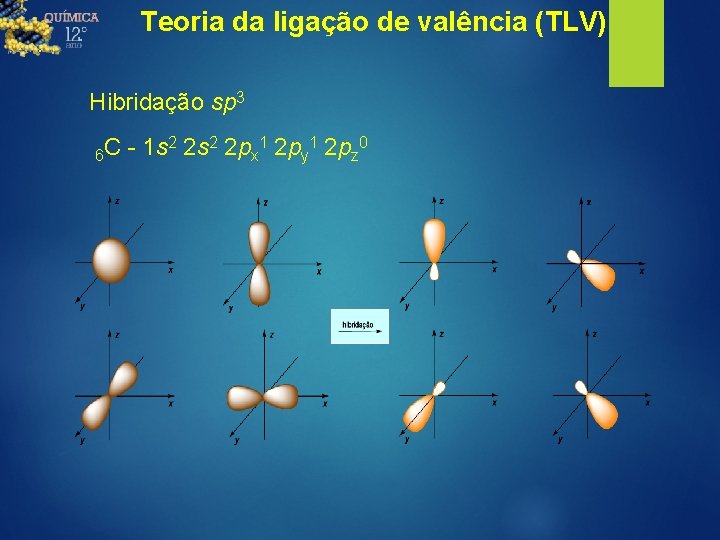
Teoria da ligação de valência (TLV) Hibridação sp 3 2 2 s 2 2 p 1 2 p 0 C 1 s 6 x y z Uma orbital s e três orbitais p, produzem uma hibridação sp 3 hibridação s p sp 3

Teoria da ligação de valência (TLV) Hibridação sp 3 2 2 s 2 2 p 1 2 p 0 C 1 s 6 x y z

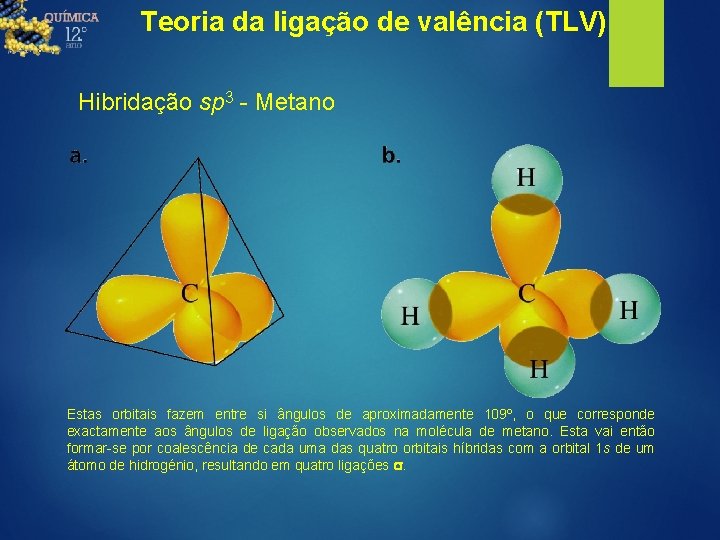
Teoria da ligação de valência (TLV) Hibridação sp 3 - Metano Estas orbitais fazem entre si ângulos de aproximadamente 109º, o que corresponde exactamente aos ângulos de ligação observados na molécula de metano. Esta vai então formar-se por coalescência de cada uma das quatro orbitais híbridas com a orbital 1 s de um átomo de hidrogénio, resultando em quatro ligações s.

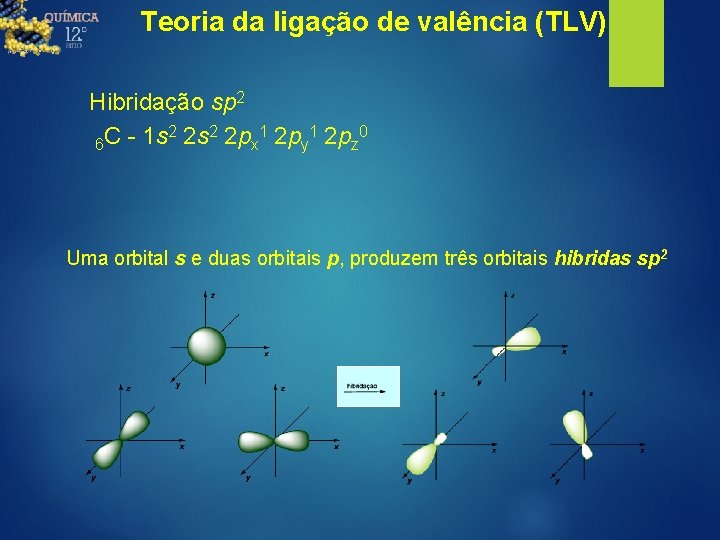
Teoria da ligação de valência (TLV) Hibridação sp 2 2 2 1 1 0 6 C - 1 s 2 s 2 px 2 py 2 pz Uma orbital s e duas orbitais p, produzem a hibridação sp 2 hibridação s p sp 2 p

Teoria da ligação de valência (TLV) Hibridação sp 2 2 2 1 1 0 6 C - 1 s 2 s 2 px 2 py 2 pz Uma orbital s e duas orbitais p, produzem três orbitais hibridas sp 2

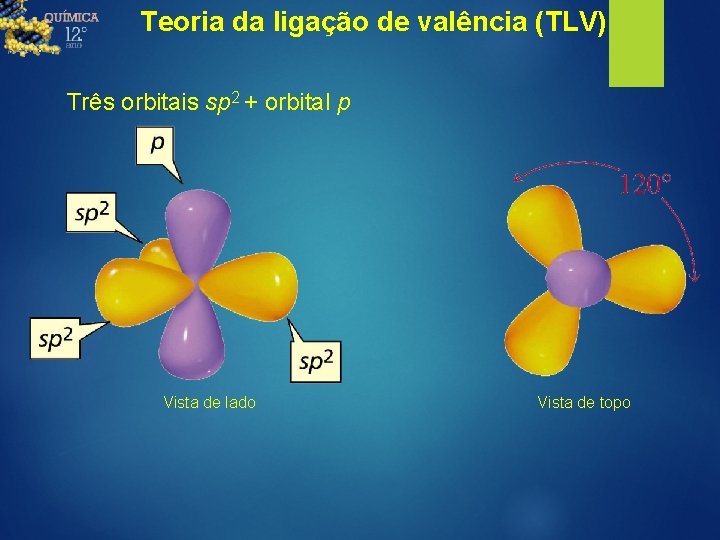
Teoria da ligação de valência (TLV) Três orbitais sp 2 + orbital p Vista de lado Vista de topo

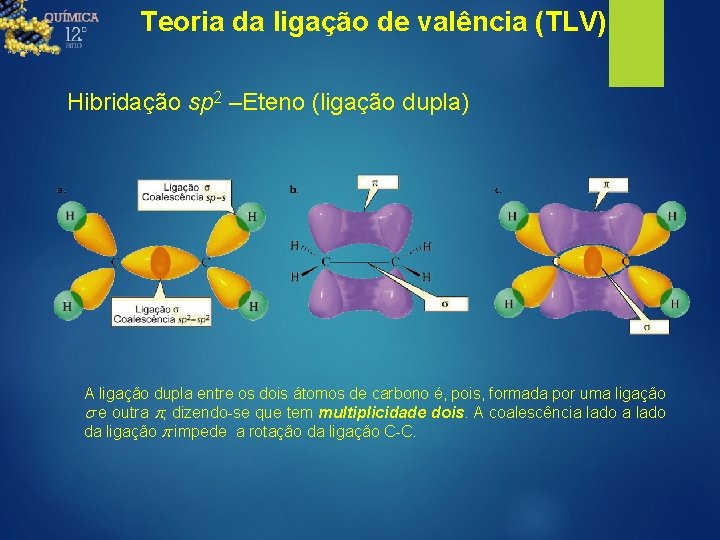
Teoria da ligação de valência (TLV) Hibridação sp 2 –Eteno (ligação dupla) A ligação dupla entre os dois átomos de carbono é, pois, formada por uma ligação s e outra p, dizendo-se que tem multiplicidade dois. A coalescência lado da ligação p impede a rotação da ligação C-C.

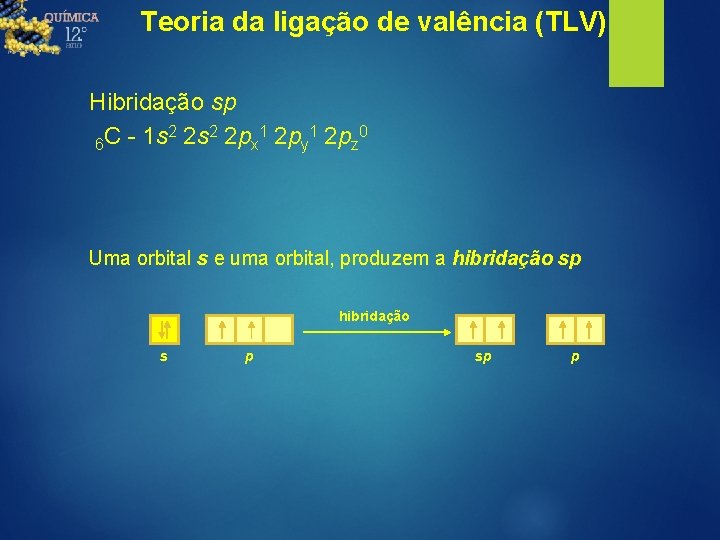
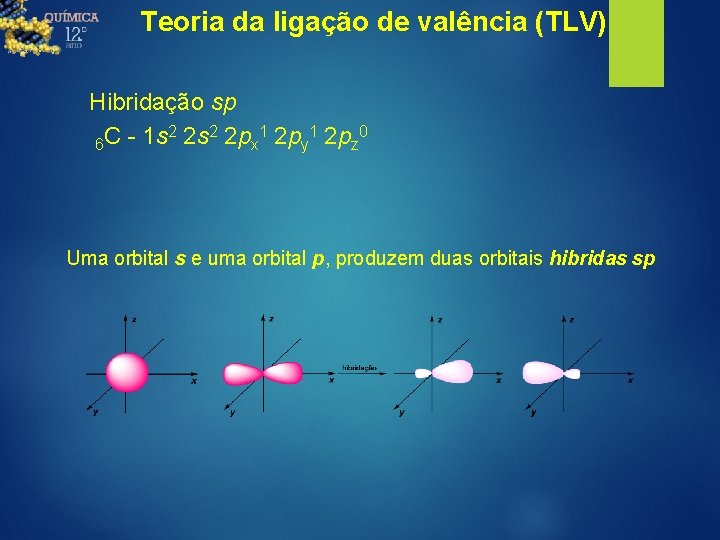
Teoria da ligação de valência (TLV) Hibridação sp 2 2 1 1 0 6 C - 1 s 2 s 2 px 2 py 2 pz Uma orbital s e uma orbital, produzem a hibridação sp hibridação s p sp p

Teoria da ligação de valência (TLV) Hibridação sp 2 2 1 1 0 6 C - 1 s 2 s 2 px 2 py 2 pz Uma orbital s e uma orbital p, produzem duas orbitais hibridas sp

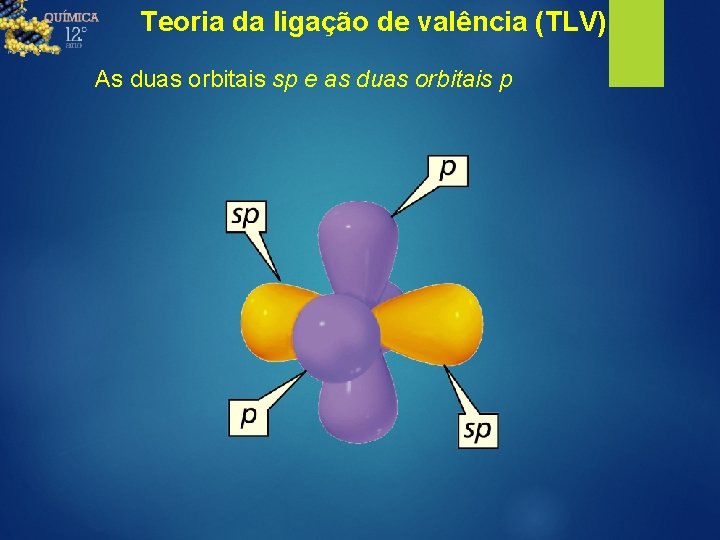
Teoria da ligação de valência (TLV) As duas orbitais sp e as duas orbitais p

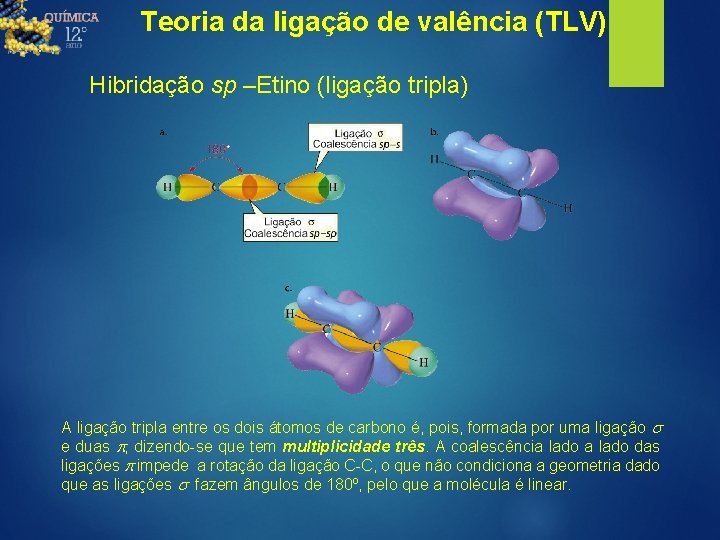
Teoria da ligação de valência (TLV) Hibridação sp –Etino (ligação tripla) A ligação tripla entre os dois átomos de carbono é, pois, formada por uma ligação s e duas p, dizendo-se que tem multiplicidade três. A coalescência lado das ligações p impede a rotação da ligação C-C, o que não condiciona a geometria dado que as ligações s fazem ângulos de 180º, pelo que a molécula é linear.

Teoria das Orbitais Moleculares (TOM) Segundo a Teoria das Orbitais Moleculares, a sobreposição de duas orbitais atómicas leva à formação de duas orbitais moleculares: uma orbital molecular ligante (s ou p), de menor energia, e uma orbital molecular antiligante (s* ou p*), de maior energia. Quando as orbitais que se combinam são s ou px (considerando a aproximação dos átomos segundo o eixo xx), as orbitais moleculares obtidas designam-se sigma (s), enquanto que da combinação das orbitais atómicas py e pz, resulta a formação de orbitais moleculares p.

Teoria das Orbitais Moleculares (TOM) Ordem da Ligação Os eletrões das orbitais moleculares ligantes (s ou p) são eletrões ligantes e os das orbitais moleculares antiligantes (s* ou p*) são eletrões antiligantes. A diferença entre os eletrões ligantes e os electrões antiligantes dá-nos o número de eletrões efetivamente ligantes. Aqueles cujo efeito é mutuamente anulado chamam-se eletrões não-ligantes.

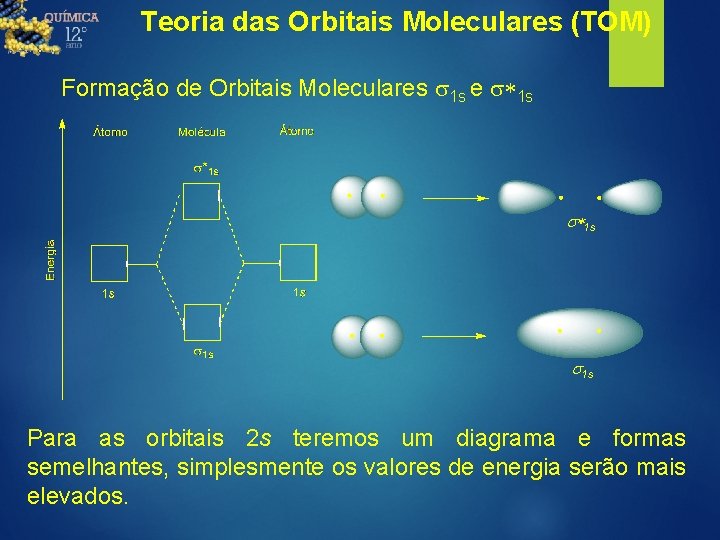
Teoria das Orbitais Moleculares (TOM) Formação de Orbitais Moleculares s 1 s e s*1 s s 1 s Para as orbitais 2 s teremos um diagrama e formas semelhantes, simplesmente os valores de energia serão mais elevados.

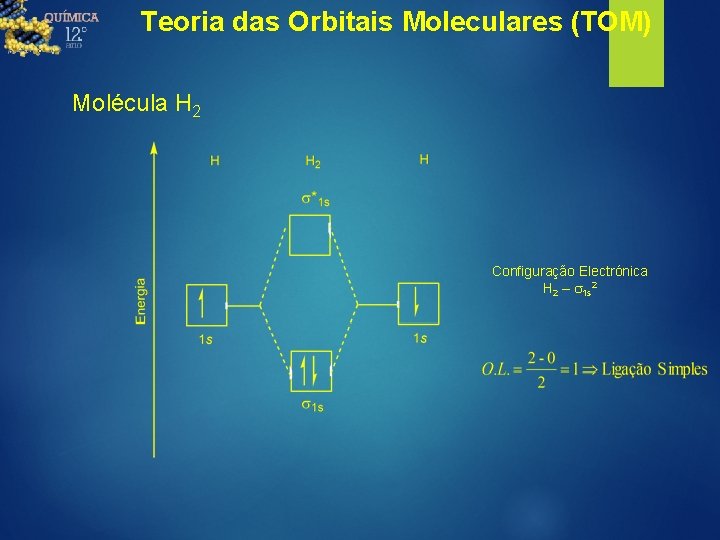
Teoria das Orbitais Moleculares (TOM) Molécula H 2 Configuração Electrónica H 2 – s 1 s 2

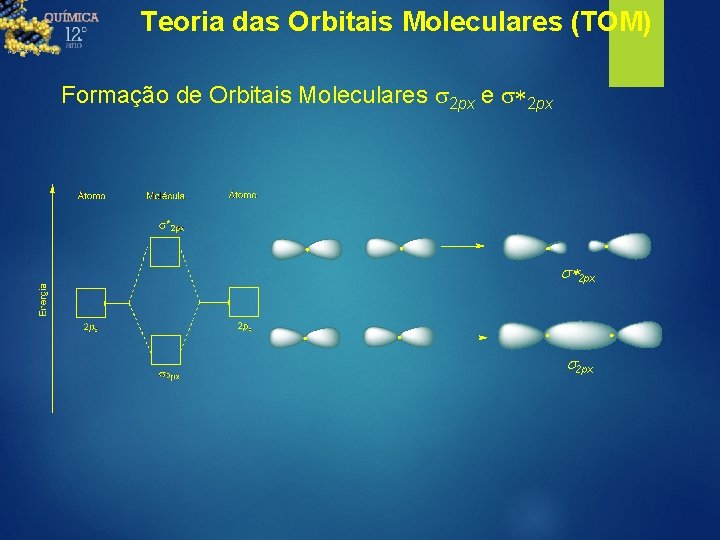
Teoria das Orbitais Moleculares (TOM) Formação de Orbitais Moleculares s 2 px e s*2 px s 2 px

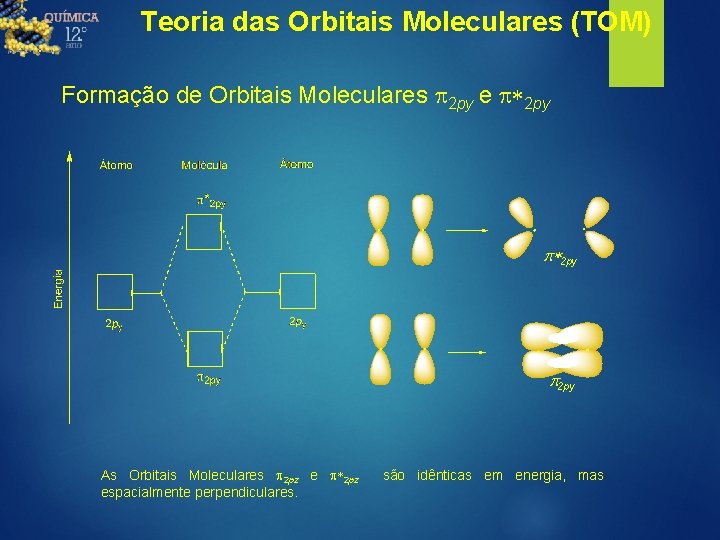
Teoria das Orbitais Moleculares (TOM) Formação de Orbitais Moleculares p 2 py e p*2 py p 2 py As Orbitais Moleculares p 2 pz e p*2 pz espacialmente perpendiculares. são idênticas em energia, mas

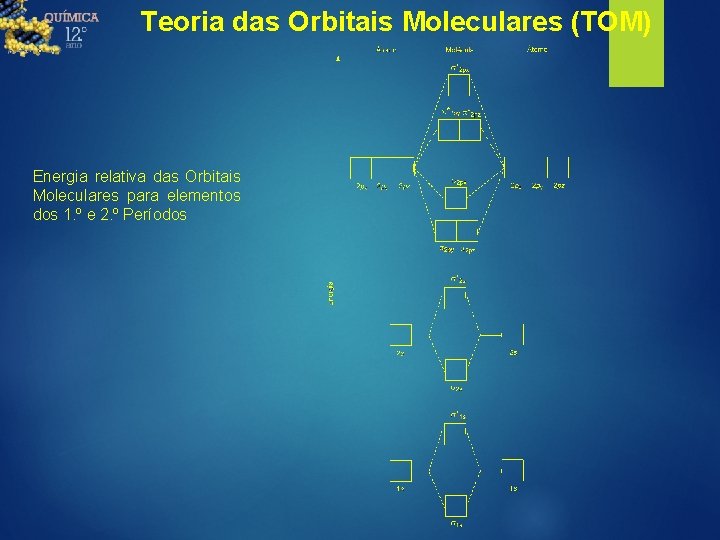
Teoria das Orbitais Moleculares (TOM) Energia relativa das Orbitais Moleculares para elementos dos 1. º e 2. º Períodos

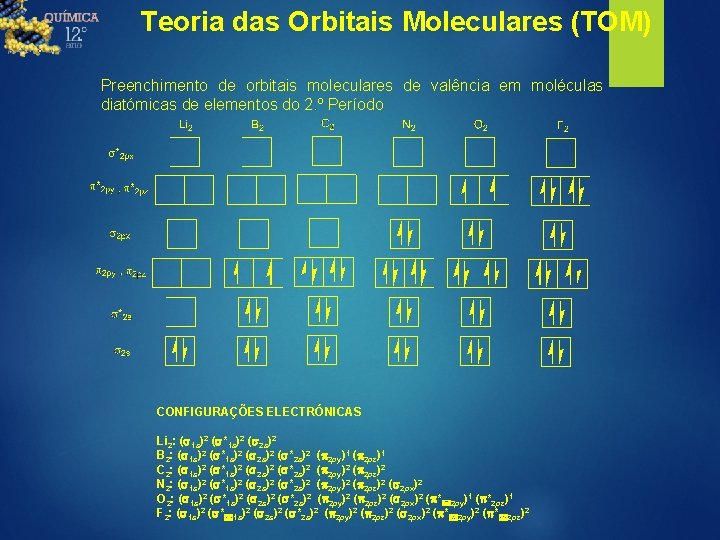
Teoria das Orbitais Moleculares (TOM) Preenchimento de orbitais moleculares de valência em moléculas diatómicas de elementos do 2. º Período CONFIGURAÇÕES ELECTRÓNICAS Li 2: (s 1 s)2 (s*1 s)2 (s 2 s)2 B 2: (s 1 s)2 (s*1 s)2 (s 2 s)2 (s*2 s)2 (p 2 py)1 (p 2 pz)1 C 2: (s 1 s)2 (s*1 s)2 (s 2 s)2 (s*2 s)2 (p 2 py)2 (p 2 pz)2 N 2: (s 1 s)2 (s*1 s)2 (s 2 s)2 (s*2 s)2 (p 2 py)2 (p 2 pz)2 (s 2 px)2 O 2: (s 1 s)2 (s*1 s)2 (s 2 s)2 (s*2 s)2 (p 2 py)2 (p 2 pz)2 (s 2 px)2 (p* 2 py)1 (p*2 pz)1 F 2: (s 1 s)2 (s* 1 s)2 (s 2 s)2 (s*2 s)2 (p 2 py)2 (p 2 pz)2 (s 2 px)2 (p* 2 py)2 (p* 2 pz)2

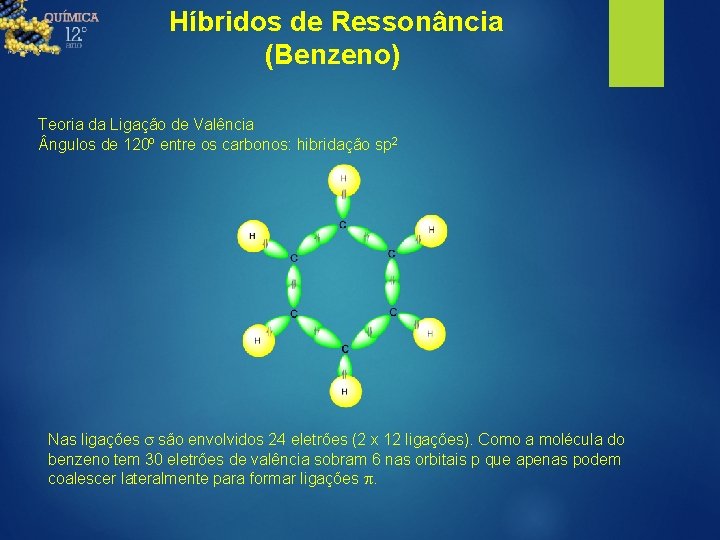
Híbridos de Ressonância (Benzeno) Teoria da Ligação de Valência ngulos de 120º entre os carbonos: hibridação sp 2 Nas ligações s são envolvidos 24 eletrões (2 x 12 ligações). Como a molécula do benzeno tem 30 eletrões de valência sobram 6 nas orbitais p que apenas podem coalescer lateralmente para formar ligações p.

Híbridos de Ressonância (Benzeno) Como a molécula do benzeno tem 30 eletrões de valência sobram 6 nas orbitais p que apenas podem coalescer lateralmente para formar ligações p. Qualquer uma das duas estruturas tem ligações simples e duplas, no entanto… Comprimento das ligações: Simples (C-C): 154 pm Dupla (C=C): 133 pm Benzeno: 140 pm (todas iguais) Como explicar?

Híbridos de Ressonância (Benzeno) August Kekulé (1829 -1896)

Híbridos de Ressonância (Benzeno) Kekulé sugeriu que o benzeno seria uma estrutura híbrida entre as duas representações de Lewis. August Kekulé (1829 -1896)

Híbridos de Ressonância (Benzeno) Os 6 eletrões p encontram-se assim deslocalizados por toda a estrutura. As ligações na molécula de benzeno são assim todas iguais, com ordem de ligação de 1, 5.

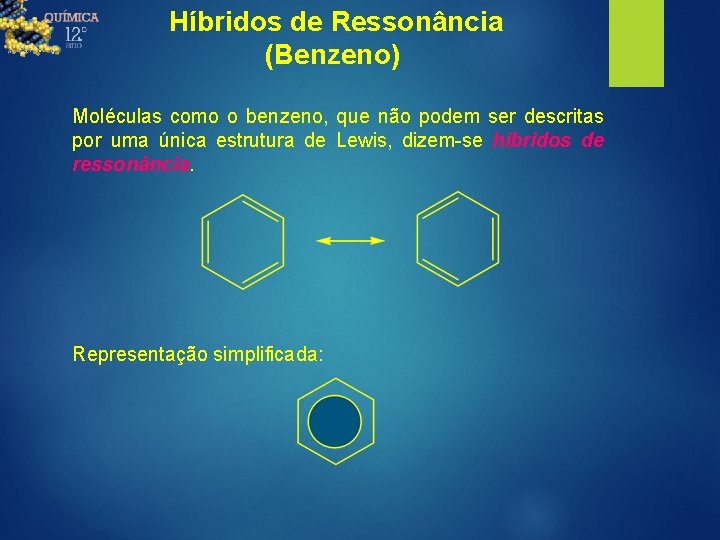
Híbridos de Ressonância (Benzeno) Moléculas como o benzeno, que não podem ser descritas por uma única estrutura de Lewis, dizem-se híbridos de ressonância. Representação simplificada:

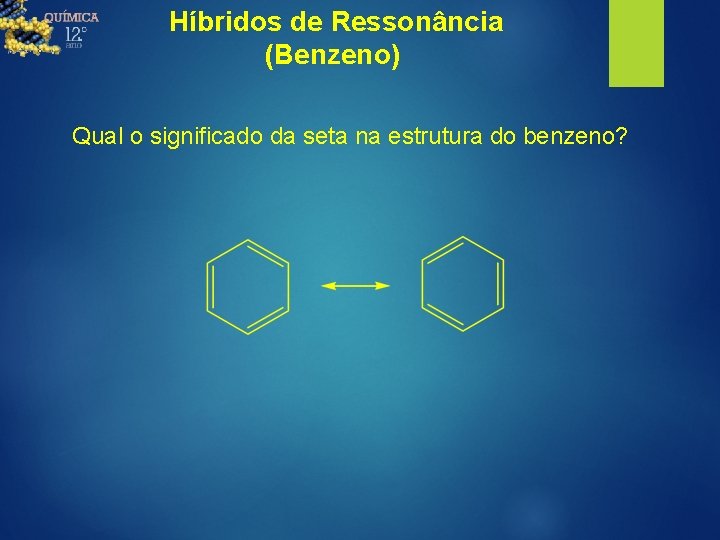
Híbridos de Ressonância (Benzeno) Qual o significado da seta na estrutura do benzeno?

Híbridos de Ressonância (Benzeno) A seta significa que a estrutura é hibrida: nem é uma, nem é outra, mas uma mistura das duas. Não confundir com a seta de equilíbrio químico em que há interconversão!!!!!

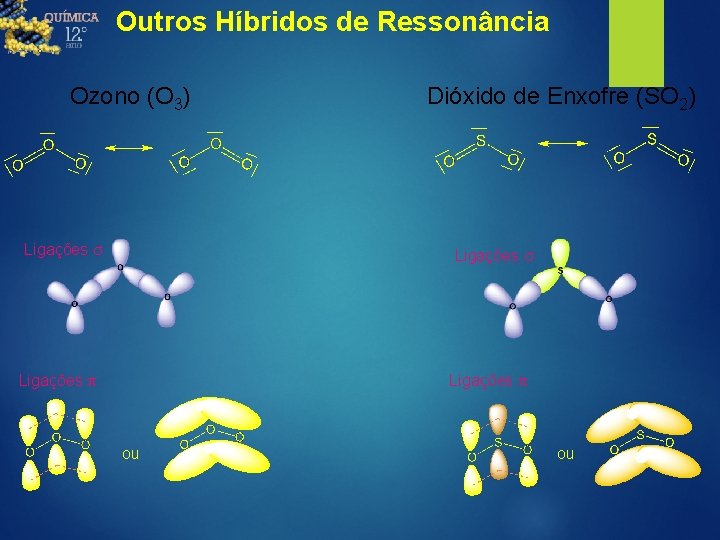
Outros Híbridos de Ressonância Ozono (O 3) Ligações s Dióxido de Enxofre (SO 2) Ligações s Ligações p ou ou