Liceo Bicentenario Via del Mar Qumica del Carbono

Liceo Bicentenario Viña del Mar. Química del Carbono. Química Electiva 4° medio A

QUÍMICA DEL CARBÓN • El C forma una gran cantidad y variedad de compuestos: más de 13 millones. • Los elementos que acompañan al C comúnmente son el H, O, N, S, P, y los halógenos. • La enorme cantidad y complejidad de los compuestos de C se debe a que pueden formar cadenas largas. • Pueden formar anillos y enlazarse a través de enlaces sencillos dobles o triples. • 30 átomos de C y 62 de H se pueden formar 4000 compuestos diferentes. • Distintos arreglos de los mismos átomos generan compuestos diferentes. QUIMICA ORGÁNICA En el pasado se creía que éstos compuestos provenían forzosamente de organismos vivos, teoría conocida como la “fuerza vital”. Fue hasta 1828 que el químico alemán Federico Wöhler (1800 -1882) obtuvo urea H 2 N-CO-NH 2 calentando HCNO (ácido ciánico) y NH 3 (amoniaco) cuando intentaba preparar NH 4 CNO (cianato de amonio), con la cual se echó por tierra la teoría de la fuerza vital.

EL CARBONO EN LA NATURALEZA El carbono es un elemento no metálico que se presenta en formas muy variadas. Puede aparecer combinado, formando una gran cantidad de compuestos, o libre (sin enlazarse con otros elementos). 4 Combinado § En la atmósfera: atmósfera en forma de dióxido de carbono CO 2 § En la corteza terrestre: terrestre formando carbonatos, como la caliza Ca. CO 3 § En el interior de la corteza terrestre: terrestre en el petróleo, carbón y gas natural En la materia viva animal y vegetal: es el componente esencial y forma parte de compuestos muy diversos: glúcidos, lípidos, proteínas y ácidos nucleicos. En el cuerpo humano, por ejemplo, llega a representar el 18% de su masa. Glúcidos Lípidos Proteínas Ácidos nucleicos

1. El dióxido de carbono de la atmósfera es absorbido por las plantas y convertido en azúcar, por el proceso de fotosíntesis. 2. Los animales comen plantas y al descomponer los azúcares dejan salir carbono a la atmósfera, los océanos o el suelo. 3. Bacterias y hongos descomponen las plantas muertas y la materia animal, devolviendo carbono al medio ambiente. 4. El carbono también se intercambia entre los océanos y la atmósfera. Esto sucede en ambos sentidos en la interacción entre el aire y el agua 28/12/2021 CICLO DEL CARBONO 4

Formas Alotrópicas del Carbono. • Estas son las formas elementales en las que se encuentra el carbono en la naturaleza. Los alotropos son compuestos constituidos por el mismo elemento , pero difieren en sus estructuras y propiedades físicas y químicas. 5

4 Libre EL CARBONO EN LA NATURALEZA § Diamante Variedad de carbono que se encuentra en forma de cristales transparentes de gran dureza. Es una rara forma que tiene su origen en el interior de la Tierra donde el carbono está sometido a temperaturas y presiones muy elevadas. Los átomos de carbono forman una red cristalina atómica en la que cada átomo esta unido a los cuatro de su entorno por fuertes enlaces covalentes. Es muy duro y etable. § Grafito Variedad de carbono muy difundida en la naturaleza. Es una sustancia negra, brillante, blanda y untosa al tacto. Se presenta en escamas o láminas cristalinas ligeramente adheridas entre si, que pueden www. kalipedia. com/ciencias-tierra-universo/tema/geosfera/grafito resbalar unas sobre otras. Los átomos de carbono se disponen en láminas planas formando hexágonos. Cada átomo está unido a otros tres por medio de enlaces covalentes. El cuarto electrón se sitúa entre las láminas y posee movilidad. Por esto el grafito es fácilmente exfoliable y un excelente conductor del calor y la electricidad.

Combustibles fósiles: En algunos casos el carbono presente en las moléculas biológicas no regresa inmediatamente al ambiente abiótico, por ejemplo el carbono presente en la madera de los árboles. O el que formó parte de los depósitos de hulla a partir de restos de árboles antiguos quedaron sepultados en condiciones anaerobias antes de descomponerse. Hulla, petróleo y gas natural son llamados combustibles fósiles porque se formaron a partir de restos de organismos antiguos y contienen grandes cantidades de compuestos carbonados como resultado de la fotosíntesis ocurrida hace millones de años. 28/12/2021 7
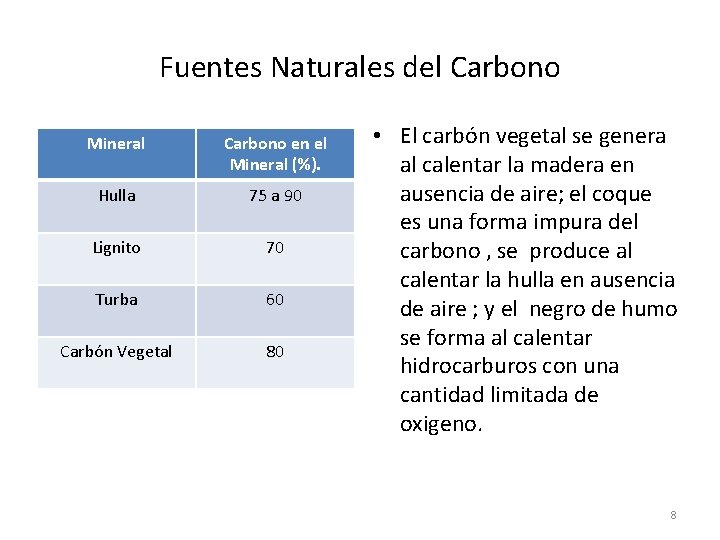
Fuentes Naturales del Carbono Mineral Carbono en el Mineral (%). Hulla 75 a 90 Lignito 70 Turba 60 Carbón Vegetal 80 • El carbón vegetal se genera al calentar la madera en ausencia de aire; el coque es una forma impura del carbono , se produce al calentar la hulla en ausencia de aire ; y el negro de humo se forma al calentar hidrocarburos con una cantidad limitada de oxigeno. 8
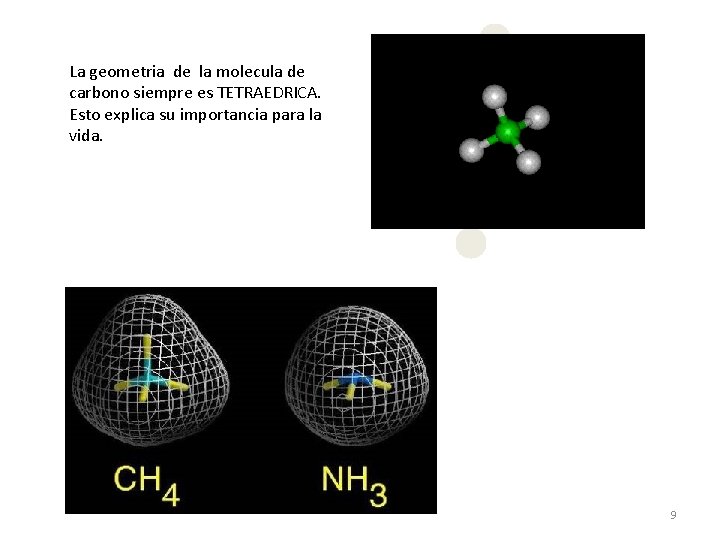
La geometria de la molecula de carbono siempre es TETRAEDRICA. Esto explica su importancia para la vida. 9
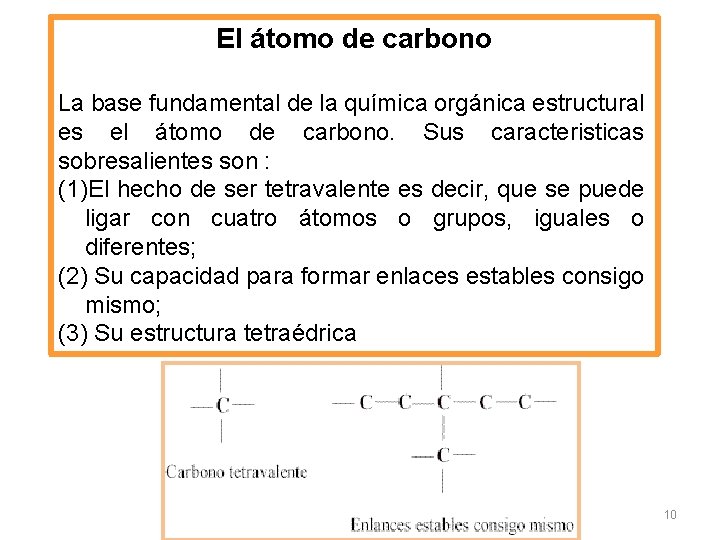
El átomo de carbono La base fundamental de la química orgánica estructural es el átomo de carbono. Sus caracteristicas sobresalientes son : (1)El hecho de ser tetravalente es decir, que se puede ligar con cuatro átomos o grupos, iguales o diferentes; (2) Su capacidad para formar enlaces estables consigo mismo; (3) Su estructura tetraédrica 10
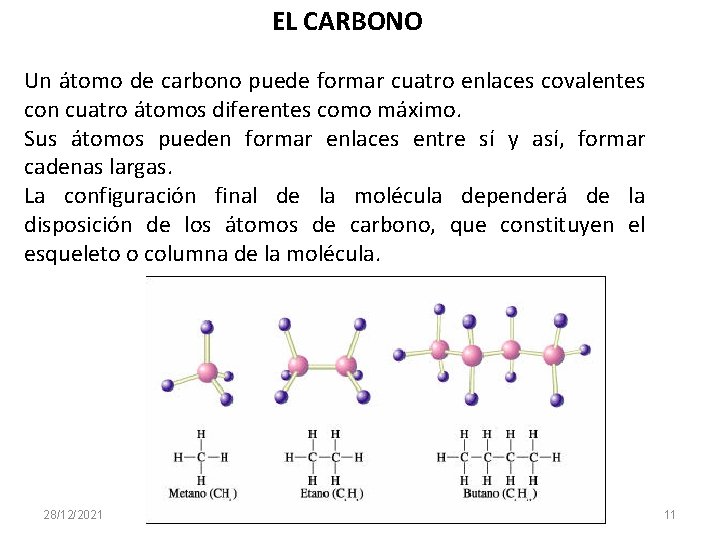
EL CARBONO Un átomo de carbono puede formar cuatro enlaces covalentes con cuatro átomos diferentes como máximo. Sus átomos pueden formar enlaces entre sí y así, formar cadenas largas. La configuración final de la molécula dependerá de la disposición de los átomos de carbono, que constituyen el esqueleto o columna de la molécula. 28/12/2021 Gloria Maria Mejia Z. 11

Propiedades del carbono • Tiene 4 electrones de valencia, por lo mismo puede formar 4 enlaces covalentes. • Puede formar enlaces sencillos, C-C; enlaces dobles, C=C; y enlaces triples C≡C. • Las cadenas de átomos de carbono pueden ser ramificadas o no ramificadas. • Pueden unirse entre si y a otros átomos distintos para producir una variedad de formas moleculares tridimensionales. • Pueden formar isómeros. 28/12/2021 12
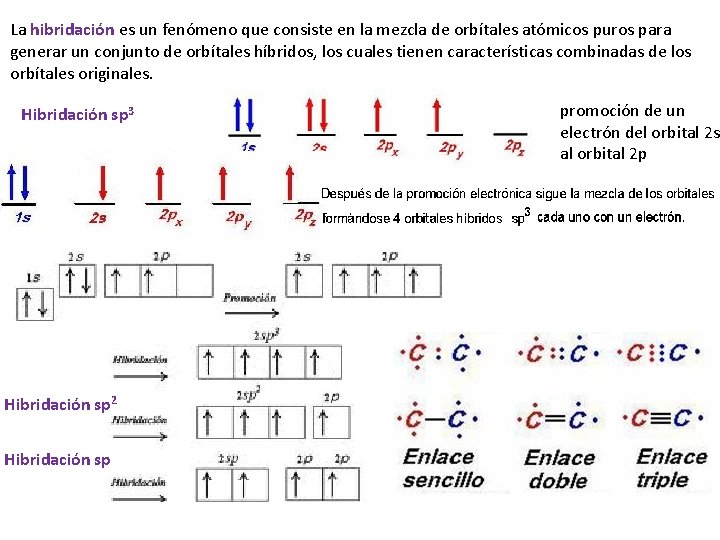
La hibridación es un fenómeno que consiste en la mezcla de orbítales atómicos puros para generar un conjunto de orbítales híbridos, los cuales tienen características combinadas de los orbítales originales. Hibridación sp 3 Hibridación sp 2 Hibridación sp promoción de un electrón del orbital 2 s al orbital 2 p

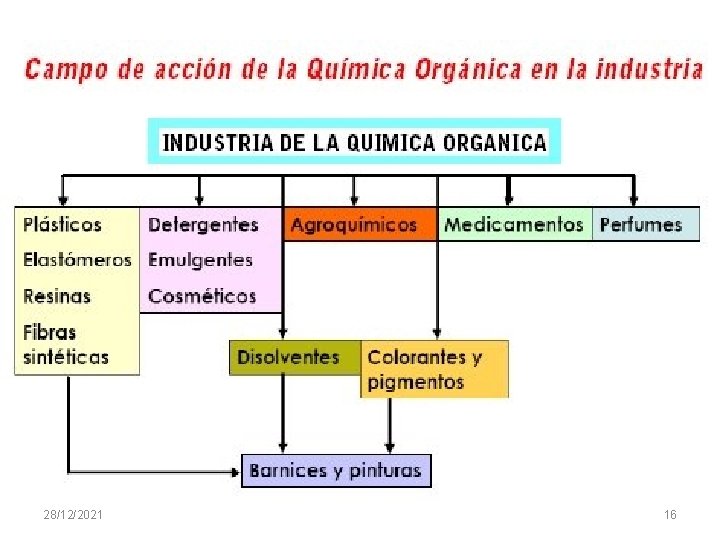
LOS COMPUESTOS DE CARBONO El estudio de los compuestos del carbono constituye una parte fundamental y muy extensa de la química, que se denomina química orgánica o química del carbono. Este hecho se debe a diversos motivos: § La gran cantidad de compuestos del carbono que se conocen. § Este elemento forma más compuestos que todos los otros juntos, los cuales constituyen otra parte de la química llamada química inorgánica. § Las propiedades especiales de los compuestos del carbono. § La importancia de estos compuestos. Además de formar parte de la materia viva, hay muchos que son de uso común, como combustibles, alimentos y plásticos, fibras sintéticas, medicamentos, colorantes, etc.

Propiedades de los compuestos de carbono Los compuestos del carbono forman moléculas cuyos átomos están unidos por fuertes enlaces covalentes, mientras que entre una molécula y otra, cuando las sustancias son sólidas o líquidas, hay unas fuerzas de enlace muy débiles. Por ello decimos que estos compuestos son sustancias covalentes moleculares. Propiedades �Insolubles en agua y solubles en disolventes orgánicos § Temperaturas de fusión y ebullición bajas. § No conducen la corriente eléctrica ni en estado líquido ni en disolución § Poseen poca estabilidad térmica, es decir, se descomponen o se inflaman fácilmente cuando se calientan. § Suelen reaccionar lentamente debido a la gran estabilidad de los enlaces covalentes que unen sus átomos.
28/12/2021 16

Ingredientes de los alimentos Industria Farmacéutica Industria Textil Industria de la Madera Cosmetología

REPRESENTACIÓN DE LEWIS DE LAS MOLÉCULAS ORGÁNICAS. • Cuando dos átomos comparten dos electrones entre sí se forma entre ellos un enlace covalente. Los átomos, de acuerdo con su configuración electrónica, pueden cumplir la regla del octeto con pares de electrones compartidos (electrones enlazantes) y pares de electrones sin compartir (electrones no enlazantes). 28/12/2021 18
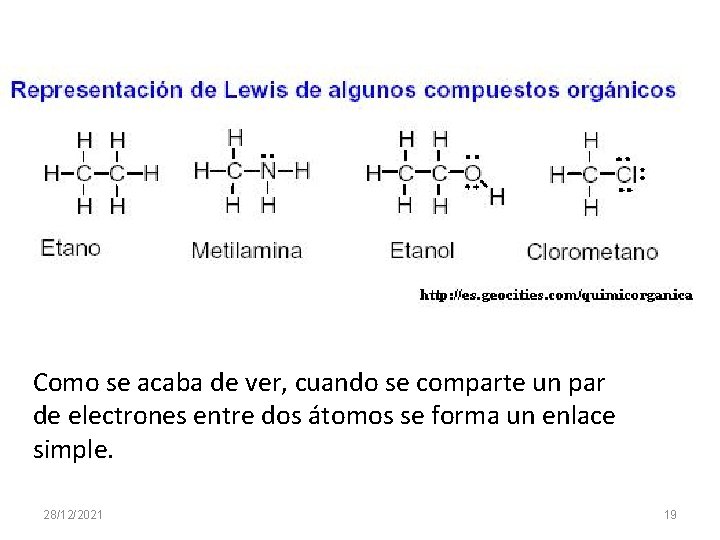
Como se acaba de ver, cuando se comparte un par de electrones entre dos átomos se forma un enlace simple. 28/12/2021 19

Moléculas polares y no polares Existen enlaces con polaridad muy variada. Así, podemos encontrar desde enlaces covalentes no polares y enlaces covalentes polares, hasta enlaces totalmente iónicos. En los ejemplos siguientes, el etano tiene un enlace covalente no polar C-C. La metilamina, el metanol y el clorometano tienen enlaces covalentes cada vez más polares (C-N, C-O y C-Cl). El cloruro de metilamonio (CH 3 NH 3+Cl-) tiene un enlace iónico entre el ión metilamonio y el ión cloruro. 28/12/2021 20
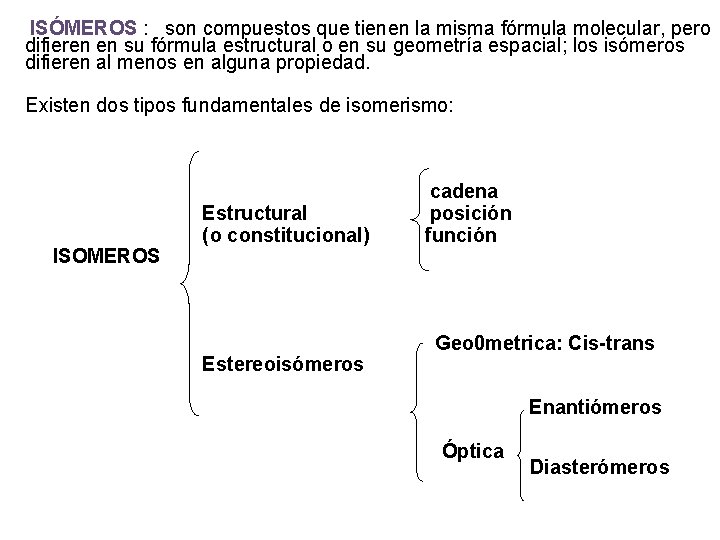
ISÓMEROS : son compuestos que tienen la misma fórmula molecular, pero difieren en su fórmula estructural o en su geometría espacial; los isómeros difieren al menos en alguna propiedad. Existen dos tipos fundamentales de isomerismo: ISOMEROS Estructural (o constitucional) Estereoisómeros cadena posición función Geo 0 metrica: Cis-trans Enantiómeros Óptica Diasterómeros
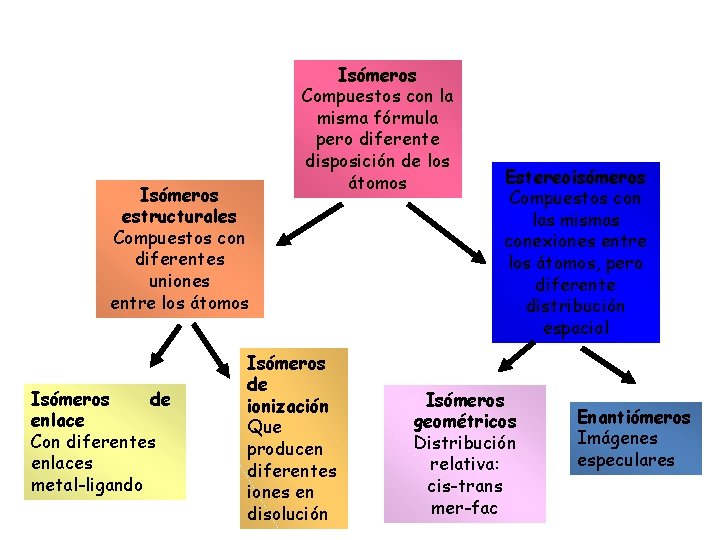
Isómeros estructurales Compuestos con diferentes uniones entre los átomos Isómeros de enlace Con diferentes enlaces metal-ligando Isómeros Compuestos con la misma fórmula pero diferente disposición de los átomos Isómeros de ionización Que producen diferentes iones en disolución Estereoisómeros Compuestos con las mismas conexiones entre los átomos, pero diferente distribución espacial Isómeros geométricos Distribución relativa: cis-trans mer-fac Enantiómeros Imágenes especulares
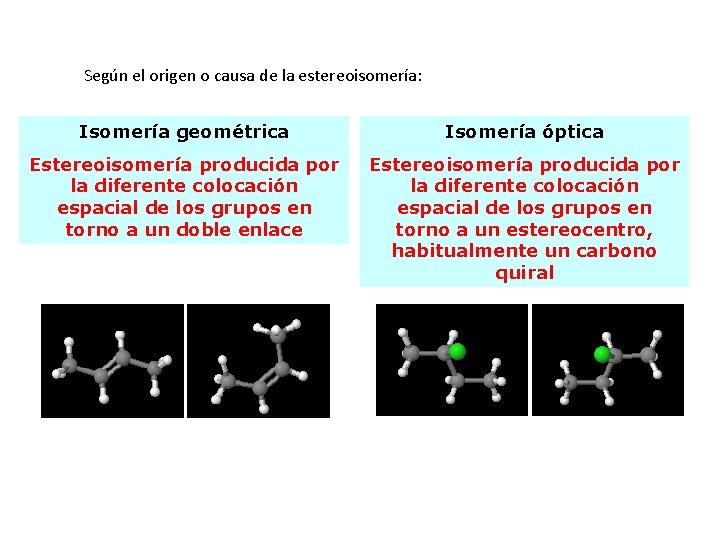
Según el origen o causa de la estereoisomería: Isomería geométrica Isomería óptica Estereoisomería producida por la diferente colocación espacial de los grupos en torno a un doble enlace Estereoisomería producida por la diferente colocación espacial de los grupos en torno a un estereocentro, habitualmente un carbono quiral
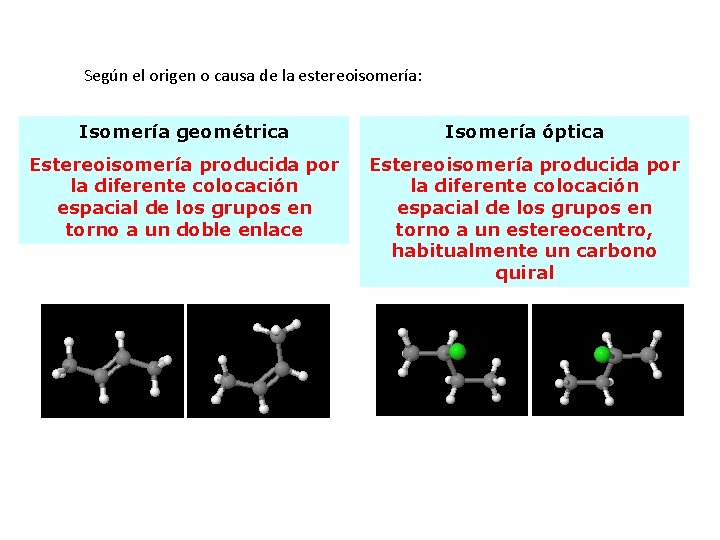
Según el origen o causa de la estereoisomería: Isomería geométrica Isomería óptica Estereoisomería producida por la diferente colocación espacial de los grupos en torno a un doble enlace Estereoisomería producida por la diferente colocación espacial de los grupos en torno a un estereocentro, habitualmente un carbono quiral
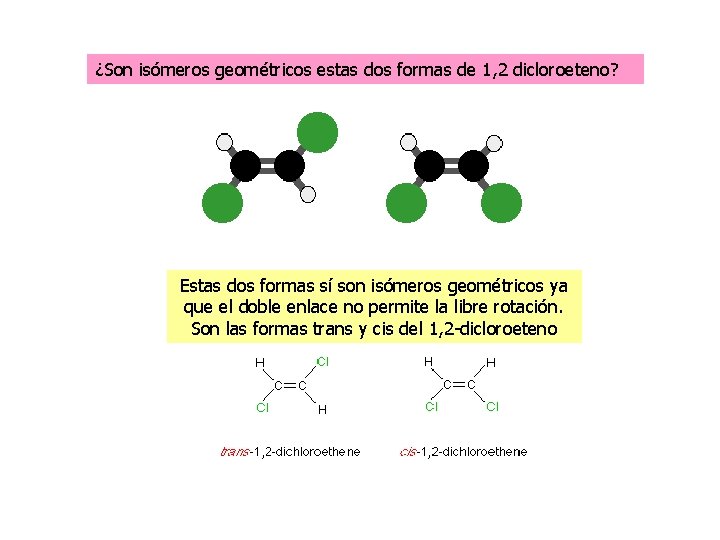
¿Son isómeros geométricos estas dos formas de 1, 2 dicloroeteno? Estas dos formas sí son isómeros geométricos ya que el doble enlace no permite la libre rotación. Son las formas trans y cis del 1, 2 -dicloroeteno
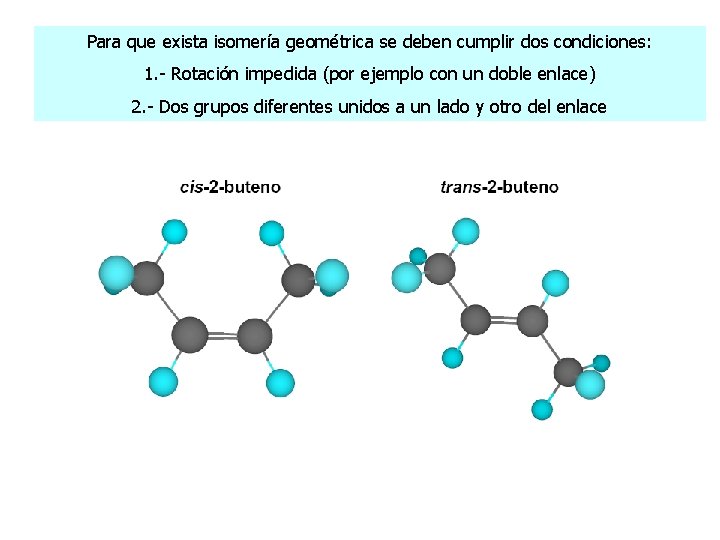
Para que exista isomería geométrica se deben cumplir dos condiciones: 1. - Rotación impedida (por ejemplo con un doble enlace) 2. - Dos grupos diferentes unidos a un lado y otro del enlace

• • Comparación entre Compuestos Orgánicos e Inorgánicos. Orgánicos Inorgánicos 1. Generalmente iónicos. • Generalmente solo covalentes. 2. Puntos de Fusión muy • Puntos de fusión no muy altos (>500°C). altos <250°C. Punto de ebullición muy • Puntos de ebullición no muy alto (>1000°C). altos <350°C. Conducen la electricidad. • No conducen la electricidad. Solubles en Agua. • Insolubles en agua. Insolubles en solventes apolares. • Solubles en solventes apolares. Generalmente no arden. • Generalmente arden. Dan reacciones iónicas simples y rápidas. • Reaccionan lentamente ; reacciones complejas. 27
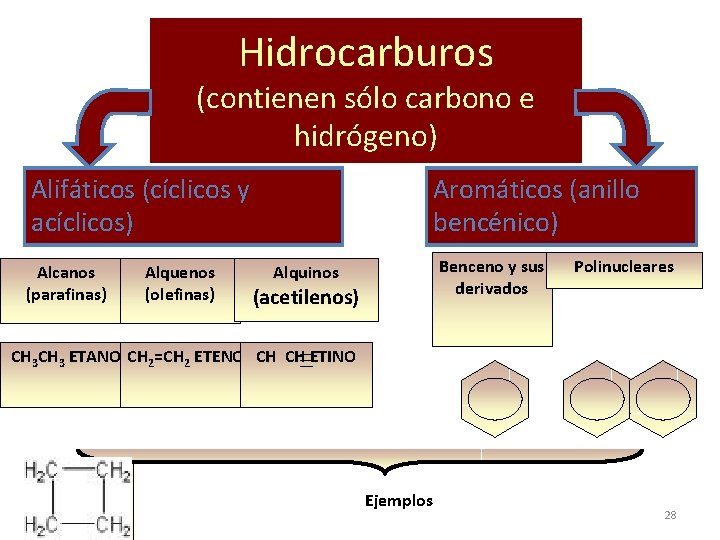
Hidrocarburos (contienen sólo carbono e hidrógeno) Alifáticos (cíclicos y acíclicos) Alcanos (parafinas) Alquenos (olefinas) Aromáticos (anillo bencénico) Benceno y sus derivados Alquinos (acetilenos) Polinucleares CH 3 ETANO CH 2=CH 2 ETENO CH CH ETINO Ejemplos 28

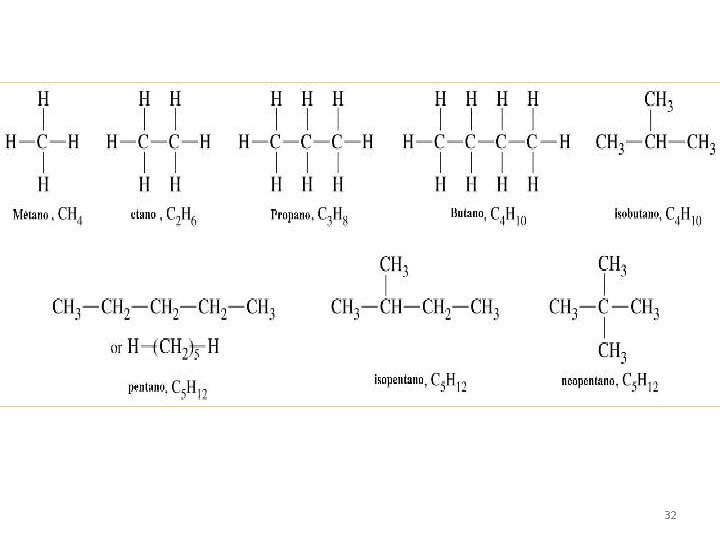
Nomenclatura Hidrocarburos 1. Se determina cuál es la cadena continua de átomos de carbono más larga de la estructura que es la cadena principal para la nomenclatura. 2. Se agrega un prefijo en –ano que especifique el número de átomos de carbono en la cadena principal. 29

Los prefijos, hasta C-10, son los siguientes: met- 1 C hex- 6 C et- 2 C hept- 7 C TERMINACIÓN-ano prop- 3 C oct- 8 C but- 4 C non- 9 C pent- 5 C dec- 10 C En el caso de los cicloalcanos, la aplicación es así: Ciclopropano, ciclobutano, ciclohexano, etc. 30

• A partir del butano los nombres de los compuestos orgánicos llevan el prefijo: • Penta 5 átomos de C • Hexa 6 átomos de C • Hepta 7 átomos de C • Octo 8 átomos de C • Nona 9 átomos de C • Deca 10 átomos de C • Undeca 11 átomos de C Sabias que. . . Al aumentar el número de Carbonos en los alcanos se van modificando sus propiedades físicas, por ejemplo los primeros cuatro alcanos son gases a temperatura ambiente y del Pentano al Decano son líquidos. Además al aumentar el tamaño mole-cular (⇡ Nº de C), se incrementa el punto de ebullición. 31
32
33
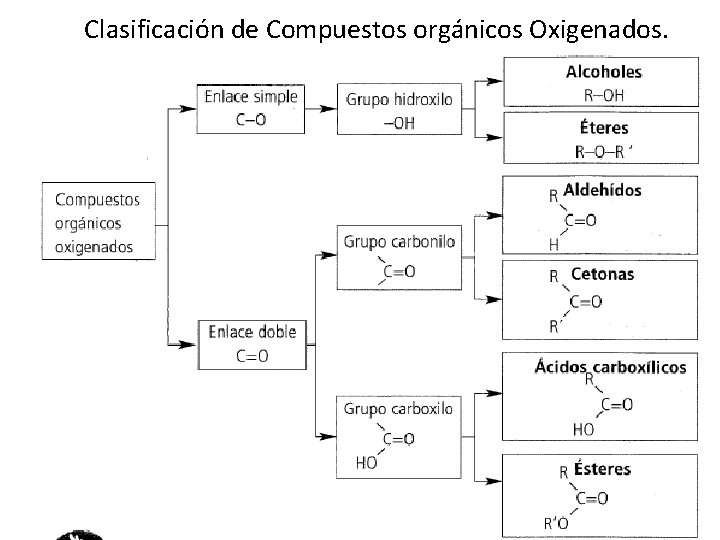
Clasificación de Compuestos orgánicos Oxigenados. 34
- Slides: 34