LICENCIATURA EM ENFERMAGEM 2009 2013 BIOQUMICA 1 SEMESTRE

LICENCIATURA EM ENFERMAGEM 2009 -2013 BIOQUÍMICA – 1º SEMESTRE PROF. ENGº. NUNO COSTA

CARGA HORÁRIA • TOTAL - 37 AULAS 33 AULAS TEÓRICAS E TEÓRICO-PRÁTICAS 2 AULAS DE APRESENTAÇÃO DE TRABALHOS DE GRUPO 2 AULAS PARA FREQUÊNCIA FINAL

CRITÉRIOS GERAIS DE AVALIAÇÃO % Critérios Itens de Avaliação Instrumentos 50 Domínio do Conhecimento Específico Aquisição e compreensão Aplicação Relacionação Análise Registo contínuo de Comunicação Oral e Escrita 20 30 Métodos de Trabalho Compreensão Expressão Técnicas de pesquisa, selecção, organização e apresentação de informação Criatividade Sentido crítico avaliação Trabalhos práticos (individuais ou em grupo) Apresentação de um trabalho Participação na aula Teste (FREQUÊNCIA) BIOQUÍMICA 2/3 DA NOTA FINAL – 14 VALORES

MANUAIS ADOPTADOS Lehninger, (2005). Principles of Biochemistry. 4 th Ed. Murray, (2003). Harper's Illustrated Biochemistry. Mc. Graw-Hill Medical, 26 th Ed.

BIBLIOGRAFIA FUNDAMENTAL • GARRET, R. H. & GRISHAM, CH. M. (1995). Biochemistry. Saunders Col. . Fort Horth. • MARKS, D. B. , MARKS, A. D. & SMITH, C. M. (1996). Basic Medical Biochemistry. A Clinical Approach. Williams & Wilkins. • STRYER, L. (2005). Biochemistry. 5ª ed. , W. H. Freeman and Company, New York, Bib. • WEIL, J. H. (2000). Bioquímica Geral. 2ª Edição. Lisboa, Fundação Calouste Gulbenkian.

CURRÍCULO DA CADEIRA 1 - PRINCÍPIOS DA BIOQUÍMICA ◦ NOÇÕES DE BIOLOGIA CELULAR ◦ NOÇÕES DE QUÍMICA ◦ PRINCÍPIOS FÍSICOS ◦ PRINCÍPIOS GENÉTICOS ◦ PRINCÍPIOS DA EVOLUÇÃO GENÉTICA

2 - ESTRUTURA E CATÁLISE ▫ ÁGUA ▫ AMINOÁCIDOS, PÉPTIDOS E PROTEÍNAS ▫ ESTRUTURA TRIDIMENSIONAL DAS PROTEÍNAS ▫ FUNÇÕES DAS PROTEÍNAS ▫ ENZIMAS ▫ HIDRATOS DE CARBONO E GLICOBIOLOGIA ▫ NUCLEÓTIDOS E ÁCIDOS NUCLEICOS ▫ LÍPIDOS ▫ MEMBRANAS BIOLÓGICAS E TRANSPORTE ▫ PERCURSORES BIOLÓGICOS

3 - BIOENERGÉTICA E METABOLISMO ▫ PRINCÍPIOS DA BIOENERGÉTICA ▫ GLICÓLISE, GÉNESE GLUCOGÉNICA ▫ PRINCÍPIOS DA REGULAÇÃO METABÓLICA ▫ CICLO DO ÁCIDO CÍTRICO (CLICLO DE KREBS) ▫ CATABOLISMO DOS ÁCIDOS GORDOS ▫ OXIDAÇÃO DOS AMINOÁCIDOS E PRODUÇÃO DA UREIA

4. PERCURSORES DE INFORMAÇÃO ▫ GENES E CROMOSOMAS ▫ METABOLISMO DO DNA ▫ METABOLISMO DO RNA ▫ METABOLISMO DAS PROTEÍNAS ▫ REGULAÇÃO GENÉTICA

ORIGEM DA BIOQUÍMICA • Paracelsus (1493 -1541) fundador da latroquímica (Química Médica). • Schelle (1742 -1786) e Lavoisier (1743 -1794) – Bases científicas fundamentais de estruturação da Bioquímica. Papel importante na descoberta de compostos existentes nos organismos ou produzidos por estes Mostrou que as reacções químicas estão subordinadas ao princípio da conservação da matéria • Wöhler (1800 -1882) – síntese da ureia e Kolbe (1814 -1884) – síntese do ácido acético e Berthelot (1827 -1884) – síntese de vários compostos biológicos. Provaram que os compostos de origem biológica podiam ser sintetizados artificialmente. • Büchner (1887) mostrou que as reacções biológicas continuam a ocorrer em extractos isentos de células (homogenatos).

BIOQUÍMICA • A Bioquímica é a única ciência que nasceu no século XX. • É uma ciência que estuda principalmente a química dos processos biológicos que ocorrem em todos os seres vivos. • Os bioquímicos utilizam ferramentas e conceitos da química orgânica e físico-química. • Baseia-se principalmente no estudo da estrutura e função de componentes celulares como proteínas, hidratos de carbono, lípidos, ácidos nucleicos e outras biomoléculas. • Recentemente a Bioquímica tem se focalizado mais especificamente na química das reacções enzimáticas e nas propriedades das proteínas.
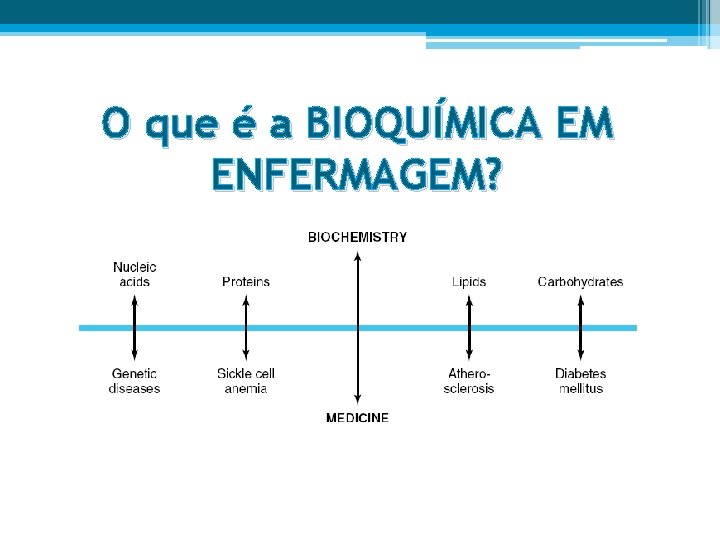
O que é a BIOQUÍMICA EM ENFERMAGEM?

• BIOQUÍMICA e ENFERMAGEM estão intimamente relacionadas. • A Saúde depende dum balanço hormonioso das reacções bioquímicas ocorrentes no corpo humano, e a Doença reflete anormalidades nas biomoléculas, reacções bioquímicas ou processos bioquímicos. • O conhecimento bioquímico é fundamental na compreensão das causas doenças e na análise do diagnóstico e terapias apropriadas.

CAUSAS DOENÇAS • 1. Agentes físicos: Trauma mecânico, temperatura extrema, mudanças repentinas na pressão atmosférica, radiação, choques eléctricos. • 2. Agentes químicos (incluem as drogas): Compostos tóxicos, drogas terapêuticas, etc. • 3. Agentes biológicos: Vírus, bactérias, fungos, formas avançadas de parasitas. • 4. Falta de oxigénio: Falta de aprovisionamento de sangue, decandência na capacidade do sangue transportar oxigénio, envenenamento dos enzimas oxidativos. • 5. Desordens genéticas: Congénitas e moleculares. • 6. Reacções imunológicas: doenças auto-imunes. • 7. Desequilíbrios nutricionais: Deficiências e excessos. • 8. Desequilíbrios endócrinos: Deficiências hormonais, excessos.

UNIDADES DO SISTEMA INTERNACIONAL (SI) UNIDADES BÁSICAS SI GRANDEZA COMPRIMENTO MASSA TEMPERATURA QUANTIDADE DE MATÉRIA UNIDADE ABREVIATURA METRO m QUILOGRAMA Kg KELVIN K MOLE mol T(K) = t(ºc) + 273, 15
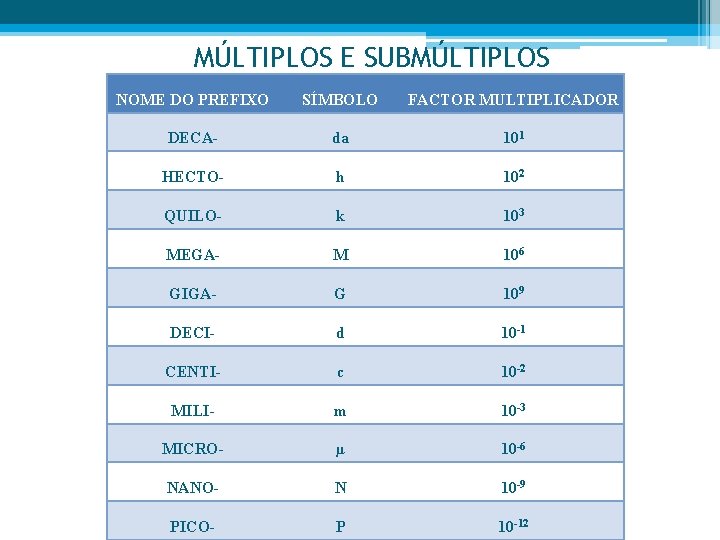
MÚLTIPLOS E SUBMÚLTIPLOS NOME DO PREFIXO SÍMBOLO FACTOR MULTIPLICADOR DECA- da 101 HECTO- h 102 QUILO- k 103 MEGA- M 106 GIGA- G 109 DECI- d 10 -1 CENTI- c 10 -2 MILI- m 10 -3 MICRO- µ 10 -6 NANO- N 10 -9 PICO- P 10 -12

MÉTODOS E CONCEITOS • O objecto de estudo da Bioquímica apresenta um conjunto de especialidades e que permitem distingui-la das outras ciências. • Dimensões do objecto de estudo: ▫ Tamanho - µm e nm: Metabolitos (alanina, 0, 5 nm: glicose, 0, 7 nm) Macromoléculas (fosfolípidos, 3, 0 nm; ribonuclease, 4, 0 nm; imunoglobina G, 14 nm) Complexos supramoleculares (ribossomas, 18 nm; piruvato desidrogenase, 60 nm) Organelos (mitrocôndrias, 1, 5 nm) Célula (célula hepática, 20 µm)

• Massas moleculares (D – Dalton) 1 DALTON = 1 /NA (6, 022 X 1023) = 1, 6605 X 10 -24 g ▫ Metabolitos (alanina, 89 D; glicose, 180 D) ▫ Macromoléculas (fosfolípidos, 750 D; ribonuclease, 12, 6 k. D) ▫ Complexos supramoleculares (ribossomas, 2, 52 m. D; piruvato desidrogenase, 7 m. D ou 1, 17 x 10 -5 pg) ▫ Organelos (mitrocôndrias, 1, 5 pg) ▫ Célula (célula hepática, 8 ng)

• Concentrações entre p. M (10 -12 e as m. M 10 -3) ▫ Metabolitos (glicose, 5 m. M) ▫ Macromoléculas (imunoglobina E, 1, 7 n. M) Componentes do organismo Microcomponentes Macrocomponentes (hormonas, vitaminas, e elementos metálicos) (açucares, proteínas e lípidos)
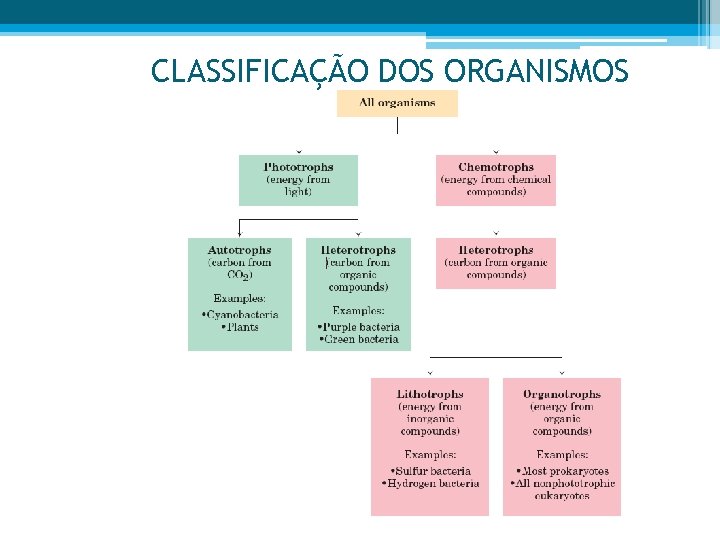
CLASSIFICAÇÃO DOS ORGANISMOS
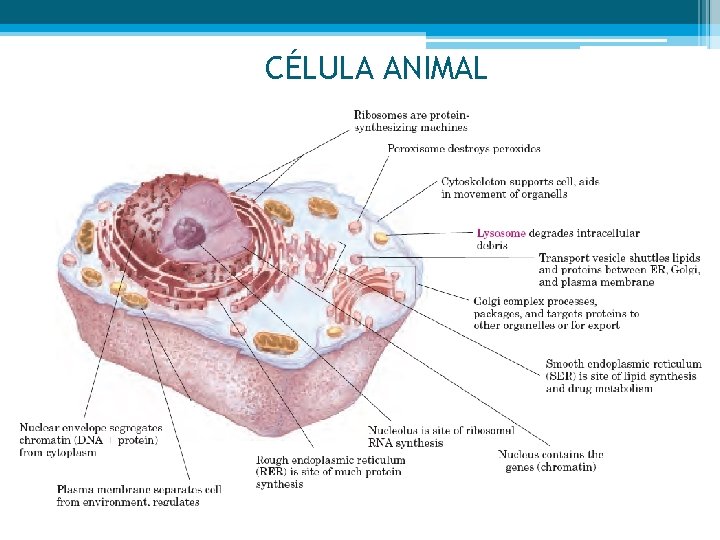
CÉLULA ANIMAL

CITOPLASMA • O volume interno limitado pela membrana de plasma (citoplasma) é composto por uma solução aquosa, o citosol, é composto por uma grande variedade de partículas em suspenção cada uma com as suas funções específicas.

• O citosol é uma solução altamente concentrada contendo: ▫ Enzimas e moléculas de RNA; ▫ Componentes - (aminoácidos e nucleótidos); ▫ Metabolitos - centenas de moléculas orgânicas de pequena dimensão, intermediários nas reacções biossintéticas e degradativas; ▫ Coenzimas - compostos essenciais para reacções catalíticas; ▫ Iões inorgânicos – catiões e aniões; ▫ Ribossomas - pequenas partículas (compostas por moléculas de proteínas e RNA) são locais onde ocorre a síntese de proteínas.

• Todas as células são delimitadas por uma membrana de plasma, os metabolitos estão dipersados no citosol que contém os coenzimas, iões inorgânicos e enzimas; contêm uma diversidade de genes contidos no nucleótido (procatióticos) ou no núcleo (eucarióticos). • Os fototrofos utilizam a luz solar para viverem; • Os quimiotrofos oxidam combustíveis, passam os electrões para os aceitadores de electrões: compostos inorgânicos, orgânicos ou oxigénio molecular. • As proteínas do citoesqueleto são grandes filamentos que dão às células a sua forma e rigidez e servem de passagem onde os organelos celulares movem-se pela célula.
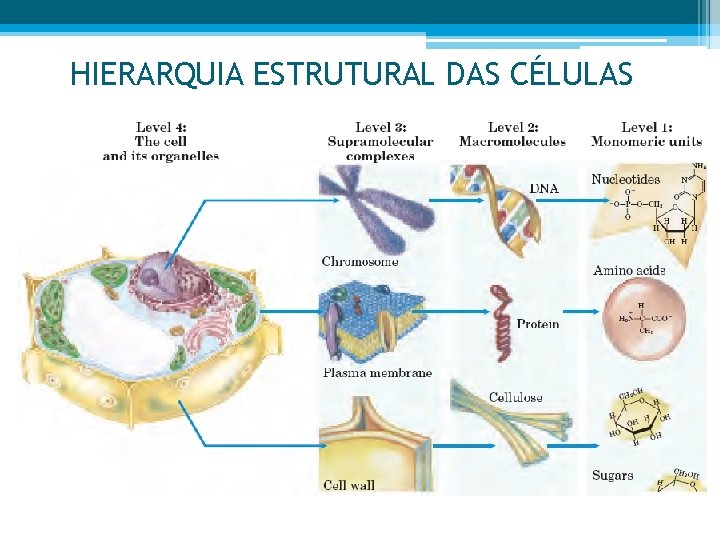
HIERARQUIA ESTRUTURAL DAS CÉLULAS

AMINOÁCIDOS
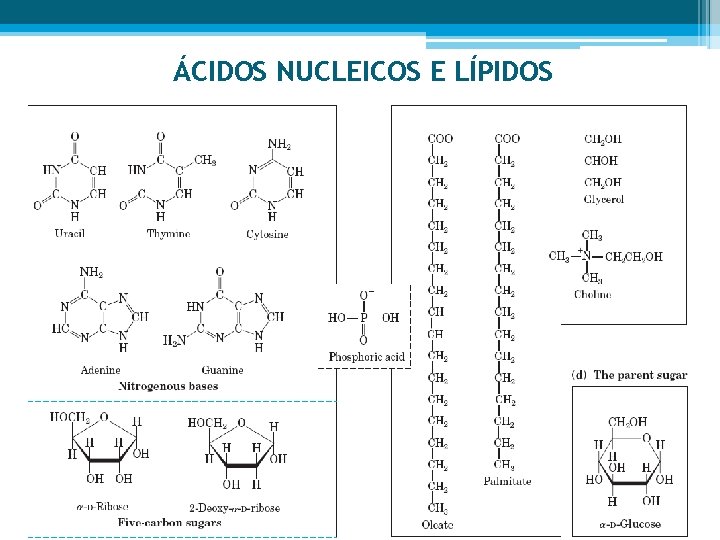
ÁCIDOS NUCLEICOS E LÍPIDOS

ELEMENTOS ESSÊNCIAIS PARA A VIDA HUMANA Componentes estruturais das células e tecidos - são necessários para a dieta do dia a dia (g). As necessidades são menores: para os humanos bastam algums miligramas diários de Fe, Cu, e Zn.

LIGAÇÕES CARBONO
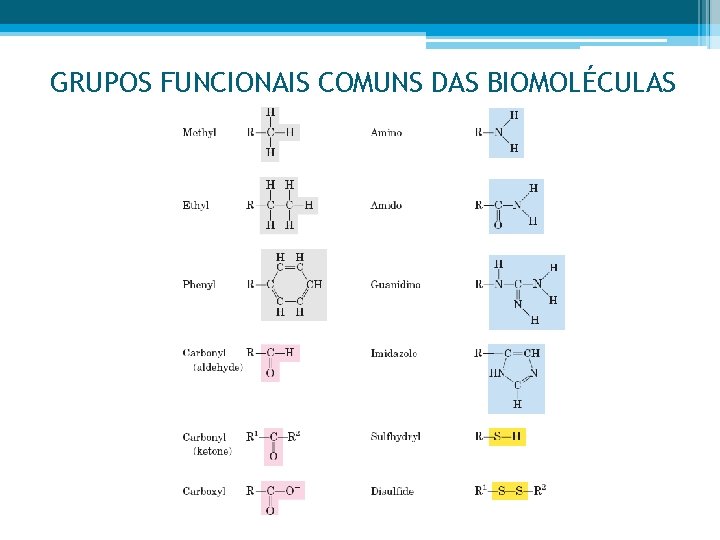
GRUPOS FUNCIONAIS COMUNS DAS BIOMOLÉCULAS

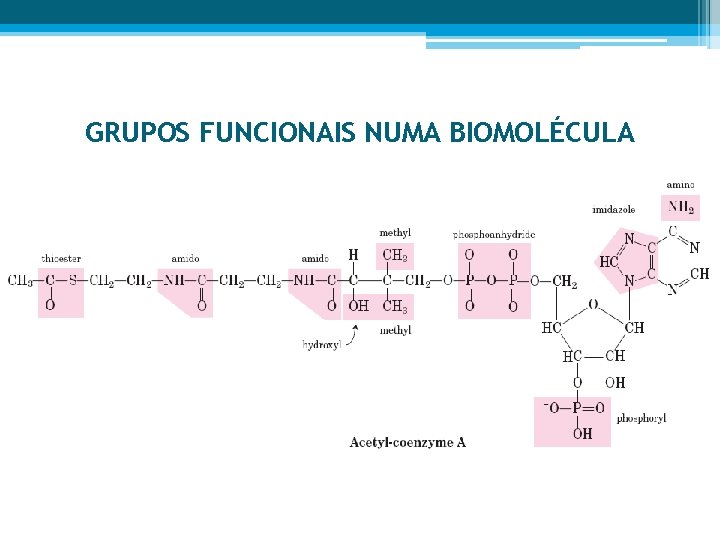
GRUPOS FUNCIONAIS NUMA BIOMOLÉCULA

MACROMOLÉCULAS • Constituintes em maior quantidade nas células. • A síntese de macromoléculas é o processo que consome mais energia nas células. • Estas produzem complexos supramoleculares, formando unidades funcionais tais como os ribossomas. Proteínas, polímeros de aminoácidos, constituem a maior fracção nas células. Algumas proteínas têm actividade catalítica (enzimas). Ácidos nucleicos, DNA e RNA, são polímeros de nucleótidos. Eles contêm e transmitem a informação genética. Polissacarídos, são polímeros de glucose que possuem duas importantes funções: contentores de energia e elementos estruturais que se ligam a certas proteínas. Lípidos são componentes estruturais das membranas (bicamada). Contêm grandes quantidades de energia, pigmentos e sinalização intracelular.

ISOMERIA • Um composto contendo carbono existe como esteroisómero na natureza, moléculas com as mesmas ligações químicas mas com diferente estereoquímica, isto é, com diferente configuração (arranjo espacial dos átomos). • As interações entre biomoléculas são estereoespecíficas, necessitando uma estereoquímica específica nas moléculas interagidas. Representação da Alanina (a) Fórmula estrutural em prespectiva (b) Modelo mostrando os comprimentos relativos das ligações e os ângulos de ligação. (c) Modelos espacial onde cada átomo é mostrado correctamente no seu raio de Van Der Waals.
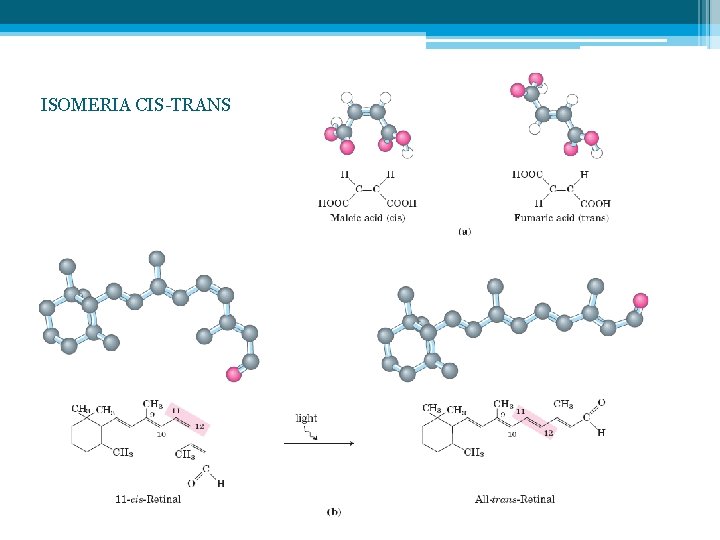
ISOMERIA CIS-TRANS
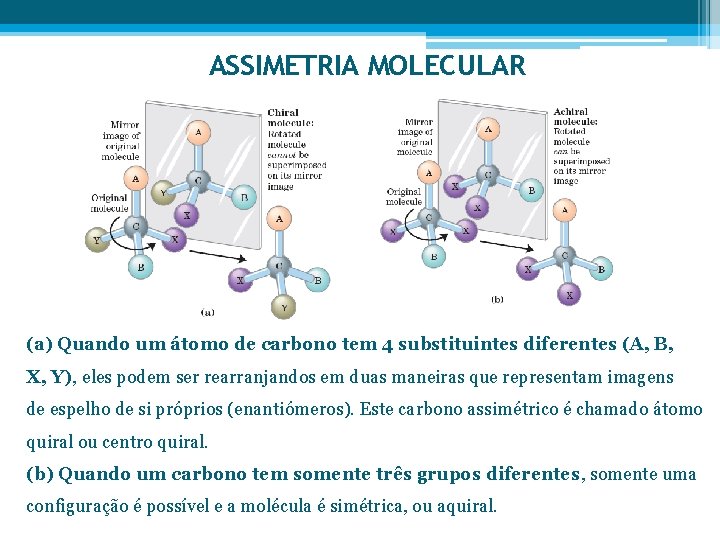
ASSIMETRIA MOLECULAR (a) Quando um átomo de carbono tem 4 substituintes diferentes (A, B, X, Y), eles podem ser rearranjandos em duas maneiras que representam imagens de espelho de si próprios (enantiómeros). Este carbono assimétrico é chamado átomo quiral ou centro quiral. (b) Quando um carbono tem somente três grupos diferentes, somente uma configuração é possível e a molécula é simétrica, ou aquiral.
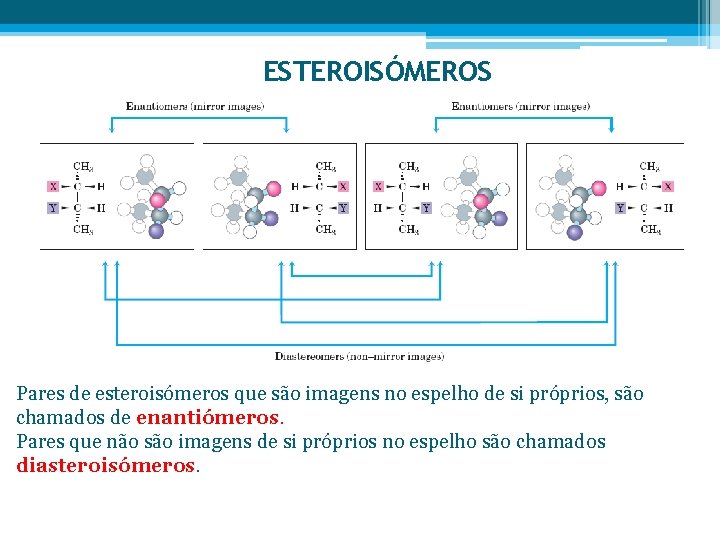
ESTEROISÓMEROS Pares de esteroisómeros que são imagens no espelho de si próprios, são chamados de enantiómeros. Pares que não são imagens de si próprios no espelho são chamados diasteroisómeros.

ORGANISMOS TRANSFORMAM ENERGIA E MATÉRIA • Um sistema tem presente todos os reagentes e produtos, o solvente contém todos eles num espaço confinado. • O Sistema e a Vizinhança constituiem o Universo. • Se o sistema não troca energia nem matéria com a vizinhança, denomina-se sistema isolado. • Se o sistema troca energia mas não troca matéria com a vizinhança, este denomina-se sistema fechado. • Se o sistema troca energia e matéria com a vizinhança este demomina-se sistema aberto. Um organismo vivo é um sistema aberto
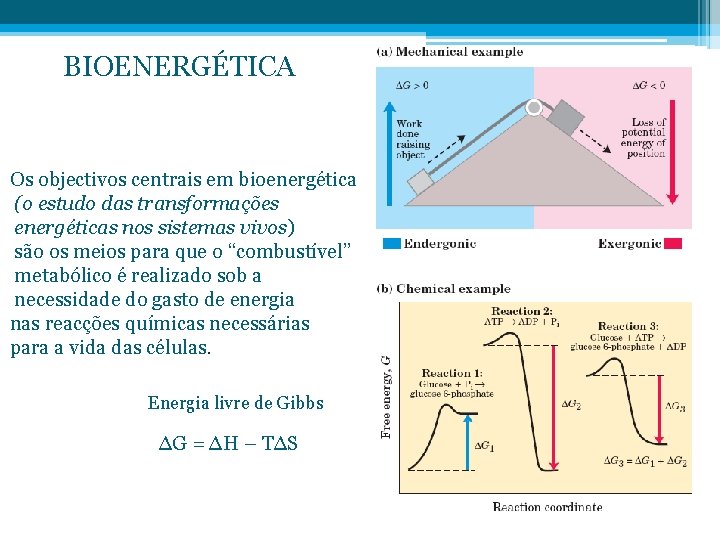
BIOENERGÉTICA Os objectivos centrais em bioenergética (o estudo das transformações energéticas nos sistemas vivos) são os meios para que o “combustível” metabólico é realizado sob a necessidade do gasto de energia nas reacções químicas necessárias para a vida das células. Energia livre de Gibbs ∆G = ∆H – T∆S
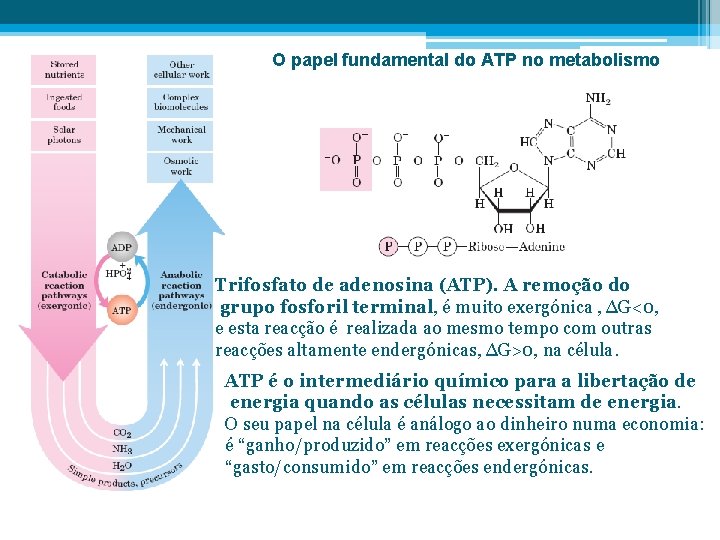
O papel fundamental do ATP no metabolismo Trifosfato de adenosina (ATP). A remoção do grupo fosforil terminal, é muito exergónica , ∆G<0, e esta reacção é realizada ao mesmo tempo com outras reacções altamente endergónicas, ∆G>0, na célula. ATP é o intermediário químico para a libertação de energia quando as células necessitam de energia. O seu papel na célula é análogo ao dinheiro numa economia: é “ganho/produzido” em reacções exergónicas e “gasto/consumido” em reacções endergónicas.

GENÉTICA • A propriedade mais fascinante das células e organismos vivos é a sua capacidade de se reproduzir em incontáveis gerações com grande perfeição e fidelidade. Esta continuidade implica estabilidade, ao longo de milhões de anos, na estrutura das moléculas que contêm a informação genética. • Uma das maiores descobertas do século vinte foi a natureza química e a estrutura tridimensional do material genético, Ácido desoxiribonucleico, DNA. • A sequenciação das subunidades monoméricas, os nucleótidos deste polímero lienar dá-nos as intruções para formação de outros componentes celulares. • O arquivamento eficiente, reprodução das mensagens genéticas define as espécies individuais, distingue uma espécie de outra, e assegura a sua continuidade por gerações sucessivas.

EVOLUÇÃO DA VIDA
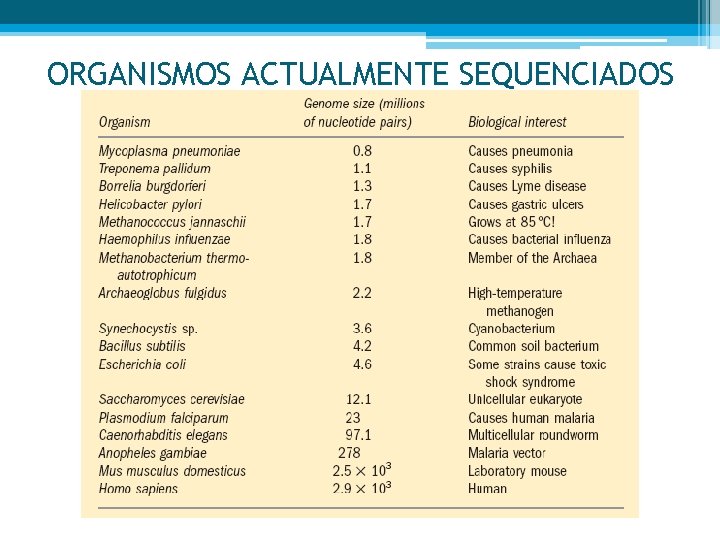
ORGANISMOS ACTUALMENTE SEQUENCIADOS
- Slides: 43