Licence Biologie UE physiologie cellulaire et animale losmolarit

Licence Biologie UE physiologie cellulaire et animale l’osmolarité Etienne Roux Laboratoire de Physiologie Cellulaire Respiratoire INSERM U 885 UFR des Sciences de la Vie Université Victor Segalen Bordeaux 2 contact: etienne. roux@u-bordeaux 2. fr support de cours : e-fisio. net site de l’UFR des sciences de la Vie

l’osmolarité I. mise en évidence de la pression osmotique II. caractéristiques physiques de l’osmolarité III. osmolarité et volume cellulaire : les cellules dans l’organisme IV. pression oncotique : les compartiments de l’organisme V. eau et osmolarité : l’organisme dans son milieu plan

I. mise en évidence de la pression osmotique observation expérimentale définitions pression osmotique osmose osmolarité – osmolalité concentration ionique
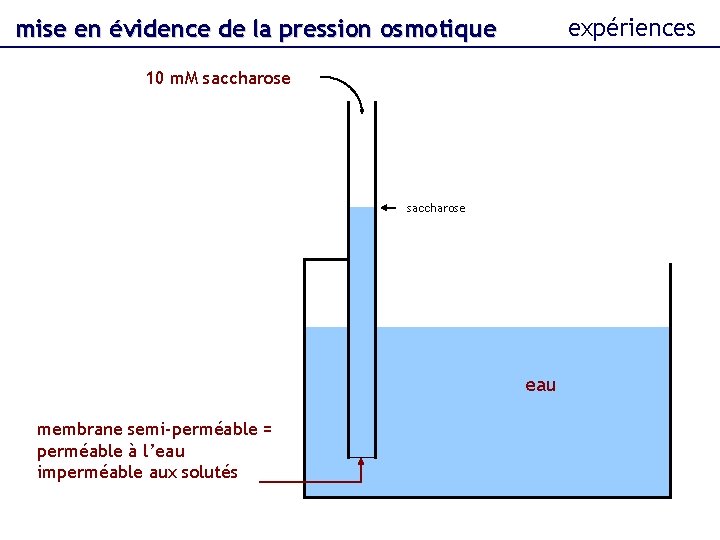
expériences mise en évidence de la pression osmotique 10 m. M saccharose eau membrane semi-perméable = perméable à l’eau imperméable aux solutés
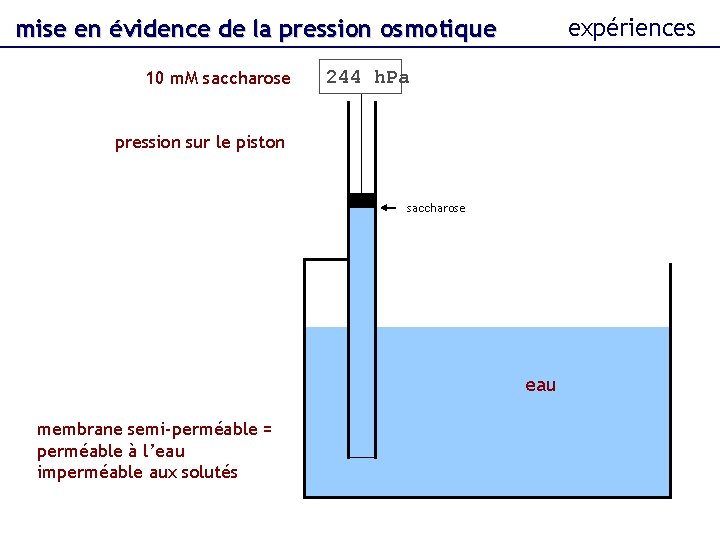
expériences mise en évidence de la pression osmotique 10 m. M saccharose 244 h. Pa pression sur le piston saccharose eau membrane semi-perméable = perméable à l’eau imperméable aux solutés
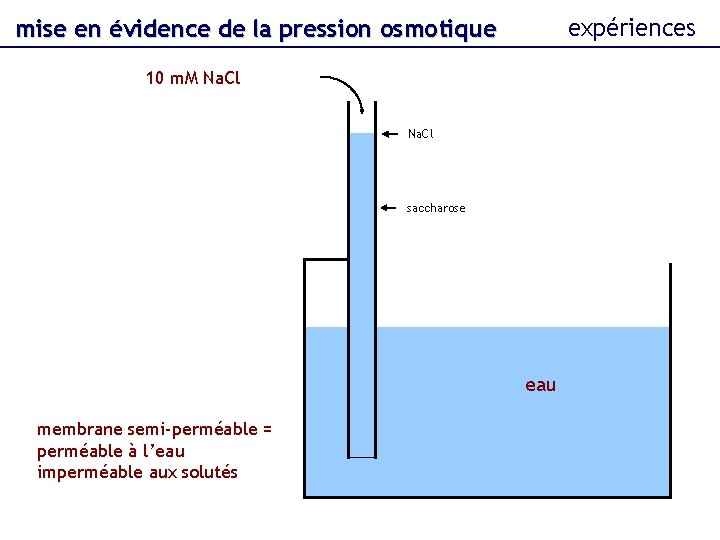
expériences mise en évidence de la pression osmotique 10 m. M Na. Cl saccharose eau membrane semi-perméable = perméable à l’eau imperméable aux solutés
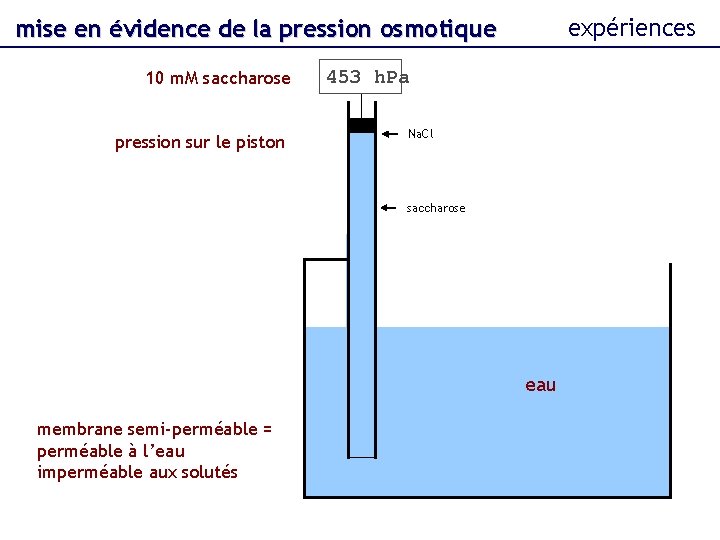
expériences mise en évidence de la pression osmotique 10 m. M saccharose pression sur le piston 453 h. Pa Na. Cl saccharose eau membrane semi-perméable = perméable à l’eau imperméable aux solutés

mise en évidence de la pression osmotique définition pression osmotique La pression osmotique est la pression exercée par les particules en solution, et responsable de l’osmose mouvement d’eau à travers une membrane semi-perméable, du compartiment le moins concentré en particules en solution vers le compartiment le plus en particules en solution. osmolarité L’osmolarité d’une solution est le nombre de moles de particules en solution dans 1 litre de solution. 1 osmole (osm) correspond à une mole de particules.

mise en évidence de la pression osmotique définition molarité et molalité La molarité est la concentration exprimée en moles par litre de solution. Une solution qui contient une mole par litre est une solution molaire. La molalité est la concentration exprimée en moles par kg d’eau. Une solution qui contient une mole par kg d’eau est une solution molale. osmolarité et osmolalité L’osmolarité d’une solution est le nombre de moles de particules en solution dans 1 litre de solution. L’osmolalité est le nombre de moles de particules en solution dans 1 kg d’eau.

mise en évidence de la pression osmotique définition NB : concentration ionique La concentration ionique d’une solution est le nombre de moles de charges présentes dans la solution. Son unité est l’équivalent (Eq) par volume de solution. exemple : calcul de la concentration ionique d’une solution de 10 m. M de Na. Cl est à la concentration de 10 m. M. Na. Cl se dissocie en Na+ et Cl-. Chaque mole de Na. Cl porte une mole de charges + et une de charges -. La concentration ionique de la solution est donc : 2 x 10 = 20 m. Eq. l-1. concentration ionique osmolarité

II. physique de l’osmolarité d’une solution ; coefficient osmotique exemples de calculs coefficient osmotique la loi de van’t Hoff définition unités exemples osmolarité d’un mélange de solutés osmolarité efficace solutés imperméants solutés perméants dynamique de l’osmose et conductivité hydraulique

physique de l’osmolarité L’osmolarité d’une solution est le nombre de moles de particules en solution dans 1 litre de solution. 1 osmole (osm) correspond à une mole de particules. exemple : calcul de l’osmolarité d’une solution de 10 m. M de saccharose 10 m. M = 0, 001 mol/L = 10 -3 mol/ L = 10 mol/m 3 saccharose = soluble dans l’eau en solution : ne se dissocie pas 1 molécule de sacharose en solution = 1 particule en solution 10 m. M de saccharose 10 milliosmoles de saccharose

physique de l’osmolarité L’osmolarité d’une solution est le nombre de moles de particules en solution dans 1 litre de solution. 1 osmole (osm) correspond à une mole de particules. exemple : calcul de l’osmolarité d’une solution de 10 m. M de Na. Cl 10 m. M = 0, 001 mol/L = 10 -3 mol/ L = 10 mol/m 3 Na. Cl = soluble dans l’eau en solution : se dissocie en Na+ et Cl 1 molécule de Na. Cl en solution 2 particules en solution* (*tout le Na. Cl ne de dissocie pas en Na+ et Cl-) 10 m. M de Na. Cl 20 milliosmoles de Na. Cl

physique de l’osmolarité coefficient osmotique l’osmolarité dépend de : concentration en solutés nombre de particules effectivement formées par la dissociation du soluté: nombre de particules formées par la dissociation d’une molécule de soluté facteur de correction : toutes les molécules de soluté ne se dissocient pas en solution

osmolarité physique de l’osmolarité coefficient osmotique osmolarité = (n/V). i. F n: nombre de moles de soluté V: volume n/V = molarité de la solution i : nombre de particules formées par dissociation du soluté F (phi) : coefficient osmotique = facteur de correction F 1 (F = 1 100% de dissociation) exemples : Mg. Cl 2 : F = 0, 89 i = 3 Na. Cl : F = 0, 93 i = 2

physique de l’osmolarité loi de van’t Hoff définition La pression osmotique d’une solution est donnée par la loi de van’t Hoff, dérivée de la loi sur les gaz parfaits. p = R. T. (n/V). i. F R : constante des gaz parfaits T : température n: nombre de moles de soluté V: volume (!!! l’unité internationale de volume est le m 3, et non le litre) i : nombre de particules formées par dissociation du soluté F (phi) : coefficient osmotique = facteur de correction

loi de van’t Hoff physique de l’osmolarité unités calcul de la pression osmotique en unités internationale : Pascal (Pa) p = R. T. (n/V). i. F Pa osmolarité : 1 atm = 101, 3 k. Pa = 760 mm. Hg en mol/m 3 en m. M R = 8, 314 (UI) T : en Kelvin (0 K = -273, 15°C ; 1 K = 1°C) n: sans unité i : sans unité F : sans unité V: !!! l’unité internationale de volume est le m 3, et non le litre

loi de van’t Hoff physique de l’osmolarité unités calcul de la pression osmotique en unités internationale : Pascal (Pa) p = R. T. (n/V). i. F k. Pa osmolarité : en mol/L (M) 1 atm = 101, 3 k. Pa = 760 mm. Hg R = 8, 314 (UI) T : en Kelvin (0 K = -273, 15°C ; 1 K = 1°C) n: sans unité i : sans unité F : sans unité V: !!! l’unité internationale de volume est le m 3, et non le litre

physique de l’osmolarité exemples loi de van’t Hoff p = R. T. (n/V). i. F exemple : calcul de la pression osmotique due à une solution de 10 m. M de saccharose, à 20°C. n/V = 10 m. M saccharose en solution : ne se dissocie pas i=1 F=1 p = 8, 314 x (20+273, 15) x 10 x 1 = 24372 Pa 244 h. Pa

physique de l’osmolarité exemples loi de van’t Hoff p = R. T. (n/V). i. F exemple : calcul de la pression osmotique due à une solution de 10 m. M de Na. Cl, à 20°C. n/V = 10 m. M Na. Cl en solution : se dissocie en Na+ et Cl i=2 F = 0, 93 p = 8, 314 x (20+273, 15) x 10 x 2 x 0, 93 = 45333 Pa 453 h. Pa

physique de l’osmolarité d’un mélange osmolarité d’un soluté osmolarité = molarité x(i. F) osmolarité d’un mélange de solutés osmolarité totale = S osmolarité de chaque soluté exemple : calcul de l’osmolarité d’une solution contenant 10 m. M de sacharose et 10 m. M de Na. Cl osmolarité du saccharose : 10 x 1 osmolarité du Na. Cl : 20 x 2 x 0, 93 = 10 mosm. L-1 = 18, 6 mosm. L-1 osmolarité totale = 28, 6 mosm. L-1
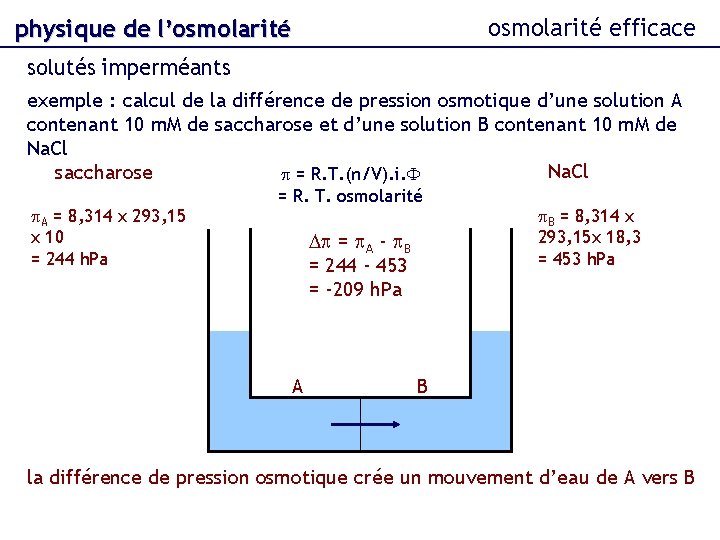
osmolarité efficace physique de l’osmolarité solutés imperméants exemple : calcul de la différence de pression osmotique d’une solution A contenant 10 m. M de saccharose et d’une solution B contenant 10 m. M de Na. Cl saccharose p = R. T. (n/V). i. F p. A = 8, 314 x 293, 15 x 10 = 244 h. Pa = R. T. osmolarité Dp = p. A - p. B = 244 - 453 = -209 h. Pa A p. B = 8, 314 x 293, 15 x 18, 3 = 453 h. Pa B la différence de pression osmotique crée un mouvement d’eau de A vers B
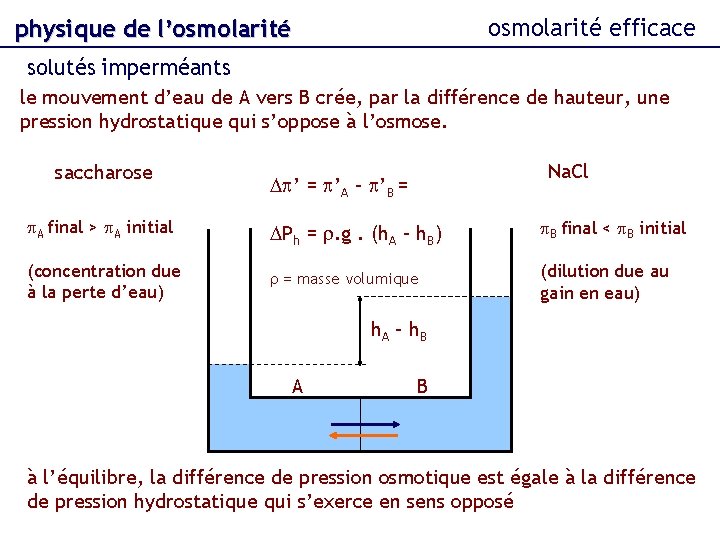
osmolarité efficace physique de l’osmolarité solutés imperméants le mouvement d’eau de A vers B crée, par la différence de hauteur, une pression hydrostatique qui s’oppose à l’osmose. saccharose Na. Cl Dp’ = p’A – p’B = p. A final > p. A initial DPh = r. g. (h. A – h. B) p. B final < p. B initial (concentration due à la perte d’eau) r = masse volumique (dilution due au gain en eau) h. A – h B A B à l’équilibre, la différence de pression osmotique est égale à la différence de pression hydrostatique qui s’exerce en sens opposé

physique de l’osmolarité efficace solutés perméants certains solutés traversent la membrane semi-perméable exemple : calcul de l’osmolarité et de la pression osmotique d’une solution contenant 10 m. M d’urée osmolarité = molarité x(i. F) osmolarité : 10 x 1 = 10 mosm. L-1 p = R. T. (n/V). i. F = R. T. osmolarité purée = 8, 314 x 293, 15 x 10 = 244 h. Pa
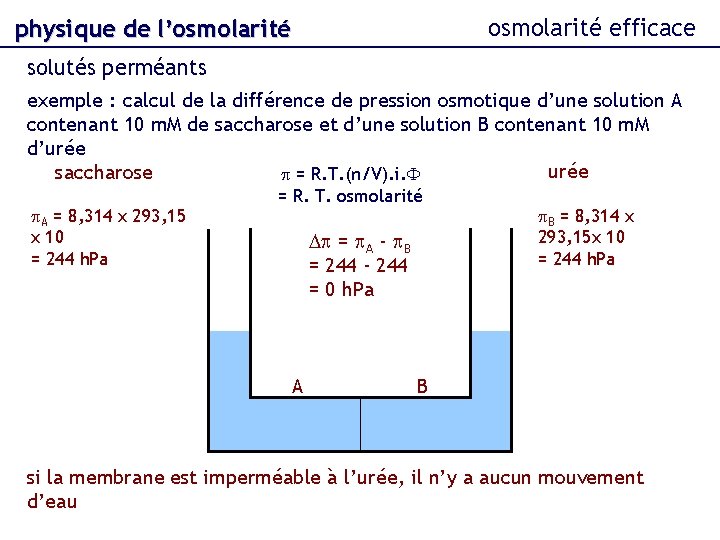
osmolarité efficace physique de l’osmolarité solutés perméants exemple : calcul de la différence de pression osmotique d’une solution A contenant 10 m. M de saccharose et d’une solution B contenant 10 m. M d’urée saccharose p = R. T. (n/V). i. F p. A = 8, 314 x 293, 15 x 10 = 244 h. Pa = R. T. osmolarité Dp = p. A - p. B = 244 - 244 = 0 h. Pa A p. B = 8, 314 x 293, 15 x 10 = 244 h. Pa B si la membrane est imperméable à l’urée, il n’y a aucun mouvement d’eau
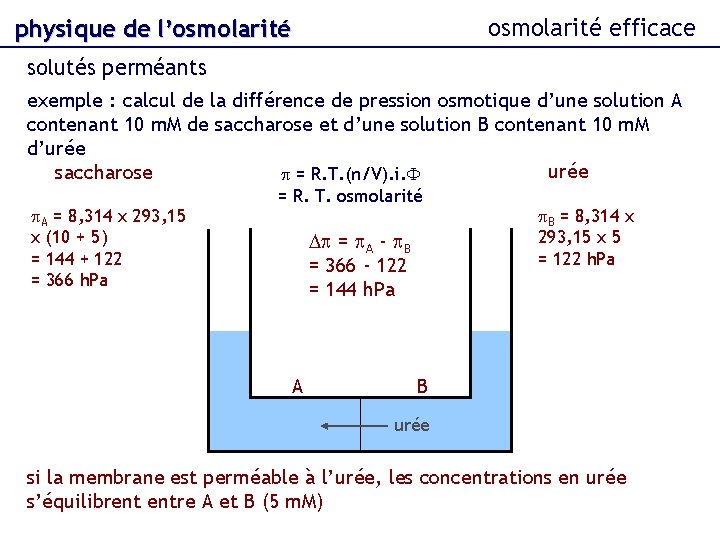
osmolarité efficace physique de l’osmolarité solutés perméants exemple : calcul de la différence de pression osmotique d’une solution A contenant 10 m. M de saccharose et d’une solution B contenant 10 m. M d’urée saccharose p = R. T. (n/V). i. F p. A = 8, 314 x 293, 15 x (10 + 5) = 144 + 122 = 366 h. Pa = R. T. osmolarité Dp = p. A - p. B = 366 - 122 = 144 h. Pa A p. B = 8, 314 x 293, 15 x 5 = 122 h. Pa B urée si la membrane est perméable à l’urée, les concentrations en urée s’équilibrent entre A et B (5 m. M)

osmolarité efficace physique de l’osmolarité solutés perméants exemple : calcul de la différence de pression osmotique d’une solution A contenant 10 m. M de saccharose et d’une solution B contenant 10 m. M d’urée saccharose p = R. T. (n/V). i. F p. A = 8, 314 x 293, 15 x (10 + 5) = 144 + 122 = 366 h. Pa = R. T. osmolarité Dp = p. A - p. B = 366 - 122 = 144 h. Pa A p. B = 8, 314 x 293, 15 x 5 = 122 h. Pa B si la membrane est perméable à l’urée, la pression osmotique est due au saccharose

physique de l’osmolarité efficace solutés perméants dans le cas d’un solution contenant des solutés perméants et non perméants, la pression osmotique à l’équilibre est due aux solutés imperméants osmolarité efficace : osmolarité des solutés non perméants NB : les flux d’eau et de particules n’étant pas instantanés, la situation d’aquilibre n’est pas obtenue immédiatement variations transitoires d’osmolarité, de pression osmotique et de volume

osmolarité efficace physique de l’osmolarité conductivité hydraulique débit d’eau à travers une membrane : différence de pression de part et d’autre de la membrane Jeau = d. V/dt = L x DP débit conductivité hydraulique (perméabilité de la membrane à l’eau) A p. A < p. B B cas d’un soluté perméant : flux du soluté à travers la membrane : Jparticule = perméabilité x DC NB : les variables sont interdépendantes différence de concentration de part et d’autre de la membrane
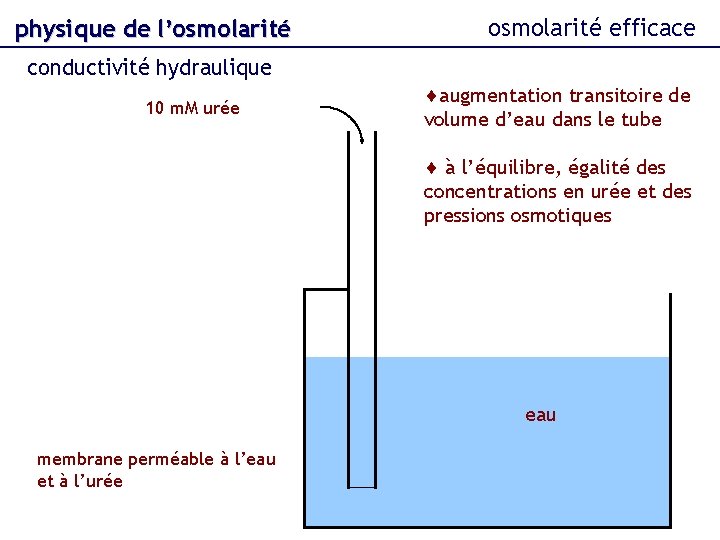
physique de l’osmolarité efficace conductivité hydraulique 10 m. M urée augmentation transitoire de volume d’eau dans le tube à l’équilibre, égalité des concentrations en urée et des pressions osmotiques eau membrane perméable à l’eau et à l’urée

III. osmolarité et volume cellulaire : les cellules dans l’organisme composition des milieux intérieurs liquide intersticiel milieu intracellulaire osmolarité cellulaire isosmolarité - isotonicité applications pratiques

osmolarité et volume cellulaire sang lymphe liquide extracellaire liquide céphalo-rachidien liquide extracellulaire cérébral liquide synovial urine. . . milieux intérieurs
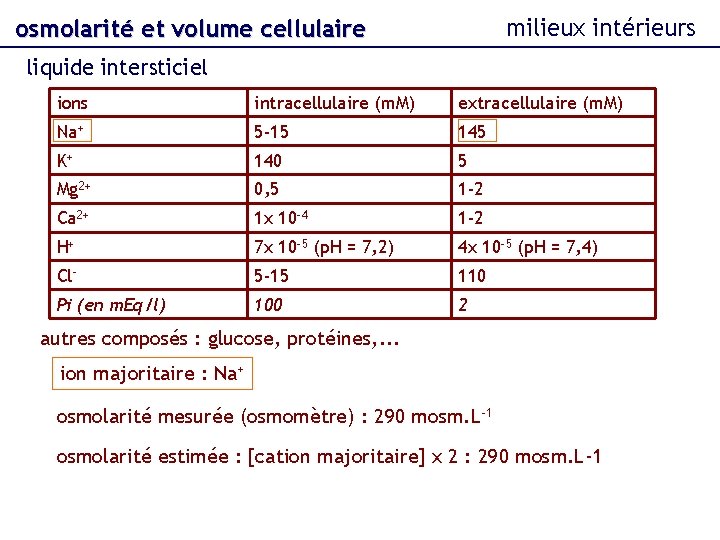
milieux intérieurs osmolarité et volume cellulaire liquide intersticiel ions intracellulaire (m. M) extracellulaire (m. M) Na+ 5 -15 145 K+ 140 5 Mg 2+ 0, 5 1 -2 Ca 2+ 1 x 10 -4 1 -2 H+ 7 x 10 -5 (p. H = 7, 2) 4 x 10 -5 (p. H = 7, 4) Cl- 5 -15 110 Pi (en m. Eq/l) 100 2 autres composés : glucose, protéines, . . . ion majoritaire : Na+ osmolarité mesurée (osmomètre) : 290 mosm. L-1 osmolarité estimée : [cation majoritaire] x 2 : 290 mosm. L-1
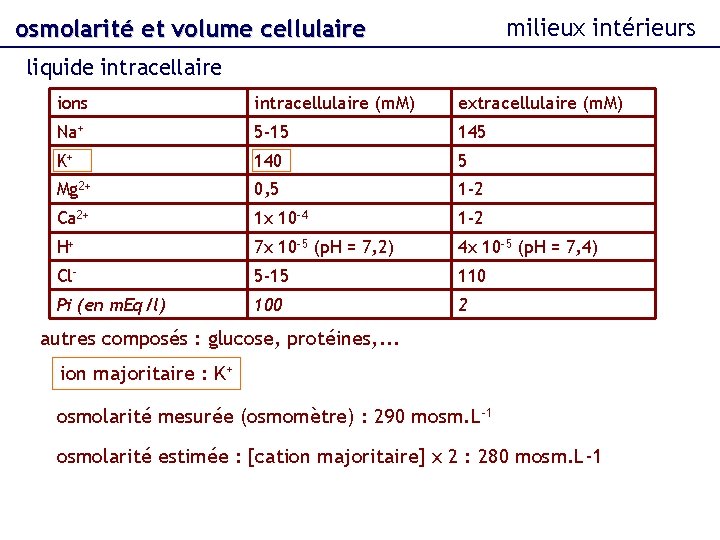
milieux intérieurs osmolarité et volume cellulaire liquide intracellaire ions intracellulaire (m. M) extracellulaire (m. M) Na+ 5 -15 145 K+ 140 5 Mg 2+ 0, 5 1 -2 Ca 2+ 1 x 10 -4 1 -2 H+ 7 x 10 -5 (p. H = 7, 2) 4 x 10 -5 (p. H = 7, 4) Cl- 5 -15 110 Pi (en m. Eq/l) 100 2 autres composés : glucose, protéines, . . . ion majoritaire : K+ osmolarité mesurée (osmomètre) : 290 mosm. L-1 osmolarité estimée : [cation majoritaire] x 2 : 280 mosm. L-1

osmolarité et volume cellulaire milieux intérieurs liquides intersticiel et intracellulaire les milieux extracellulaire et intracellulaire sont isomostiques l’osmolarité des différents milieux est obtenue différemment mesure et calcul de l’osmolarité d’une solution : mesure de l’osmolarité d’une solution : osmomètre osmolarité estimée d’un liquide biologique intérieur : [cation majoritaire] x 2 (équilibre des charges) osmolarité calculée d’une solution de composition déterminée : osmolarité = (n/V). i. F

osmolarité et volume cellulaire osmolarité cellulaire isosmolarité - isotonicité deux solutions sont isosmolaires si leurs osmolarités sont égales une solution est isotonique si son osmolarité efficace est égale à l’osmolarité cellulaire osmolarité et volume cellulaire solution isotonique volume cellulaire constant solution hypotonique augmentation du volume cellulaire solution hypertonique diminution du volume cellulaire

osmolarité et volume cellulaire osmolarité cellulaire application pratique détermination de la composition d’un solution de Na. Cl isotonique ex : perfusion sanguine osmolarité cellulaire : 290 mosm. L-1 osmolarité voulue de la solution de Na. Cl : 290 mosm. L-1 osmolarité = molarité. i. F molarité = osmolarité/(i. F) molarité de la solution de Na. Cl = 290 /(2 x 0, 93) = 156 m. M

IV. pression oncotique : les compartiments de l’organisme mise en évidence de la pression oncotique définition de la pression oncotique due à des colloïdes neutres pression oncotique due aux protéines : effet Donnan pression oncotique plasmatique et pression hydrostatique pression oncotique et filtration glomérulaire
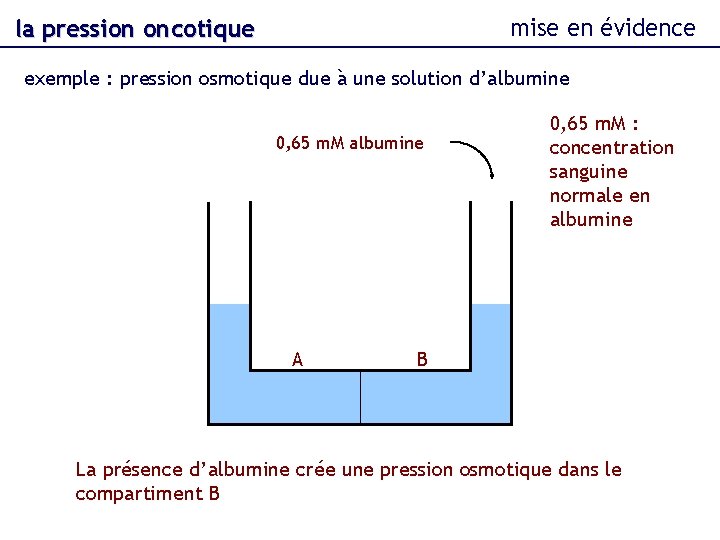
mise en évidence la pression oncotique exemple : pression osmotique due à une solution d’albumine 0, 65 m. M albumine A 0, 65 m. M : concentration sanguine normale en albumine B La présence d’albumine crée une pression osmotique dans le compartiment B
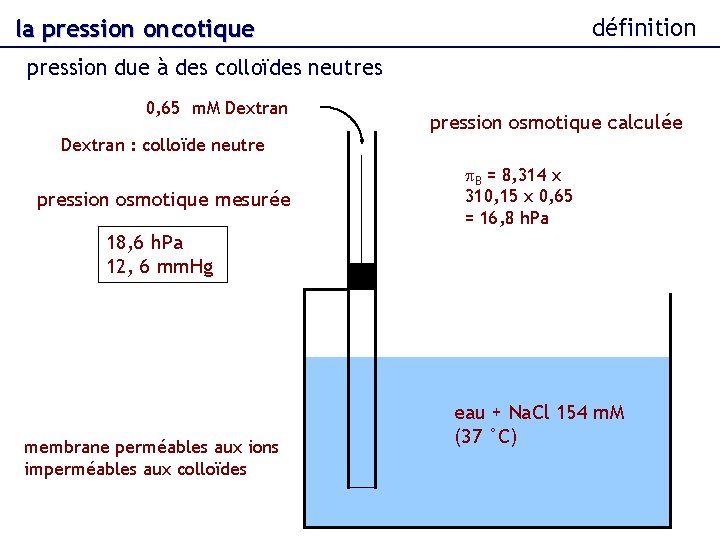
définition la pression oncotique pression due à des colloïdes neutres 0, 65 m. M Dextran pression osmotique calculée Dextran : colloïde neutre pression osmotique mesurée p. B = 8, 314 x 310, 15 x 0, 65 = 16, 8 h. Pa 18, 6 h. Pa 12, 6 mm. Hg membrane perméables aux ions imperméables aux colloïdes eau + Na. Cl 154 m. M (37 °C)
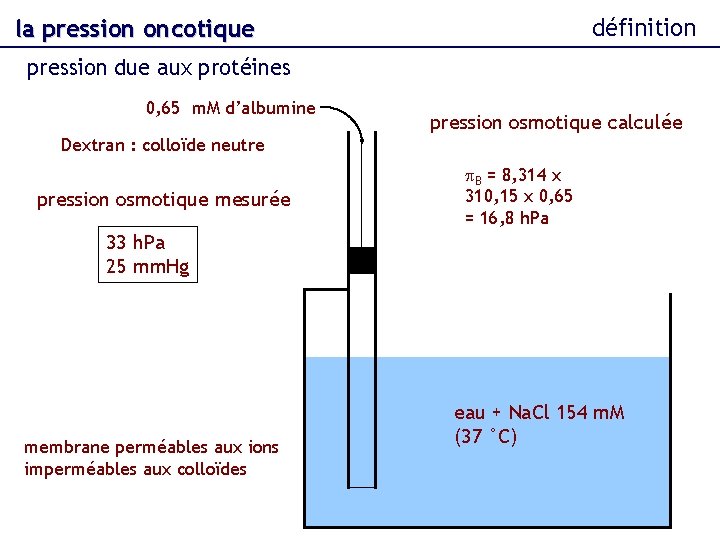
définition la pression oncotique pression due aux protéines 0, 65 m. M d’albumine pression osmotique calculée Dextran : colloïde neutre pression osmotique mesurée p. B = 8, 314 x 310, 15 x 0, 65 = 16, 8 h. Pa 33 h. Pa 25 mm. Hg membrane perméables aux ions imperméables aux colloïdes eau + Na. Cl 154 m. M (37 °C)

la pression oncotique pression due aux protéines définition effet Donnan pression oncotique = pression colloïdo-osmotique = pression osmotique due aux colloïdes : « aspect de colle » : intermédiaire homogène entre suspension et solution vraie (taille entre 2 et 20 nm) pression oncotique due aux protéines : pression oncotique « vraie » + effet Donnan membrane « de Donnan » : membrane perméable à certaines particules chargées et pas à d’autres.

définition la pression oncotique pression due aux protéines effet Donnan osmolarité de chaque compartiment ? exemple: [X+] = 2 M [Y-] = 1 M [Z-] = 1 M membrane perméable à X et Y, imperméable à Z [Z-] = 1 M [X+] [Y-] A [X+] [Y-] B si les solutés X, Y et Z ne sont pas chargés : osmolarité efficace : osmolarité de Z osmolarité A – osmolarité B = osmolarité Z = 1 osm. L-1

définition la pression oncotique pression due aux protéines effet Donnan osmolarité de chaque compartiment ? exemple: [X+] = 2 M [Y-] = 1 M [Z-] = 1 M membrane perméable à X et Y, imperméable à Z [Z-] = 1 M [X+] [Y-] A B si les solutés X, Y et Z sont chargés : équation de Gibbs-Donnan [X+]A [Y-]A = [X+]B [Y-]B + électroneutralité + conservation de la matière répartition inégale de X+ et Y- entre A et B

définition la pression oncotique pression due aux protéines effet Donnan osmolarité de chaque compartiment ? exemple: [X+] = 2 M [Y-] = 1 M [Z-] = 1 M [X+] = 1, 33 [Y-] = 0, 33 [X+] = 0, 67 [Y-] = 0, 67 A membrane perméable à X et Y, imperméable à Z B A : osmolarité = 1 +1, 33 + 0, 33 B : osmolarité = 1, 33 osmolarité A – osmolarité B = 1, 33 osm. L-1 > osmolarité Z répartition inégale de X+ et Y- entre A et B

la pression oncotique pression due aux protéines définition effet Donnan pression oncotique due aux protéines : pression oncotique « vraie » + effet Donnan membrane « de Donnan » : membrane perméable à certaines particules chargées et pas à d’autres. albumine : protéines chargée négativement effet Donnan pression oncotique > pression oncotique “vraie” (les solutés chargés sont plus concentrés dans le compartiment où se trouvent le soluté chargé imperméant)

la pression oncotique pressions oncotique et hydrostatique mouvement d’eau entre le plasma et le milieu intersticiel individu 60 Kg : 36 L d’eau (60 %) plasma liquide intersticiel eau cellulaire 3 L 9 L 24 L paroi capillaire membrane plasmique perméable à l’eau perméable aux solutés imperméable aux protéines perméable à l’eau perméable à certains solutés imperméable aux protéines plasma : protéines (albumine) liquide intersticiel : peu de protéines

la pression oncotique pressions oncotique et hydrostatique mouvement d’eau entre le plasma et le milieu intersticiel individu 60 Kg : 36 L d’eau (60 %) plasma liquide intersticiel eau cellulaire 3 L 9 L 24 L paroi capillaire plasma : protéines (albumine) liquide intersticiel : peu de protéines osmolarité efficace = osmolarité oncotique pression oncotique osmose du milieu intersticiel vers le milieu plasmatique
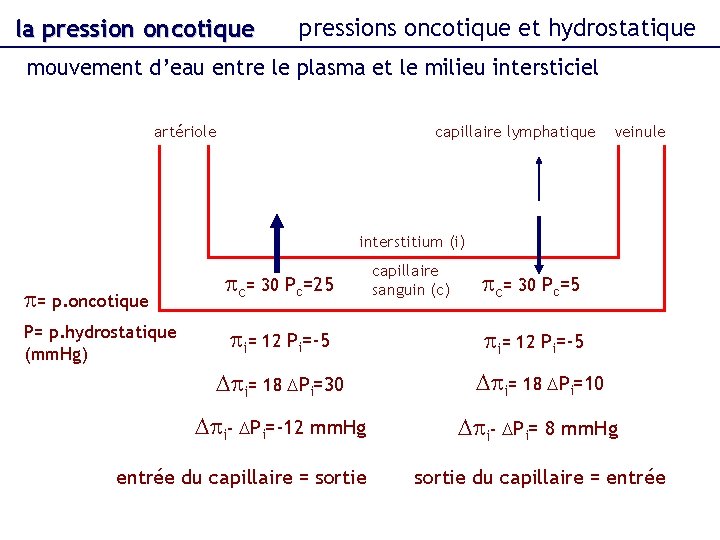
la pression oncotique pressions oncotique et hydrostatique mouvement d’eau entre le plasma et le milieu intersticiel artériole capillaire lymphatique veinule interstitium (i) p= p. oncotique P= p. hydrostatique (mm. Hg) pc= 30 Pc=25 capillaire sanguin (c) pc= 30 Pc=5 pi= 12 Pi=-5 Dpi= 18 DPi=30 Dpi= 18 DPi=10 Dpi- DPi=-12 mm. Hg Dpi- DPi= 8 mm. Hg entrée du capillaire = sortie du capillaire = entrée

la pression oncotique pressions oncotique et hydrostatique mouvement d’eau entre le plasma et le milieu intersticiel entrée du capillaire : sortie de liquide du capillaire (filtration) (homme : 20 L/jour) sortie du capillaire : entrée de liquide dans le capillaire (réabsorption) (homme : 18 L/jour) capillaire lymphatique : entrée de liquide dans le S. lymphatique (homme : 2 L/jour) hypoalbuminémie (<20 g. L-1) : diminution pc augmentation filtration ; diminution réabsorption : oedème
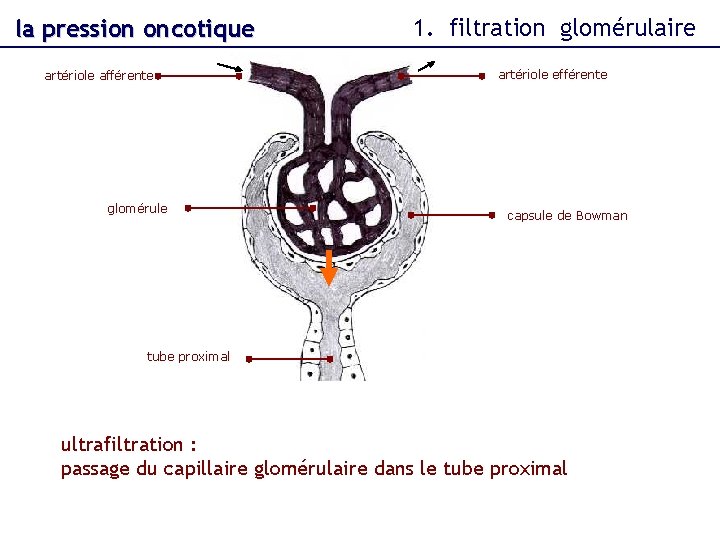
la pression oncotique artériole afférente glomérule 1. filtration glomérulaire artériole efférente capsule de Bowman tube proximal ultrafiltration : passage du capillaire glomérulaire dans le tube proximal
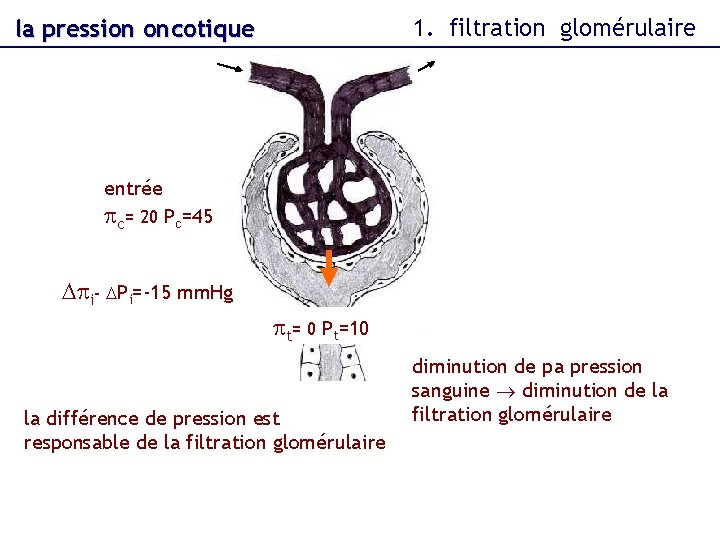
1. filtration glomérulaire la pression oncotique entrée pc= 20 Pc=45 Dpi- DPi=-15 mm. Hg pt= 0 Pt=10 la différence de pression est responsable de la filtration glomérulaire diminution de pa pression sanguine diminution de la filtration glomérulaire

V. osmolarité et milieu de vie : l’organisme dans son milieu osmolarité et milieu marin composition et osmolarité de l’eau de mer conséquences biologiques animaux osmoconformes et osmorégulateurs animaux osmoconformes animaux osmorégulateurs osmolarité et milieu d’eau douce composition et osmolarité de l’eau douce conséquences biologiques osmorégulation des animaux dulçaquicoles
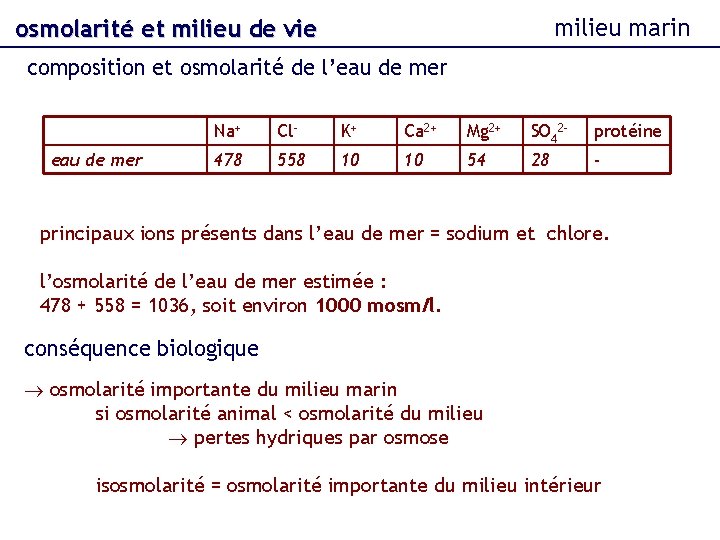
milieu marin osmolarité et milieu de vie composition et osmolarité de l’eau de mer Na+ Cl- K+ Ca 2+ Mg 2+ SO 42 - protéine 478 558 10 10 54 28 - principaux ions présents dans l’eau de mer = sodium et chlore. l’osmolarité de l’eau de mer estimée : 478 + 558 = 1036, soit environ 1000 mosm/l. conséquence biologique osmolarité importante du milieu marin si osmolarité animal < osmolarité du milieu pertes hydriques par osmose isosmolarité = osmolarité importante du milieu intérieur
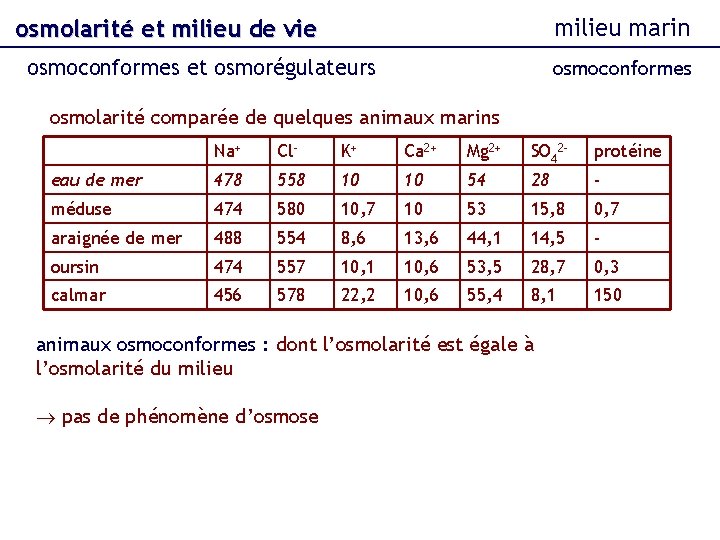
milieu marin osmolarité et milieu de vie osmoconformes et osmorégulateurs osmoconformes osmolarité comparée de quelques animaux marins Na+ Cl- K+ Ca 2+ Mg 2+ SO 42 - protéine eau de mer 478 558 10 10 54 28 - méduse 474 580 10, 7 10 53 15, 8 0, 7 araignée de mer 488 554 8, 6 13, 6 44, 1 14, 5 - oursin 474 557 10, 1 10, 6 53, 5 28, 7 0, 3 calmar 456 578 22, 2 10, 6 55, 4 8, 1 150 animaux osmoconformes : dont l’osmolarité est égale à l’osmolarité du milieu pas de phénomène d’osmose
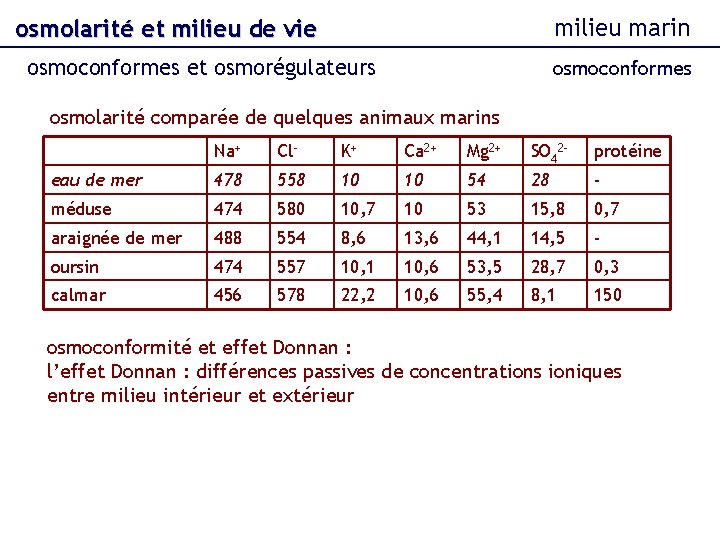
milieu marin osmolarité et milieu de vie osmoconformes et osmorégulateurs osmoconformes osmolarité comparée de quelques animaux marins Na+ Cl- K+ Ca 2+ Mg 2+ SO 42 - protéine eau de mer 478 558 10 10 54 28 - méduse 474 580 10, 7 10 53 15, 8 0, 7 araignée de mer 488 554 8, 6 13, 6 44, 1 14, 5 - oursin 474 557 10, 1 10, 6 53, 5 28, 7 0, 3 calmar 456 578 22, 2 10, 6 55, 4 8, 1 150 osmoconformité et effet Donnan : l’effet Donnan : différences passives de concentrations ioniques entre milieu intérieur et extérieur

osmolarité et milieu de vie osmoconformes et osmorégulateurs milieu marin osmoconformes estimation de l’effet Donnan : Robertson (1956) échantillons de LEC dans un sac semi-perméable en Cellophane, mis dans l’eau de mer. Les concentrations ioniques s’équilibrent de manière passive de part et d’autre de la membrane de cellophane (phénomène de dialyse). Les compositions ioniques ainsi obtenues sont comparées avec les concentrations in vivo.
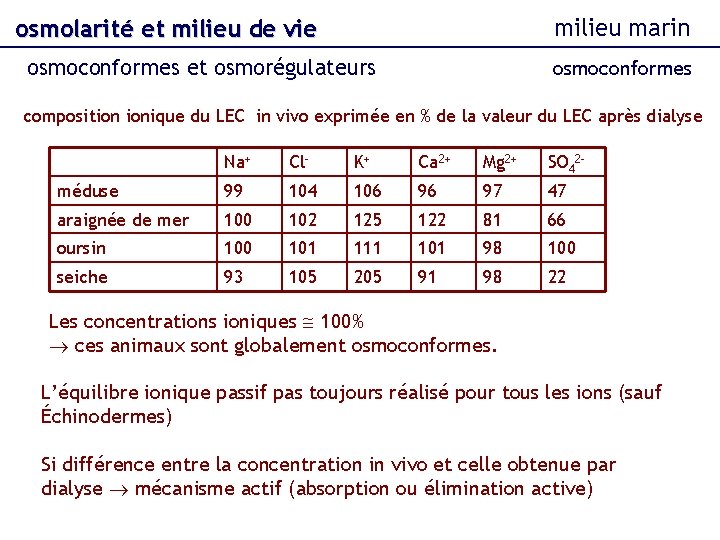
milieu marin osmolarité et milieu de vie osmoconformes et osmorégulateurs osmoconformes composition ionique du LEC in vivo exprimée en % de la valeur du LEC après dialyse Na+ Cl- K+ Ca 2+ Mg 2+ SO 42 - méduse 99 104 106 96 97 47 araignée de mer 100 102 125 122 81 66 oursin 100 101 111 101 98 100 seiche 93 105 205 91 98 22 Les concentrations ioniques 100% ces animaux sont globalement osmoconformes. L’équilibre ionique passif pas toujours réalisé pour tous les ions (sauf Échinodermes) Si différence entre la concentration in vivo et celle obtenue par dialyse mécanisme actif (absorption ou élimination active)
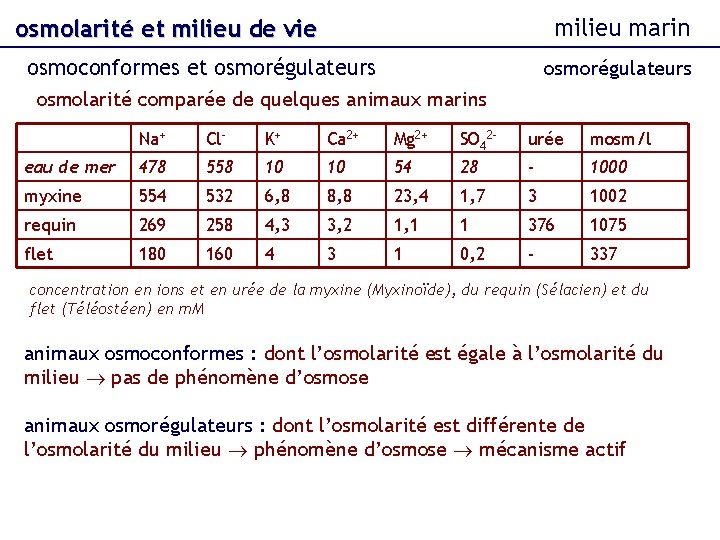
milieu marin osmolarité et milieu de vie osmoconformes et osmorégulateurs osmolarité comparée de quelques animaux marins Na+ Cl- K+ Ca 2+ Mg 2+ SO 42 - urée mosm/l eau de mer 478 558 10 10 54 28 - 1000 myxine 554 532 6, 8 8, 8 23, 4 1, 7 3 1002 requin 269 258 4, 3 3, 2 1, 1 1 376 1075 flet 180 160 4 3 1 0, 2 - 337 concentration en ions et en urée de la myxine (Myxinoïde), du requin (Sélacien) et du flet (Téléostéen) en m. M animaux osmoconformes : dont l’osmolarité est égale à l’osmolarité du milieu pas de phénomène d’osmose animaux osmorégulateurs : dont l’osmolarité est différente de l’osmolarité du milieu phénomène d’osmose mécanisme actif
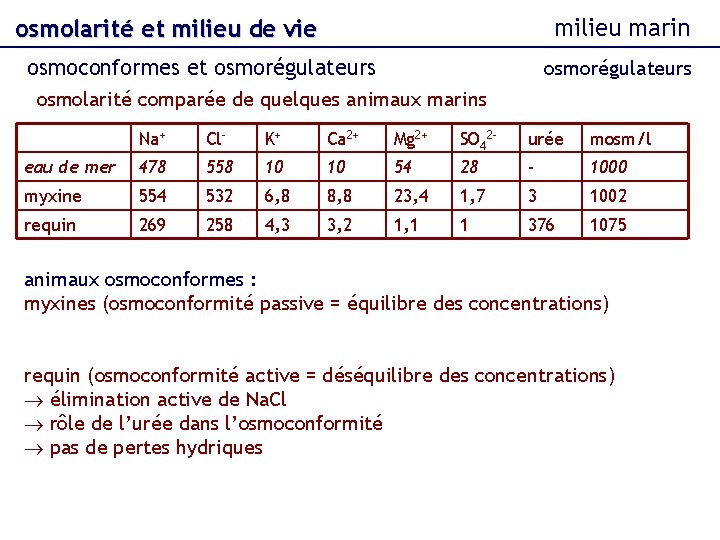
milieu marin osmolarité et milieu de vie osmoconformes et osmorégulateurs osmolarité comparée de quelques animaux marins Na+ Cl- K+ Ca 2+ Mg 2+ SO 42 - urée mosm/l eau de mer 478 558 10 10 54 28 - 1000 myxine 554 532 6, 8 8, 8 23, 4 1, 7 3 1002 requin 269 258 4, 3 3, 2 1, 1 1 376 1075 animaux osmoconformes : myxines (osmoconformité passive = équilibre des concentrations) requin (osmoconformité active = déséquilibre des concentrations) élimination active de Na. Cl rôle de l’urée dans l’osmoconformité pas de pertes hydriques
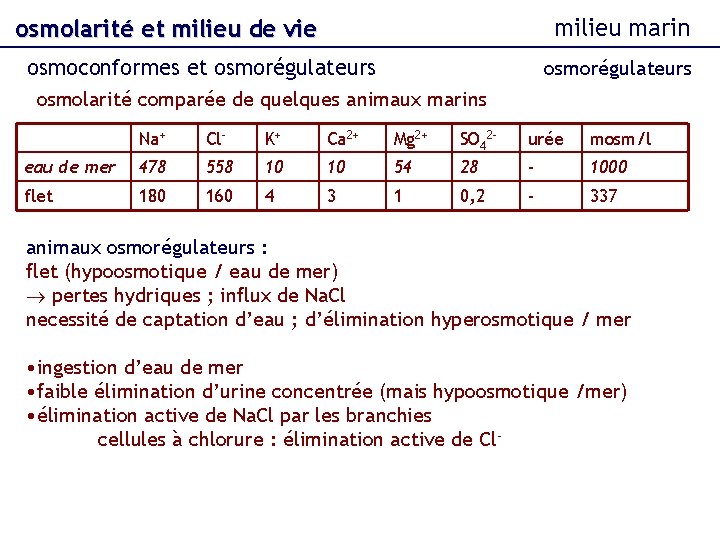
milieu marin osmolarité et milieu de vie osmoconformes et osmorégulateurs osmolarité comparée de quelques animaux marins Na+ Cl- K+ Ca 2+ Mg 2+ SO 42 - urée mosm/l eau de mer 478 558 10 10 54 28 - 1000 flet 180 160 4 3 1 0, 2 - 337 animaux osmorégulateurs : flet (hypoosmotique / eau de mer) pertes hydriques ; influx de Na. Cl necessité de captation d’eau ; d’élimination hyperosmotique / mer • ingestion d’eau de mer • faible élimination d’urine concentrée (mais hypoosmotique /mer) • élimination active de Na. Cl par les branchies cellules à chlorure : élimination active de Cl-
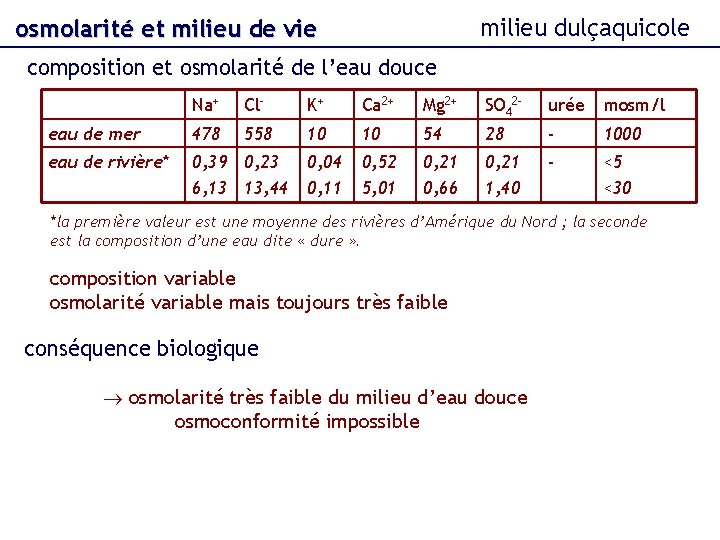
milieu dulçaquicole osmolarité et milieu de vie composition et osmolarité de l’eau douce Na+ Cl- K+ Ca 2+ Mg 2+ SO 42 - urée mosm/l eau de mer 478 558 10 10 54 28 - 1000 eau de rivière* 0, 39 0, 23 6, 13 13, 44 0, 04 0, 11 0, 52 5, 01 0, 21 0, 66 0, 21 1, 40 - <5 <30 *la première valeur est une moyenne des rivières d’Amérique du Nord ; la seconde est la composition d’une eau dite « dure » . composition variable osmolarité variable mais toujours très faible conséquence biologique osmolarité très faible du milieu d’eau douce osmoconformité impossible
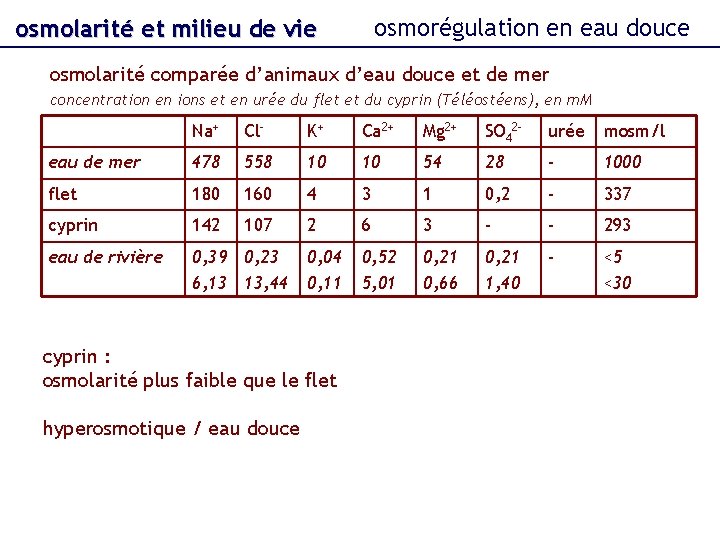
osmorégulation en eau douce osmolarité et milieu de vie osmolarité comparée d’animaux d’eau douce et de mer concentration en ions et en urée du flet et du cyprin (Téléostéens), en m. M Na+ Cl- K+ Ca 2+ Mg 2+ SO 42 - urée mosm/l eau de mer 478 558 10 10 54 28 - 1000 flet 180 160 4 3 1 0, 2 - 337 cyprin 142 107 2 6 3 - - 293 eau de rivière 0, 39 0, 23 6, 13 13, 44 0, 04 0, 11 0, 52 5, 01 0, 21 0, 66 0, 21 1, 40 - <5 <30 cyprin : osmolarité plus faible que le flet hyperosmotique / eau douce
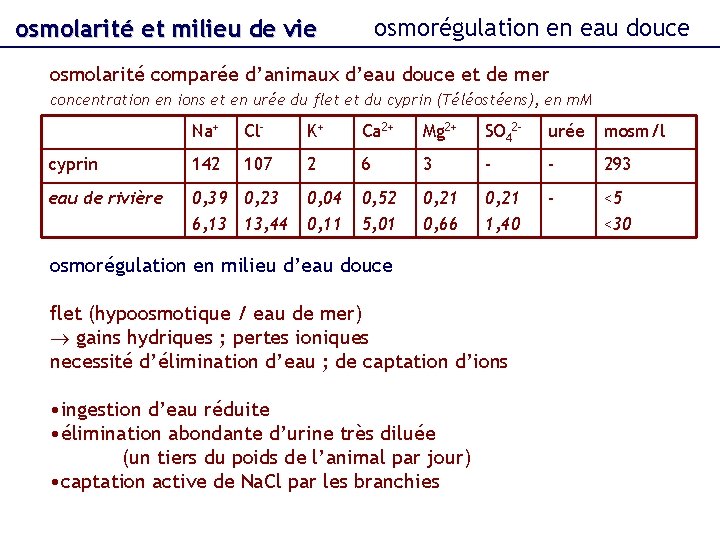
osmorégulation en eau douce osmolarité et milieu de vie osmolarité comparée d’animaux d’eau douce et de mer concentration en ions et en urée du flet et du cyprin (Téléostéens), en m. M Na+ Cl- K+ Ca 2+ Mg 2+ SO 42 - urée mosm/l cyprin 142 107 2 6 3 - - 293 eau de rivière 0, 39 0, 23 6, 13 13, 44 0, 04 0, 11 0, 52 5, 01 0, 21 0, 66 0, 21 1, 40 - <5 <30 osmorégulation en milieu d’eau douce flet (hypoosmotique / eau de mer) gains hydriques ; pertes ioniques necessité d’élimination d’eau ; de captation d’ions • ingestion d’eau réduite • élimination abondante d’urine très diluée (un tiers du poids de l’animal par jour) • captation active de Na. Cl par les branchies
- Slides: 64