Lic classicoA D Azuni Sassari Prof Paolo Abis

Lic. classico”A. D. Azuni” - Sassari Prof. Paolo Abis Legge delle proporzioni multiple John Dalton (1766 - 1844) Difficile da capire ? http: //web. tiscali. it/abitec_2/

Legge delle proporzioni multiple "Quando due elementi si combinano tra loro per formare composti diversi, le quantità di uno di essi che si combinano con una quantità fissa dell'altro, stanno fra loro in rapporti semplici, esprimibili mediante numeri interi, generalmente piccoli. ". n Composto 1 A 2 + 2 B 2 n 2 AB 2 Composto 2 A 2 + 2 B 2 2 AB 2

Legge delle proporzioni multiple "Quando due elementi si combinano tra loro per formare composti diversi, le quantità di uno di essi che si combinano con una quantità fissa dell'altro, stanno fra loro in rapporti semplici, esprimibili mediante numeri interi, generalmente piccoli. ". n Composto 1 1 A 2 + 2 B 2 n Composto 2 A 2 + B 2 2 AB 2 2 1 2 AB 1 3

Legge delle proporzioni multiple "Quando due elementi si combinano tra loro per formare composti diversi, le quantità di uno di essi che si combinano con una quantità fissa dell'altro, stanno fra loro in rapporti semplici, esprimibili mediante numeri interi, generalmente piccoli. ". n Composto. Quantità 1 1 A 2 + 2 B 2 n Composto 2 A 2 + B 2 2 AB B 22 2 1 B 2 AB 1 4

Legge delle proporzioni multiple "Quando due elementi si combinano tra loro per formare composti diversi, le quantità di uno di essi che si combinano con una quantità fissa dell'altro, stanno fra loro in rapporti semplici, esprimibili interi generalmente piccoli. ". mediante numeri interi, Quantità B 2 Rapporto 2 : B N. intero =2 1 5

Conclusioni n La legge delle proporzioni multiple può essere considerata un’estensione della legge delle proporzioni definite L. proporzioni multiple Gli elementi si combinano secondo proporzioni definite e costanti, per formare un composto • Gli elementi possono formare più composti • Uno degli elementi rimane in quantità fisse (A) • L’altro varia nelle quantità (B) • Le quantità di B nei due composti stanno tra loro in rapporto esprimibile con un numero intero 6

Esempio n Il carbonio può combinarsi con l’ossigeno in due modi diversi : + Carbonio 1 g Ossigeno 1, 33 g Ossido di carbonio 2, 33 g Ossigeno 2, 66 g Anidride carbonica 3, 66 g + Carbonio 1 g 7

Esempio n Abbiamo sempre le stesse quantità del carbonio: 1 g + Carbonio 1 g Ossigeno 1, 33 g Ossido di carbonio 2, 33 g Ossigeno 2, 66 g Anidride carbonica 3, 66 g + Carbonio 1 g 8

Esempio n Ma quantità diverse di ossigeno : 1, 33 g e 2, 66 g + Carbonio 1 g Ossigeno 1, 33 g Ossido di carbonio 2, 33 g Ossigeno 2, 66 g Anidride carbonica 3, 66 g + Carbonio 1 g 9

Esempio n Il rapporto fra le quantità di ossigeno è : 2, 66 /1, 33 = 2/1 + n Carbonio 1 g Ossigeno 1, 33 g Ossido di carbonio 2, 33 g Carbonio 1 g Ossigeno 2, 66 g Anidride carbonica 3, 66 g Da ciò si deduce che le quantità di ossigeno che si combinano con la stessa quantità di carbonio (per formare due composti diversi) sono l’una il doppio + dell’altra 10
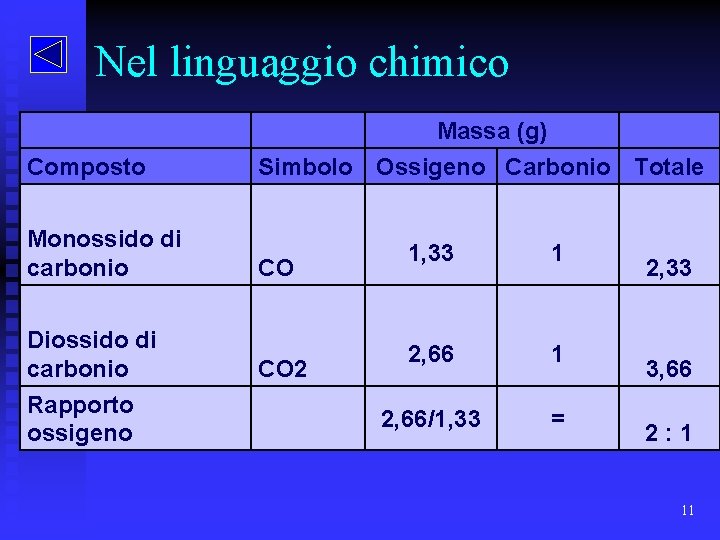
Nel linguaggio chimico Composto Massa (g) Simbolo Ossigeno Carbonio Totale Monossido di carbonio CO Diossido di carbonio Rapporto ossigeno CO 2 1, 33 1 2, 66/1, 33 = 2, 33 3, 66 2: 1 11

Altro esempio, stessi composti 12
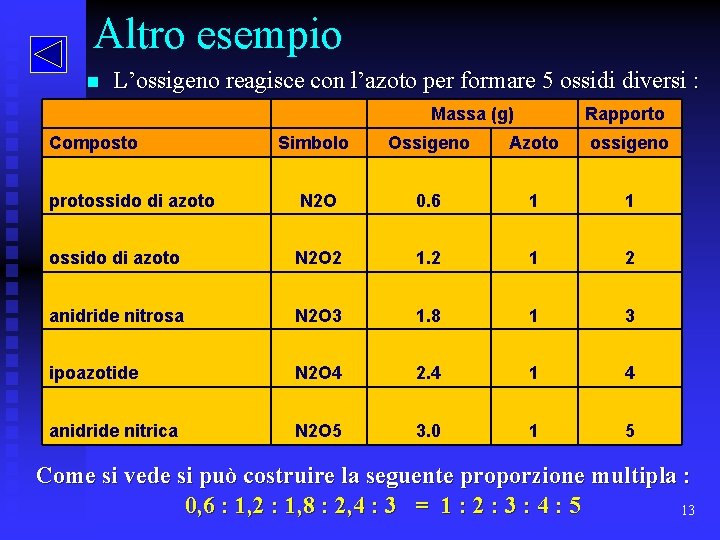
Altro esempio n L’ossigeno reagisce con l’azoto per formare 5 ossidi diversi : Massa (g) Composto Simbolo Rapporto Ossigeno Azoto ossigeno protossido di azoto N 2 O 0. 6 1 1 ossido di azoto N 2 O 2 1 2 anidride nitrosa N 2 O 3 1. 8 1 3 ipoazotide N 2 O 4 2. 4 1 4 anidride nitrica N 2 O 5 3. 0 1 5 Come si vede si può costruire la seguente proporzione multipla : 0, 6 : 1, 2 : 1, 8 : 2, 4 : 3 = 1 : 2 : 3 : 4 : 5 13

Conseguenze della legge secondo Dalton: la teoria atomica n Dal fatto che lo studio di svariatissime reazioni chimiche continuava a far apparire numeri interi lo scienziato dedusse che questa fosse una manifestazione della natura discontinua o atomica della materia: un atomo può combinarsi con uno o due o tre o. . . altri atomi, mai con 1/2, 2/3, . . . di atomo, n Pertanto la materia è fatta di atomi 14

Teoria atomica La Materia e’ composta da Atomi che non possono essere nè creati nè distrutti John Dalton (1766 -1844) 15

La teoria atomica di Dalton poggia su queste ipotesi: n n 1)- ogni forma di materia è costituita da atomi; gli atomi sono tutti inalterabili ed indivisibili; 2)- in una stessa sostanza ( elemento ) gli atomi sono tutti uguali; 3)- gli atomi di diversi elementi non sono uguali fra loro e non possiedono la stessa massa; 4)- le trasformazioni chimiche avvengono per unione o separazione di atomi tra di loro. 16

In definitiva … n L’atomo è la più piccola quantità di un elemento che può essere presente nei composti soltanto come multiplo intero. Atomo : la più piccola particella di un elemento che, da sola o riunita in molecole, da luogo all’elemento stesso. • Esistono elementi monoatomici : Gas nobili elio, neon, argon ecc. • Elementi bi-atomioci: ossigeno, idrogeno, fluoro ecc. • Elementi pluri-atomici : fosforo (P 4), zolfo (S 8) … 17

Le molecole Molecola : La più piccola particella di una sostanza che della sostanza stessa conserva tutte le proprietà. n Le molecole sono costituite da atomi. n Molecola dell’acqua Molecola del DNA 18

Macroscopico e microscopico n n Una molecola possiede le proprietà chimiche dell’elemento o del composto da cui proviene, ma non ne possiede le proprietà fisiche. Non ha senso, infatti, parlare di punto di ebollizione o di punto di fusione riferiti ad una singola molecola. Le proprietà fisiche sono proprietà macroscopiche Le proprietà chimiche sono proprietà microscopiche 19
- Slides: 19