Lezione 4 Collagene Proteine globulari Folding e misfolding

Lezione 4 Collagene Proteine globulari Folding e misfolding 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 0

Il collagene – struttura primaria • La struttura primaria è un’unità tripeptidica ripetuta …-G-X-Y-G-X-Y-… • La glicina è il 33% della somma degli amminoacidi • X è spesso (25%) Prolina (Pro) • Y è spesso (16%) 4 -idrossiprolina (Hyp) 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 1

Il collagene – struttura primaria …-G-X-Y-G-… 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 2
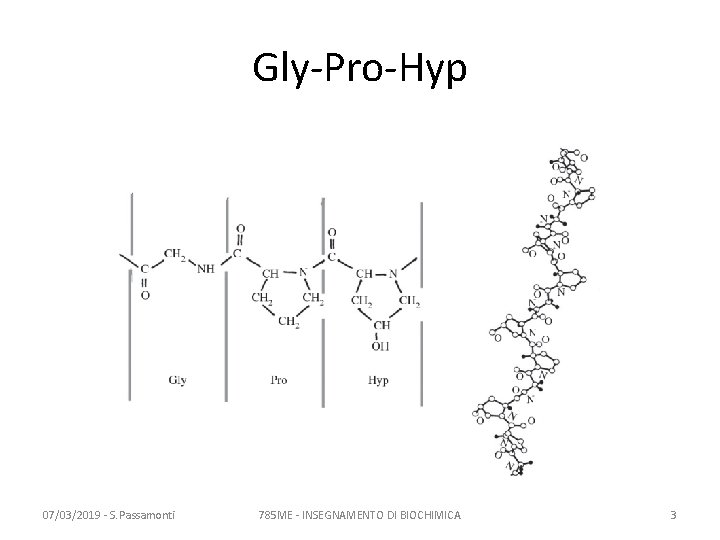
Gly-Pro-Hyp 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 3
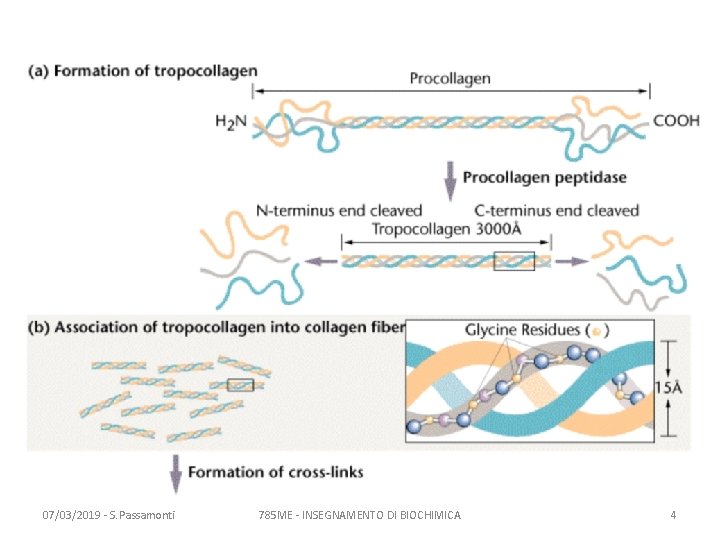
07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 4
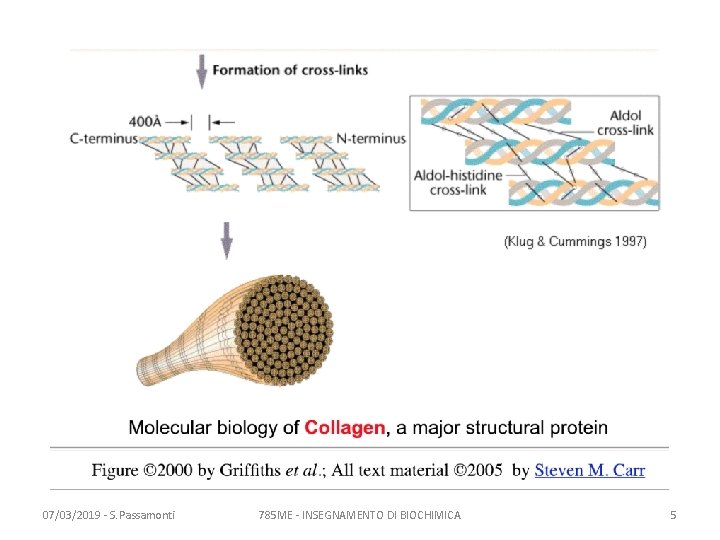
07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 5

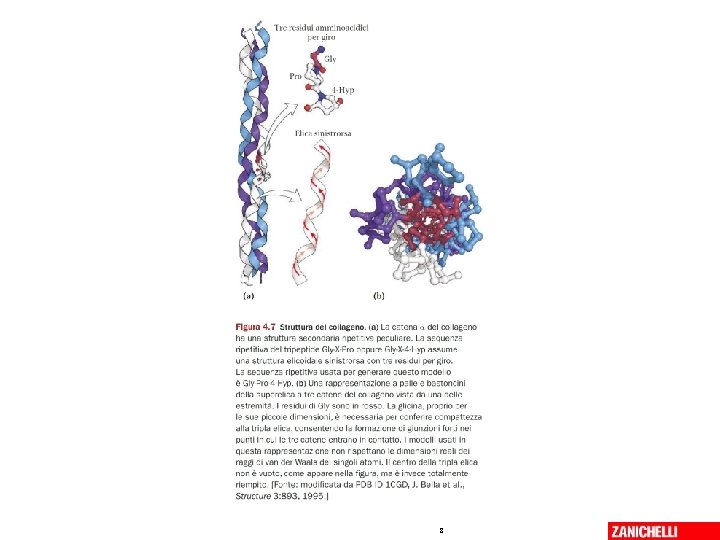
L’elica del collagene • E’ diversa dall’alfa elica • E’ sinistrosa • Tre eliche (dette eliche alfa) si aggregano a formare una super-elica, destrorsa • Legami covalenti inter-catena stabilizzano la super-elica 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 6
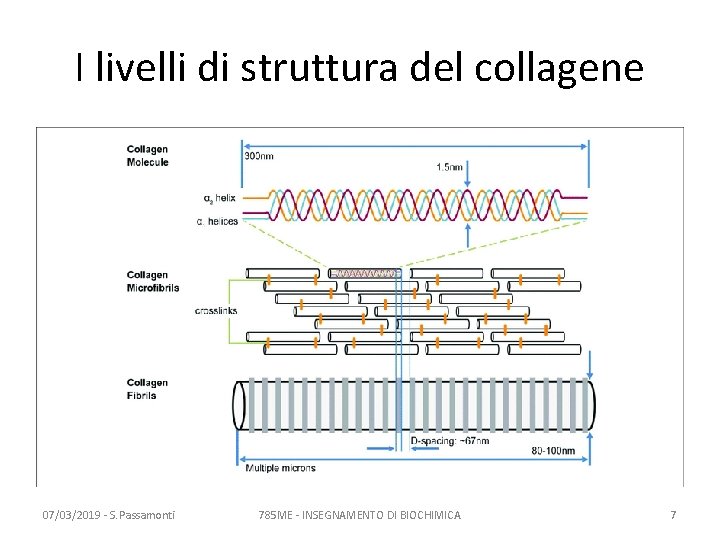
I livelli di struttura del collagene 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 7
8
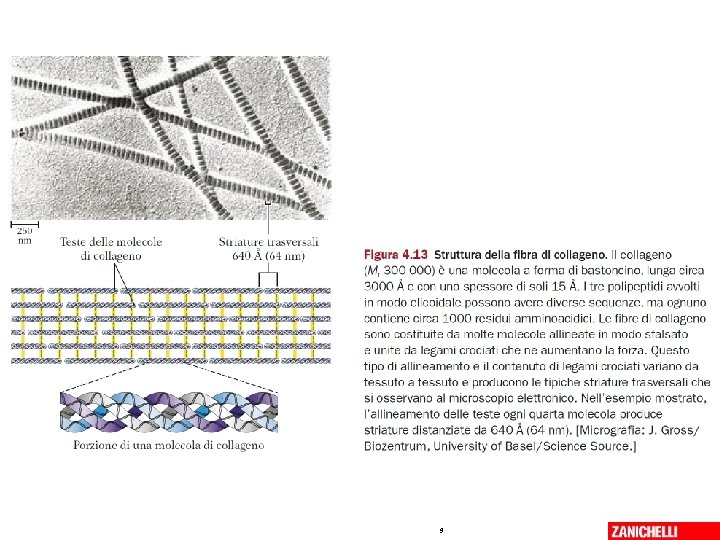
9
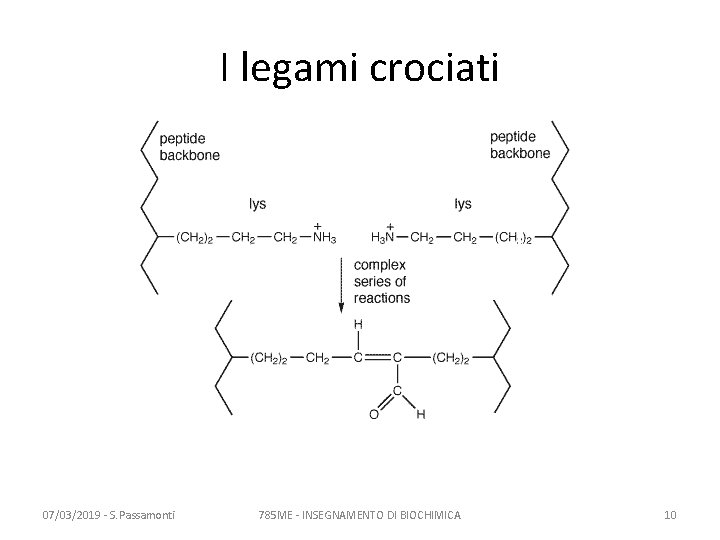
I legami crociati 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 10

I legami crociati 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 11
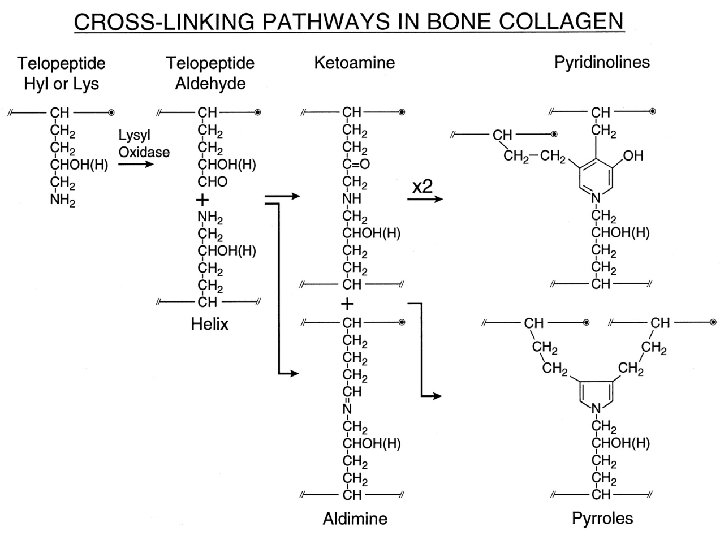
07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 12

componente del tessuto connettivo componente della matrice extracellualre • • ossa tendini legamenti sclera vasi sanguigni polmone … FONDAMENTALE RUOLO MECCANICO … 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 13

I diversi tipi di collagene • • • 18 geni (COL 1 -18) 18 polipeptidi sintesi intracellulare secrezione extracellulare “maturazione” (formazione di legami crociati) difetti genici mutazioni nucleotidiche mutazioni amminoacidiche alterazioni della struttura secondaria-terziaria-quaternaria gravi fragilità dei tessuti 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 14
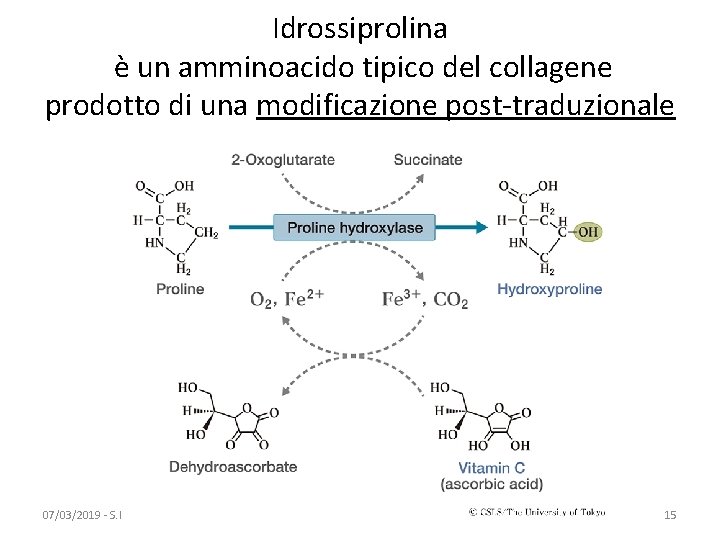
Idrossiprolina è un amminoacido tipico del collagene prodotto di una modificazione post-traduzionale 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 15
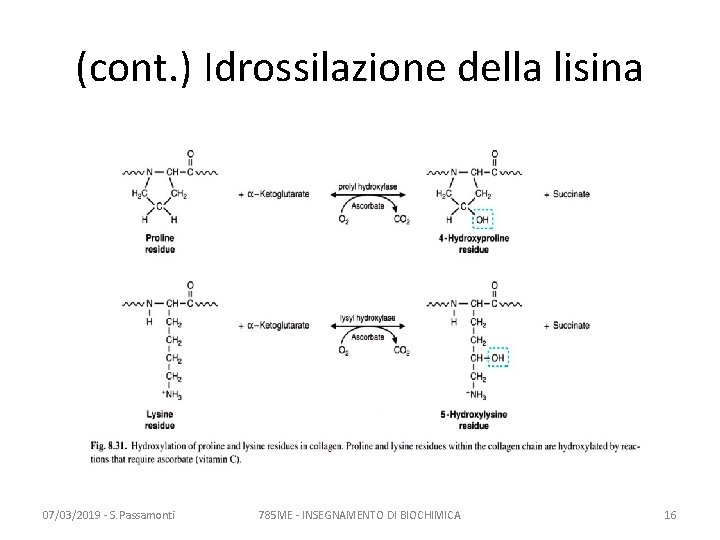
(cont. ) Idrossilazione della lisina 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 16

Carenza di vitamina C • Difetti di idrossilazione di – prolina – lisina • Difetti di formazione di legami crociati nel collagene • Fragilità strutturale SCORBUTO 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 17

Fabbisogno di vit. C 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 18

Alimenti che contengono vit. C • • • Agrumi kiwi pepe rosso e verde broccoli pomodori 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 19

Le proteine globulari Sono strutture molto compatte 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 20

21

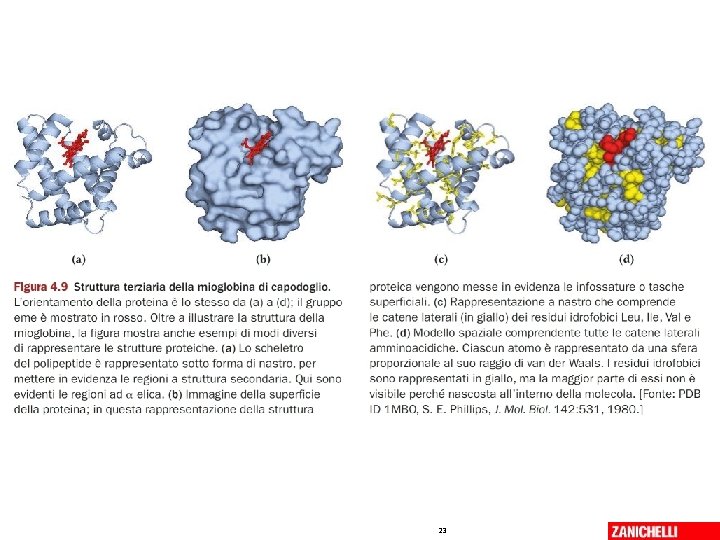
Tipica proteina globulare La miogloblina • • • Nel muscolo 153 amminoacidi Massa molecolare (Mr) 16. 700 Da Coniugata con il gruppo eme Lega l’Ossigeno Otto segmenti in struttura ad alfa-elica – 70% della sequenza ha struttura alfa elica ( compattezza) 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 22
23

Tipica proteina globulare La miogloblina • Quasi tutti i gruppi R apolari sono all’interno • Tutti i gruppi R polari, tranne due, sono all’esterno e intergiscono con l’acqua • All’interno della molecola c’è spazio per solo 4 molecole d’acqua • Il gruppo prostetico eme sta all’interno della proteina 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 24
25

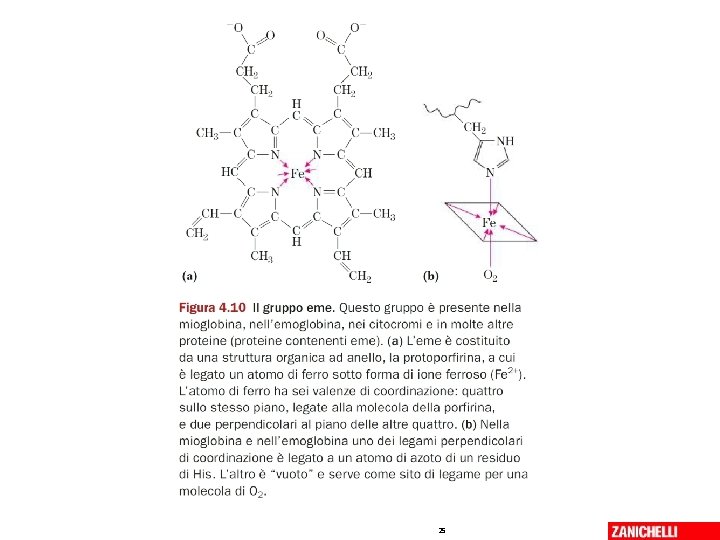
L’eme nella mioglobina • L’eme lega il Fe 2+ • Due legami di coordinazione sono perpendicolari al piano dell’eme – Un legame di coordinazione del Fe 2+ dell’eme è con l’istidina 93 – L’altro legame di coordinazione è con O 2 (ossigeno MOLECOLARE) • L’eme NON interagisce con l’acqua – così il Fe 2+ non può cedere e- al solvente (e ossidarsi a Fe 3+) 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 26

Le proteine globulari hanno diversi contenuti di strutture secondarie 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 27

I MOTIVI strutturali delle proteine globulari • I motivi sono combinazioni di strutture secondarie, separate da sequenze di raccordo: – Ansa beta-alfa-beta • --BETA-raccordo-ALFA-raccordo-BETA-- – BARILE • --BETA-raccordo 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 28
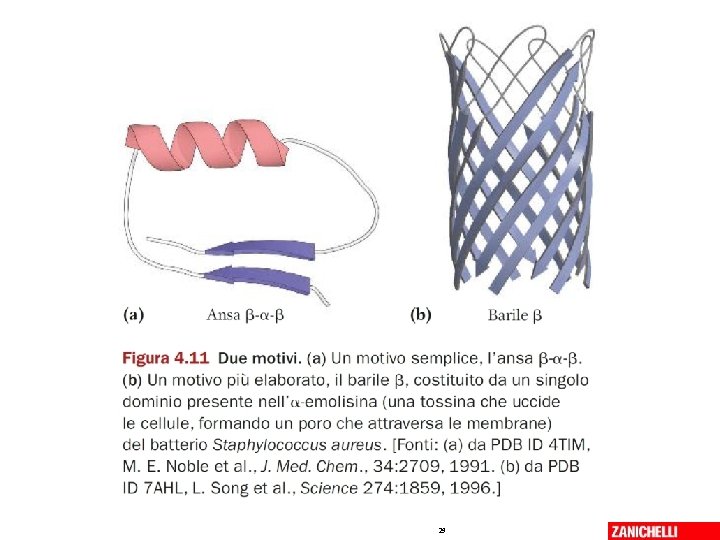
29

I motivi strutturali sono ricorrenti • 1200 motivi diversi si ritrovano in 80. 000 diverse proteine – si deduce che lo stesso motivo può formarsi in polipeptidi aventi diverse sequenze • La presenza di motivi comuni consente di raggruppare le proteine in famiglie • I motivi determinano caratteristiche funzionali essenziali per la vita della cellula 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 30

Le proteine globulari disordinate • Circa un terzo di tutte le proteine note NON hanno strutture secondarie • Esse sono intrinsecamente disordinate – NON hanno un nucleo idrofobico, NON sono compatte – Sono ricche di gruppi R polari e carichi (Lys, Arg, Glu) – Sono ricche di Pro, che impediscono la formazione di alfa leiche 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 31

La funzione delle proteine intrinsecamente disordinate • Possono avere numerose conformazioni • Queste consentono le interazioni con altre proteine • Il legame reversibile proteina-proteina determina variazioni conformazionali delle specie proteiche e quindi le loro funzioni • proteina A (lega) + proteina B (catalizza) complesso AB (lega e non catalizza) 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 32

La denaturazione delle proteine Perdita della struttura tridimensionale di una proteina e della sua funzione • CAUSE: Rottura del sistema di legami deboli che stabilizzano i livelli di struttura quaternaria, terziaria e secondaria • AGENTI DENATURANTI – temperatura – p. H – soluti che alterano il reticolo dell’acqua (solventi e sali) 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 33
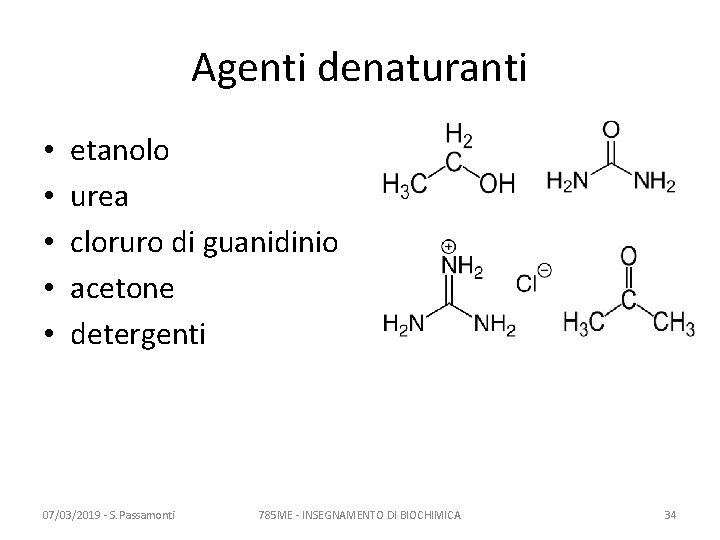
Agenti denaturanti • • • etanolo urea cloruro di guanidinio acetone detergenti 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 34
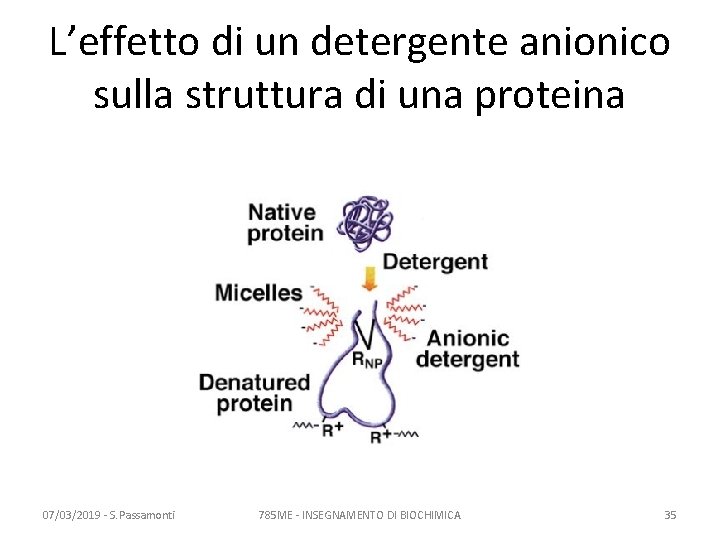
L’effetto di un detergente anionico sulla struttura di una proteina 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 35
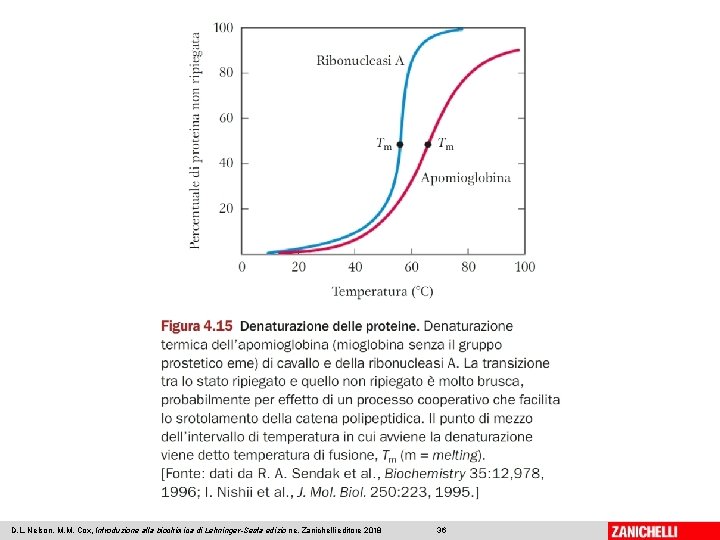
D. L. Nelson, M. M. Cox, Introduzione alla biochimica di Lehninger-Sesta edizio ne, Zanichelli editore 2018 36
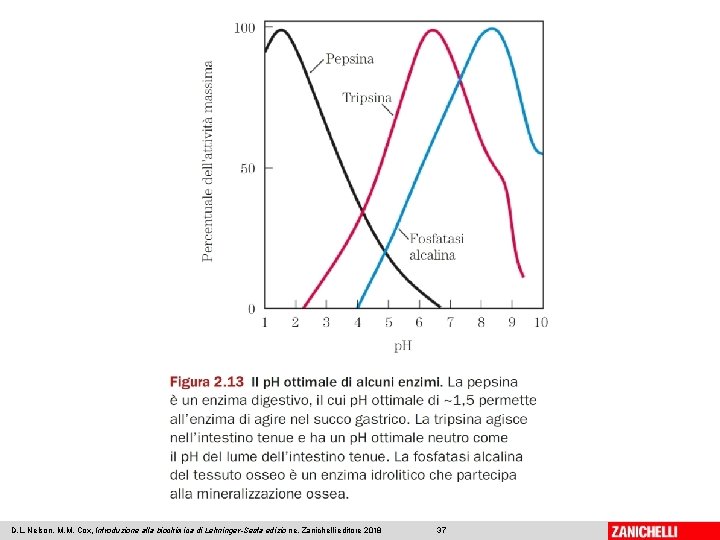
D. L. Nelson, M. M. Cox, Introduzione alla biochimica di Lehninger-Sesta edizio ne, Zanichelli editore 2018 37

La denaturazione può essere reversibile 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 38
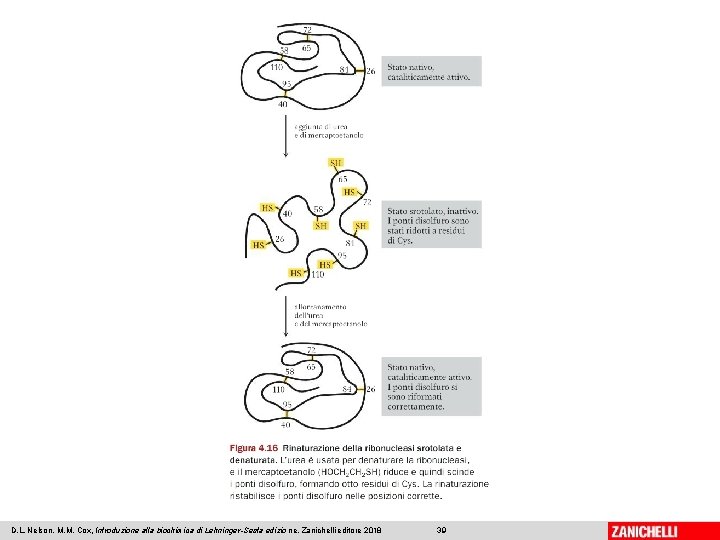
D. L. Nelson, M. M. Cox, Introduzione alla biochimica di Lehninger-Sesta edizio ne, Zanichelli editore 2018 39

Gli stadi del Folding 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 40
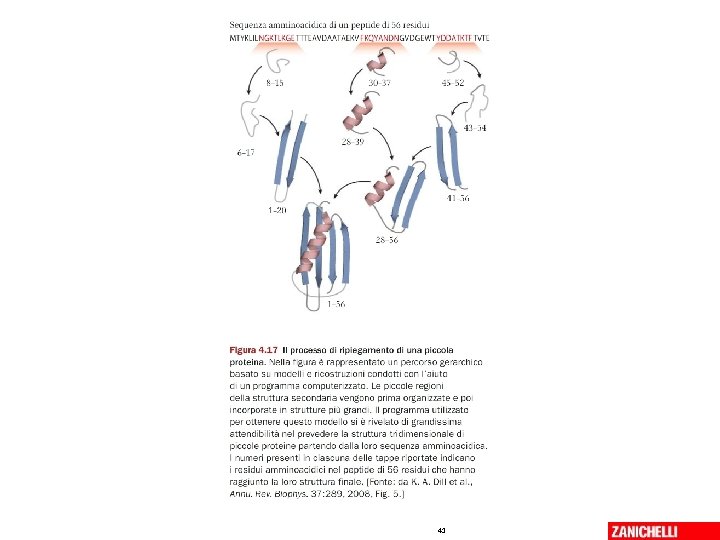
41

La proteostasi • Mantenimento di una data proteina nel suo stato biologicamente funzionale • E’ un processo complesso, che dipende da: – sintesi proteica (a livello dei ribosomi) – transizione dalla struttura primaria a quella secondaria, terziaria e quaternaria – eliminazione controllata dei polipeptidi non ripiegati 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 42
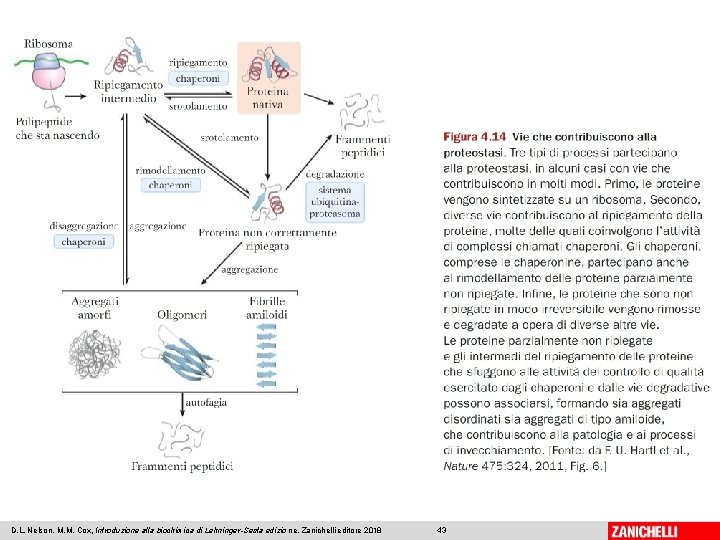
D. L. Nelson, M. M. Cox, Introduzione alla biochimica di Lehninger-Sesta edizio ne, Zanichelli editore 2018 43

Il controllo della proteostasi Avviene a tutti i livelli: • sintesi proteica (a livello dei ribosomi) – espressione dei geni (trascrizione) • transizione dalla struttura primaria a quella secondaria, terziaria e quaternaria – chaperoni • eliminazione controllata dei polipeptidi non ripiegati – sistema ubiquitina-proteasoma – autofagia 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 44

I chaperoni INTERESSANTE Guidano e accelerano gli avvolgimenti polipetidici (FOLDING) mediante interazioni proteina-proteina 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 45

I chaperoni Due principali FAMIGLIE di chaperoni • Heat shock protein 70 (HSP 70) – Mr 70. 000 dalton – La loro espressione intracellulare aumenta in batteri trattati con calore – Interagiscono con porzioni idrofobiche di proteine misfolded • chaperonine – nell’uomo è HSP 60 – Idrolizzano ATP (energia metabolica) per catalizzare il folding 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 46

Gli enzimi che assistono il folding • Proteina disolfuro isomerasi (PDI) • Prolil cis-trans isomerasi 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 47
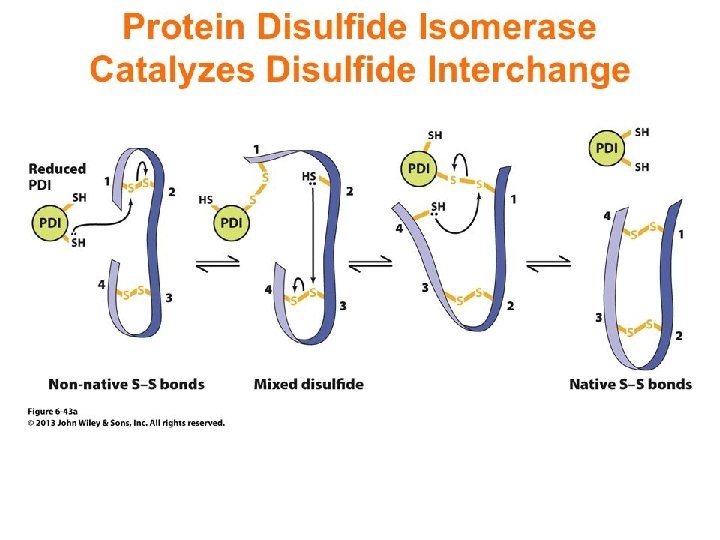
07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 48
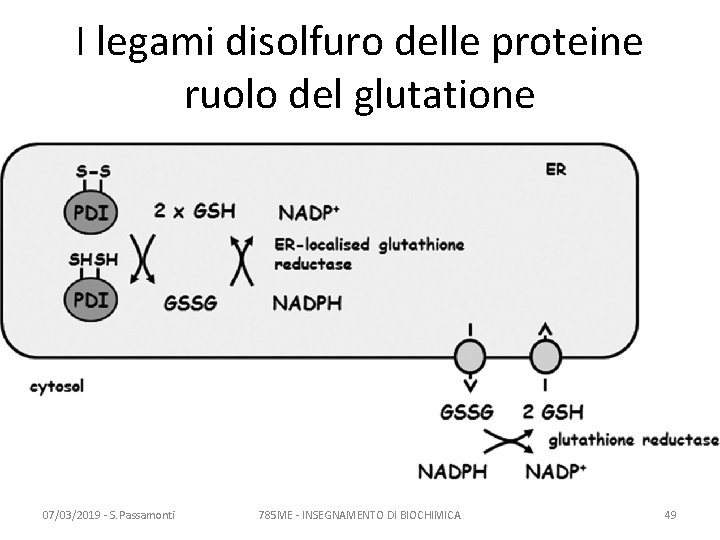
I legami disolfuro delle proteine ruolo del glutatione 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 49
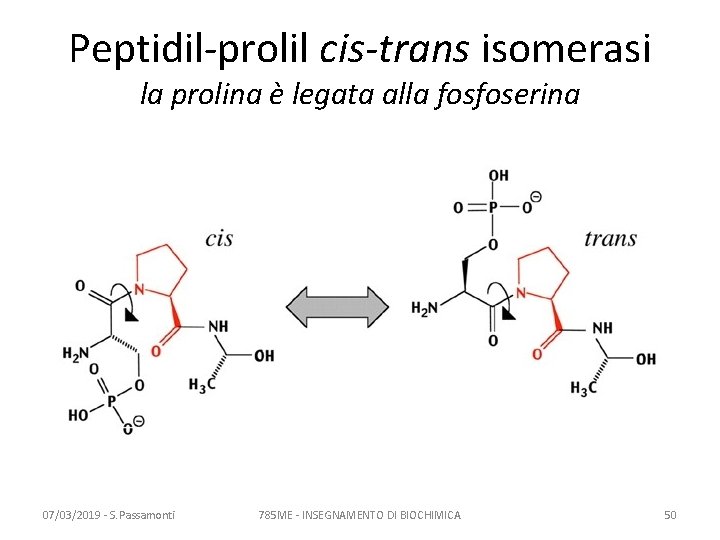
Peptidil-prolil cis-trans isomerasi la prolina è legata alla fosfoserina 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 50

I difetti del Folding • I polipeptidi parzialmente ripiegati espongono al solvente i loro gruppi R idrofobici (o carichi) • Si formano interazioni idrofobiche e elettrostatiche con altri polipeptidi – Aggregati insolubili, tipo AMILOIDE Patologie da accumulo cellulare AMILOIDOSI Nei neuroni– Morbo di Alzheimer, Morbo di Parkinson Nelle cellule beta del pancreas - Diabete 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 51
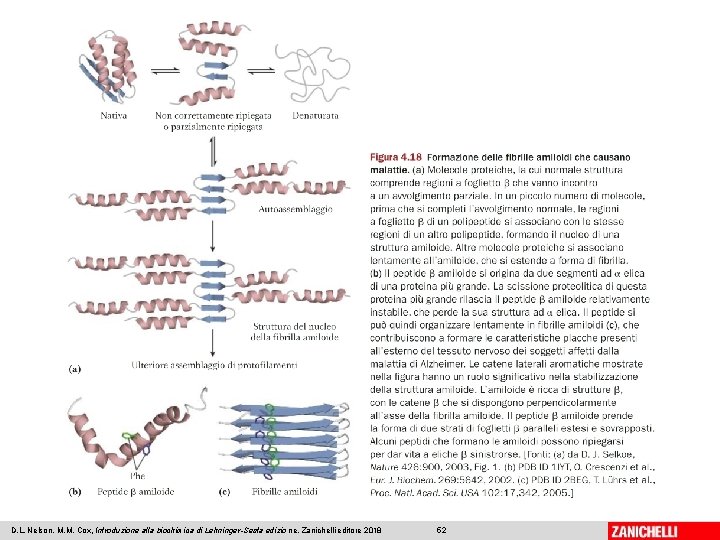
D. L. Nelson, M. M. Cox, Introduzione alla biochimica di Lehninger-Sesta edizio ne, Zanichelli editore 2018 52

Fine A domani • Funzione di trasporto dell’ossigeno della mioglobina e dell’emoglobina 07/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 53
- Slides: 54