Lewise struktuurid 1916 Keemiline side moodustub kahe elektroni

Lewise struktuurid (1916) Keemiline side moodustub kahe elektroni abil, mis kuluvad kahe aatomile või kahe radikaalile Või doonor-aktseptori mehhanismi järgi, kui üks aatom annab elektronpaari ja teine vaba orbitaali sideme moodustamiseks CO, HNO 3 ja tema ioon, NH 4+, O 3 Gilbert Newton Lewis
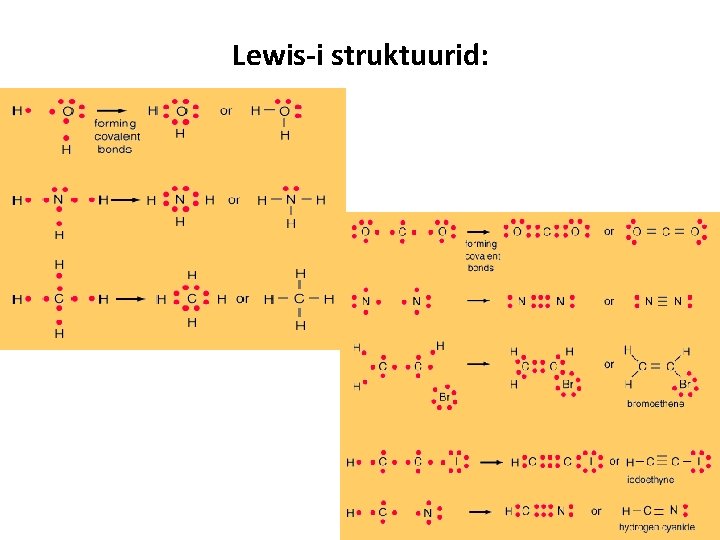
Lewis-i struktuurid:

Kuidas kirjutatakse Lewis-i struktuurid? 1. Arvutada kõikide elementide, mis on molekulis, valentselektroonide arvu; 2. Valida aatomi, mis peab olema molekuli tsentris-see on tavaliselt aatom väiksema elektronegatiivsusega (H aatom ei saa kunagi tsentris olla); 3. Kirjuatada molekuli struktuuri ja ühendada aatomeid üksiksidemete kaudu; 4. Lisada ülejaanud elektrone oktetreegli järgi ning viimasena tegevusena kirjutada elektrone tsentraalse aatomi jaoks nii, et tema joaks okteetreegel ei rikku ka (H aatomi jaoks on 2 elektroni võimalik kirjutada); 5. Kui tsentraalse aatomi jaoks rikkub okteet (v. a. prooton!!!) reegel, siis peab ta seotama mingi teise aatomiga kaksik-, või kolmik side kaudu; (3. ja järgmiste perioodide elementide jaoks okteet reegel ei pea kehtima) CO 2: 4 + 2(6)=16 e-
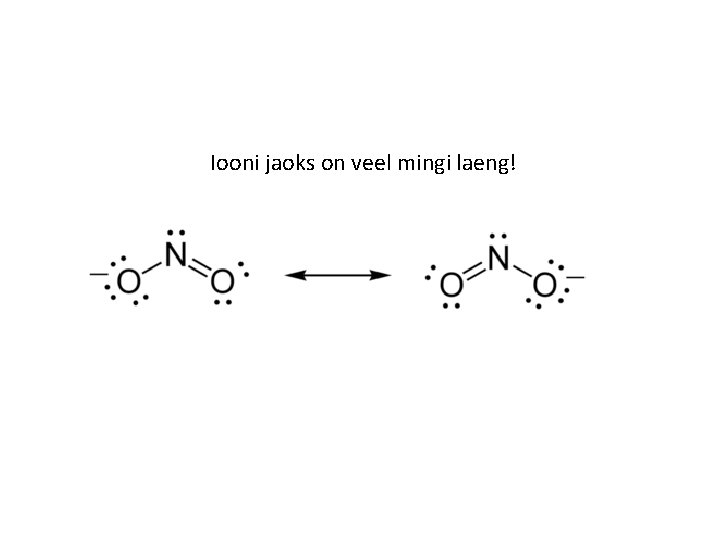
Iooni jaoks on veel mingi laeng!
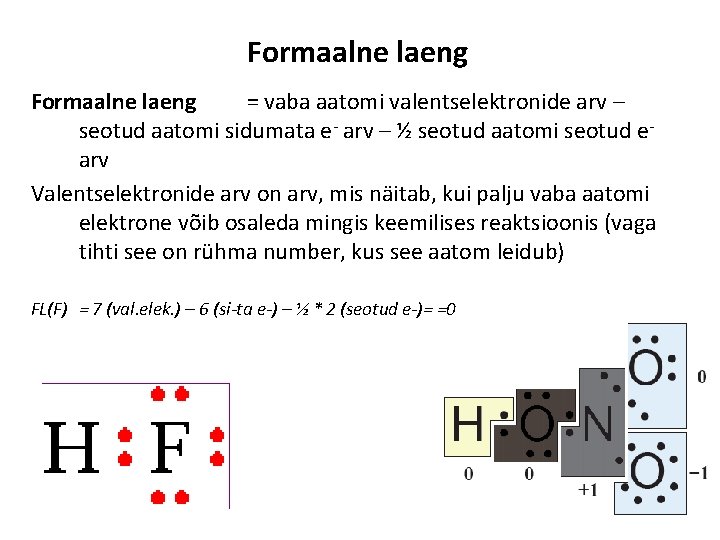
Formaalne laeng = vaba aatomi valentselektronide arv – seotud aatomi sidumata e- arv – ½ seotud aatomi seotud earv Valentselektronide arv on arv, mis näitab, kui palju vaba aatomi elektrone võib osaleda mingis keemilises reaktsioonis (vaga tihti see on rühma number, kus see aatom leidub) FL(F) = 7 (val. elek. ) – 6 (si-ta e-) – ½ * 2 (seotud e-)= =0
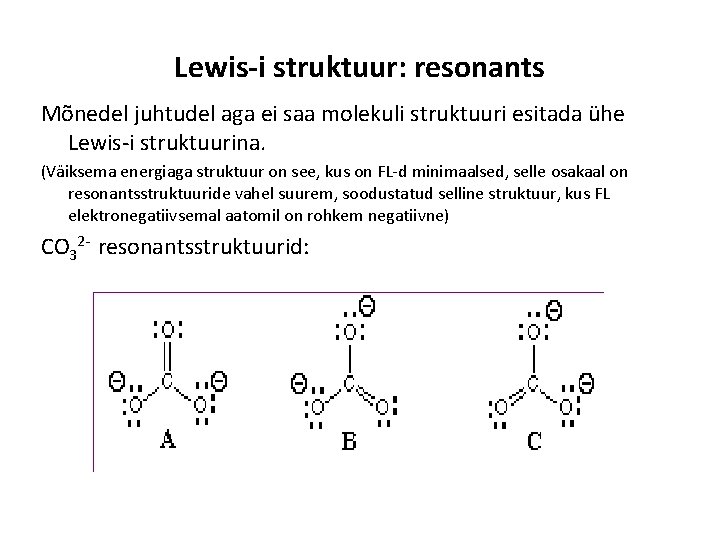
Lewis-i struktuur: resonants Mõnedel juhtudel aga ei saa molekuli struktuuri esitada ühe Lewis-i struktuurina. (Väiksema energiaga struktuur on see, kus on FL-d minimaalsed, selle osakaal on resonantsstruktuuride vahel suurem, soodustatud selline struktuur, kus FL elektronegatiivsemal aatomil on rohkem negatiivne) CO 32 - resonantsstruktuurid:

Lewise struktuurid väga hästi näitavad sidemete ja elektroonpaari paiknemist molekulides (kasutatakse orgaanilises keemias), kuigi need struktuurid ei kirjelda molekulide kolmedimensionaalset kuju

VSEPR teooria (Valence shell electron pair repulsion (VSEPR) theory, 1957 ) Ronald Sydney Nyholm Ronald James Gillespie

VSEPR teooria (Valence shell electron pair repulsion (VSEPR) theory 1957 ) • https: //en. wikipedia. org/wiki/VSEPR_theory Vaba elektronpaar muutub nurgasid molekulis nii, et tõukumine oleks minimaalne (energeetiliselt soodsam struktuur)
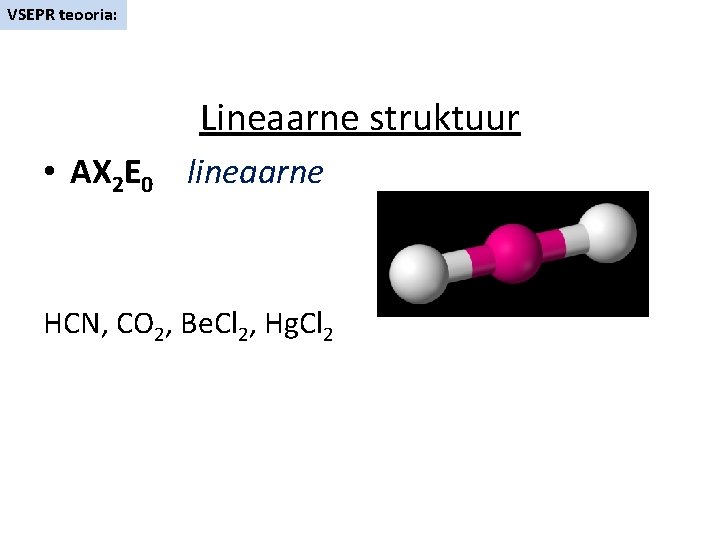
VSEPR teooria: Lineaarne struktuur • AX 2 E 0 lineaarne HCN, CO 2, Be. Cl 2, Hg. Cl 2
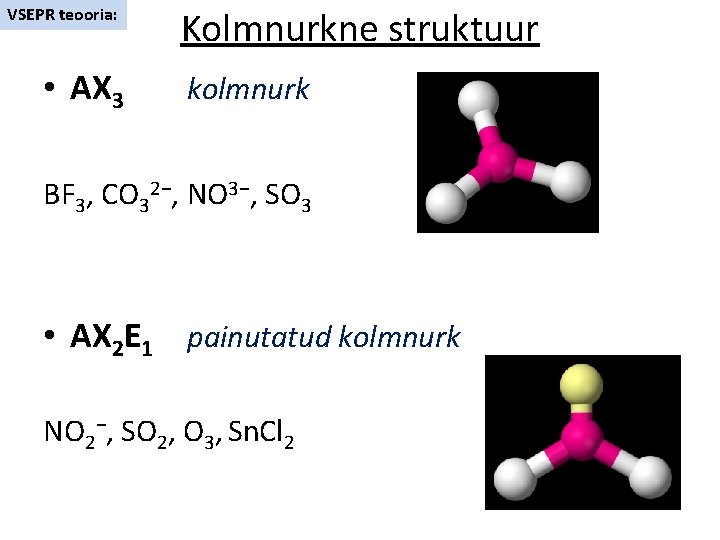
VSEPR teooria: • AX 3 Kolmnurkne struktuur kolmnurk BF 3, CO 32−, NO 3−, SO 3 • AX 2 E 1 painutatud kolmnurk NO 2−, SO 2, O 3, Sn. Cl 2
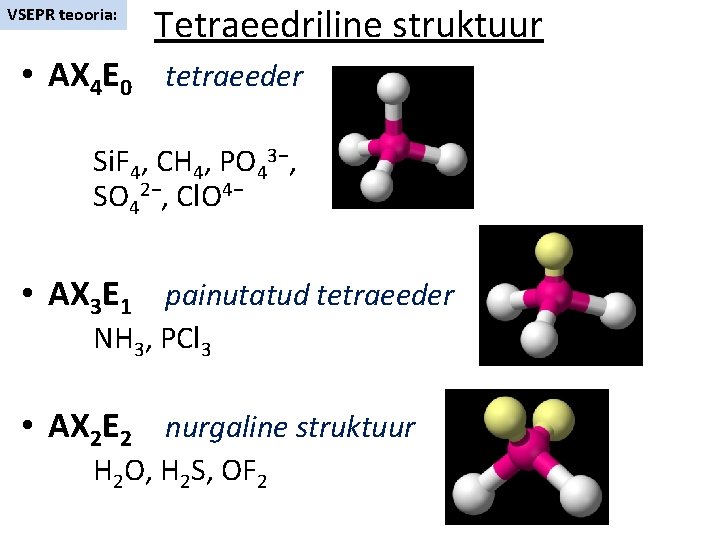
VSEPR teooria: Tetraeedriline struktuur • AX 4 E 0 tetraeeder Si. F 4, CH 4, PO 43−, SO 42−, Cl. O 4− • AX 3 E 1 painutatud tetraeeder NH 3, PCl 3 • AX 2 E 2 nurgaline struktuur H 2 O, H 2 S, OF 2
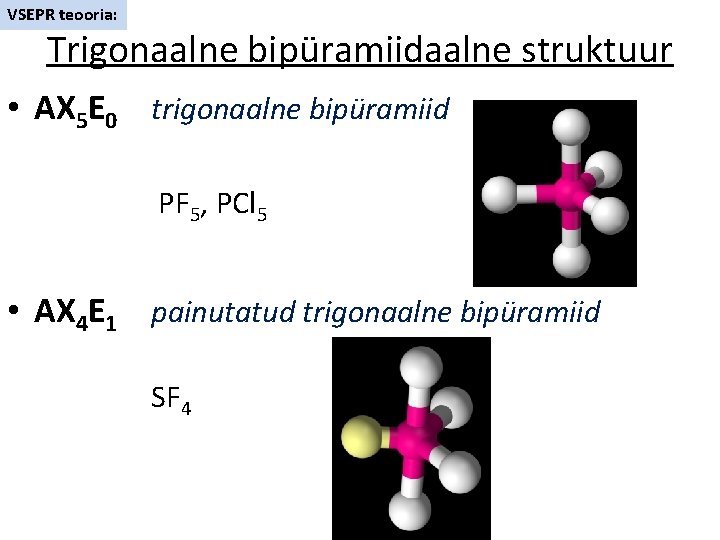
VSEPR teooria: Trigonaalne bipüramiidaalne struktuur • AX 5 E 0 trigonaalne bipüramiid PF 5, PCl 5 • AX 4 E 1 painutatud trigonaalne bipüramiid SF 4
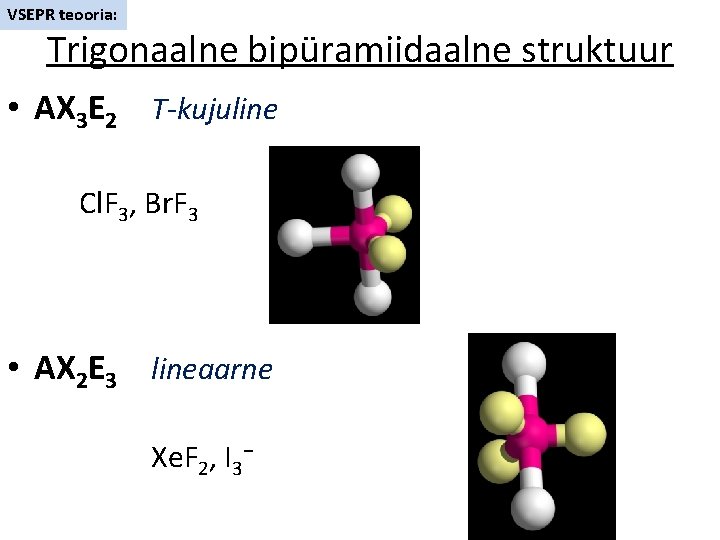
VSEPR teooria: Trigonaalne bipüramiidaalne struktuur • AX 3 E 2 T-kujuline Cl. F 3, Br. F 3 • AX 2 E 3 lineaarne Xe. F 2, I 3−
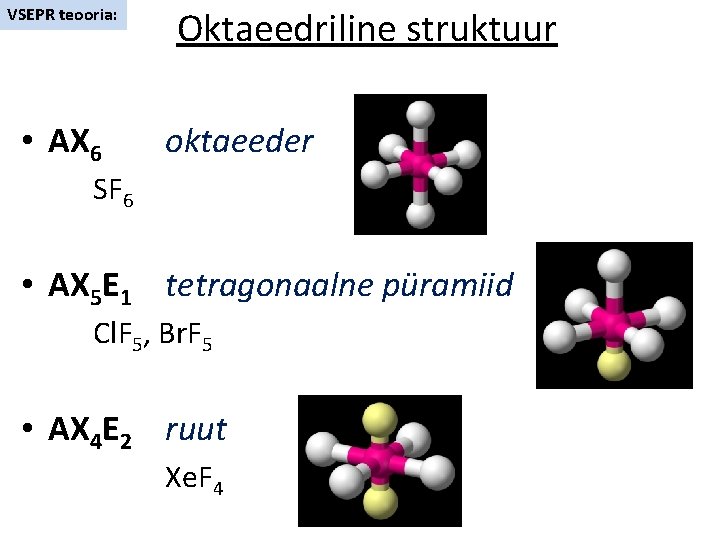
VSEPR teooria: • AX 6 Oktaeedriline struktuur oktaeeder SF 6 • AX 5 E 1 tetragonaalne püramiid Cl. F 5, Br. F 5 • AX 4 E 2 ruut Xe. F 4
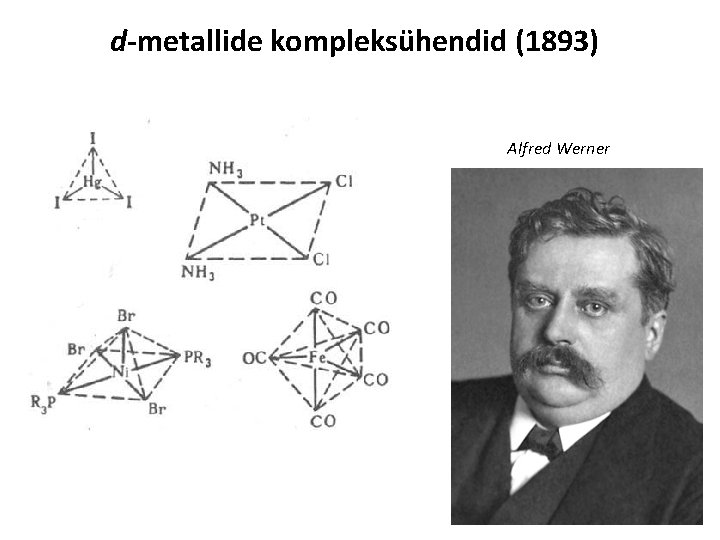
d-metallide kompleksühendid (1893) Alfred Werner
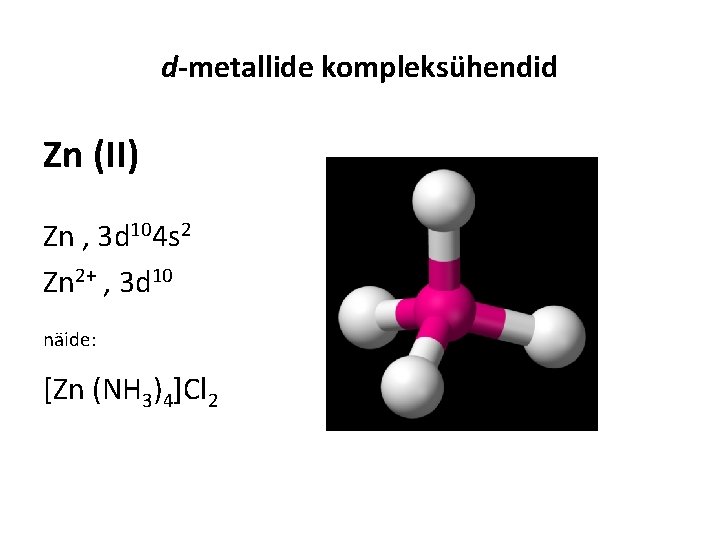
d-metallide kompleksühendid Zn (II) Zn , 3 d 104 s 2 Zn 2+ , 3 d 10 näide: [Zn (NH 3)4]Cl 2
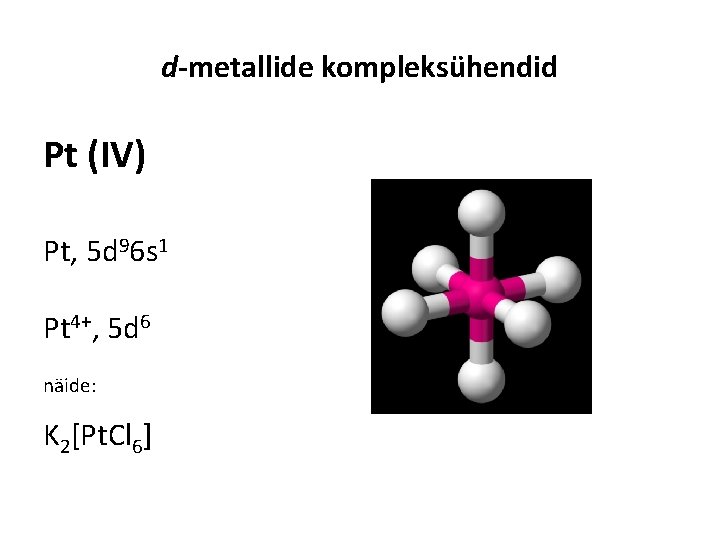
d-metallide kompleksühendid Pt (IV) Pt, 5 d 96 s 1 Pt 4+, 5 d 6 näide: K 2[Pt. Cl 6]
![Komplekside struktuuride tabel: Koord. arv Konfig. Kompleksimoodustaja 2 Lineaarne Ag(I), Cu(I), Hg(II) [Ag(NH 3)2]+, Komplekside struktuuride tabel: Koord. arv Konfig. Kompleksimoodustaja 2 Lineaarne Ag(I), Cu(I), Hg(II) [Ag(NH 3)2]+,](http://slidetodoc.com/presentation_image_h2/5922c02d7ca3ff2eabc5d51b856a64dd/image-19.jpg)
Komplekside struktuuride tabel: Koord. arv Konfig. Kompleksimoodustaja 2 Lineaarne Ag(I), Cu(I), Hg(II) [Ag(NH 3)2]+, [Cu. Cl 2]- 3 Kolmnurk Hg (II) [Hg. I 3]- 4 6 Tetraeeder Sn(II) [Sn. Cl 3]- Tetraeeder Be(II), Fe(II), Co(II), Zn(II) [Zn. Cl 4]2 -, [Hg(CN)4]2 -, [Zn(NH 3)4]2+ Ruut Pt(II), Au(III) [Pt. Cl 4]2 -, [Ni(CN)4]2 -, [Cu(NH 3)4]2+ Oktaeeder Cr(III), Mn(II), Fe(III), [Pt. Cl 6]2 -, [Fe(CN)6]3 -, [Sn. Cl 6]2 -, Co(II), Co(III), Ni(II), Al(III), Cd(II), [Co(NO 2)6]3 -, [Al(H 2 O)2(OH)4]Pt(IV) Ruut kõikide jaoks
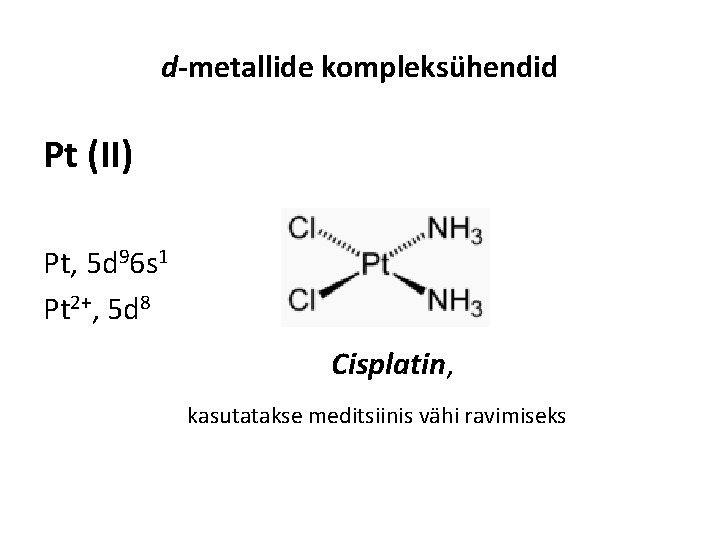
d-metallide kompleksühendid Pt (II) Pt, 5 d 96 s 1 Pt 2+, 5 d 8 Cisplatin, kasutatakse meditsiinis vähi ravimiseks
![paramagn. [Fe. F 6]4 - diamagn. [Fe(CN)6]4 - Ligandide spektrokeemiline rida I− < Br− paramagn. [Fe. F 6]4 - diamagn. [Fe(CN)6]4 - Ligandide spektrokeemiline rida I− < Br−](http://slidetodoc.com/presentation_image_h2/5922c02d7ca3ff2eabc5d51b856a64dd/image-21.jpg)
paramagn. [Fe. F 6]4 - diamagn. [Fe(CN)6]4 - Ligandide spektrokeemiline rida I− < Br− < S 2− < SCN− < Cl− < NO 3− < N 3− < F− < OH− < C 2 O 42− ≈ H 2 O < NCS− < CH 3 CN < py (pyridine) < NH 3 < en (ethylenediamine) < bipy (2, 2'-bipyridine) < phen (1, 10 phenanthroline) < NO 2− < PPh 3 < CN− ≈ CO
- Slides: 22