Les thrapeutiques cibles dans le cancer du sein

Les thérapeutiques ciblées dans le cancer du sein Mythes ou réalités ? Dr. Thomas Bachelot Centre Léon Bérard, Lyon

It’s a Great Time to Be Working in Oncology (D. Von. Hoff, 2002) Hanahan and Weinberg. Cell 100(1): 57 -70, 2000.
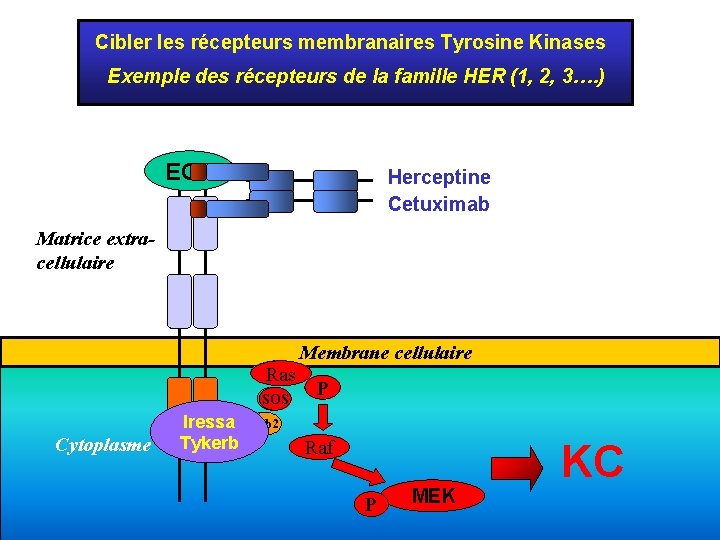
Cibler les récepteurs membranaires Tyrosine Kinases Exemple des récepteurs de la famille HER (1, 2, 3…. ) EGF Herceptine Cetuximab Matrice extracellulaire Ras SOS Cytoplasme Iressa Grb 2 Shc Tykerb Membrane cellulaire P Raf P MEK KC
Thérapeutiques ciblées : Ciblées sur quoi? Thérapeutiques bien ciblées sur des anomalies moléculaires causales Imatinib dans les GIST : 70% de réponse !

Thérapeutiques ciblées : Ciblées sur quoi? • Anomalie moléculaire causale – Précoce – Constante • Anomalie moléculaire fréquente – Plus tardive – Inconstante – Pronostique • RR: >50% RR: 10 - 20% Une cible présente – Rôle dans la transformation? RR: ~ 0%

Quelles sont les cibles moléculaire précises connues pour jouer un rôle oncogénique majeur dans le cancer du sein ? – Les récepteurs hormonaux – Le récepteur HER 2 – L’angiogenèse – …… Les cancers du sein sont très hétérogènes !
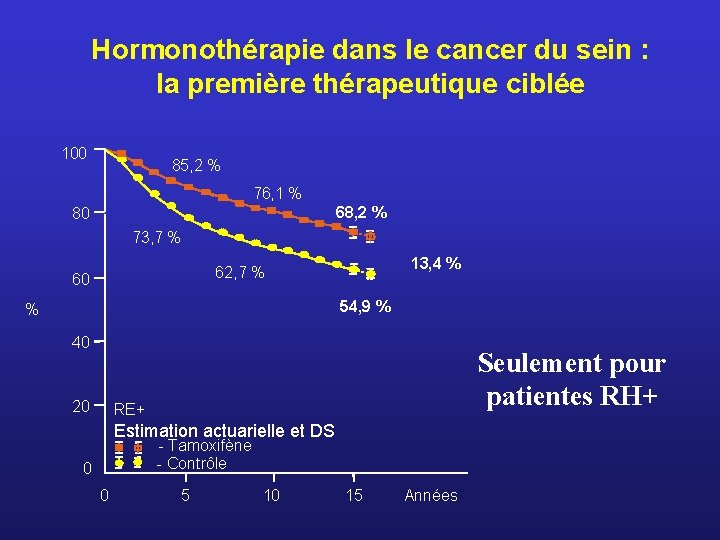
Hormonothérapie dans le cancer du sein : la première thérapeutique ciblée 100 85, 2 % 76, 1 % 68, 2 % 80 73, 7 % 13, 4 % 62, 7 % 60 54, 9 % % 40 20 Seulement pour patientes RH+ RE+ Estimation actuarielle et DS - Tamoxifène - Contrôle 0 0 5 10 15 Années
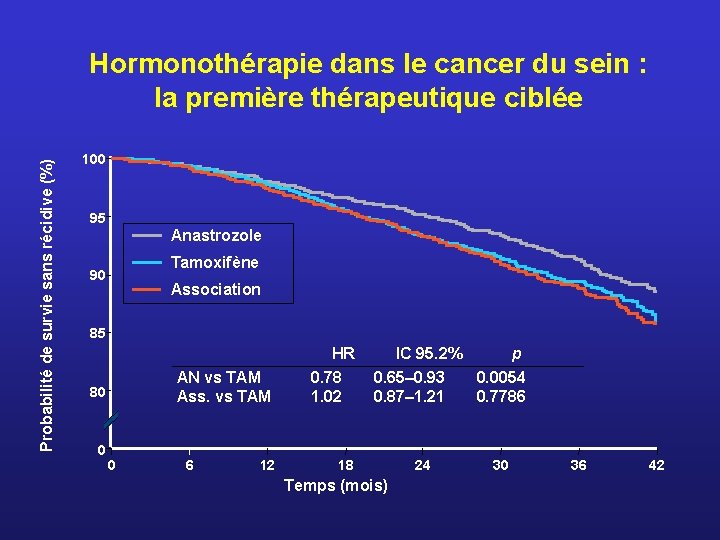
Probabilité de survie sans récidive (%) Hormonothérapie dans le cancer du sein : la première thérapeutique ciblée 100 95 Anastrozole Tamoxifène 90 Association 85 HR AN vs TAM Ass. vs TAM 80 0 0 6 12 0. 78 1. 02 IC 95. 2% 0. 65– 0. 93 0. 87– 1. 21 18 Temps (mois) 24 p 0. 0054 0. 7786 30 36 42

Hormonothérapie dans le cancer du sein : Quelles leçons en tirer pour les traitements ciblés ? 1) Les thérapeutiques ciblées sont efficaces 2) La même cible peut être atteinte avec différentes molécules ayant différents mécanismes d’action 3) Les résultats sont meilleurs pour les formes peu avancées 4) La mise au point d’un test fiable pour identifier la cible chez les patientes est fondamentale 5) Le test sélectionne les non-répondeuses 6) Nécessité de comprendre l’interaction de la cible avec d’autres facteurs cellulaires D’après G. N. Hortobagyi, Sem Oncol 31, Février 2004
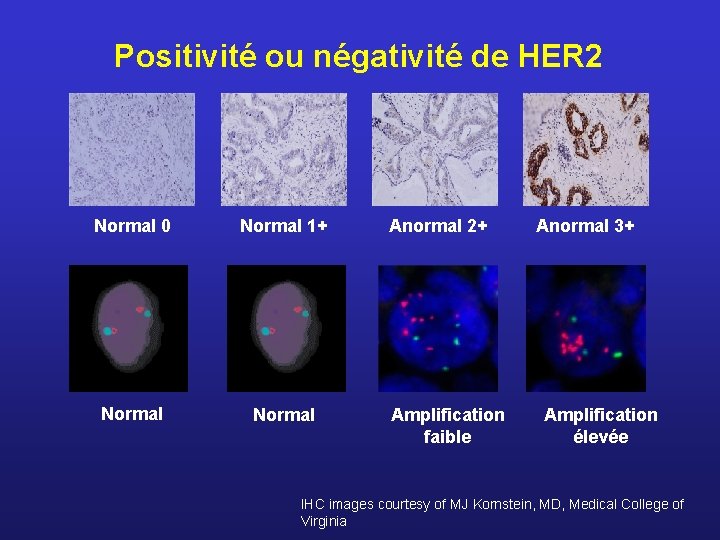
Positivité ou négativité de HER 2 Normal 0 Normal 1+ Normal Anormal 2+ Amplification faible Anormal 3+ Amplification élevée IHC images courtesy of MJ Kornstein, MD, Medical College of Virginia

Conséquences de l’amplification de HER 2 sur des cellules humaines de cancer du sein Cellules humaines de cancer du sein MCF-7 HER 2 négative Transfection par le gène HER 2 Synthèse d’ADN de 50 -75% Croissance cellulaire MCF-7 de 30 -50% Croissance en Agar HER 2 positive de 225% Tumorigénicité chez la souris nude 220% du potentiel métastatique chez la souris nude
Trastuzumab ou Herceptin • Anticorps monoclonal humanisé anti-HER 2 • in-vitro : inhibe la prolifération des lignées HER 2+. • in-vivo : inhibe la croissance tumorale des lignées HER 2+.
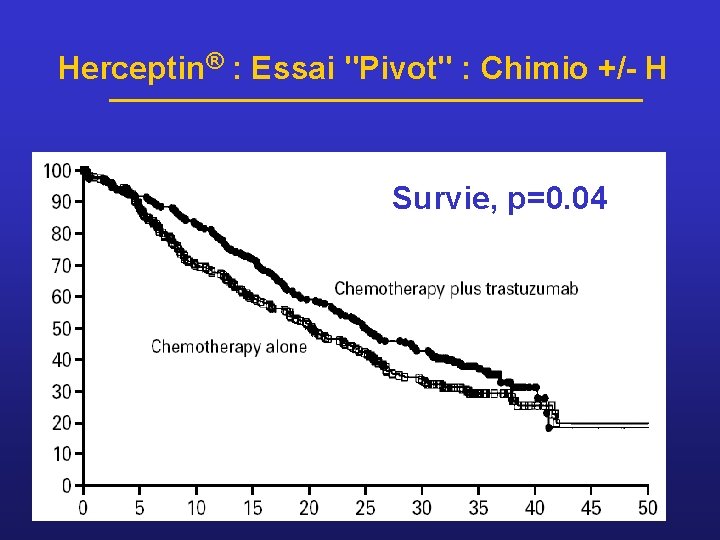
Herceptin® : Essai "Pivot" : Chimio +/- H Survie, p=0. 04
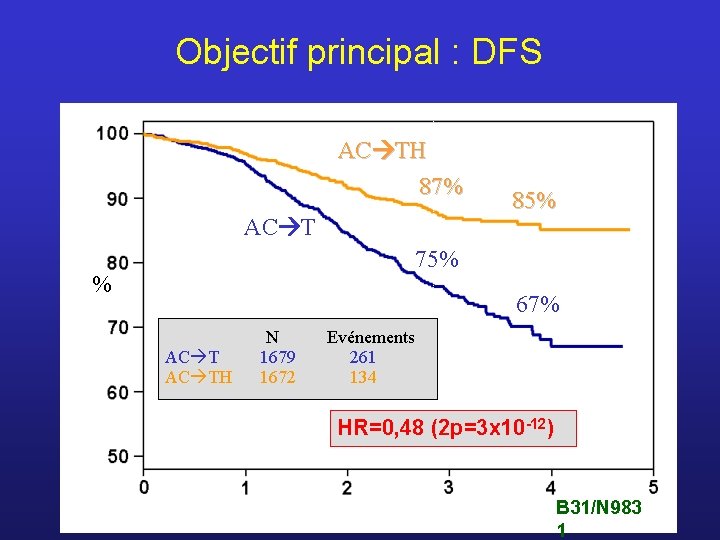
Objectif principal : DFS AC TH 87% AC T 85% 75% % 67% AC TH N 1679 1672 Evénements 261 134 HR=0, 48 (2 p=3 x 10 -12) Years From Randomization B 31/N 983 1
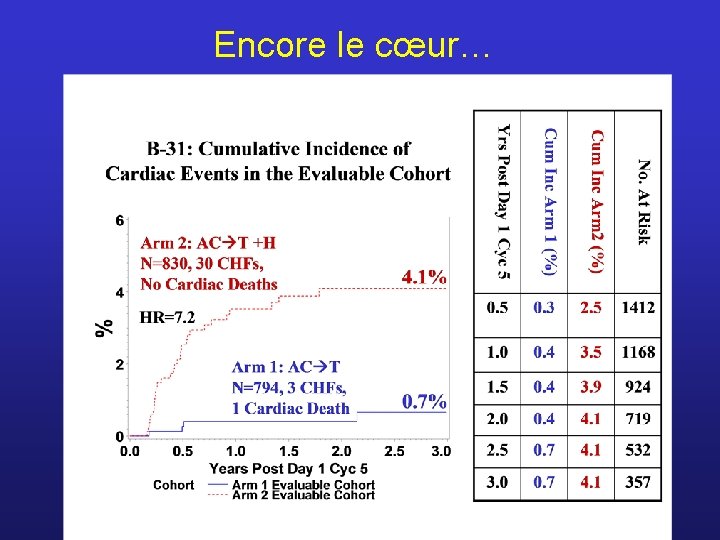
Encore le cœur…
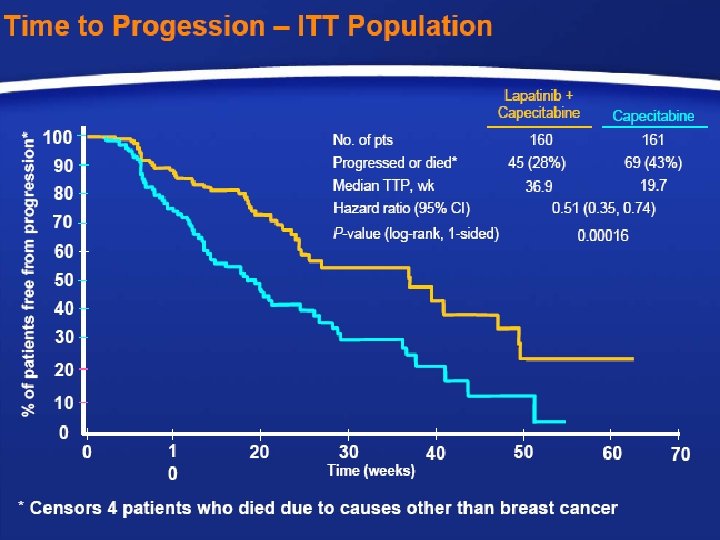
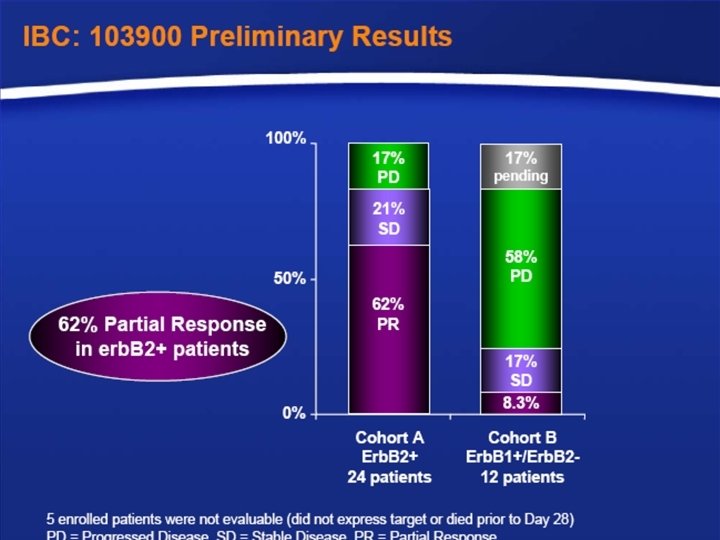
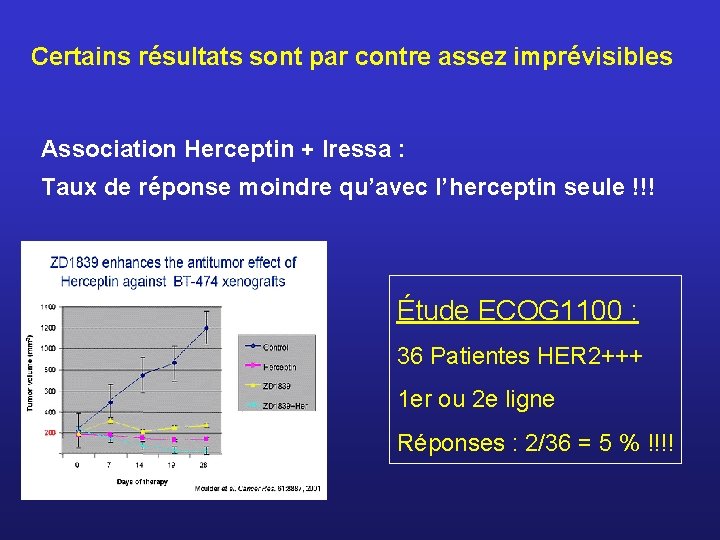
Certains résultats sont par contre assez imprévisibles Association Herceptin + Iressa : Taux de réponse moindre qu’avec l’herceptin seule !!! Étude ECOG 1100 : 36 Patientes HER 2+++ 1 er ou 2 e ligne Réponses : 2/36 = 5 % !!!!

HER 2 comme cible thérapeutique dans le cancer du sein : Quelles leçons en tirer ? 1) Les thérapeutiques ciblées sont efficaces 2) La même cible peut être atteinte avec différentes molécules ayant différents mécanismes d’action 3) Les résultats sont meilleurs pour les formes peu avancées 4) La mise au point d’un test fiable pour identifier la cible chez les patientes est fondamentale 5) Le test sélectionne les non-répondeuses 6) Nécessité de comprendre l’interaction de la cible avec d’autres facteurs cellulaires D’après G. N. Hortobagyi, Sem Oncol 31, Février 2004

HER 2 comme cible thérapeutique dans le cancer du sein : Quelles leçons en tirer ? 7) Tous les testes ne sont pas égaux 8) Les modèles pré-cliniques doivent être interprété avec suspicion 9) Soyez prudent envers une thérapeutique « non toxique » D’après G. N. Hortobagyi, Sem Oncol 31, Février 2004
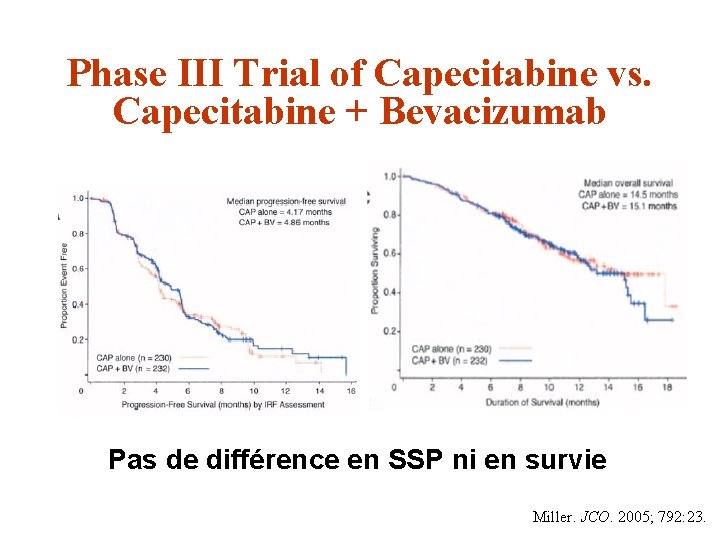
Phase III Trial of Capecitabine vs. Capecitabine + Bevacizumab Pas de différence en SSP ni en survie Miller. JCO. 2005; 792: 23.
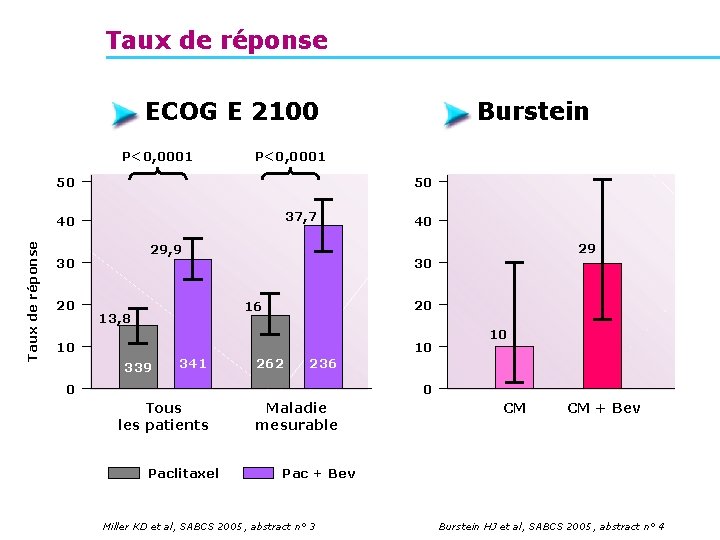
Taux de réponse ECOG E 2100 P<0, 0001 50 50 37, 7 Taux de réponse 40 29, 9 30 20 Burstein 20 10 10 339 341 29 30 16 13, 8 40 262 10 236 0 0 Tous les patients Paclitaxel Maladie mesurable CM CM + Bev Pac + Bev Miller KD et al, SABCS 2005, abstract n° 3 Burstein HJ et al, SABCS 2005, abstract n° 4
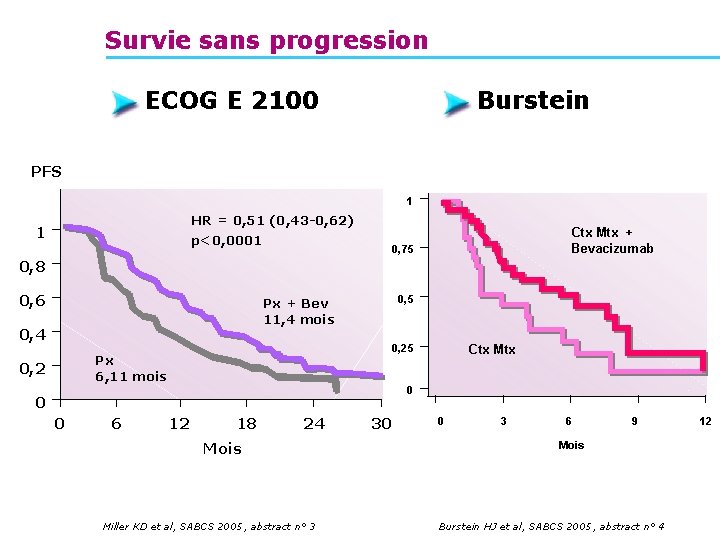
Survie sans progression ECOG E 2100 Burstein PFS 1 HR = 0, 51 (0, 43 -0, 62) 1 p<0, 0001 Ctx Mtx + Bevacizumab 0, 75 0, 8 0, 6 0, 5 Px + Bev 11, 4 mois 0, 4 0, 2 Ctx Mtx 0, 25 Px 6, 11 mois 0 0 0 6 12 18 24 Mois Miller KD et al, SABCS 2005, abstract n° 3 30 0 3 6 9 Mois Burstein HJ et al, SABCS 2005, abstract n° 4 12
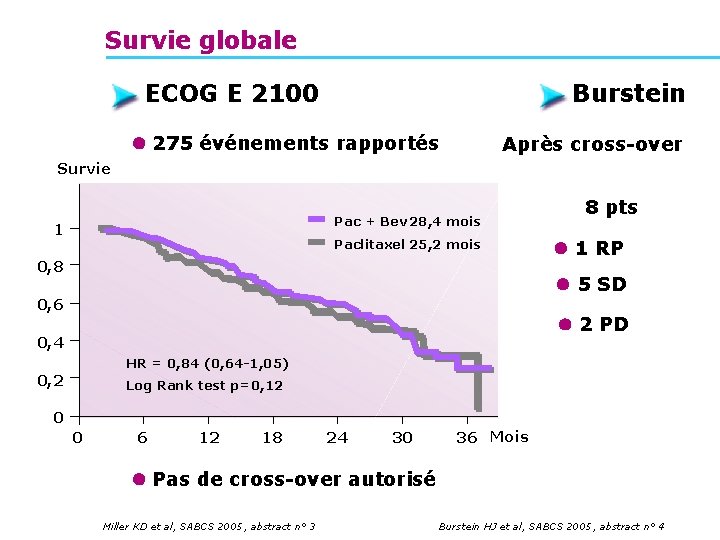
Survie globale ECOG E 2100 Burstein 275 événements rapportés Après cross-over Survie Pac + Bev 28, 4 mois 1 Paclitaxel 25, 2 mois 0, 8 8 pts 1 RP 5 SD 0, 6 2 PD 0, 4 HR = 0, 84 (0, 64 -1, 05) 0, 2 Log Rank test p=0, 12 0 0 6 12 18 24 30 36 Mois Pas de cross-over autorisé Miller KD et al, SABCS 2005, abstract n° 3 Burstein HJ et al, SABCS 2005, abstract n° 4
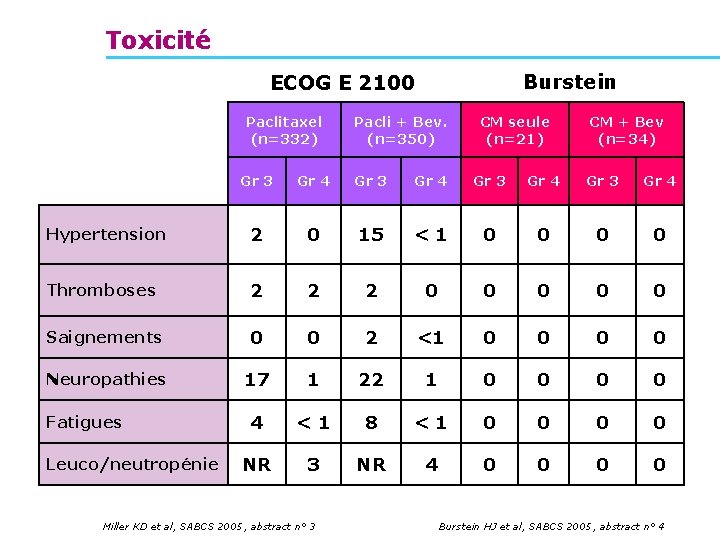
Toxicité Burstein ECOG E 2100 Paclitaxel (n=332) Pacli + Bev. (n=350) CM seule (n=21) CM + Bev (n=34) Gr 3 Gr 4 Hypertension 2 0 15 <1 0 0 Thromboses 2 2 2 0 0 0 Saignements 0 0 2 <1 0 0 Neuropathies 17 1 22 1 0 0 4 <1 8 <1 0 0 NR 3 NR 4 0 0 Fatigues Leuco/neutropénie Miller KD et al, SABCS 2005, abstract n° 3 Burstein HJ et al, SABCS 2005, abstract n° 4

VEGF comme thérapeutique ciblée : Quelles leçons en tirer ? Le Bevacizumab à été développé comme une drogue « classique » de chimiothérapie • Les patientes n’ont pas été sélectionnées : ce n’est pas ciblé ! • On ne peut pas développer une molécule de manière satisfaisante si il n’existe pas de test de sensibilité (ou de non sensibilité) facilement utilisable en pratique clinique

Autres thérapeutiques dites « ciblées » essayées sans ciblage dans le cancer du sein : Glivec : PDGF KI : RP = 0% Iressa : HER 1 KI : RP = 7% CCI-779 : m. TOR inhibiteur : RP = 12% Ro 31 -7453 : PKC KI : RP = 6% Bevacizumab : VEGF m. AB : RP = 7 %

Émergence d’une nouvelle cible : PARP BRCA 1 et BRCA 2 sont impliqués dans la réparation de l’ADN par recombinaison homologue BRCA 1 ou BRCA 2 mutés entraînent une instabilité génétique prédisposant au cancer La Poly(ADP-ribose) Polymerase (PARP) à un rôle majeur dans la réparation des cassures simple brin de l’ADN L’association d’une anomalie de la recombinaison homologue (BRCA) et de la réparation des cassures simple brin (PARP) est létale pour la cellule
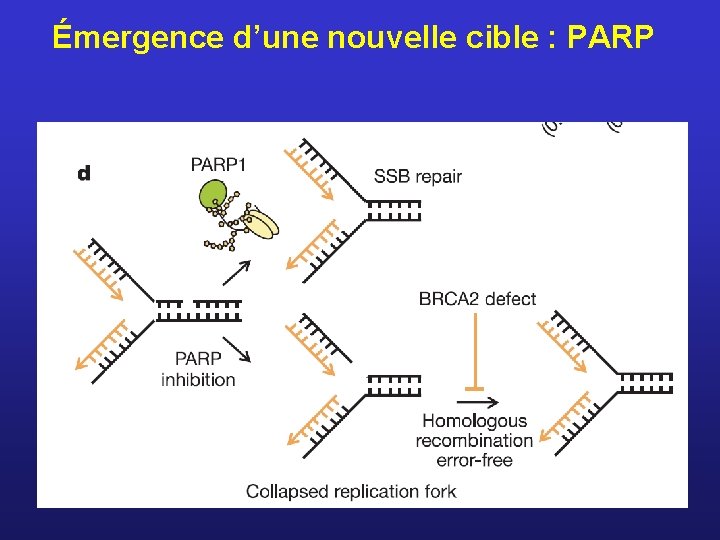
Émergence d’une nouvelle cible : PARP

Phase 1 PARP inhibiteur KU-0059436 (Astra. Zeneca) • • • 44 patients traités (17 M; 27 F) 11 BRCA+ et 2 probables Traitement jusqu’à 600 mg bid Neurotox grade 3 résolutif chez 1 patient Plusieurs réponses partielles chez des patientes porteuses de mutation BRCA (ASCO 07) • Phase II proposée De Bono J. et al. TAT 2007 Abs O 704

Les thérapeutiques ciblées dans le cancer du sein Ciblées sur quoi ? Sur une anomalie importante Ciblées pour qui ? Pour les patientes dont la tumeur en dépend
- Slides: 31