Les tampons et leur limite Objectifs du cours

Les tampons et leur limite

Objectifs du cours À la fin de ce cours vous serez en mesure de: 1. d’appliquer les notions sur les acides et les bases aux réactions en solution 2. calculer le p. H dans le cas des mélanges de solutions (acide/base faible avec son sel, acide fort et base faible, acide faible et base forte) 3. appliquer les notions relatives aux solutions tampons à diverses situations problématiques

La fermentation du lait • Pourquoi fermente-t-on le lait? • Quels produits peut-on obtenir avec la fermentation du lait? • Que peut-il arriver si le lait est fermenté de la mauvaise façon?
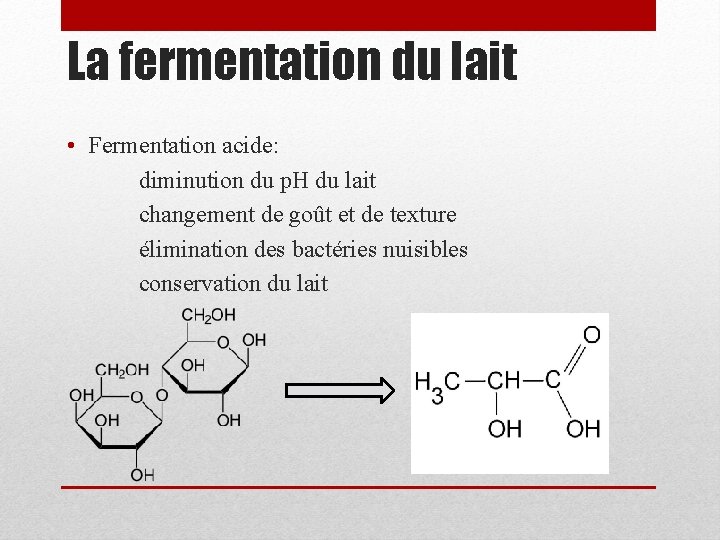
La fermentation du lait • Fermentation acide: diminution du p. H du lait changement de goût et de texture élimination des bactéries nuisibles conservation du lait

Question du jour • Le lait contient des solutions tampons, comment peut-il être acidifié?

p. H et capacité, un rappel •

Variation du p. H, un exemple Une solution tampon de 1, 00 L est constituée de 0, 100 mol/L de CH 3 COOH et de 0, 100 mol/L de CH 3 COONa. On y ajoute 0, 0100 mol de HCl. Déterminez la variation de p. H de la solution tampon. Ka = 1, 80 x 10 -5 (négligez la variation de volume causée par l’ajout) Voir fichier Les exemples dans la section exemples du site internet.

Limite • Qu'est-ce que la limite d’une solution tampon? La limite d’une solution tampon est atteinte lorsque le pouvoir tampon ou la capacité est dépassé.

Limite •

Limite, un exemple Une solution ayant un volume de 1, 00 L est constituée de 5, 00 x 10 -2 mol de HCOOH et de 5, 10 x 10 -2 mol de HCOONa. p. Ka = 3, 75 Déterminez : 1 - Si la solution initiale est un tampon et son p. H. 2 - Si la solution initiale est encore un tampon après l’ajout de 5, 00 x 10 -2 mol de HCl. 3 - Le p. H de la solution finale. Voir fichier Les exemples dans la section exemples du site internet.

Question du jours • Le lait contient des solutions tampons, comment peut-il être acidifié?
À faire: Voir fichier Les exercice dans la section à faire du site internet.

Référence • Hill, J. W. et Petrucci, R. H. (2003). Chimie des solutions. Saint-Laurent (Québec) : aux Éditions du Renouveau Pédagogique Inc. • Allard, J. C. et Flamand, E. (2003). Chimie des solutions (2 e édition). Mont-Royal (Québec) : aux Éditions Modulo.
- Slides: 13