Les ractions acide base q Acidit Basicit Dfinitions

Les réactions acide - base q Acidité – Basicité – Définitions q Acide faible – Base faible q Diagramme de prédominance q Calculs de p. H en milieu aqueux q Neutralisation acide – base q Les solutions tampons

Acidité – Basicité - Définitions q Caractéristiques générales des acides et des bases Acide : saveur piquante (vinaigre, citron) change la couleur des colorants des plantes change la couleur des indicateurs colorés Base : saveur caustique semble glissant au toucher change la couleur des colorants des plantes change la couleur des indicateurs colorés Théories successives

q Qu’est ce qu’un acide ou une base ? ü Arrhénius (1887) : Acide : capable de libérer un ou des ions H+ Base : capable de donner un ou des ions OHØ Exemples : HCl H+ + Cl. R-CO 2 H R-CO 2 - + H+ Na. OH Na+ + OHü Brönsted-Lowry (1922) : Acide : capable de libérer un ou des ions H+ Base : capable de capter un ou des ions H+ ü Lewis (1923) : Acide : capable d’accepter des électrons Base : capable de donner des électrons

q Acidité – Notion de p. H Théorie de Brönsted-Lowry : un acide libère un ou plusieurs protons L’acidité dépend de [H+] Or : 10 -14 M < [H 3 O+] < 1 M L’acidité est définie par : ([H 3 O+] en milieu H 2 O) Utilisation des logarithmes (plus commodes à manipuler) où = activité de l’ion H 3 O+ On notera : activité coefficient concentration mol. L-1 d’activité Pour des solutions peu concentrées, on assimilera l’activité à la concentration 0 p. H 14

q Mesure de p. H : p. Hmètre - une électrode de verre - un millivoltmètre Permet une mesure précise (à ± 0. 01 unité p. H après étalonnage de l’appareil)

q Mesure de p. H : papier p. H Mesure approximative du p. H par comparaison de couleurs
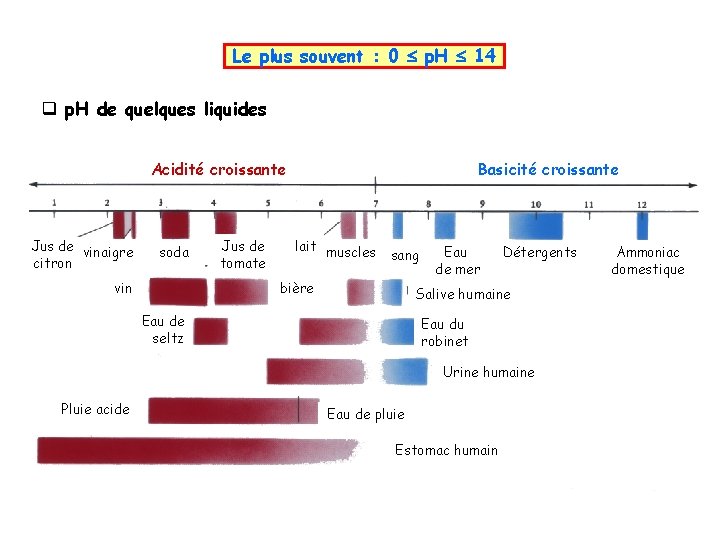
Le plus souvent : 0 p. H 14 q p. H de quelques liquides Acidité croissante Jus de vinaigre citron soda vin Jus de tomate Basicité croissante lait muscles sang bière Eau de mer Détergents Salive humaine Eau de seltz Eau du robinet Urine humaine Pluie acide Eau de pluie Estomac humain Ammoniac domestique

q Rôle du solvant: Solvant - sert de relais aux échanges de protons - permet aux équilibres de s’établir - permet aux acides et aux bases de révéler leurs propriétés acido-basiques Ø Solvant = eau : • Action de l’eau sur les acides : HA + H 2 O H 3 O + + A Dans l’eau, le proton est hydraté et existe sous forme H 3 O+ • Action de l’eau sur les bases : B + H 2 O BH+ + OH-
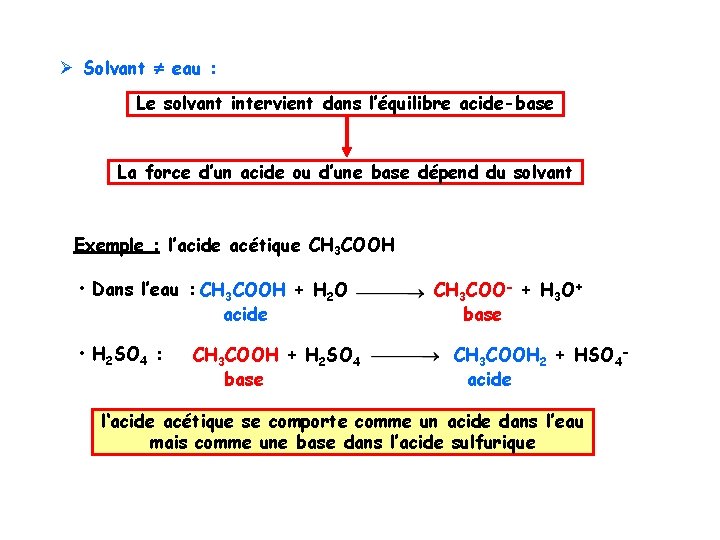
Ø Solvant eau : Le solvant intervient dans l’équilibre acide-base La force d’un acide ou d’une base dépend du solvant Exemple : l’acide acétique CH 3 COOH • Dans l’eau : CH 3 COOH + H 2 O acide • H 2 SO 4 : CH 3 COOH + H 2 SO 4 base CH 3 COO- + H 3 O+ base CH 3 COOH 2 + HSO 4 acide l‘acide acétique se comporte comme un acide dans l’eau mais comme une base dans l’acide sulfurique
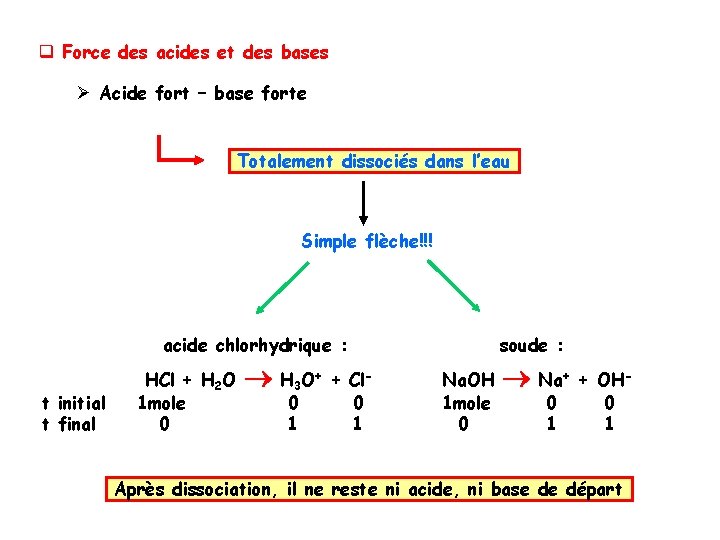
q Force des acides et des bases Ø Acide fort – base forte Totalement dissociés dans l’eau Simple flèche!!! acide chlorhydrique : t initial t final HCl + H 2 O 1 mole 0 soude : H 3 O+ + Cl 0 1 Na. OH 1 mole 0 Na+ + OH 0 1 Après dissociation, il ne reste ni acide, ni base de départ
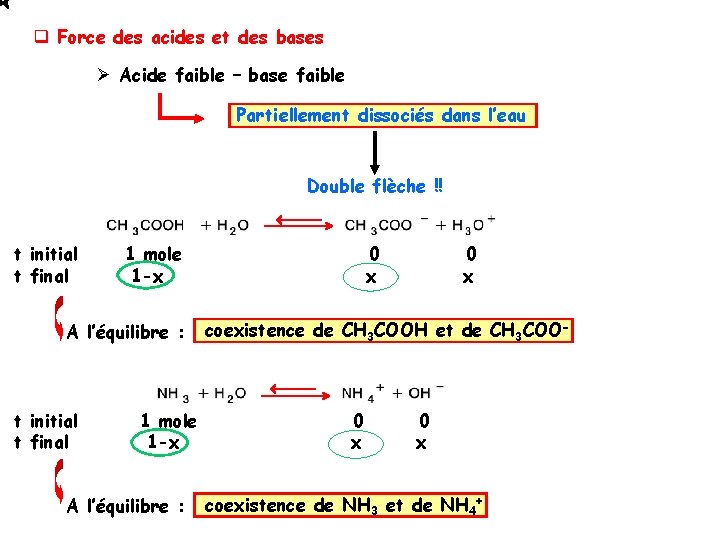
q Force des acides et des bases Ø Acide faible – base faible Partiellement dissociés dans l’eau Double flèche !! t initial t final 1 mole 1 -x A l’équilibre : 0 x coexistence de CH 3 COOH et de CH 3 COO- 0 x coexistence de NH 3 et de NH 4+

Les réactions acide - base q Acidité – Basicité – Définitions q Acide faible – Base faible q Diagramme de prédominance q Calculs de p. H en milieu aqueux q Neutralisation acide – base q. Les solutions tampons

Acide faible – Base faible (Définitions de la théorie de Brönsted-Lowry) q Couple acide/base conjugué Un acide HA libère un proton selon la réaction de dissociation (partielle): Cette réaction est réversible (double flèche : équilibre) A- peut donc capter un proton pour donner : Par conséquent, selon la théorie de Brönsted-Lowry, A- est une base A- est appelée base conjuguée de l’acide HA HA et A- forment un couple d’acide et de base conjugués Notation : HA/A-

q Acide faible – base faible : constantes d’acidité Ka et de basicité Kb Soit l’équilibre : Constante d’acidité : Si on considère l’équilibre : Constante de basicité : On donne le plus souvent les constantes d’acidité et de basicité sous forme de logarithme : p. Ka = -log. Ka Relation : p. Ka + p. Kb = 14 p. Kb = -log. Kb On ne travaillera qu’avec Ka Souvent : 0 ≤ p. Ka ≤ 14
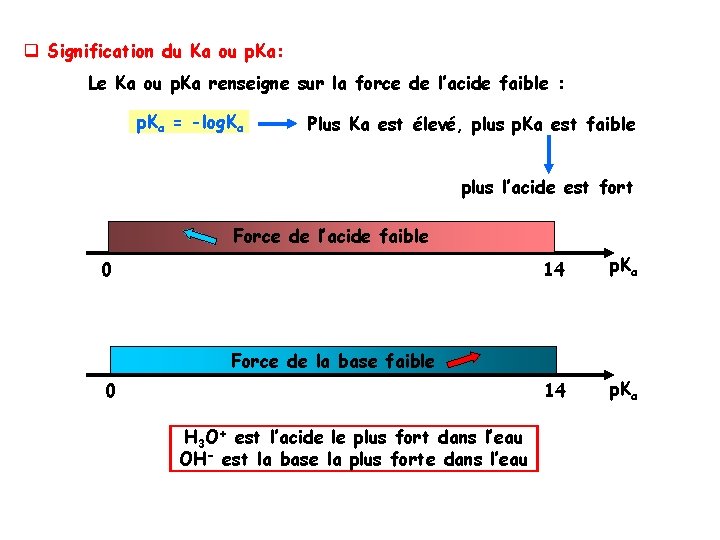
q Signification du Ka ou p. Ka: Le Ka ou p. Ka renseigne sur la force de l’acide faible : p. Ka = -log. Ka Plus Ka est élevé, plus p. Ka est faible plus l’acide est fort Force de l’acide faible 0 14 p. Ka Force de la base faible 0 H 3 O+ est l’acide le plus fort dans l’eau OH- est la base la plus forte dans l’eau

Ø Application : Couple 1 : HNO 2/NO 2 - : p. Ka 1 = 3, 30 Couple 2 : CH 3 COOH/CH 3 COO- : p. Ka 2 = 4, 75 3, 30 4, 75 p. Ka 1 < p. Ka 2 l’acide (1) HNO 2 est plus fort que l’acide (2) CH 3 COOH la base (1) NO 2 - est plus faible que la base (2) CH 3 COO-
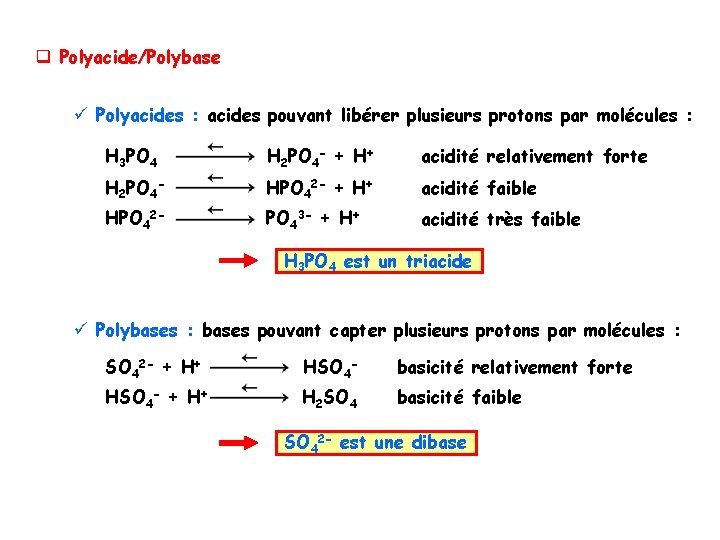
q Polyacide/Polybase ü Polyacides : acides pouvant libérer plusieurs protons par molécules : H 3 PO 4 H 2 PO 4 - + H+ acidité relativement forte H 2 PO 4 - HPO 42 - + H+ acidité faible HPO 42 - PO 43 - + H+ acidité très faible H 3 PO 4 est un triacide ü Polybases : bases pouvant capter plusieurs protons par molécules : SO 42 - + H+ HSO 4 - basicité relativement forte HSO 4 - + H+ H 2 SO 4 basicité faible SO 42 - est une dibase

Chaque acidité est caractérisée par une valeur de p. Ka : Ø Acide phosphorique : tricacide 3 acidités • H 3 PO 4/H 2 PO 4 - p. Ka 1 = 2. 2 • H 2 PO 4 -/HPO 42 - p. Ka 2 = 7. 2 • HPO 42 -/PO 43 - p. Ka 3 = 12. 3 p. Ka 1 1ère acidité > < p. Ka 2 < 2ème acidité Ø Acide oxalique : diacacide p. Ka 3 > 3ème acidité 2 acidités • H 2 C 2 O 4/HC 2 O 4 - p. Ka 1 = 1. 2 • HC 2 O 4 -/C 2 O 42 - p. Ka 2 = 4. 3 3 p. Ka 1 < p. Ka 2 1ère acidité > 2ème acidité 2 p. Ka
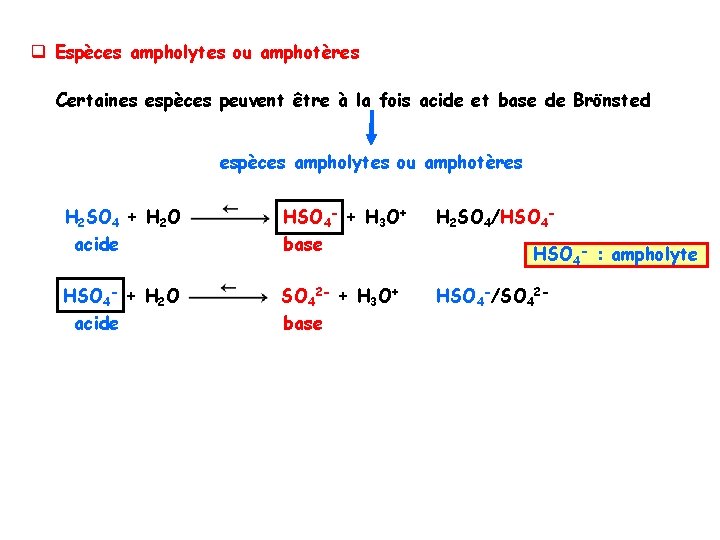
q Espèces ampholytes ou amphotères Certaines espèces peuvent être à la fois acide et base de Brönsted espèces ampholytes ou amphotères H 2 SO 4 + H 2 O acide HSO 4 - + H 3 O+ base SO 42 - + H 3 O+ base H 2 SO 4/HSO 4 - : ampholyte HSO 4 -/SO 42 -
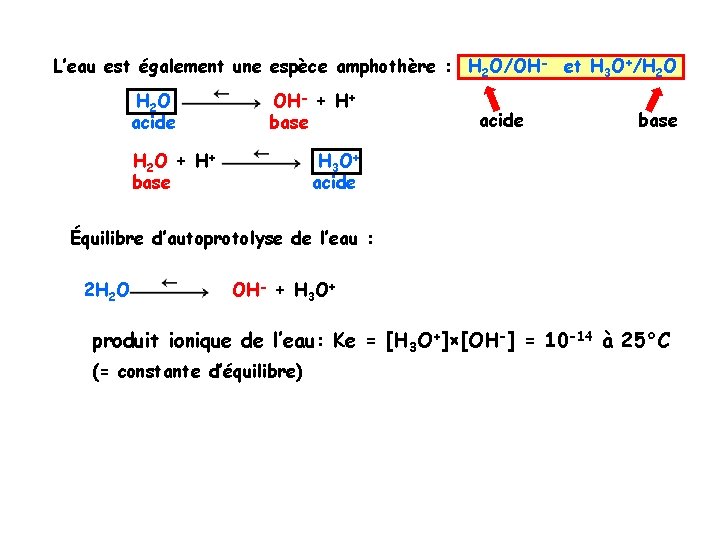
L’eau est également une espèce amphothère : H 2 O/OH- et H 3 O+/H 2 O H 2 O acide OH- + H+ base H 2 O + H + base acide base H 3 O + acide Équilibre d’autoprotolyse de l’eau : 2 H 2 O OH- + H 3 O+ produit ionique de l’eau: Ke = [H 3 O+]×[OH-] = 10 -14 à 25°C (= constante d’équilibre)

q Coefficient de dissociation a d’un acide Coefficient de protonation a d’une base faible : Acide dissociation partielle Coexistence de l’acide et de la base conjuguée Le coefficient de dissociation a sert à quantifier la dissociation : - t 0 téq C 0 0 0 ? ? ? 0 a 1
![t 0 téq [HA]0 [HA]éq 0 [A-]éq Or : [HA]éq = [HA]0 - [HA]dissocié t 0 téq [HA]0 [HA]éq 0 [A-]éq Or : [HA]éq = [HA]0 - [HA]dissocié](http://slidetodoc.com/presentation_image_h2/3a958bd835b260dc91da0799f0013b64/image-22.jpg)
t 0 téq [HA]0 [HA]éq 0 [A-]éq Or : [HA]éq = [HA]0 - [HA]dissocié [HA]éq = [HA]0 - [A-]éq avec [HA]0 = C 0 [HA]éq = [HA]0 - a [HA]0 [HA]éq = [HA]0 (1 -a) [HA]éq = C 0(1 -a) 0 C 0 a on peut calculer a
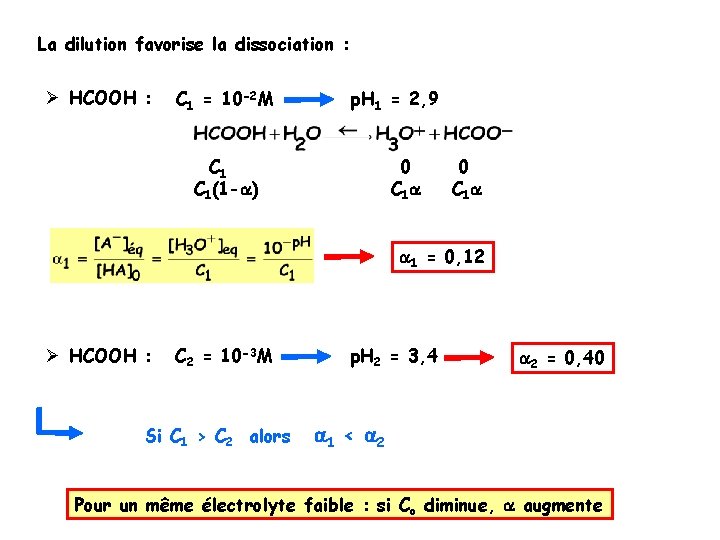
La dilution favorise la dissociation : Ø HCOOH : C 1 = 10 -2 M p. H 1 = 2, 9 C 1(1 -a) 0 C 1 a a 1 = 0, 12 Ø HCOOH : C 2 = 10 -3 M Si C 1 > C 2 alors p. H 2 = 3, 4 a 2 = 0, 40 a 1 < a 2 Pour un même électrolyte faible : si Co diminue, a augmente

Les réactions acide - base q Acidité – Basicité – Définitions q Acide faible – Base faible q Diagramme de prédominance q Calculs de p. H en milieu aqueux q Neutralisation acide – base q. Les solutions tampons
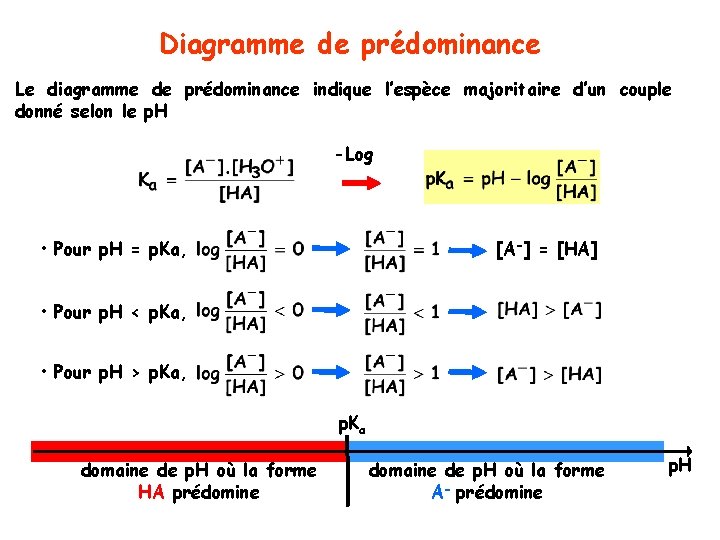
Diagramme de prédominance Le diagramme de prédominance indique l’espèce majoritaire d’un couple donné selon le p. H -Log • Pour p. H = p. Ka, [A-] = [HA] • Pour p. H < p. Ka, • Pour p. H > p. Ka, p. Ka domaine de p. H où la forme HA prédomine domaine de p. H où la forme A- prédomine p. H
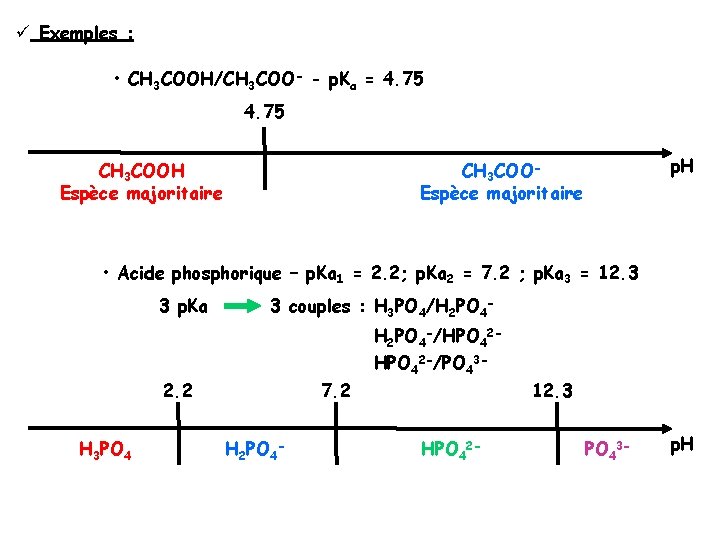
ü Exemples : • CH 3 COOH/CH 3 COO- - p. Ka = 4. 75 CH 3 COOH Espèce majoritaire p. H CH 3 COOEspèce majoritaire • Acide phosphorique – p. Ka 1 = 2. 2; p. Ka 2 = 7. 2 ; p. Ka 3 = 12. 3 3 p. Ka 3 couples : H 3 PO 4/H 2 PO 4 -/HPO 42 -/PO 43 - 2. 2 H 3 PO 4 7. 2 H 2 PO 4 - 12. 3 HPO 42 - PO 43 - p. H
- Slides: 26