Les produits sanguins labiles Nature et indication ARS

Les produits sanguins labiles Nature et indication ARS - EFS Version 2 - 2017

Ont participé à la révision de ce diaporama : - Madame Véronique BOURCIER, Médecin Correspondante d’Hémovigilance et de Sécurité Transfusionnelle du CHU de Besançon - Madame Catherine HUMBRECHT, Médecin au Département de médecine transfusionnelle à l’Etablissement Français du Sang Grand Est - Monsieur Jean-Pierre RAIDOT, Médecin Responsable du site de Colmar à l’EFS Grand Est - Madame Sylvie SCHLANGER, Médecin Coordonnateur Régional d’Hémovigilance et de Sécurité Transfusionnelle à l’Agence Régionale de Santé Grand Est – Délégation Territoriale Alsace - Madame Sophie SOMME, Médecin Responsable adjointe Pôle Vigilances à l’Etablissement Français du Sang Grand Est ARS - EFS 2

Les Produits Sanguins Labiles (PSL) • Recommandations transfusionnelles de l’HAS (Haute Autorité de Santé) – Pour les CGR (11/2014) – Pour les plaquettes (10/2015) – Pour le PFC (2012) • disponibles sur http: //www. has-sante. fr • cliquez sur évaluations et recommandations , puis recommandations de bonnes pratiques (format pdf imprimable) ARS - EFS 3

Les Produits Sanguins Labiles (PSL) À partir des prélèvements de donneurs volontaires, l’EFS prépare essentiellement - des Concentrés de Globules Rouges (CGR) - des Concentrés de Plaquettes (CP) - du Plasma Frais Congelé (PFC) ARS - EFS 4
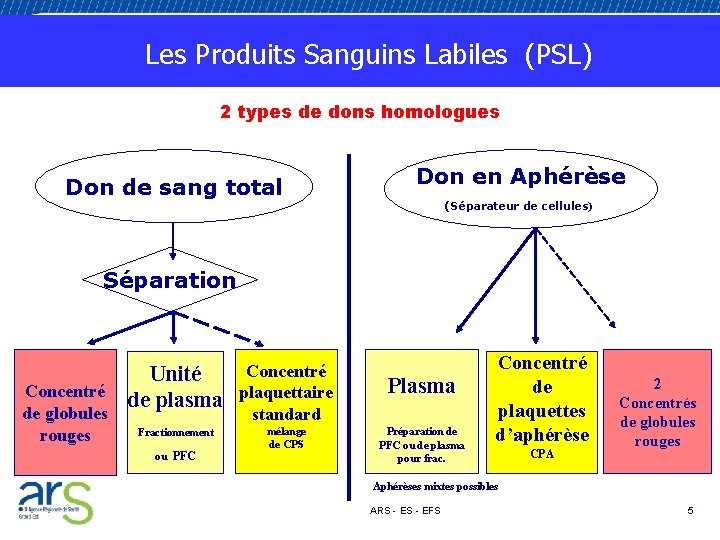
Les Produits Sanguins Labiles (PSL) 2 types de dons homologues Don de sang total Don en Aphérèse (Séparateur de cellules) Séparation Concentré de globules rouges Concentré Unité de plasma plaquettaire Plasma standard Fractionnement ou PFC mélange de CPS Préparation de PFC ou de plasma pour frac. Concentré de plaquettes d’aphérèse CPA 2 Concentrés de globules rouges Aphérèses mixtes possibles ARS - EFS 5
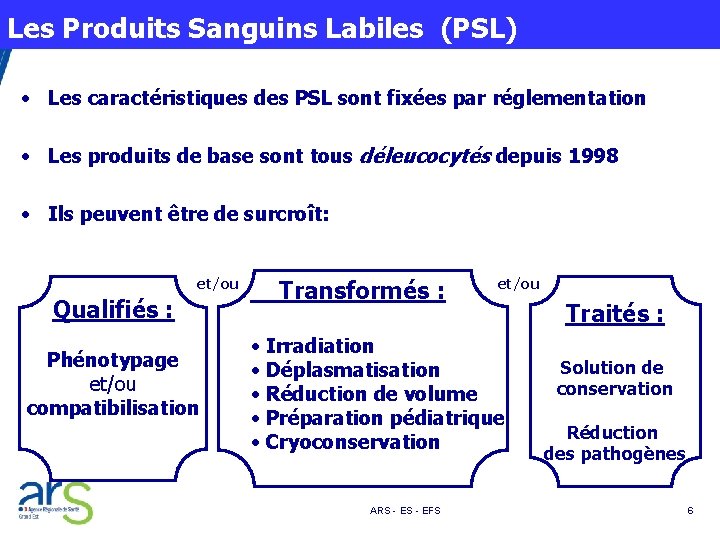
Les Produits Sanguins Labiles (PSL) • Les caractéristiques des PSL sont fixées par réglementation • Les produits de base sont tous déleucocytés depuis 1998 • Ils peuvent être de surcroît: et/ou Qualifiés : Phénotypage et/ou compatibilisation Transformés : et/ou • Irradiation • Déplasmatisation • Réduction de volume • Préparation pédiatrique • Cryoconservation ARS - EFS Traités : Solution de conservation Réduction des pathogènes 6

GR Les Concentrés de Globules Rouges (CGR) ARS - EFS 7

Les CGR: caractéristiques générales • donneur unique • hématocrite 50 -70% • contient au moins 40 g d’hémoglobine • leucocytes résiduels: < 1 x 106 par unité • conservation EFS pendant 42 jours entre +2 et +6°C ARS - EFS 8
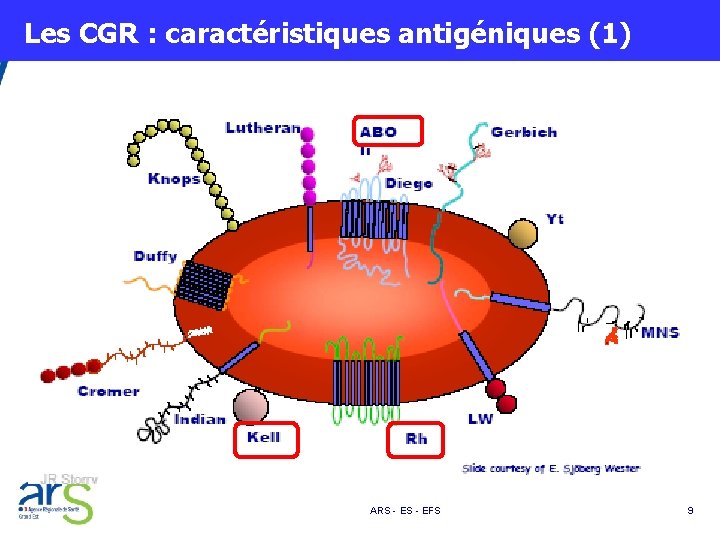
Les CGR : caractéristiques antigéniques (1) ARS - EFS 9
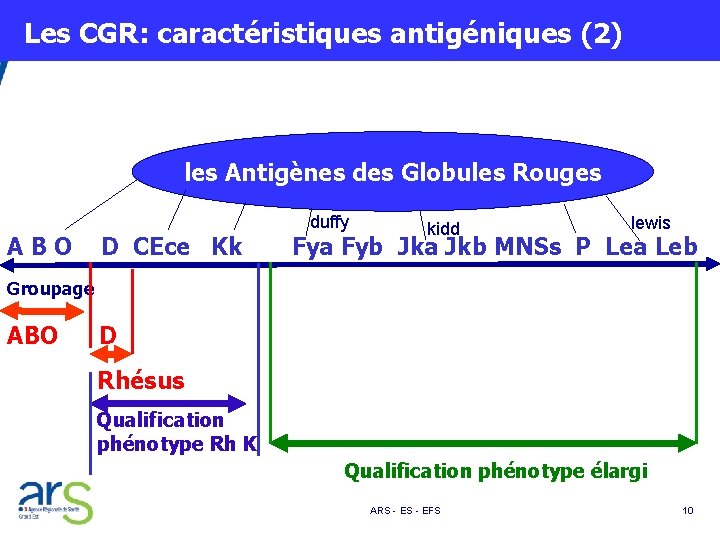
Les CGR: caractéristiques antigéniques (2) les Antigènes des Globules Rouges duffy kidd lewis A B O D CEce Kk Fya Fyb Jka Jkb MNSs P Lea Leb Groupage ABO D Rhésus Qualification phénotype Rh K Qualification phénotype élargi ARS - EFS 10

Les CGR: caractéristiques antigéniques (3) Exemple d’un groupage avec phénotype élargi A positif : A + C- E+ c+ e- K- Fy(a-b+) Jk(a+b-) Le (a-b-) M+N+S-s+, P+ Nomenclature internationale A + RH : 1, -2 , 3, 4, -5 KEL : -1 FY : -1, 2 JK : 1, -2 LE: -1, -2 MNS : 1, 2, -3, 4 P : 1 ARS - EFS 11
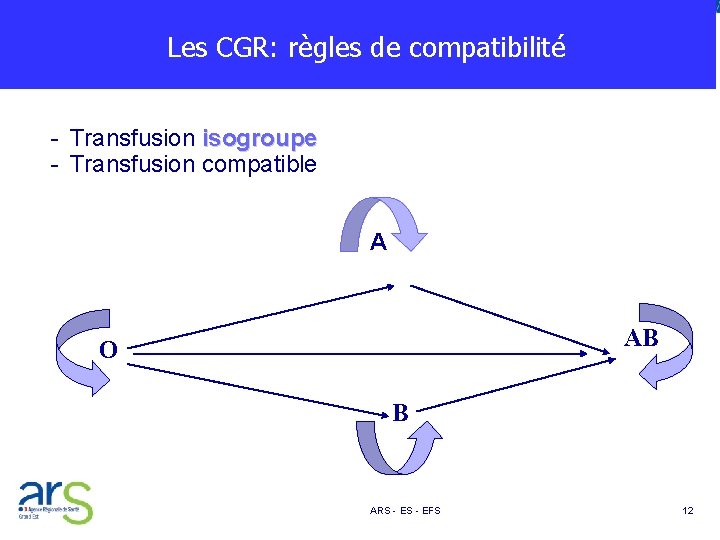
Les CGR: règles de compatibilité - Transfusion isogroupe - Transfusion compatible A AB O B ARS - EFS 12

Les CGR: qualification phénotypé (1) • PHÉNOTYPÉ Rhesus (D, C, E, c, e), Kell • correspond à RH: 1, 2, 3, 4, 5 et KEL 1 en nomenclature internationale = patients RAI + ARS - EFS 13

Les CGR: qualification phénotypé (2) • PHÉNOTYPÉ Rhesus (D, C, E, c, e), Kell • correspond à RH: 1, 2, 3, 4, 5 et KEL 1 en nomenclature internationale ARS - EFS 14

Les CGR: qualification phénotypage étendu • Phénotypage étendu : respect des antigènes des autres systèmes que le Rhésus et le Kell: • Duffy (Fya, Fyb ou FY 1, 2) • Kidd (Jka, Jkb ou JK 1, 2) • Lewis (Lea, Leb ou LE 1, 2) • MNSs ( M, N, S, s ou MNS 1, 2, 3, 4) • Obligatoire si RAI positive selon la spécificité de l’anticorps • Recommandé chez les drépanocytaires ARS - EFS 15

Les CGR: qualification compatibilisé • Compatibilisation: épreuve au laboratoire qui met en présence les GR à transfuser avec le plasma du patient en utilisant la même technique la RAI • Indications : RAI + ou ancien Ac « dangereux » Nouveau-né de mère ayant 1 Ac anti-D Drépanocytaire • Tes nécessaire à la réalisation : environ 60 mn • Durée de validité du résultat de la compatibilité : 72 h en l’absence de transfusion • En cas de transfusion dans l’intervalle, il est conseillé de refaire une RAI avant la nouvelle transfusion (réactivation possible d’une immunisation antérieure) ARS - EFS 16

Les CGR: qualification CMV négatif • La qualification CMV négatif n’est plus recommandée selon les recommandations HAS de novembre 2014 • La déleucocytation systématique (< 106/CGR) assure la prévention de la transmission du CMV ARS - EFS 17

Les CGR: transformation irradié Transformation «irradié» : à quoi cela sert-il? L’irradiation de 25 à 45 grays (rayons ) évite la réaction du greffon contre l’hôte (GVH) La GVH est due à la prolifération des lymphocytes T résiduels du donneur chez un sujet immunodéprimé avec un tableau clinique gravissime ARS - EFS 18

Les CGR: indications de l’irradiation • Déficit congénital immunitaire cellulaire • Greffes de cellules-souches hématopoïétiques: • • • – 7 jours avant et pendant un recueil – Au moins 3 mois pour les autogreffes – Au moins 12 mois pour les allogreffes Certaines chimiothérapies Certaines immunosuppressions T (hors VIH) Transfusion intra-utérine Exsanguino-transfusion massive chez le prématuré Don dirigé intra-familial Indications surtout hématologiques Ne pas hésiter à contacter le référent du patient ARS - EFS 19

Les CGR: transformation déplasmatisé Soustraction de la majeure partie du plasma du donneur et remplacement par une solution physiologique adaptée par « lavage » Indications : ARS - EFS 20

Les CGR: autres transformations Préparation pédiatrique – Division aseptique d’un CGR en plusieurs unités utilisables successivement pour un même patient Réduction de volume – Élimination aseptique d’une partie du milieu de suspension Indication : le nouveau-né § Réduction solution de conservation et potassium § Réduction surcharge volémique Sang total reconstitué – Mélange d’un CGR avec un PFC Indication : Nouveau-né pour les exsanguino-transfusions ou les techniques d’assistance cardio-vasculaire. ARS - EFS 21
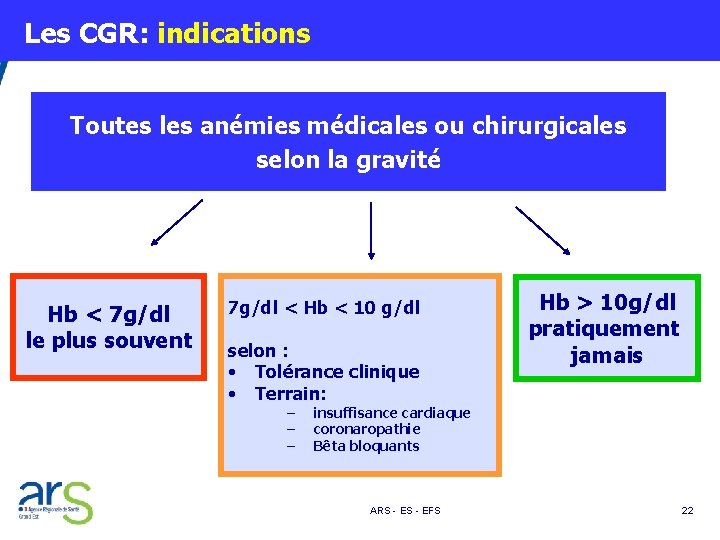
Les CGR: indications Toutes les anémies médicales ou chirurgicales selon la gravité Hb < 7 g/dl le plus souvent 7 g/dl < Hb < 10 g/dl selon : • Tolérance clinique • Terrain: – – – Hb > 10 g/dl pratiquement jamais insuffisance cardiaque coronaropathie Bêta bloquants ARS - EFS 22

Les CGR: indications en anesthésie-réanimation • Anesthésie • Polytraumatisés • Réanimation ARS - EFS 23

Les CGR: indications en médecine • Hémorragie digestive • Oncologie et hématologie: • Gériatrie ARS - EFS 24

Les CGR: indications en néonatologie • Recommandations très détaillées en fonction: – Du poids de naissance – De l’âge gestationnel – Des paramètres ventilatoires • Se référer directement aux recommandations sur le site de la HAS, pages 46 à 61 ARS - EFS 25

CGR: posologie En l’absence d’hémorragie active: Chez l’adulte : 1 CGR augmente le taux d’Hémoglobine (Hb) de 1 g/d. L Chez l’enfant : 3 à 4 m. L/kg augmentent le taux d’Hb de 1 g/d. L ARS - EFS 26

CGR : non-indications Rappel: les hypovolémies se traitent d’abord par des solutés de remplissage Na. Cl 0, 9% macromolécules Il n’y a pas d’indications aux CGR dans les chocs cardiogéniques, septiques, anaphylactiques ARS - EFS 27

CGR : alternatives à la transfusion (1) • Fer: recommandé seulement en présence d’une carence avérée, en privilégiant la voie orale • Carences en folates et B 12 bien tolérées: supplémentation • EPO: recommandé en onco-hémato et préOP pour la chirurgie orthopédique ARS - EFS 28

CGR : alternatives à la transfusion (2) • Acide tranexamique (Exacyl®): chirurgie et polytraumatisés dans les 3 premières heures (1 g IVL sur 10 min, puis 1 g/8 h) • Facteurs de coagulation et Facteur VII activé (Novoseven®) • Cell. Saver® en per-OP • Autotransfusion programmée si groupe sanguin rare ou patient polyimmunisé ARS - EFS 29

plaquette Les concentrés de plaquettes ARS - EFS 30

Les CP: caractéristiques • Mélange de concentrés plaquettaires (MCP) Plusieurs donneurs de même groupe ABO Actuellement, en moyenne: ≈ 4. 1011 plaquettes / produit • Concentré de plaquettes d’aphérèse (CPA) Un seul donneur 2 à 6. 1011 plaquettes / produit Les plaquettes sont en suspension dans 200 à 600 ml de plasma ou de solution de conservation Nb: la quantité de plaquettes est indiquée sur l’étiquette ARS - EFS 31

Les CP: caractéristiques • Equivalence thérapeutique entre MCP et CPA • Il ne reste que 2 indications résiduelles pour CPA: • patient allo-immunisé anti-HLA • réductions de volume pour la pédiatrie • Qualification possible: • phénotypage HLA/HPA • Traitement possible: réduction des pathogènes (actuellement amotosalen) • Transformations possibles: • déplasmatisation • réduction de volume ou division pour préparation pédiatrique • irradiation ARS - EFS 32
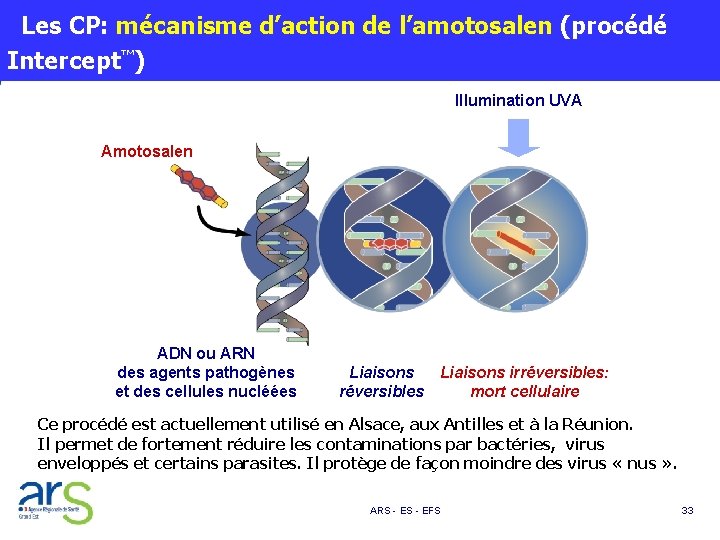
Les CP: mécanisme d’action de l’amotosalen (procédé Intercept™) Illumination UVA Amotosalen ADN ou ARN des agents pathogènes et des cellules nucléées Liaisons réversibles Liaisons irréversibles: mort cellulaire Ce procédé est actuellement utilisé en Alsace, aux Antilles et à la Réunion. Il permet de fortement réduire les contaminations par bactéries, virus enveloppés et certains parasites. Il protège de façon moindre des virus « nus » . ARS - EFS 33

Les CP: conservation Conservation des CPA et MCP à l’EFS : • sous agitation douce et continue à T° régulée 20°C à 24°C • pour une durée MAXIMALE de 5 jours à partir du jour et de l’heure de prélèvement ARS - EFS 34

Les CP: règles de compatibilité • Compatibilité A B O chaque fois que possible • Compatibilité Rh D recommandée pour tout receveur féminin RH : -1 en âge de procréer et hors immunosuppression profonde dans ces cas-là, si non respect du Rh D: administrer Ig. G anti-D (Rhophylac®) : au moins 100 g IV dans les 72 heures, dose suffisante pour 10 concentrés plaquettaires • Compatibilité HLA et HPA seulement si le patient est immunisé dans ces systèmes ARS - EFS 35

CP: posologie HAS 2015 • Chez l’adulte : 0, 5 à 0, 7. 1011 plaquettes pour 10 Kg de poids – Fourchette basse: obèses – Fourchette haute: situations curatives et enfants • Chez le nouveau-né: 0, 1 à 0, 2. 1011/kg de poids – permet d’augmenter la numération d’environ 20 G/L (= 20000/mm 3) – adapter selon les objectifs de numération – Exemple pour un patient de 70 kg = 7 tranches de 10 kg QPA à prescrire: entre 7 x 0, 5 = 3, 5 et 7 x 0, 7= 4, 9. 1011 plaquettes ARS - EFS 36

CP: Efficacité transfusionnelle • Arrêt du saignement (clinique) • Numération plaquettaire recommandée à H 1 et entre H 18 et H 24 • Inefficacité si absence de rendement après 2 transfusions consécutives • Calcul du rendement transfusionnel avec le Corrected Count Increment (CCI) CCI= (NP après T – NP avant T) x Surf. Corp. (m 2) x 100 nombre de plaquettes transfusées (1011) Inefficacité transfusionnelle plaquettaire quand CCI<7 Attention: le CCI n’est validé qu’en prophylaxie ARS - EFS 37

CP: seuils transfusionnels en onco- hématologie • Curatif : thrombopénies avec signes hémorragiques • Préventif : notion de seuil • Attention: ne pas transfuser des thrombopénies périphériques (sauf si saignement) ARS - EFS 38

CP: seuils transfusionnels en chirurgie ARS - EFS 39

CP: seuils transfusionnels en anesthésie ARS - EFS 40

CP: seuils transfusionnels en obstétrique § En général: ARS - EFS 41

CP: thrombopathies médicamenteuses Faut-il transfuser un patient sous antiagrégants avant geste invasif? PLAVIX*, BRILIQUE* EFIENT* ARS - EFS 42

plasma GB GR Plasma Frais Congelé (PFC) ARS - EFS 43

PFC: caractéristiques • Peut être issu d’un don de sang total ou d’une plasmaphérèse • 1 Unité Adulte ≥ 200 ml • conservation à l’EFS : 1 an à - 25° C • F VIII > 0, 7 Ui / ml ARS - EFS 44

PFC: les plasmas disponibles • Plasma sécurisé (PFC-Se): – quarantaine pendant au moins 60 jours, – le plasma est libéré seulement si le donneur revient faire un autre don, dont l’analyse biologique permet de sécuriser le don précédent (couverture de la fenêtre sérologique). • Plasma avec réduction des pathogènes (PFC-IA) • Plasma lyophilisé (PLYO): – utilisation militaire à ce jour – Essais cliniques civils en cours ARS - EFS 45

PFC: posologie • Le PFC est utilisé à la dose de: – 10 à 15 m. L/kg pour la correction des coagulopathies – 40 à 60 m. L/kg pour les échanges plasmatiques • Attention : - apport en moyenne 170 mmol/L de sodium - apport en volume (voir bilan entrées-sorties) ARS - EFS 46

PFC: indications de l’HAS 2012 Coagulopathies de consommation Avec effondrement des facteurs de coagulation Hémorragie aiguë critères reconnus : ratio Quick > 1, 5 Fibrinogène < 1, 0 g/l Avec déficit global des facteurs de coagulation Déficit complexe ou rare en facteurs de coagulation Quand les fractions correspondantes ne sont pas disponibles Microangiopathies thrombotiques ARS - EFS 47

PFC: contre-indications, précautions d’emploi • Contre-indications: les déficits congénitaux en Ig. A avec présence d’Ac anti-Ig. A • Précautions d’emploi: les atcd d’allergies au plasma ARS - EFS 48
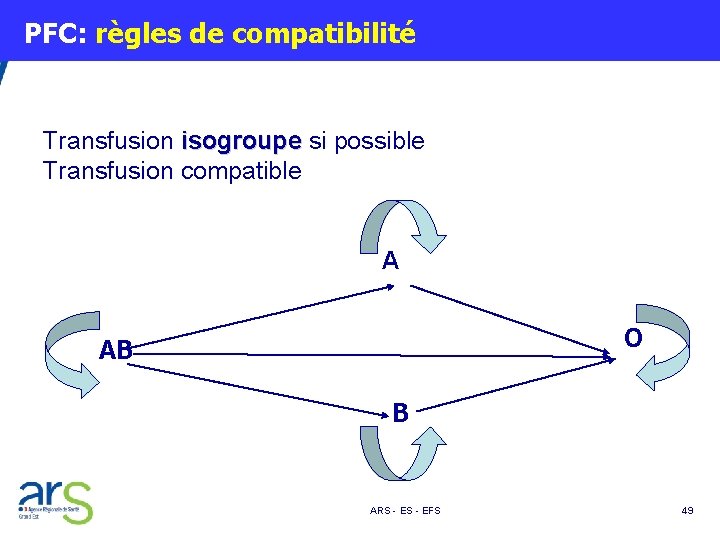
PFC: règles de compatibilité Transfusion isogroupe si possible Transfusion compatible A O AB B ARS - EFS 49

+ + Transfusion massive ARS - EFS 50

Transfusion massive • Transfusion massive = remplacement de plus de la moitié de la masse sanguine en 3 heures ou transfusion de plus de 10 CGR en 24 h • Coagulopathie précoce au cours du choc hémorragique, • • • aggravée par l’hypothermie et l’acidose sous-estimée par le labo qui standardise les tests à 37°C et p. H normal Diminution de la mortalité quand on augmente le ratio CGR: PFC et CGR: CP ARS - EFS 51

Transfusion massive • Intérêt de protocoles locaux ARS - EFS 52

Transfusion massive ARS - EFS 53

Les Produits Sanguins Labiles (PSL) QUESTIONS……? ? ? ARS - EFS 54
- Slides: 54