Les politiques de prix et remboursement des mdicaments

Les politiques de prix et remboursement des médicaments dans les pays de l’OCDE Valérie Paris, OCDE Princeps, 14 octobre 2016 Les opinions exprimées et les arguments développés ne reflètent pas nécessairement le point de vue officiel de l’OCDE ni celui de ses pays membres. Déclaration d’intérêts: Déjeuners, coûts de transports et d’hébergement occasionnellement couverts par les industries de santé. 1
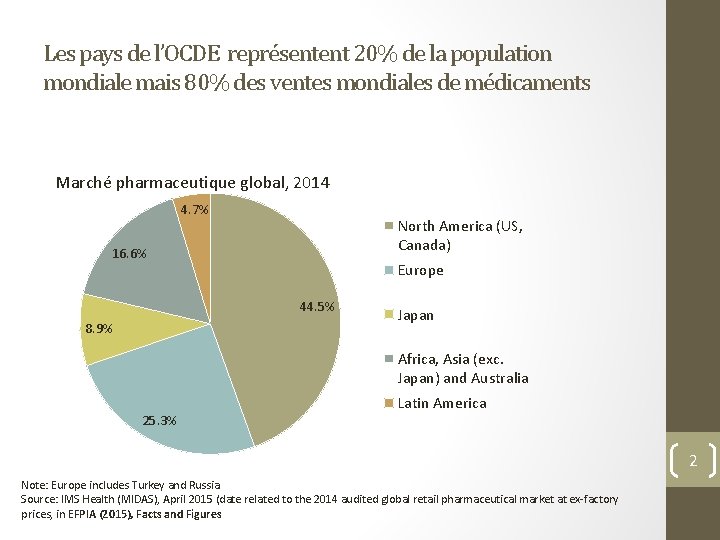
Les pays de l’OCDE représentent 20% de la population mondiale mais 80% des ventes mondiales de médicaments Marché pharmaceutique global, 2014 4. 7% North America (US, Canada) 16. 6% Europe 44. 5% 8. 9% Japan Africa, Asia (exc. Japan) and Australia 25. 3% Latin America 2 Note: Europe includes Turkey and Russia Source: IMS Health (MIDAS), April 2015 (date related to the 2014 audited global retail pharmaceutical market at ex-factory prices, in EFPIA (2015), Facts and Figures
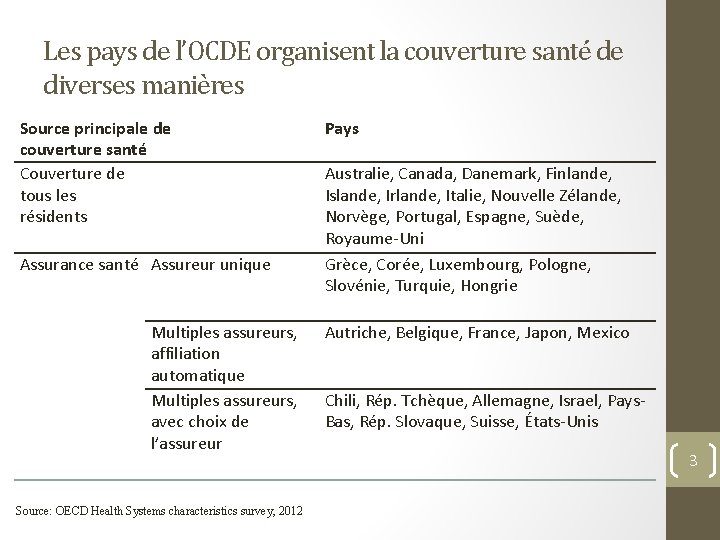
Les pays de l’OCDE organisent la couverture santé de diverses manières Source principale de couverture santé Couverture de tous les résidents Assurance santé Assureur unique Multiples assureurs, affiliation automatique Multiples assureurs, avec choix de l’assureur Source: OECD Health Systems characteristics survey, 2012 Pays Australie, Canada, Danemark, Finlande, Islande, Irlande, Italie, Nouvelle Zélande, Norvège, Portugal, Espagne, Suède, Royaume-Uni Grèce, Corée, Luxembourg, Pologne, Slovénie, Turquie, Hongrie Autriche, Belgique, France, Japon, Mexico Chili, Rép. Tchèque, Allemagne, Israel, Pays. Bas, Rép. Slovaque, Suisse, États-Unis 3

… mais la plupart des pays définissent une “liste positive” de médicaments couverts au niveau national Quelques exceptions: • Royaume-Uni: tous les médicaments couverts dès l’entrée sur le marché, sauf produits d’automédication et quelques exceptions. Quelques médicaments soumis à une évaluation médico-économique pour décider de leur financement par le Système National de santé. • Allemagne: tous les médicaments couverts, sauf quelques catégories exclues d’office (essentiellement automédication) • Canada, États-Unis, Mexique, Chile: la liste des médicaments couverts est définie par chaque assureur. Les usagers doivent le plus souvent contribuer aux coûts des médicaments, quelques exceptions: • Médicaments dispensés au cours d’une hospitalisation • Pays-Bas: pas de copaiement au-delà de la franchise annuelle (350 €) • France: médicaments coûteux • Beaucoup d’exemptions ou de plafonnement des copaiements dans les pays de l’OCDE 4
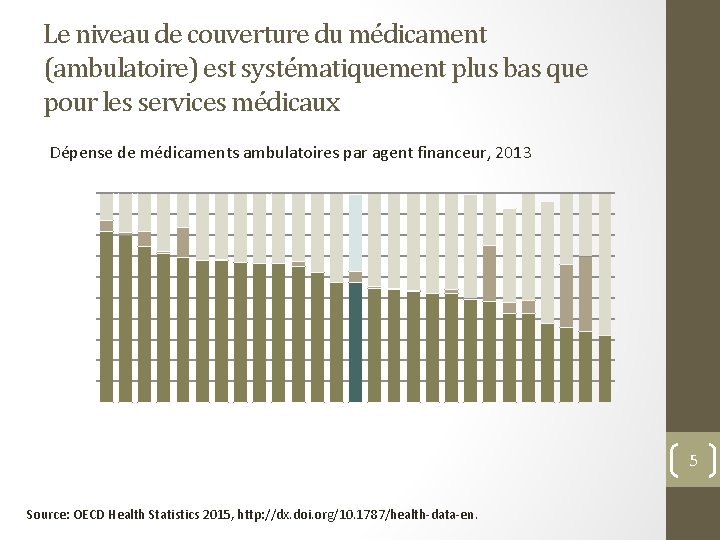
Le niveau de couverture du médicament (ambulatoire) est systématiquement plus bas que pour les services médicaux Dépense de médicaments ambulatoires par agent financeur, 2013 5 Source: OECD Health Statistics 2015, http: //dx. doi. org/10. 1787/health-data-en.
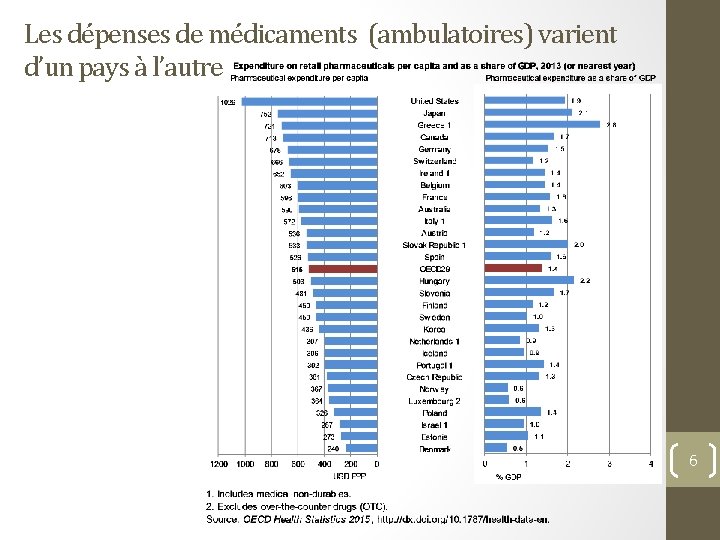
Les dépenses de médicaments (ambulatoires) varient d’un pays à l’autre 6
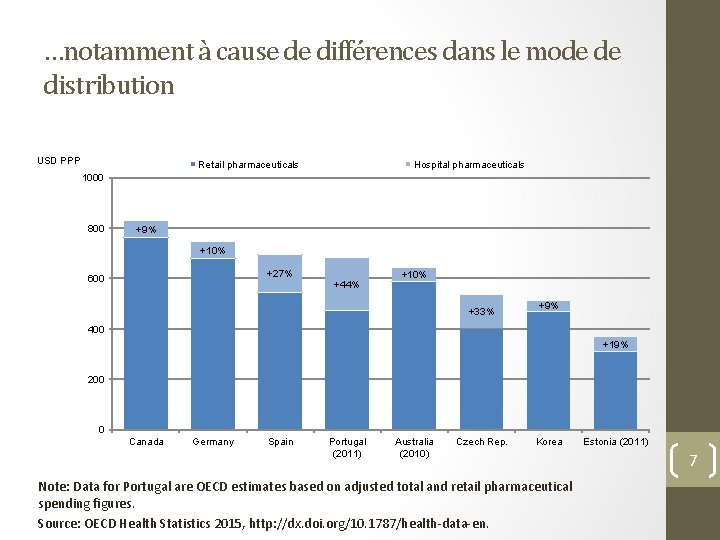
…notamment à cause de différences dans le mode de distribution USD PPP Retail pharmaceuticals Hospital pharmaceuticals 1000 800 +9% +10% +27% 600 +44% +10% +33% +9% 400 +19% 200 0 Canada Germany Spain Portugal (2011) Australia (2010) Czech Rep. Korea Note: Data for Portugal are OECD estimates based on adjusted total and retail pharmaceutical spending figures. Source: OECD Health Statistics 2015, http: //dx. doi. org/10. 1787/health-data-en. Estonia (2011) 7

Tous les pays de l’OCDE régulent les prix d’une manière ou d’une autre, au moins pour une partie du marché Dans la plupart des pays • Les prix des médicaments de prescription “ambulatoires” financés par les régimes publics sont régulés • Les prix des produits d’automédication ne sont pas régulés • Les prix des médicaments administrés à l’hôpital ne sont pas régulés (avec quelques exceptions) Exceptions: • Au Canada et au Mexique, les prix de tous les médicaments sous brevet (remboursés ou non) sont régulés – pour prévenir l’abus de monopole • Aux États-Unis, au Royaume-Uni et en Suède, les prix ne sont pas (directement) régulés 8

Les pays de l’OCDE utilisent le plus souvent plusieurs instruments pour réguler les prix • International benchmarking, référence aux prix pays à l’étranger pour déterminer un prix maximum. • Référencement thérapeutique– le prix ou le montant remboursé est déterminé en fonction des prix des médicaments existant ayant la même indication • Avec un avantage de prix si le produit apporte un bénéfice thérapeutique par rapport aux produits existants. • Évaluation médico-économique utilisée pour déterminer si le produit est coût-efficace. Régulation “indirecte” du prix. • Accords spécifiques (confidentiels) tels que les accords prix-volume ou basés sur la performance en vie réelle. • Autres: plafonnement des taux de profits (R-U), appels d’offre, etc. 9

Presque tous les pays de l’OCDE utilisent le benchmarking international Avec des objectifs et des méthodes différents: • La liste des pays considéré dépend des objectifs politique: • Canada: référence à 7 pays à haut revenu, pour apporter une “juste contribution” aux dépense de R&D. • De nombreux pays se réfèrent à des pays ayant des revenus similaires • Quelques pays se réfèrent à un grand nombre de pays (Europe) • Le niveau de prix considéré varie (prix sortie-usine ou grossiste) • La « référence » varie: prix minimum, moyen, médian • La plupart des pays recourent au BI à l’entrée sur le marché, mais quelques uns réévaluent la situation périodiquement Impact • Le BI influence les stratégies de lancement de produits des laboratoires • Le BI encourage la convergence des prix “de liste”, au moins dans l’Union Européenne • … mais aussi le développement des rabais confidentiels, qui en retour compromettent la pertinence du benchmarking 10
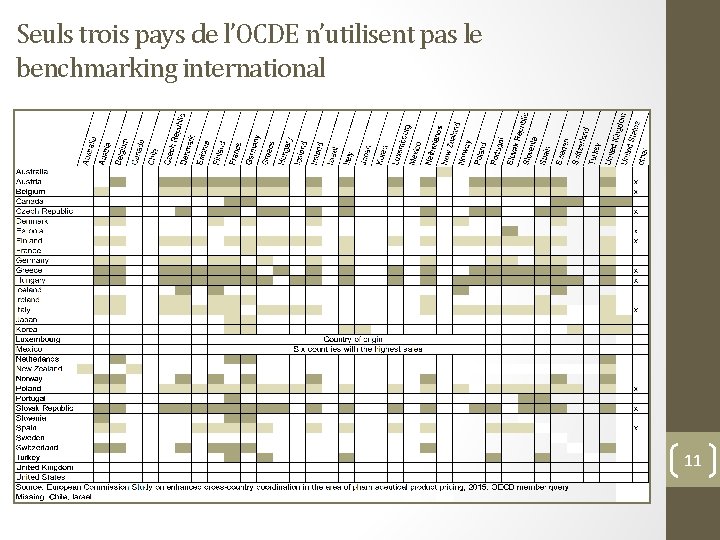
Seuls trois pays de l’OCDE n’utilisent pas le benchmarking international 11

Le référencement thérapeutique est également couramment utilisé • Reflète ce qui se passerait sur un marché concurrentiel • Principes • Évaluation de la valeur ajoutée thérapeutique par rapport aux compétiteurs • Si pas de valeur ajoutée prix ou remboursement maximum fixé au même niveau ou plus bas que le prix des comparateurs • Si valeur ajoutée Prix supérieur • Variante: « prix de référence » = Montant remboursé fixé pour un groupe de produits, mais laboratoires libres de fixer leurs prix (la différence entre prix et remboursement à la charge du consommateur) • Utilisation • E. g. Canada, France, Italie, Japon, Suisse • En général, pas de règle a priori pour le montant de la “prime”, sauf au Japon 12
Les “prix de référence” (TFR en France) s’appliquent le plus souvent à des groupes génériques Formation des groupes pour prix de références, 2011 Formation des groupes Pays Même principe actif Belgique, Rép. Tchèque, Danemark, Finlande, France, Allemagne, Hongrie, Italie, Pologne, Portugal, Espagne, Turquie Même classe pharmacologique Rép. Tchèque, Allemagne, Hongrie, Pays-Bas Même classe thérapeutique Rép. Tchèque, Allemagne, Hongrie, Pologne Ø Les médicaments sous prix de référence représentent 5% des volumes vendus en France et 75% en Allemagne Source: Dylst, Vulto, Simoens, Reference pricing systems in Europe: characteristics and consequences, Ga. BI Journal, 2012; 1(3 -4): 127 -31, and OECD estimates 13

Le principe de l’évaluation économique • 14

L’évaluation économique est de plus en plus utilisée dans les systèmes de santé Utilisée pour la première fois pour les décisions de remboursement en Australie depuis 1993 Utilisée par plus de la moitié des pays de l’OCDE, mais de différentes manières • Australie, Nouvelle-Zélande, Pays-Bas: tous les produits sont évalués pour décider du remboursement (oui/non/ avec restrictions) • Royaume-Uni: évaluation non systématique, réservée aux produits onéreux et/ou avec incertitude concernant l’efficacité, le rapport coût-efficacité et/ou impact budgétaire • France: évaluation économique des produits innovants, pour informer la négociation sur les prix 15

Les pays ne tiennent pas à révéler un seuil de coûtefficacité … et il est souvent dépassé • NICE (Angleterre) • Seuil initialement fixé un intervalle £ 20, 000 - £ 30, 000, principe de “rule of rescue” exclu (en 2008) • Position révisée en 2009 pour les traitements en fin de vie • Création du Cancer Fund en 2011 – financement sur une base individuelle des traitements onéreux rejetés par NICE • Hongrie (2 -3 x PIB/habitant), Pologne (3 x PIB/habitant), République Slovaque (18000 -26500 €), Corée (PIB/habitant) • Dans les autres pays, seuils non révélés • Les ICER acceptés diffèrent d’une classe à l’autre et sont plus élevés pour les maladies à pronostic vital engagé, les produits oncologiques, et les médicaments orphelins • Maladie de Fabry: € 351 622 - € 3 282 252 / QALY • Maladie de Pompe: € 153 405 - € 1 043 868 / QALY • Maladie de Gaucher € 43 532 - € 432 540 / QALY. • Pour certains produits, les prix dépendent plus de l’incapacité à négocier des acheteurs que d’une quelconque notion de « valeur » 16
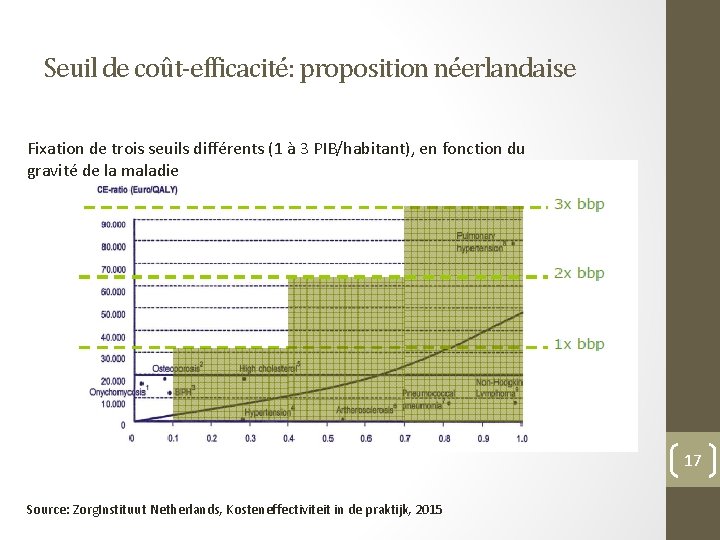
Seuil de coût-efficacité: proposition néerlandaise Fixation de trois seuils différents (1 à 3 PIB/habitant), en fonction du gravité de la maladie 17 Source: Zorg. Instituut Netherlands, Kosteneffectiviteit in de praktijk, 2015
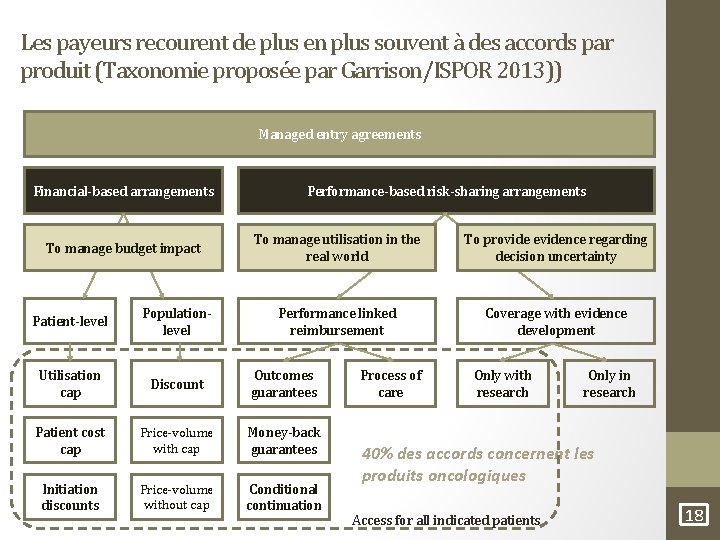
Les payeurs recourent de plus en plus souvent à des accords par produit (Taxonomie proposée par Garrison/ISPOR 2013)) Managed entry agreements Financial-based arrangements To manage budget impact Performance-based risk-sharing arrangements To manage utilisation in the real world To provide evidence regarding decision uncertainty Performance linked reimbursement Coverage with evidence development Patient-level Populationlevel Utilisation cap Discount Outcomes guarantees Patient cost cap Price-volume with cap Money-back guarantees Initiation discounts Price-volume without cap Conditional continuation Process of care Only with research Only in research 40% des accords concernent les produits oncologiques Access for all indicated patients 18
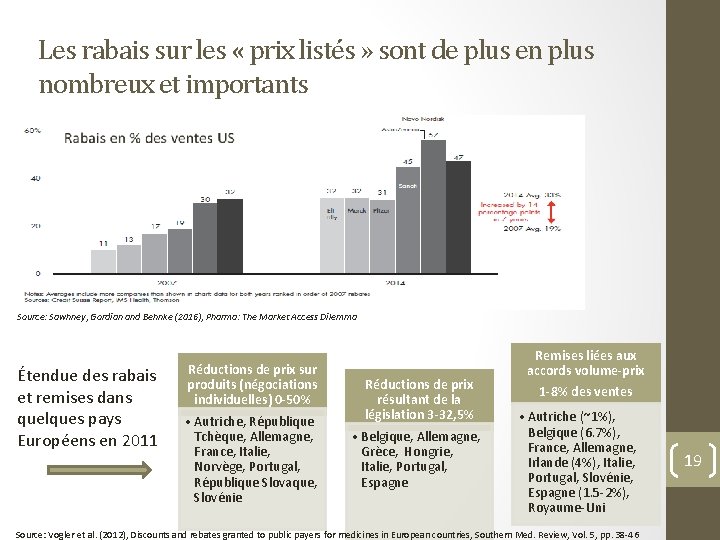
Les rabais sur les « prix listés » sont de plus en plus nombreux et importants Source: Sawhney, Gordian and Behnke (2016), Pharma: The Market Access Dilemma Étendue des rabais et remises dans quelques pays Européens en 2011 Réductions de prix sur produits (négociations individuelles) 0 -50% • Autriche, République Tchèque, Allemagne, France, Italie, Norvège, Portugal, République Slovaque, Slovénie Réductions de prix résultant de la législation 3 -32, 5% • Belgique, Allemagne, Grèce, Hongrie, Italie, Portugal, Espagne Remises liées aux accords volume-prix 1 -8% des ventes • Autriche (~1%), Belgique (6. 7%), France, Allemagne, Irlande (4%), Italie, Portugal, Slovénie, Espagne (1. 5 -2%), Royaume-Uni Source: Vogler et al. (2012), Discounts and rebates granted to public payers for medicines in European countries, Southern Med. Review, Vol. 5, pp. 38 -46 19

Où en sommes-nous avec le principe de « prix fondé sur la valeur » ? • Principe très difficile à appliquer en pratique • Quelques médicaments obtiennent des prix élevés en dépit de bénéfices thérapeutiques discutables • Reflet de “valeurs sociétales” ou déséquilibre dans le pouvoir de négociation des acheteurs et des vendeurs? • Benchmark insoutenable pour les thérapies très bénéfiques à venir • Problème de soutenabilité à long terme? • Que faire quand le produit est coût-efficace mais l’impact budgétaire trop important - (Hep C) ? • Le principe de prix basé sur la valeur ne s’applique pas aux services de santé qui restent majoritairement rémunérés en fonction des ressources engagées pour les produire (développement de paiements aux résultats) • Faut-il inventer de nouveaux modèles de détermination des prix? 20

Les défis à venir • Depuis 2010, la moitié des médicaments approuvés par la FDA sont des médicaments biologiques (+ chers), un tiers sont des médicaments orphelins • Potentiel d’économie dérivé des marchés “hors brevet”, plus limité avec les bio-similaires qu’avec les génériques. • Développement de la médecine de précision: petites populations cibles = prix élevés (oncologie) • Orientation vers des “adaptive licensing pathways” problème pour les agences d’HTA 21

Merci pour votre attention 22
- Slides: 22