Les plantes mdicinales lorigine des grands mdicaments daujourdhui







































- Slides: 61

« Les plantes médicinales à l'origine des grands médicaments d'aujourd'hui et de demain » Elisabeth SEGUIN Professeur de Pharmacognosie COBRA - UMR CNRS 6014 UFR De Médecine et de Pharmacie ________________________________________ _ 56ème journées nationales de l’Union des Professeurs de Physique et de Chimie - Rouen 28 octobre 2008

Papyrus Ebers (ca. 1600 av. J. -C. ) Traité médical rédigé pendant le règne d’Amenhotep I er

DIOSCORIDE (environ de 40 à 90 après J. C. )

DIOSCORIDE De Materia Medica (77 ap. J. C. ) Manuscrit nestorien (, (IXème) Manuscrit byzantin Manuscrit arabe (XIIIème) bibliothèque de Naples Musée de Topkapu, Istambul

Linné (1707 -1778)

Lavoisier (1743 -1794)

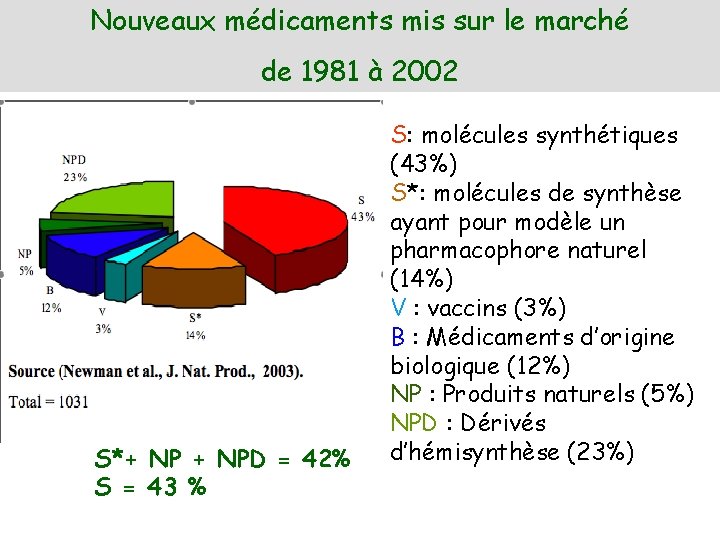
Nouveaux médicaments mis sur le marché de 1981 à 2002 S*+ NPD = 42% S = 43 % S: molécules synthétiques (43%) S*: molécules de synthèse ayant pour modèle un pharmacophore naturel (14%) V : vaccins (3%) B : Médicaments d’origine biologique (12%) NP : Produits naturels (5%) NPD : Dérivés d’hémisynthèse (23%)

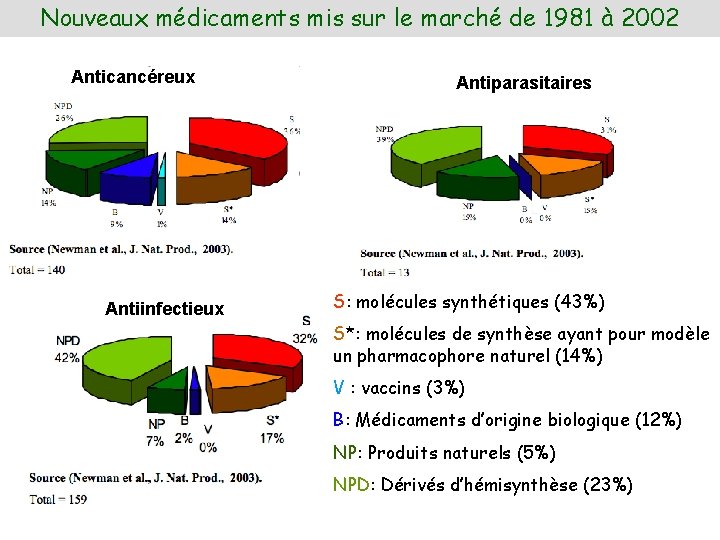
Nouveaux médicaments mis sur le marché de 1981 à 2002 Anticancéreux Antiinfectieux Antiparasitaires S: molécules synthétiques (43%) S*: molécules de synthèse ayant pour modèle un pharmacophore naturel (14%) V : vaccins (3%) B: Médicaments d’origine biologique (12%) NP: Produits naturels (5%) NPD: Dérivés d’hémisynthèse (23%)

« Les plantes médicinales à l'origine des grands médicaments d'aujourd'hui et de demain » - Médicaments d’usage traditionnel mais restant d’actualité Exemples : . morphine, . quinine - Médicaments issus d’une recherche récente dans le domaine des plantes médicinales Exemples : anticancéreux. pervenche de Madagascar. if

Le pavot source d’opium et de morphine Papaver somniferum

Déesse aux pavots, Crète (1600 -1400 av. J. -C. ) Musée d ’Héraklion

- Dioscoride emploie l’opium pour soulager les douleurs - Ingrédient de la Thériaque de Galien (médecin grec du 2ème siècle) - XVIIème siècle : principe actif du Laudanum de Sydenham (teinture d’opium safranée) Demeurera l’analgésique le plus employé jusqu’à la généralisation de l’usage du chlorhydrate de morphine

Isolement de la morphine : Sertürner (1805)

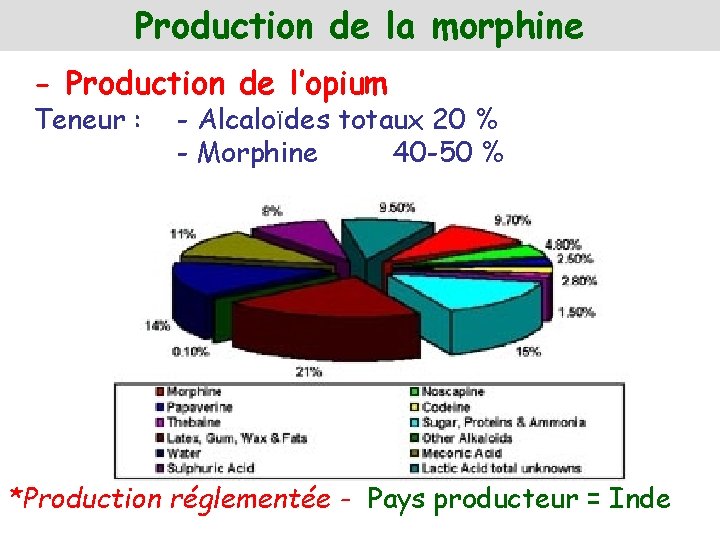
Production de la morphine - Production de l’opium Teneur : - Alcaloïdes totaux 20 % - Morphine 40 -50 % *Production réglementée - Pays producteur = Inde

Culture - Papaver somniferum var. album - climat tempéré chaud

Récolte - incision des capsules

Récolte - récolte du latex

Récolte - dessiccation du latex Production licite 1995 en Inde 50 tonnes d’équivalent morphine

Production de la morphine - Production de « paille » de pavot Teneur - Alcaloïdes totaux 1 % - Morphine 40 -50 %

Culture : - Papaver somniferum var. nigrum - climat tempéré froid Graines de pavot Pays producteurs (2005) : - Australie (51%) - Turquie (23%) - Espagne (4%) - France (21%) - 10 000 hectares Société FRANCOPIA (Champagne Ardenne, Centre, Poitou Charente) Usine d’extraction : Aramon (Gard)

Récolte - mécanisée - industrialisée Production 1995 120 tonnes d’équivalent morphine

Emplois de la morphine - En thérapeutique analgésique majeur - chlorhydrate - voies parentérale, péridurale et sous-arachnoïdienne : CHLOHYDRATE DE MORPHINE®, - voie orale soluté buvable : - sulfate MORPHINE COOPER® . - voie orale - à libération immédiate (ACTISKENAN®, SEVREDOL® ) - à libération prolongée (MOSCONTIN®, SKENAN LP®, KAPANOL LP®)

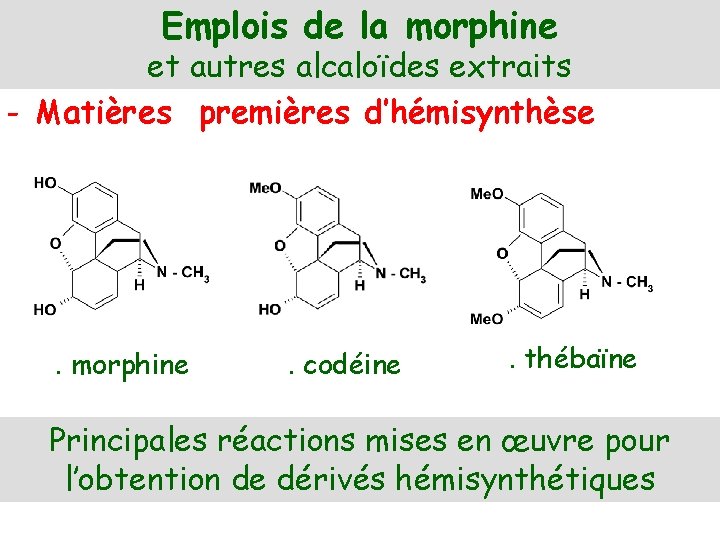
Emplois de la morphine et autres alcaloïdes extraits - Matières premières d’hémisynthèse . morphine . codéine . thébaïne Principales réactions mises en œuvre pour l’obtention de dérivés hémisynthétiques

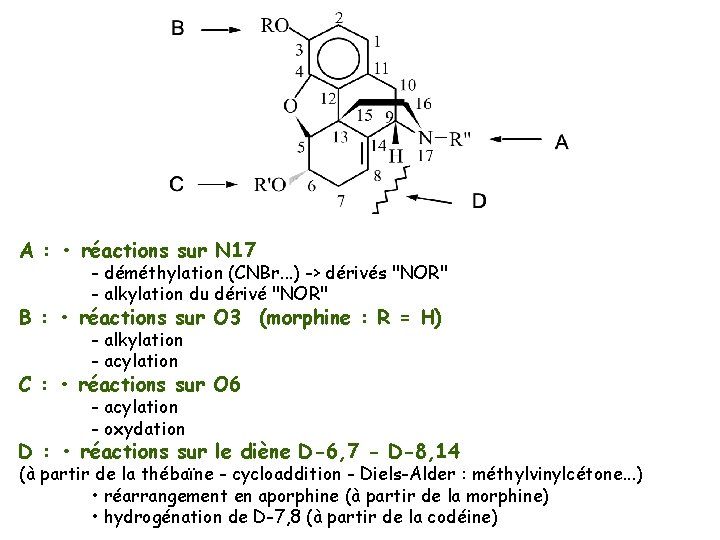
A : • réactions sur N 17 - déméthylation (CNBr. . . ) -> dérivés "NOR" - alkylation du dérivé "NOR" B : • réactions sur O 3 (morphine : R = H) - alkylation - acylation C : • réactions sur O 6 - acylation - oxydation D : • réactions sur le diène D-6, 7 - D-8, 14 (à partir de la thébaïne - cycloaddition - Diels-Alder : méthylvinylcétone. . . ) • réarrangement en aporphine (à partir de la morphine) • hydrogénation de D-7, 8 (à partir de la codéine)

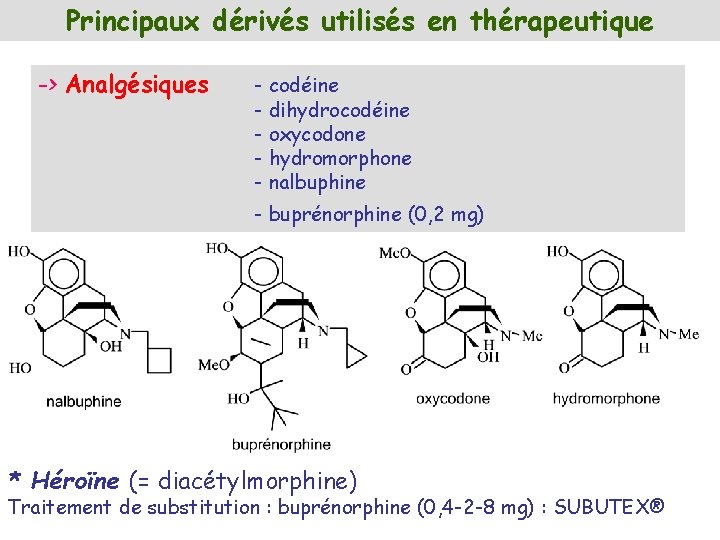
Principaux dérivés utilisés en thérapeutique -> Analgésiques - codéine - dihydrocodéine - oxycodone - hydromorphone - nalbuphine - buprénorphine (0, 2 mg) * Héroïne (= diacétylmorphine) Traitement de substitution : buprénorphine (0, 4 -2 -8 mg) : SUBUTEX®

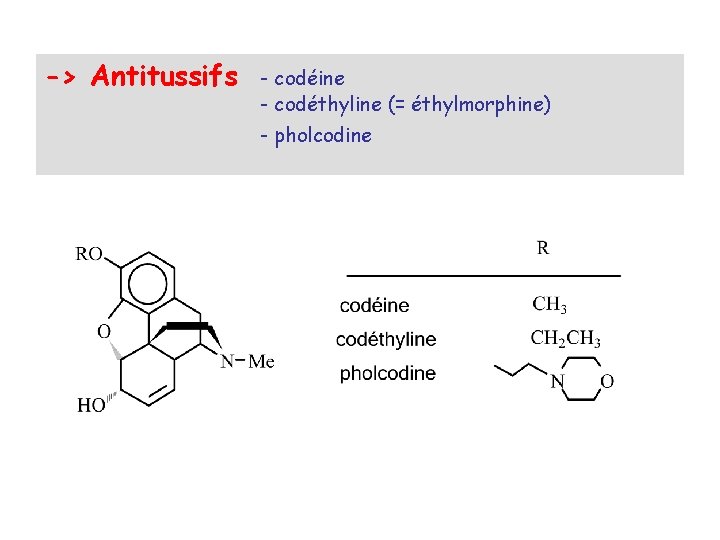
-> Antitussifs - codéine - codéthyline (= éthylmorphine) - pholcodine

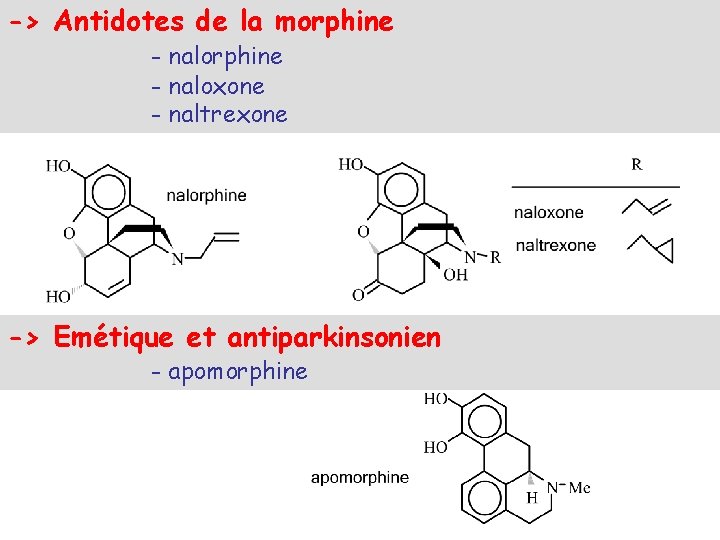
-> Antidotes de la morphine - naloxone - naltrexone -> Emétique et antiparkinsonien - apomorphine

Les quinas sources de quinine Début XVIIème - Introduit en Europe par les Jésuites pour traiter les fièvres 1663 - Reconnaissance des propriétés de « l’arbre à fièvre de la région de Loxa » ( poudre des jésuites, poudre de la Comtesse…) 1742 - Linné crée le genre Cinchona (échantillons rapportés par l’expédition de La Condamine)

Isolement de la quinine par Pelletier et Caventou (1817 -1821)

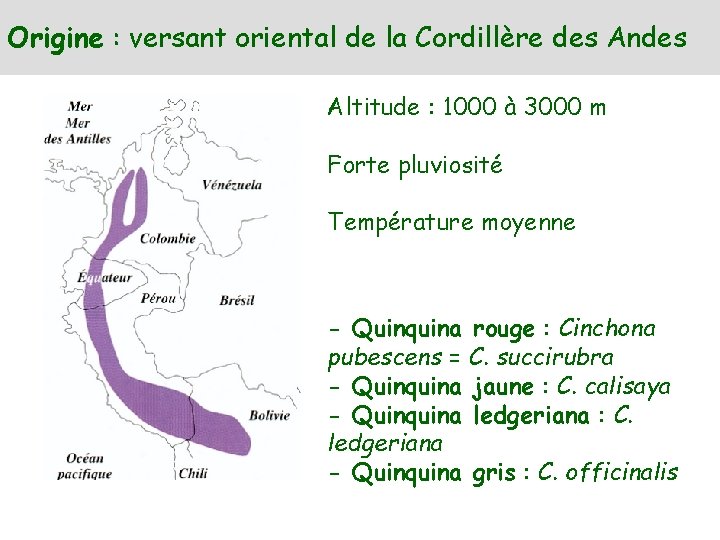
Origine : versant oriental de la Cordillère des Andes Altitude : 1000 à 3000 m Forte pluviosité Température moyenne - Quinquina rouge : Cinchona pubescens = C. succirubra - Quinquina jaune : C. calisaya - Quinquina ledgeriana : C. ledgeriana - Quinquina gris : C. officinalis

Quinquina rouge Cinchona pubescens Vahl. ( = Cinchona succirubra Pavon) Quinquina jaune (Cinchona ledgeriana Moens. )

Suron destiné au transport des écorces de quina ( ca. 1840) (Musée de Matière Médicale, Université Paris 5)

Industrialisation de l’extraction de la quinine Atelier de production de quinine (vers 1900) Échantillons (1884) : Musée de Matière Médicale, Université Paris 5

Préparation de stocks de quinine Guerre du Pacifique - 1943

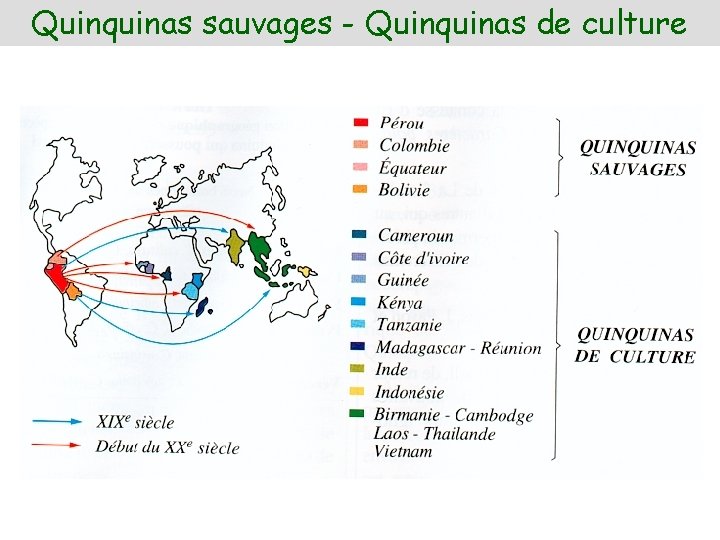
Quinquinas sauvages - Quinquinas de culture

Emplois des quinas en thérapeutique Extraction de la quinine (Q. jaune, Q. ledgeriana, hybrides)

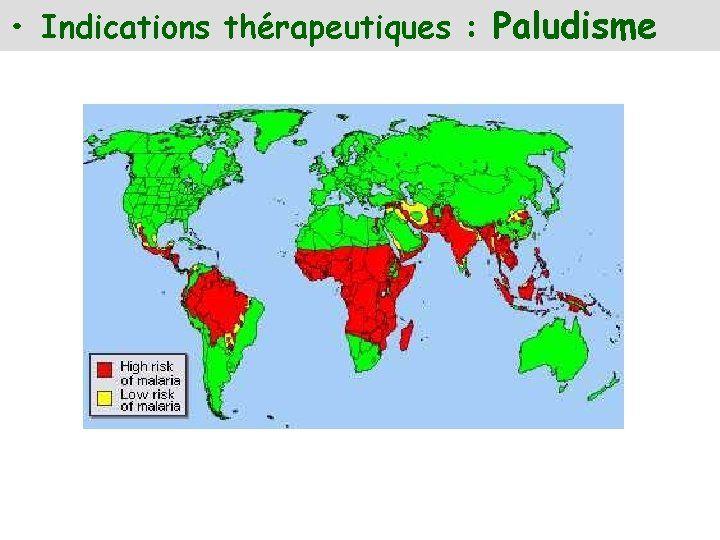
• Indications thérapeutiques : Paludisme

• Indications thérapeutiques Antipaludique (chlorhydrate : QUININE LAFRAN®, QUINIMAX®; formiate basique : QUINOFORME® ). Traitement curatif - accès pernicieux de paludisme - paludismes résistants aux 4 -aminoquinoléines de synthèse . Modèle de base molécules à activité antipaludique de synthèse (RSA)

Emplois non pharmaceutiques des quinas • Liquoristerie et préparation de boissons « toniques » Quinquina gris : C. officinalis

Emplois non pharmaceutiques des quinas • Cosmétologie

Médicaments issus d’une recherche récente dans le domaine des plantes médicinales Sources récentes de médicaments anticancéreux . pervenche de Madagascar . if

Pervenche de Madagascar Catharanthus roseus G. Don. Famille des Apocynaceae

Historique • Médecine traditionnelle malgache Usage empirique comme anorexigène et antidiabétique • 1957 : recherche de ces activités par des chercheurs canadiens Mise en évidence d’une activité leucopéniante • 1960 : criblage par les laboratoires Eli Lilly

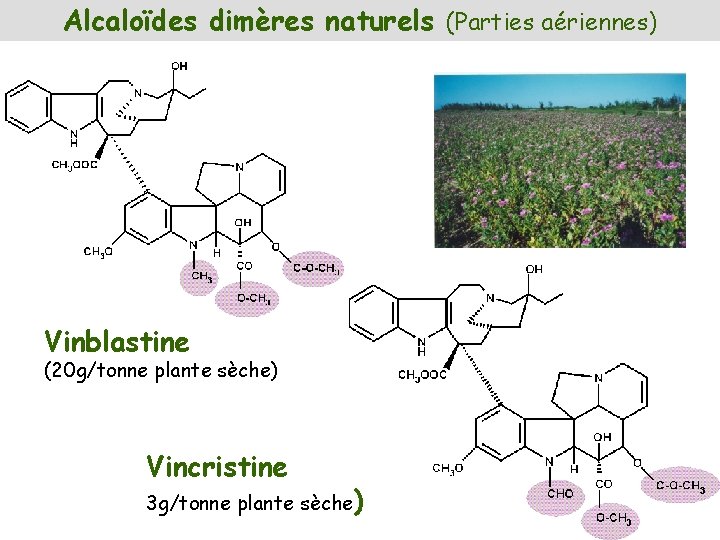
Alcaloïdes dimères naturels (Parties aériennes) Vinblastine (20 g/tonne plante sèche) Vincristine 3 g/tonne plante sèche)

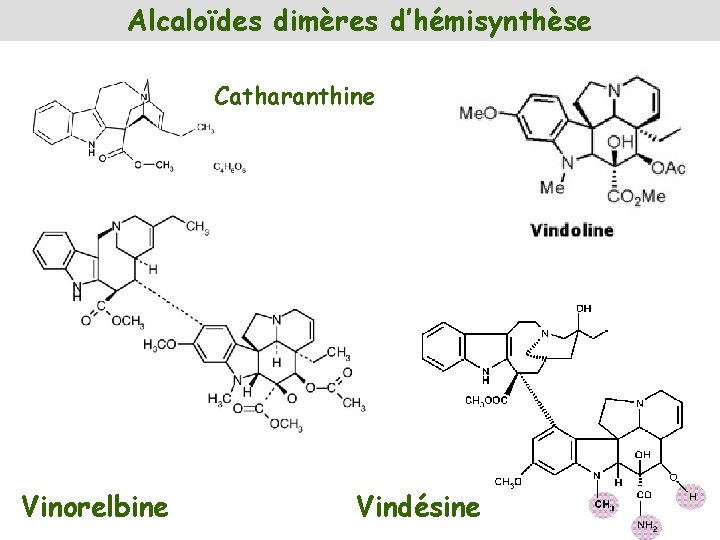
Alcaloïdes dimères d’hémisynthèse Catharanthine Vinorelbine Vindésine

Alcaloïdes de la pervenche • • Vinblastine Vincristine Vindésine Vinorelbine Pierre Potier (1934 -2006) Velbé® Oncovin® Eldisine® Navelbine® 1974 1983 1982 1989

Indications thérapeutiques • Vinblastine (Velbe®) • Vincristine(Oncovin®) • Vindésine (Eldisine®) leucémies, lymphomes et certaines tumeurs solides • Vinorelbine (Navelbine®) cancer bronchique non à petites cellules, cancer du sein

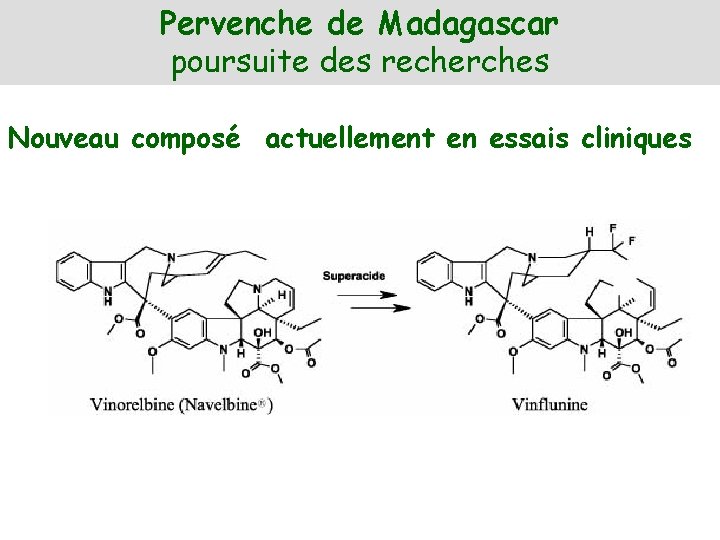
Pervenche de Madagascar poursuite des recherches Nouveau composé actuellement en essais cliniques

If du Pacifique - If d ’Europe

Historique L’if, une toxicité connue depuis toujours 1856 : découverte de la taxine 1960 : début des recherches sur les propriétés anti-tumorales de l’if au NCI isolement du Paclitaxel de l’écorce de Taxus brevifolia 1971 : Wall et Wani : isolement et structure 1979 : S. Horwitz : mécanisme d’action original 1983 : premiers essais cliniques

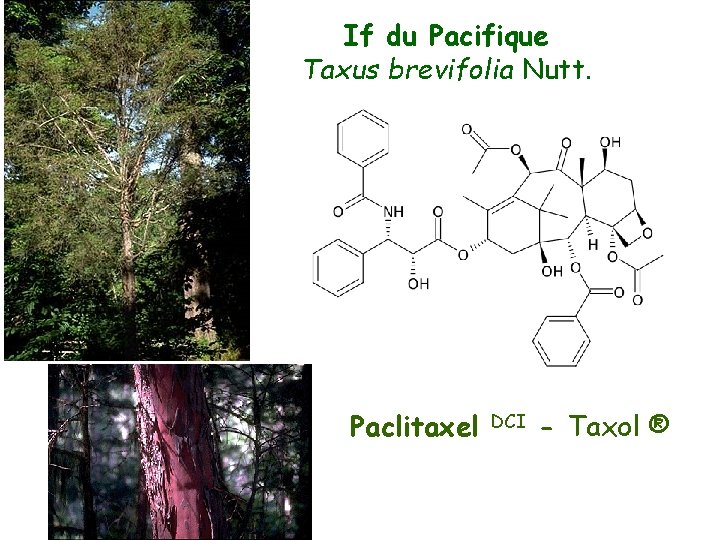
If du Pacifique Taxus brevifolia Nutt. Paclitaxel DCI - Taxol ®

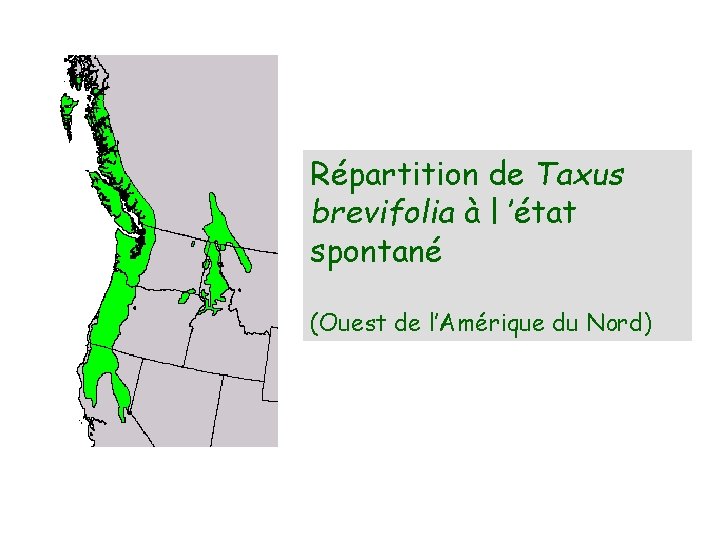
Répartition de Taxus brevifolia à l ’état spontané (Ouest de l’Amérique du Nord)

1960 : isolement du Paclitaxel de l’écorce de Taxus brevifolia 1983 : Premiers essais cliniques * Problème pour la commercialisation Ecorces = Source non renouvelable (1 g pour 10 kg d’écorces sèches - 2500 arbres pour 1 kg de paclitaxel) Disparition rapide de la source Problème écologique

If d ’Europe Taxus baccata L. Travaux sur les aiguilles

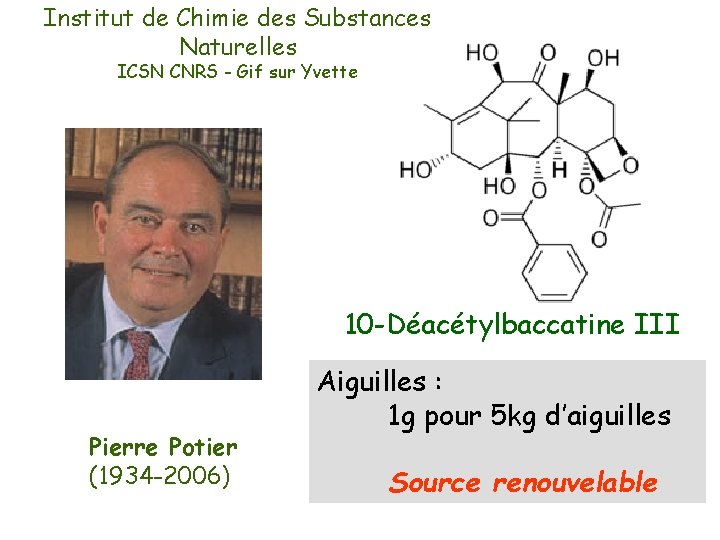
Institut de Chimie des Substances Naturelles ICSN CNRS - Gif sur Yvette 10 -Déacétylbaccatine III Pierre Potier (1934 -2006) Aiguilles : 1 g pour 5 kg d’aiguilles Source renouvelable

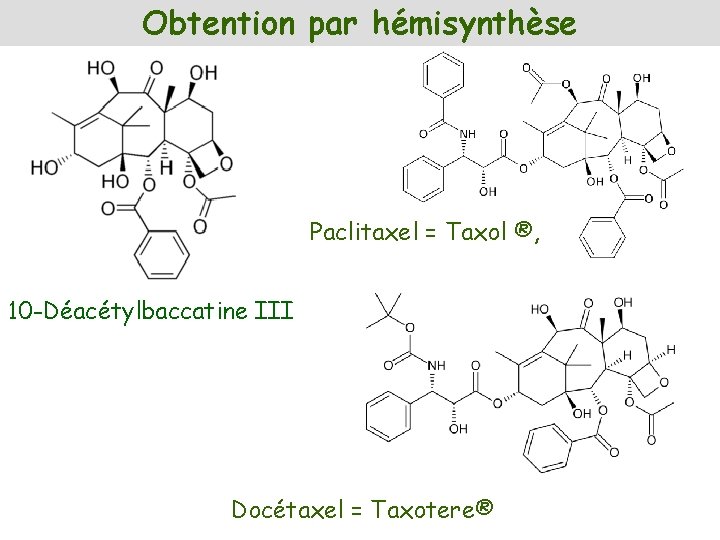
Obtention par hémisynthèse Paclitaxel = Taxol ®, 10 -Déacétylbaccatine III Docétaxel = Taxotere®

Indications thérapeutiques Paclitaxel docétaxel Taxol® Taxotère® 1993 1996 Cancer de l’ovaire Cancer du sein Cancer du poumon non à petites cellules…

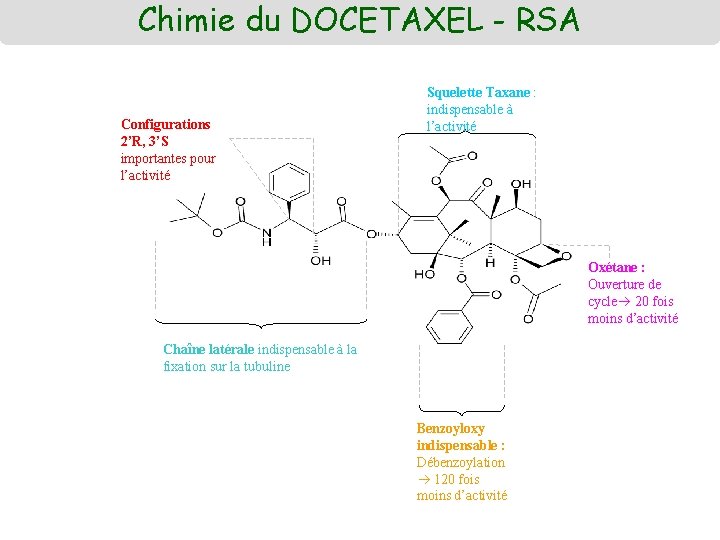
Chimie du DOCETAXEL - RSA Configurations 2’R, 3’S importantes pour l’activité Squelette Taxane : indispensable à l’activité Oxétane : Ouverture de cycle 20 fois moins d’activité Chaîne latérale indispensable à la fixation sur la tubuline Benzoyloxy indispensable : Débenzoylation 120 fois moins d’activité

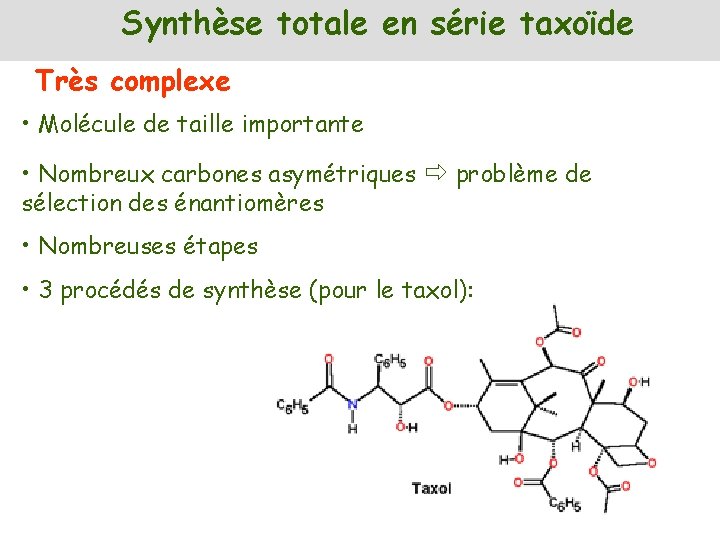
Synthèse totale en série taxoïde Très complexe • Molécule de taille importante • Nombreux carbones asymétriques problème de sélection des énantiomères • Nombreuses étapes • 3 procédés de synthèse (pour le taxol):

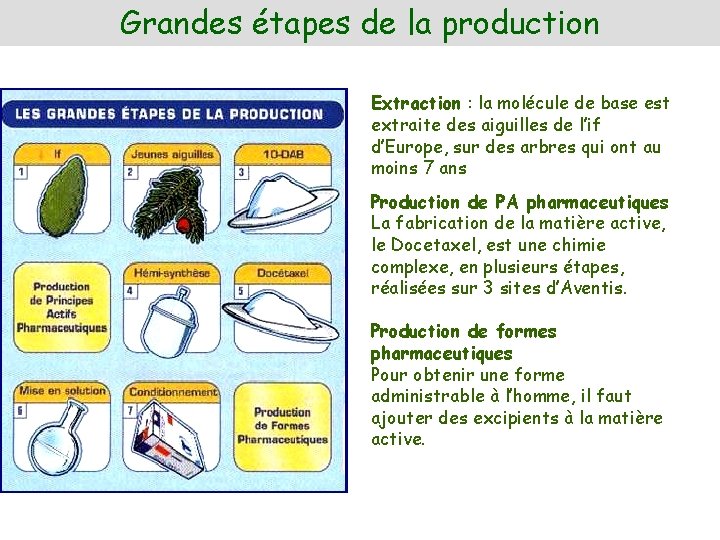
Grandes étapes de la production Extraction : la molécule de base est extraite des aiguilles de l’if d’Europe, sur des arbres qui ont au moins 7 ans Production de PA pharmaceutiques La fabrication de la matière active, le Docetaxel, est une chimie complexe, en plusieurs étapes, réalisées sur 3 sites d’Aventis. Production de formes pharmaceutiques Pour obtenir une forme administrable à l’homme, il faut ajouter des excipients à la matière active.

En conclusion… Intérêt de poursuivre des recherches sur les produits naturels dans le domaine du médicament - 250 000 espèces de végétaux supérieurs 10 % étudiées d’un point de vue phytochimique - moins de 10 % des bactéries et de 5 % des champignons étudiés - 1 000 d’insectes : moins de 1 % d’espèces étudiées - organismes marins encore très peu étudiés…