Les missions des CRPV outils bases de donnes

Les missions des CRPV, outils, bases de données, contenu et accessibilité

1. Missions et organisation de la Pharmacovigilance 2. Historique, présentation générale du CRPV de Lyon 3. Les outils à disposition 4. 2 ü La notification spontanée et les bases de données de PV ü Autres outils épidémiologiques Du signalement à la prise de mesure

Missions (Loi de décembre 2011 - Directive européenne - 8/11/2012) • • La pharmacovigilance a pour objet la surveillance, l’évaluation, la prévention et la gestion du risque d’effets indésirables des médicaments Elle comprend : • • • Définition de l’EI • 3 le signalement des effets indésirables et le recueil des informations les concernant ; l’enregistrement, l’évaluation, l’exploitation de ces informations dans un but de PRÉVENTION ; la réalisation d'études ou de travaux concernant la SECURITÉ D'EMPLOI des médicaments ; la mise en place d’actions : modification(s) des informations destinées aux professionnels de santé et aux patients, suspension, retrait de l’AMM. . . « Tout effet indésirable présumé, quelque soit les conditions d’utilisation du médicament: usage normal, mésusage, abus, erreur médicamenteuse, surdosage, exposition professionnelle»

Organisation française � � 4 Un système centralisé / décentralisé, officialisé depuis 1976 Deux niveaux d’organisation Échelon régional avec un réseau de CRPV � Favoriser les contacts de proximité � Favoriser une PV pour les patients Échelon national � Échanges d’information / Générer rapidement les signaux � Expertise / Enquête nationale / Décision � Communication Une source d’information principale � La notification spontanée � La déclaration obligatoire
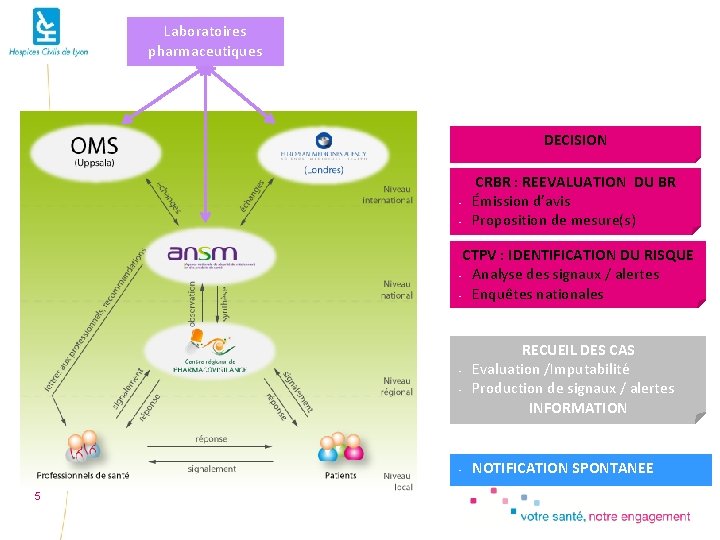
Laboratoires pharmaceutiques DECISION - CRBR : REEVALUATION DU BR Émission d’avis Proposition de mesure(s) CTPV : IDENTIFICATION DU RISQUE - Analyse des signaux / alertes - Enquêtes nationales - - 5 RECUEIL DES CAS Evaluation /Imputabilité Production de signaux / alertes INFORMATION NOTIFICATION SPONTANEE

Historique du service 6 • 1973 : Naissance du Centre de Pharmacovigilance Hospitalière • 1979 : Création formelle du CRPV en tant que service indépendant (agrément le 24 mai 1996) • 1988 : Fusion avec le Centre Antipoison • 1994 : Création du CEIP de Lyon au sein du service • 2007 : Intégration au sein du PAM Santé, Recherche, Risque et Vigilances • 2016 : fusion avec le service de pharmacologie : création du Service Hospitalo-Universitaire de Pharmaco-Toxicologie

Zone de compétence 7 • Couvre 6 des 8 départements de l’ancienne région Rhône Alpes • Population : 4, 38 millions • Nombre d’établissements de soins publics ou privés : 242 • Nombre de médecins libéraux: 8652 • Le CHU de Lyon : • 6 GH • 2ème pôle hospitalier de France • Plus de 320 000 séjours patients
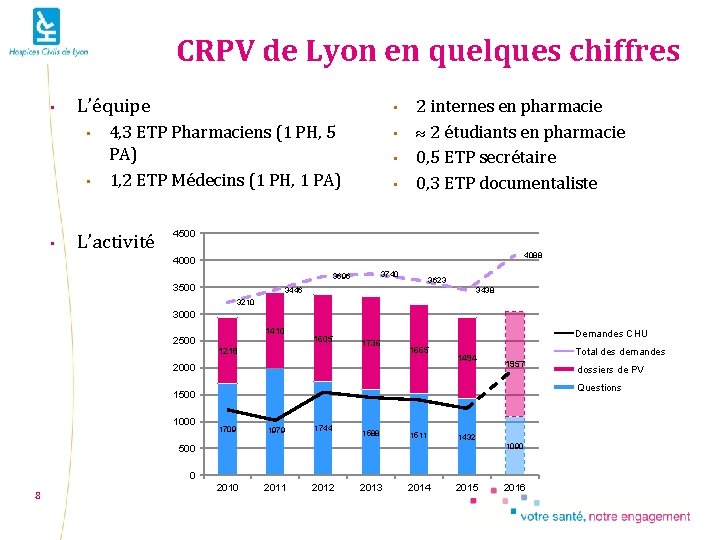
CRPV de Lyon en quelques chiffres • L’équipe • • 4, 3 ETP Pharmaciens (1 PH, 5 PA) 1, 2 ETP Médecins (1 PH, 1 PA) L’activité • • • 2 internes en pharmacie 2 étudiants en pharmacie 0, 5 ETP secrétaire 0, 3 ETP documentaliste 4500 4088 4000 3740 3696 3500 3623 3446 3438 3210 3000 2500 1410 1605 1218 1736 Demandes CHU 1665 2000 1494 Total des demandes 1957 Questions 1500 1000 1709 1979 1744 1588 1511 1432 1090 500 0 8 dossiers de PV 2010 2011 2012 2013 2014 2015 2016

Notification spontanée et bases de données Définition : Signalement par un professionnel de santé, un patient ou une association de patient d’au minimum 4 éléments : • un notificateur ou déclarant identifiable, • un patient identifiable, • la dénomination du (des) médicament(s) ou produit(s) suspect(s) • la mention d’un ou des effets suspects. • Destination : Documentées et analysées, saisies dans une base de données de pharmacovigilance (format spécifique encadré par des normes et réglementations internationales , délais réglementaires de transmission) • 9

Base nationale ANSM Chronologie Dénomination ü BNPV : Base (Banque) Nationale de Pharmacovigilance ü ANPV : Application Nationale de Pharmacovigilance Historique ü Créée en 1985 au sein des Hospices Civils de Lyon (SOS-V 6) ü Transférée sur le serveur de l'Agence du médicament en 1993 ü Redéveloppement en 1995 du système utilisé jusqu'en juin 2007 ü Mise à jour en décembre 1999 (bug an 2000) ü Pas de modification majeure entre 1995 et 2007 ü Redéveloppement initié en 2004 ü Nouvelle base mise en production en juin 2007 ü Nouvelle version sera mise en production en janvier 2017 10

Base nationale ANSM Notification Les CRPV saisissent tous les ans plus de 40000 nouvelles observations d'effets graves ou non graves ü Tendance actuelle : 60% d'effets graves Chaque année, les industriels notifient à l'ANSM plus de 20000 observations d'effets graves survenus sur le territoire français Notification des patients ü Possible depuis juin 2011 ü Volume actuellement faible ( 5%) Contenu actuel : environ 640000 observations issues des CRPV 11

Autres bases de données 12 • Bases nationales ü Lareb (Pays Bas) ü Med. Effet (Canada) ü FDA : AERS - VAERS • Bases internationales ü EMA : Eudra. Vigilance ü OMS (Uppsala Monitoring Centre) : Vigilyze

Accessibilité • • • 13 ANPV: • Pour les CRPV : • module de requête disponible (pas SMQ) avec fonctionnalités d’extraction limitées • Possibilité de faire une demande à l’ANSM • Hors CRPV : Professionnel ou non, possibilité de demande d’extraction à l’ANSM (loi CADA). Format de sortie peu exploitable. Eudravigilance (EMA): • Pour l’ANSM : module de requête spécifique (accès aux CIOMS) • Grand public : en ligne http: //www. adrreports. eu/fr/index. html joli mais scientifiquement peu exploitable Vigilyze (OMS) : • Pour les CRPV/ANSM : module de requête spécifique • Autres : en ligne http: //www. vigiaccess. org/ scientifiquement peu exploitable

Autres outils 14 • Epidémiologiques • PMSI (CHU) au-delà pas d’accès • EGB (formation prévue), accès éventuel via ANSM • SNIIRAM accès éventuel via ANSM • Autres bases de données • Biblio : Superdoc • Grossesse : Terappel, Remera

Expertise sur médicaments et grossesse • Questions grossesse = 20 à 25 % des demandes de renseignements • Évaluation individuelle du risque médicamenteux : exposition pendant la grossesse ou souhait de prescription ü ü • Recueil initial d’informations + suivi prospectif de chaque grossesse ü ü ü 15 Propositions de prise en charge, surveillance grossesse et nouveau-né Réponse individualisée, courrier systématique Saisie BNPV : cas de malformations et effets indésirables néonataux Saisie dans la base Terappel Finalité : inclusion dans des études d’évaluation du risque des médicaments pour le fœtus ou le nouveau-né

Grossesse : la base de données Terappel ü ü ü 21 Novembre 2014 16 Terappel : base de données dédiée à la gestion des suivis des grossesses, développée à Lyon en 1984 Actuellement : • Réseau Terappel = 19 CRPV • Plus de 30 000 grossesses suivies prospectivement • 96 % des expositions = médicaments • Version web en cours de développement Terappel = source de données pour études prospectives • CRPV de Lyon : coordonnateur ou participant (2 -3 études /an) • Études nationales ou internationales : réseaux Terappel, ENTIS, OTIS, REMERA

Qu’est ce qu’un signalement ? 17 • Une notification sur le formulaire dédié • Une demande d’avis • Un compte rendu d’hospitalisation/de consultation • Une plainte…
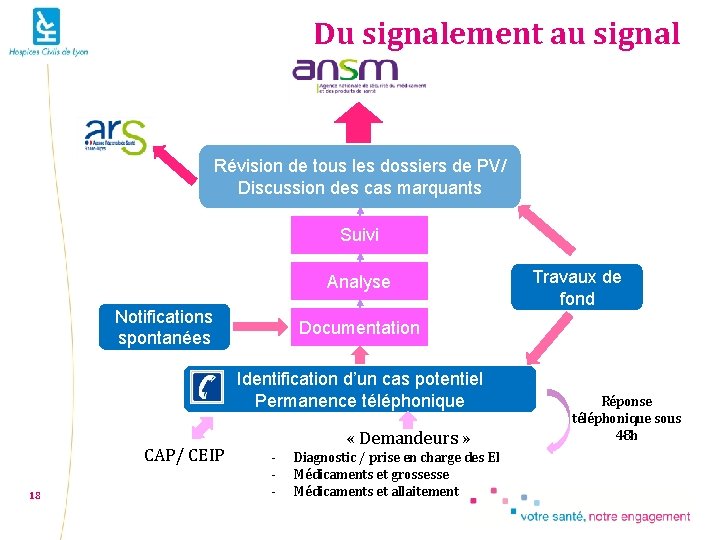
Du signalement au signal Révision de tous les dossiers de PV/ Discussion des cas marquants Suivi Analyse Notifications spontanées Documentation Identification d’un cas potentiel Permanence téléphonique CAP/ CEIP 18 Travaux de fond - « Demandeurs » Diagnostic / prise en charge des EI Médicaments et grossesse Médicaments et allaitement Réponse téléphonique sous 48 h
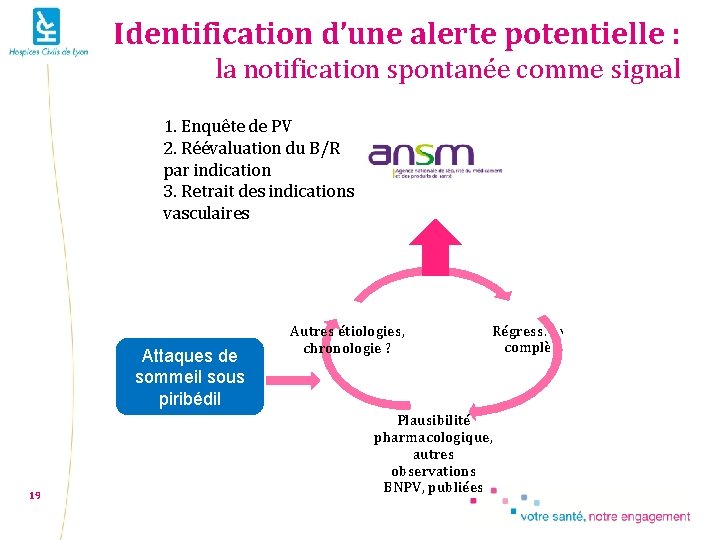
Identification d’une alerte potentielle : la notification spontanée comme signal 1. Enquête de PV 2. Réévaluation du B/R par indication 3. Retrait des indications vasculaires Attaques de sommeil sous piribédil 19 Autres étiologies, chronologie ? Régression complète Plausibilité pharmacologique, autres observations BNPV, publiées

Identification d’une alerte potentielle : Les questions et suivis… Cas marquants Analyse des données Suivi de la littérature Agammaglobulinémie néonatale et entérocolite nécrosante Permanence téléphonique « Hotline de PV » Question : Avis sur les risques d’une chimiothérapie type R-CHOP chez la femme enceinte 20 Réponse téléphonique sous 48 h

Identification d’une alerte potentielle : Les travaux de fond 1. Signal Européen 2. Modification des RCP de 5 ITK Cas marquants Identification de cas de réactivation virale VHB Analyse des données de la littérature, problématique peu abordée Permanence téléphonique « Hotline de PV » 21 Questions récurrentes sur l’interprétation et la prise en charge des anomalies hépatiques sous ITK Thèse sur les atteintes hépatiques sous ITK à partir de la BNPV
Identification d’une alerte potentielle : Gestion commune des demandes Enquête de PV Ampleur du problème ? Interrogation CAP, BNPV, Infovac Peu de données de prise en charge Injection de n fois la dose par des médecins inexpérimentés Permanence téléphonique « Hotline de PV » 22 Signalement via le CAP de plusieurs cas d’erreur médicamenteuse concernant le BCG SSI

Autres missions du CRPV : Avis pharmacologique Aide à la prise en charge du patient Participation au diagnostic d’un EI Intérêt d’un bilan complémentaire Aide à la décision thérapeutique Chercher un EI caché derrière une question Identification du médicament responsable 23

Autres missions du CRPV : Information sur le médicament, formation • Evaluation des risques ü ü • • Information générales sur le médicament Formation • 24 Prescription sur des terrains particuliers Interaction médicamenteuse Avis sur une contre-indication Chez une femme enceinte ou qui allaite • Participation à la formation initiale (médecins, pharmaciens…) Organisation du DU SMPV

Contributions à l’expertise nationale • Participation constante aux GT et commissions • Identification et évaluation des signaux contribuant à l’amélioration de la sécurité des patients • • • 25 Méthotrexate/ erreurs médicamenteuses Bromocriptine/ inhibition de la lactation Allopurinol /toxidermies sévères Buflomédil / retrait du médicament Implication importante lors des crises sanitaires: • Suivi national du Médiator® • Mise à disposition de la base de données « pilules » • Etudes grossesse oseltamivir pendant la grippe H 1 N 1
- Slides: 25