Les mcanismes de rsistance chez les bactries Gram

Les mécanismes de résistance chez les bactéries à Gram négatif Jacques Croizé MCU-PH UFR Médecine - CHU - Grenoble DU Antibiologie 17 janvier 2007

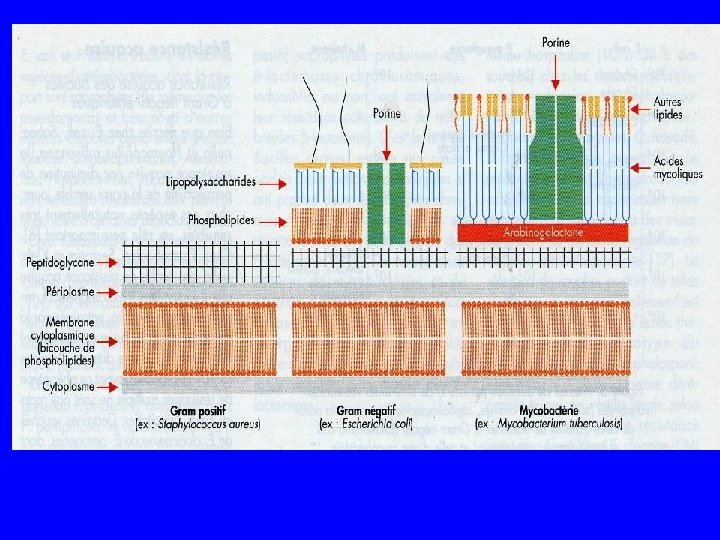
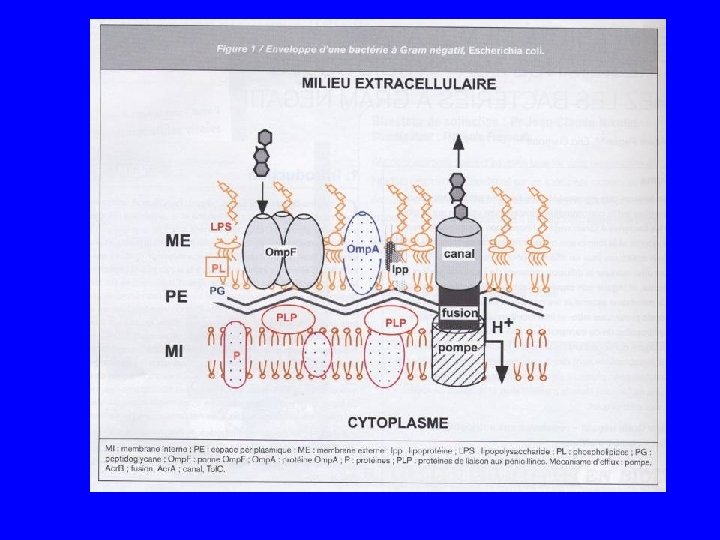
Structure d’une bactérie

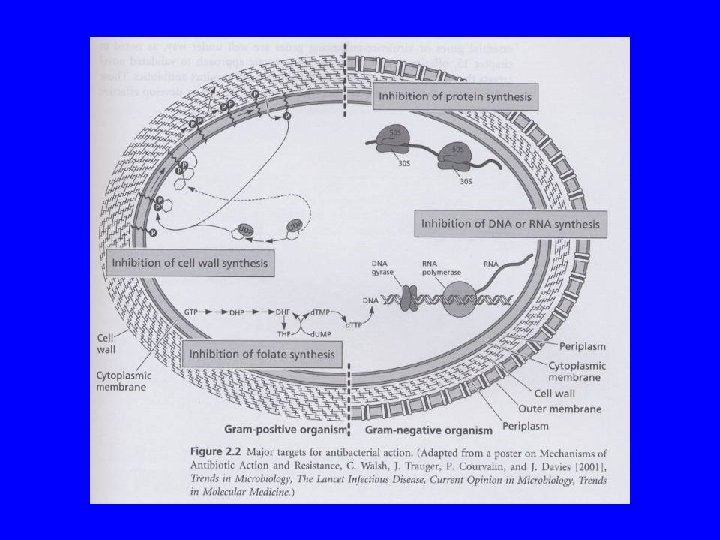
Mode d’action des antibiotiques

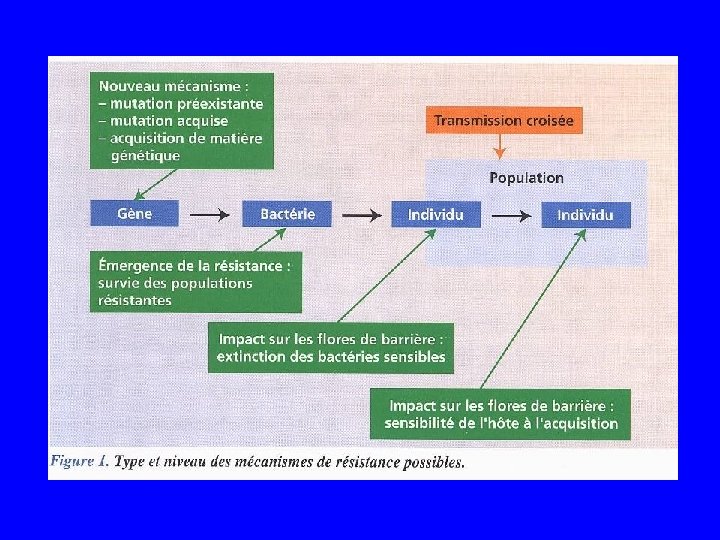
Mécanismes de résistance

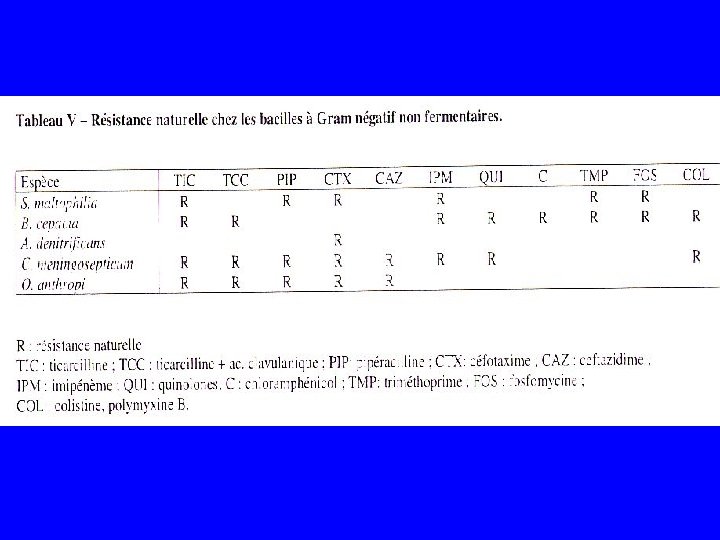
Résistance naturelle


Mécanismes biochimiques de résistance • Inactivation ou modification de l’antibiotique (B lactamines et aminosides) • Altération de la cible (macrolides) • Accumulation diminuée – Diminution de la perméabilité – Efflux augmenté • Souvent mécanismes complexes , mixtes

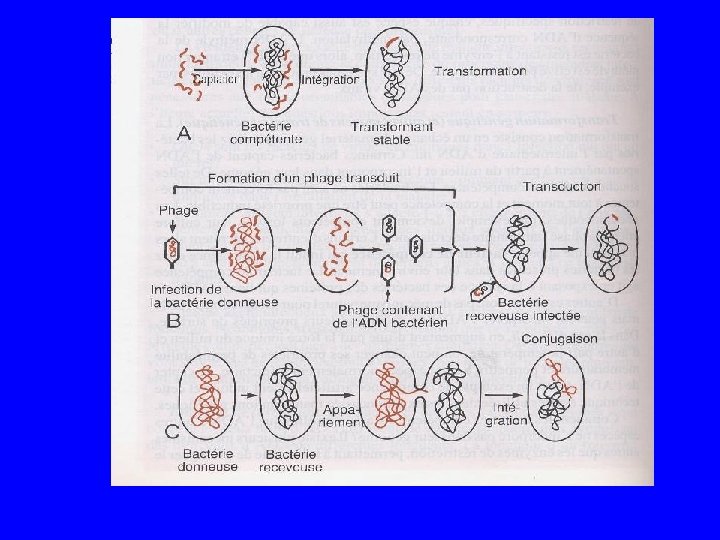
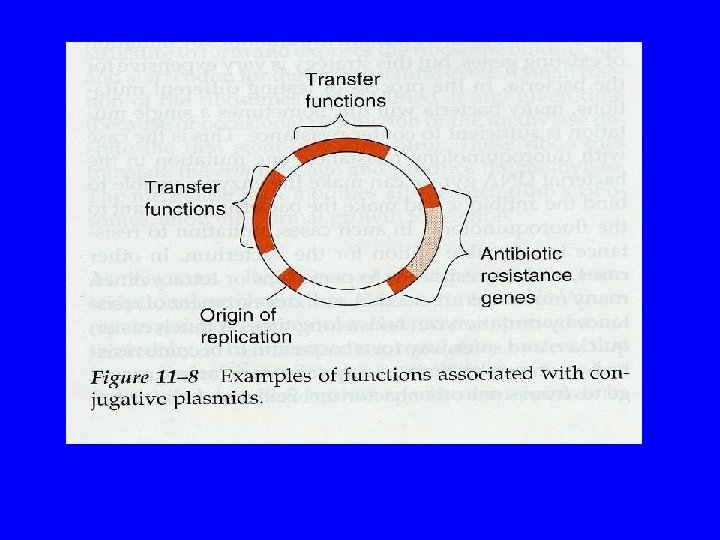
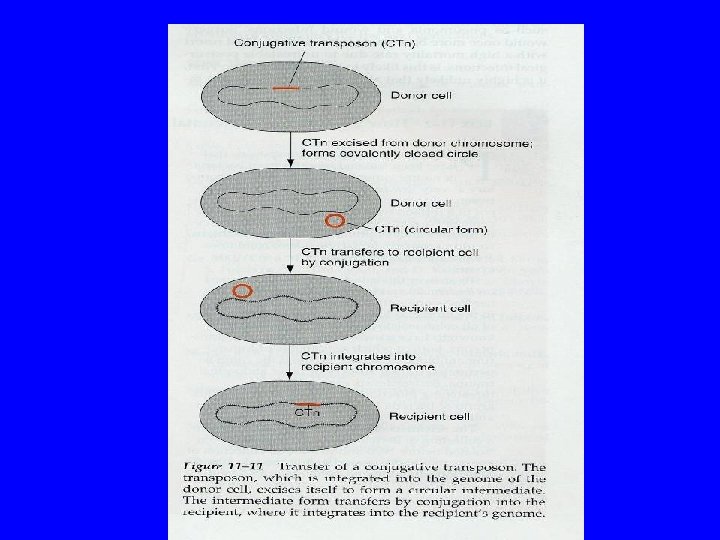
Mécanismes génétiques de résistance • Survenue de mutations dans le génome bactérien, soit dans le chromosome (transmission verticale) soit dans les éléments mobiles (plasmide ou transposon) (transmission verticale ou horizontale) • Acquisition d’ADN étranger provenant d’autres bactéries (tranposon, plasmide, intégron)

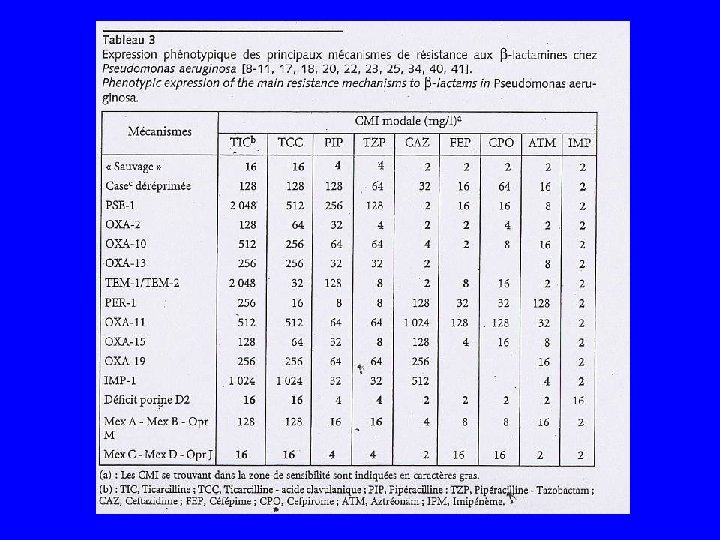
Les b lactamases

Les Béta-lactamases • Emergence continuelle de nouvelles enzymes chez entérobactéries, P. aeruginosa et Acinetobacter • Méthodes d’analyse génétique avec l’amplification génique et le séquençage ont augmenté le nombre rendant le phénomène complexe • Depuis 1960 -70, quatre classes (Ambler) – A, C, D sont des enzymes à sérine active – B sont des métallo-béta-lactamases (MBL) dont l’activité à besoin de Zn ++ pour s’exprimer

Les Béta-lactamases • Classe A : touche péni A puis C 3 G – 23 chromosomiques (départ TEM) – Plus de 120 dérivés des TEM et 50 dérivées de SHV plasmidiques dont les BLSE comprenant les céfotaximases (CTX-M) l’amplification génique et le séquençage ont augmenté le nombre • Classe B : touche C 3 G et imipénème (aztréonam sensible) – MBL chromosomiques chez les BGN oxydatifs – MBL plasmidiques chez Pyo (VIM), Acinetobacter

Les Béta-lactamases • Classe C (C 1 G puis autres) – Enzymes naturelles (Case ou Amp. C) – Hyperproduction (BLSE et Case) résistances aux « C 4 G » – Case plasmidique C 3 G touchées mais pas les C 4 G • Classe D pénicillinase peu sensible aux inhibiteurs – Oxacillinase: Surtout chez pseudomonas puis entérobactéries



Résistance plasmidique aux fluoroquinolones • Jusqu’en 1994, seule résistance par mutation : sur ADN gyrase, Topoisomérase IV, génes de régulation des systèmes d’influx (porines) ou de d’efflux • En 1994, description du gène qnr chez K. pneumoniae, transférable, sur des plasmides ou des intégrons associées souvent à des BLSE ou des cases plasmidiques • Niveau de résistance bas : Nal 32, oflo 1, cipro 0, 25 • Fréquence faible en France (étude multicentrique : 22 souches (22/487 BLSE) alors aucune souche sur les 690 R aux quinolones mais BLSE -

Mécanismes d’efflux actif et résistance par efflux actif

Système d’efflux • Définition : ce sont des mécanismes de transport membranaire universellement répandus chez des organismes vivants; ils ont un rôle clé dans la physiologie bactérienne • Rôle : préserver l’équilibre physico-chimique du milieu intracellulaire en s’opposant à l’accumulation de substances naturelles ou synthétiques toxiques : transport de substances nutritives et export de substances toxiques. • Différenciation des pompes à efflux par : – – Spécificité ou non des molécules exportées Structure : une à trois protéines Type d’énergie nécessaire : ATP ou force proton-motrice Mode expression : inductible ou constitutif

Structure des systèmes d’efflux actif • Protéine localisée dans l’épaisseur de la membrane cytoplasmique assurant la reconnaissance, le fixation et le transport de substrats proches par leur structure • La pompe comporte 4, 12 ou 14 segments peptidiques hydrophobes transmembranaires reliés entre eux par des boucles hydrophiles extramembranaires. La comparaison des séquences en acides aminés à permis de les en cinq grandes familles. • Elles sont des substrats spécifiques ou sont à spectre large (multidrug : MD) • Les pompes MD sont conservées et sont codées par le chromosome; les pompes spécifiques sont codées par des plasmides (Tn ou intégron)

Rôle des systèmes d’efflux actif dans la résistance aux antibiotiques ou aux biocides • Pompe localisée dans la membrane cytoplasmique va empêcher l’antibiotique ou le biocide d’atteindre sa cible en effectuant son efflux actif hors de la bactérie • Les antibiotiques qui ne pourront atteindre la cible intracytoplasmique seront plus touchés que ceux agissant sur des cibles à la surface de la bactérie (B lactamines, glyco et lipopeptides sont moins touchés)

Les cinq grandes familles des systèmes d’efflux actif • MFS ou MF: major facilitator superfamily – avec 12 ou 14 domaines transmembranaires • SMR : small multidrugresistance – avec 4 domaines transmembranaires • MATE : multidrug and toxic exclusion
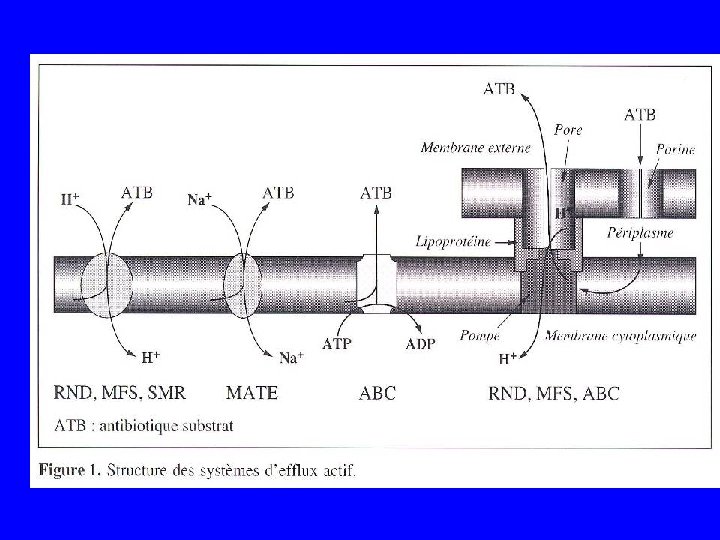

Les systèmes d’efflux actif chez les Gram négatif • Souvent de types RND • Codés par gènes chromosomiques ++ avec systèmes régulateurs complexes permettant l’adaptation de la bactérie • Peuvent aussi être codés par – plasmide ou transposon: Tet – Intégron : MFS polyrésistance chez STM DT 104

Résistance naturelle chez les Gram négatif • Ensemble de mécanismes de résistance – Modification ou hydrolyse de l’antibiotique – Faible affinité de l’antibiotique sur sa cible – Imperméabilité ou efflux actif • La résistance naturelle par efflux est importante chez les Gram négatif • La preuve de la résistance par efflux est apporté – par des expériences d’inactivation de gènes rendant les bactéries plus sensibles avec des CMI 2 à 16 fois inférieures aux souches sauvages – Par l’utilisation d’inhibiteurs de l’énergie membranaire : réserpine, CCCP

Résistance acquise chez les Gram négatif • Acquisition de gènes étrangers : tet, cml. A, flo, qac – Modification ou hydrolyse de l’antibiotique – Faible affinité de l’antibiotique sur sa cible – Imperméabilité ou efflux actif • Surproduction d’un système existant, par mutation – CMI augmentées modérément : de 4 à 8 fois – Exemples E. coli et Gonocoque Acr. AB-Tol. C et Mtr. CDE : résistance bas niveau Tét, Macro et CMP et sensibilité conservée de FQ et BL – Exemple Pyo : suexpression de Mex. AB-Opr. M : résistance à Tic et Azt et certaines FQ
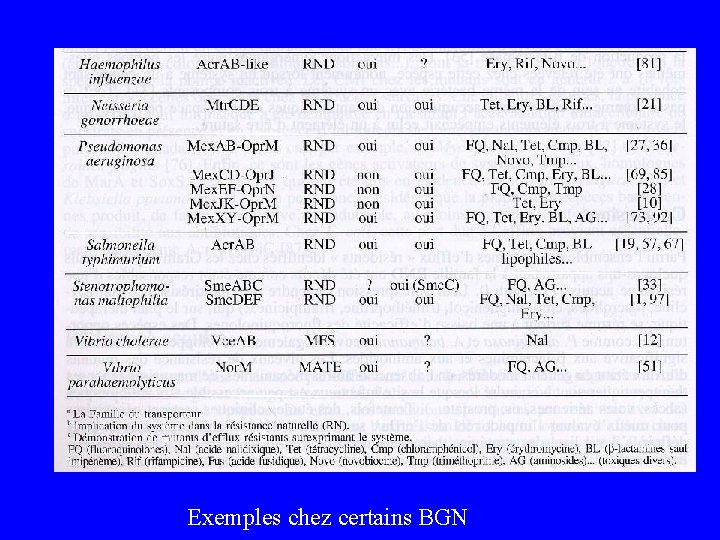
Exemples chez certains BGN

Surveillance de la résistance • A la fois résultat phénotypique (réponse I ou R) • Et mécanismes biochimiques ou enzymatiques • Mécanismes génétiques • Mécanismes moléculaires

Entérobactéries
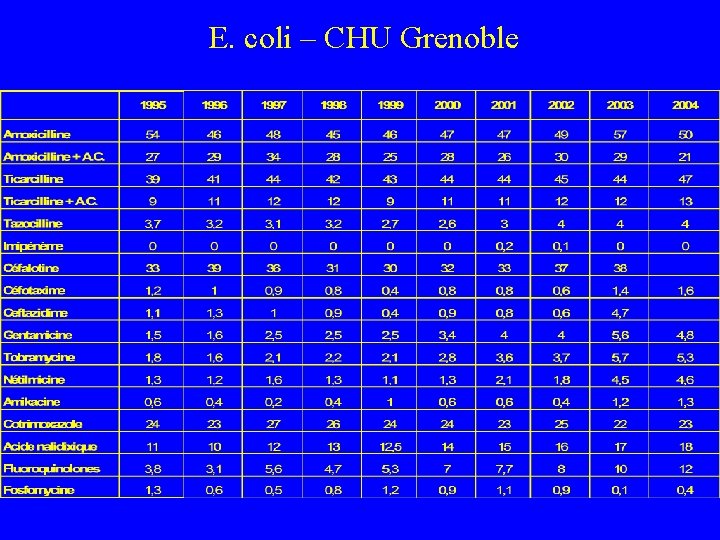
E. coli – CHU Grenoble
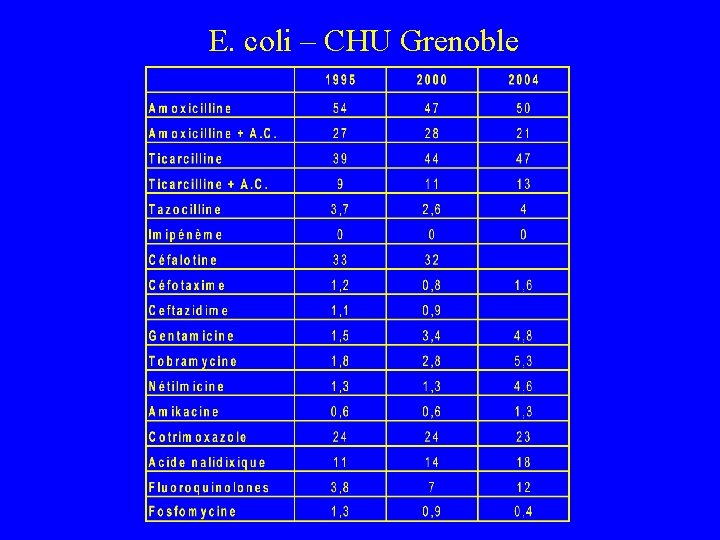
E. coli – CHU Grenoble


BGN résistants C 3 G • Résistance naturelle • Résistance acquise – Hcase – BLSE (CTXM ou non) – Case plasmidique

C 3 G hyperproduction Case naturelle

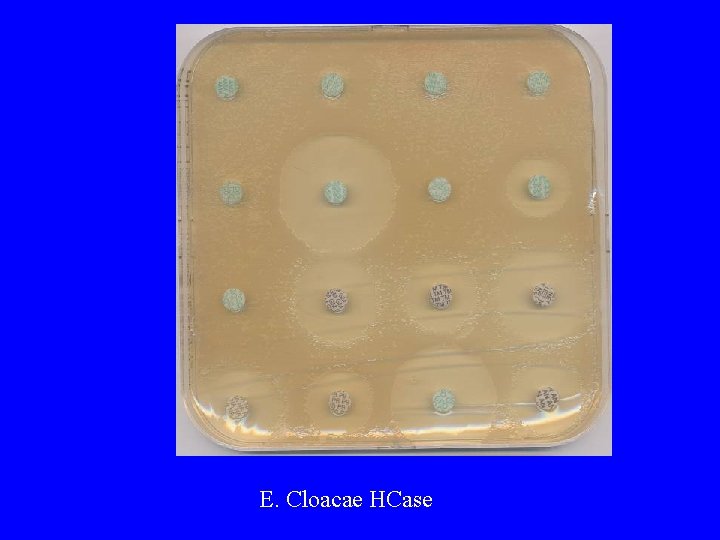
E. Cloacae HCase

C freundii Hcase

E cloacae Hcase 2006 2
C 3 G par BLSE
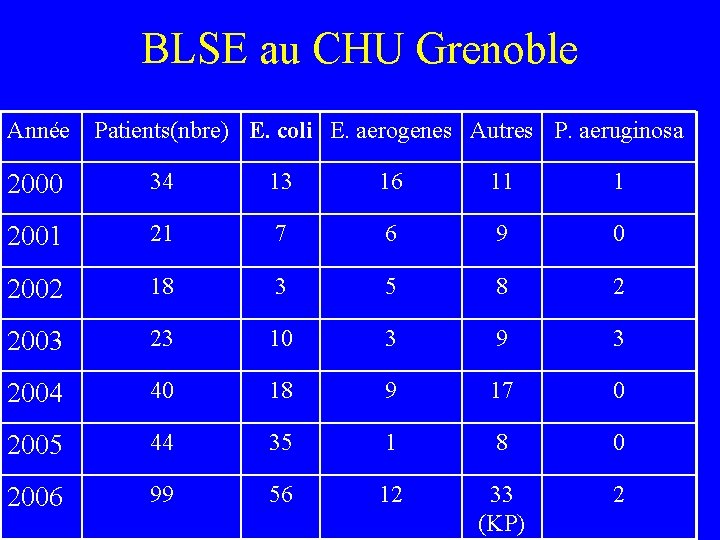
BLSE au CHU Grenoble Année Patients(nbre) E. coli E. aerogenes Autres P. aeruginosa 2000 34 13 16 11 1 2001 21 7 6 9 0 2002 18 3 5 8 2 2003 23 10 3 9 3 2004 40 18 9 17 0 2005 44 35 1 8 0 2006 99 56 12 33 (KP) 2

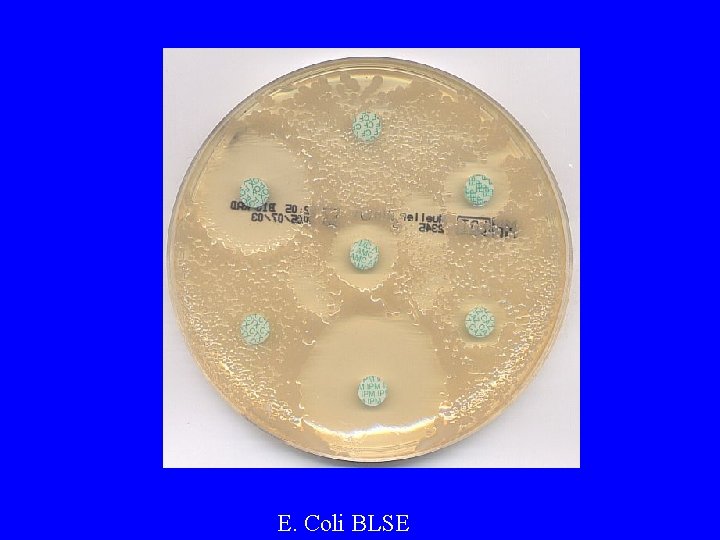
E. Coli BLSE
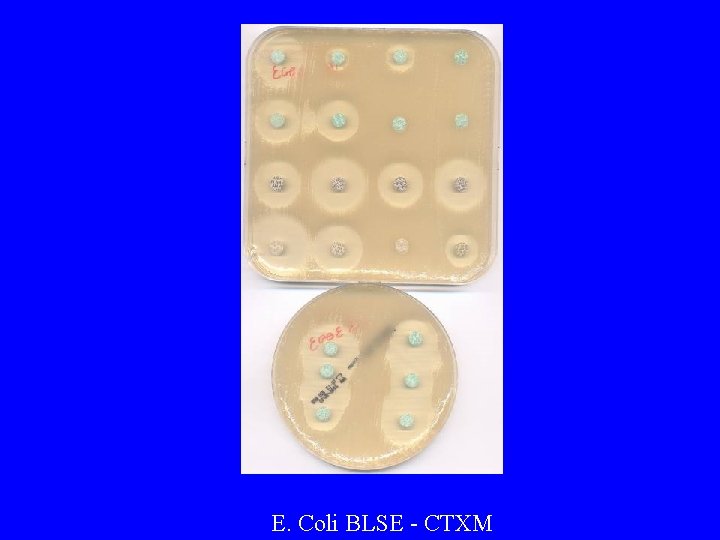
E. Coli BLSE - CTXM

C 3 G R par céphalosporinase
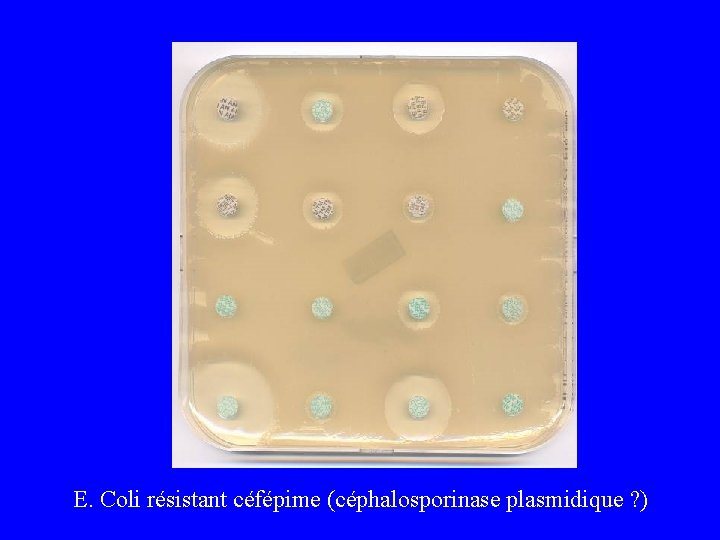
E. Coli résistant céfépime (céphalosporinase plasmidique ? )

Acinetobacter baumannii

Résistance A baumannii • Résistance naturelle • Résistance acquise polyrésistance • Sensibilisation d’une souche épidémique porteur d’une BLSE type VEB-1 par In. VS en septembre 2003 (synergie TIM avec CAZ)

Acinetobacter baumannii souche sauvage

Souche « alerte sept 2003 « – AB avec BLSE VEB-1

P. aeruginosa

P. aeruginosa • Surveillance de la résistance – Ceftazidime – Imipénème – Ciprofloxacine – Tobramycine

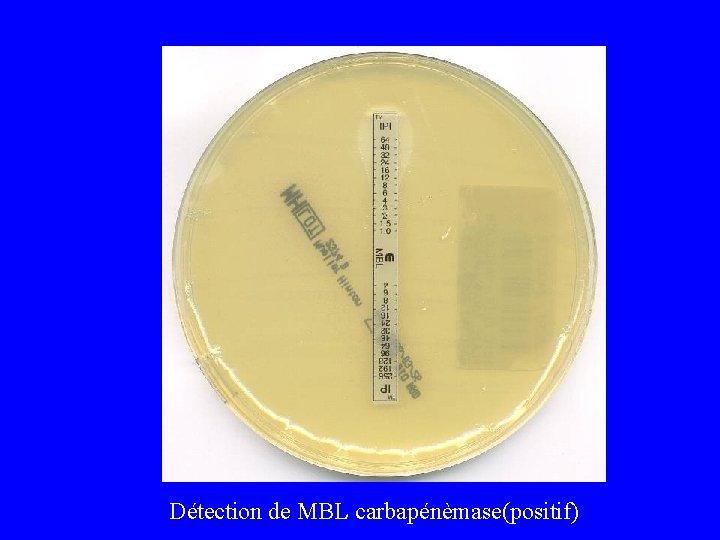
Détection de MBL carbapénèmase(positif)
P. aeruginosa muqueux sensible

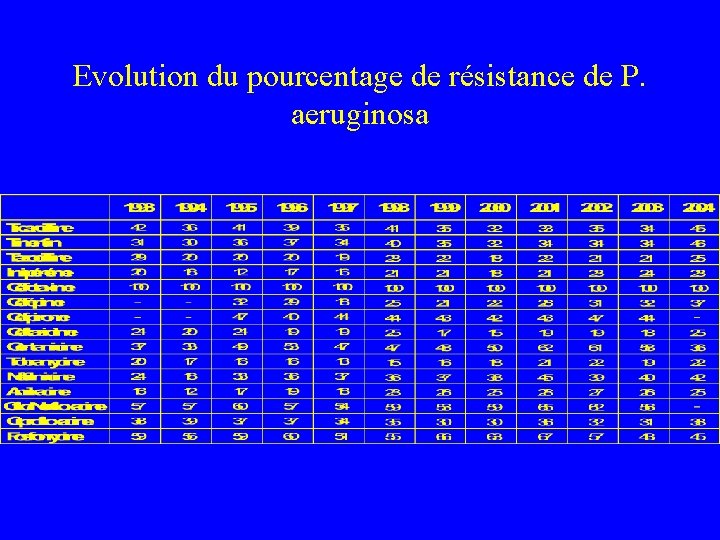
Evolution du pourcentage de résistance de P. aeruginosa
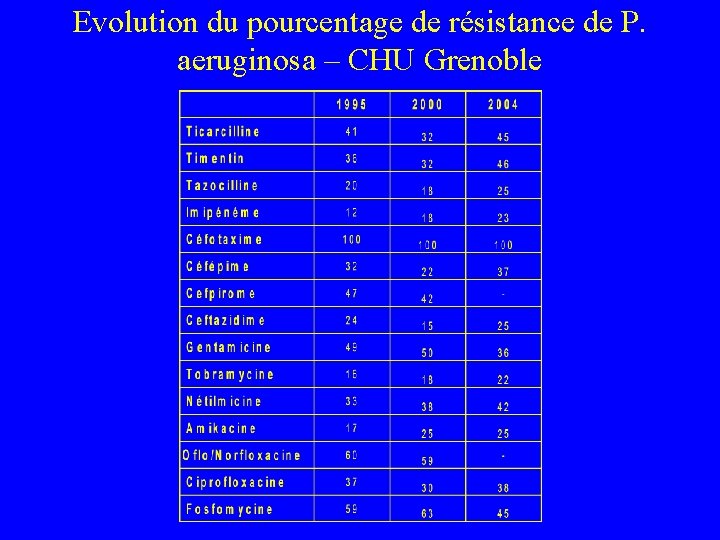
Evolution du pourcentage de résistance de P. aeruginosa – CHU Grenoble


Place des BGN dans la surveillance des BMR • Bactéries soumises aux mesures d’isolement septique – SARM, EBLSE, A baumannii; Pyo CAZR et IMPR • Autres bactéries selon leur profil de résistance – S. maltophilia

- Slides: 71