LES IMMUNOGLOBULINES VL VH CH 1 CH 2
LES IMMUNOGLOBULINES VL VH CH 1 CH 2 CH 3 CH 4 CL VL
complément CPA C y t o k i n e s
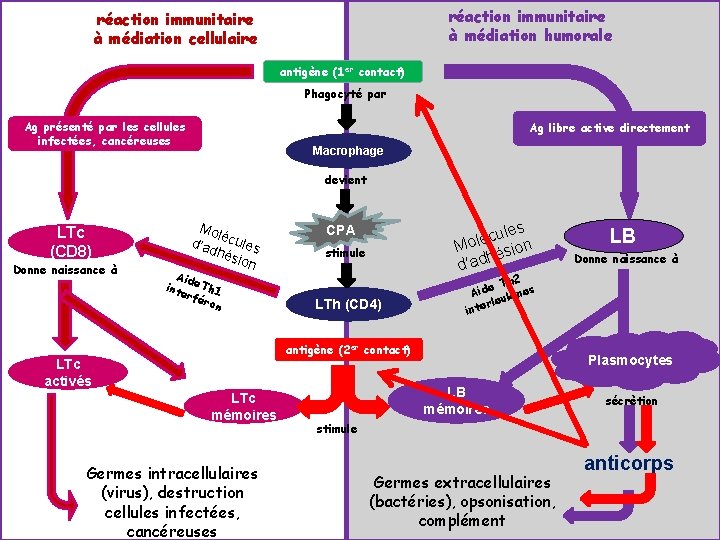
réaction immunitaire à médiation humorale réaction immunitaire à médiation cellulaire antigène (1 er contact) Phagocyté par Ag présenté par les cellules infectées, cancéreuses Ag libre active directement Macrophage devient LTc (CD 8) Donne naissance à Mol é d’ad cules hés ion Aid inte e. Th 1 rfé ron ules c é l Mo ésion h d’ad CPA stimule LTh (CD 4) LTc mémoires Germes intracellulaires (virus), destruction cellules infectées, cancéreuses Donne naissance à Th 2 s e d i e A ukin e l r inte antigène (2 er contact) LTc activés LB Plasmocytes LB mémoires sécrètion stimule Germes extracellulaires (bactéries), opsonisation, complément anticorps

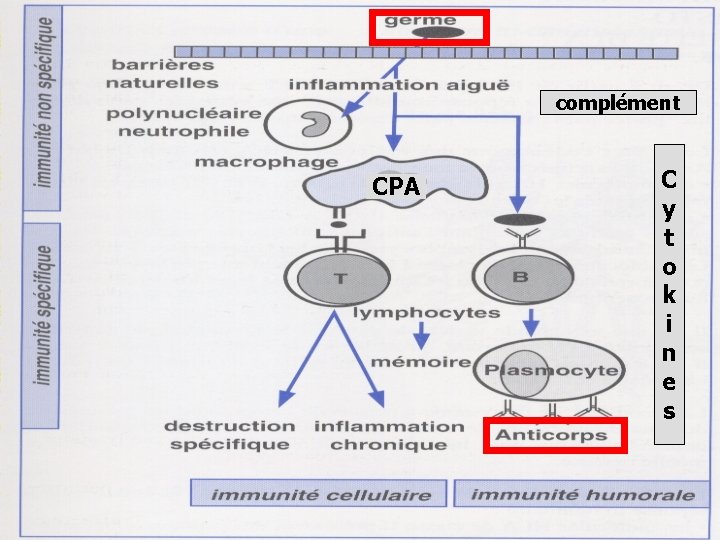
I. INTRODUCTION v Les immunoglobulines (Ig) sont des glycoprotéines ü Présentes dans : le plasma les liquides extra-vasculaires les sécrétions ü Douées d'activité anticorps Pouvoir de liaison spécifique avec le déterminant antigénique qui a provoqué leur formation. ü Produites par les plasmocytes (issus des lymphocytes B)
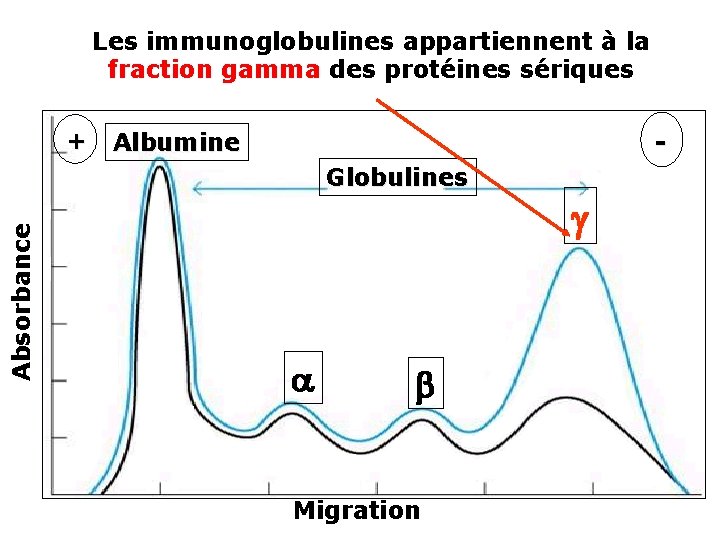
Les immunoglobulines appartiennent à la fraction gamma des protéines sériques + - Albumine Absorbance Globulines b Migration

Les Ig sont caractérisées par une très grande hétérogénéité Forment une vaste famille dont les membres sont doués de propriétés biologiques diverses, différentes de la fonction anticorps Les Ig à fonctions anticorps sont regroupées en cinq classes : Ig. G Ig. A Ig. M Ig. D Ig. E.

Un anticorps remplit deux types de fonctions : 1. Reconnaissance de l’antigène Les anticorps sont synthétisées par les plasmocytes en réponse à une substance antigénique. 1 Ac Ag 1 Ag 2 Ac 2

2. Fonctions effectrices La fixation du complément La fixation à certaines cellu (basophiles, masto, mono…) Le passage trans-placentaire (pour les Ig. G) Les réactions d'hypersensibilité (sauf de type IV)
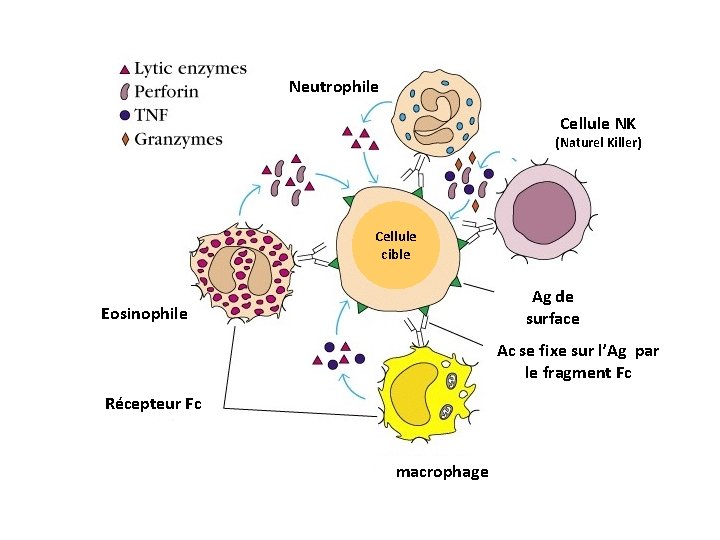
Neutrophile Cellule NK (Naturel Killer) Cellule cible Ag de surface Eosinophile Ac se fixe sur l’Ag par le fragment Fc Récepteur Fc macrophage
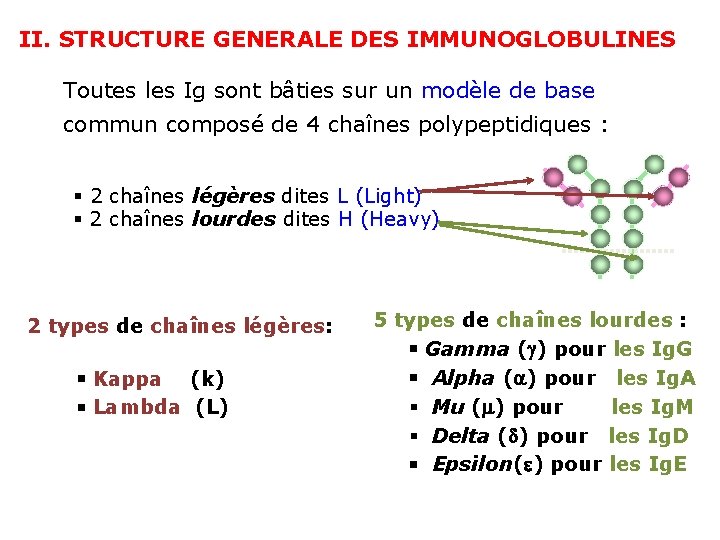
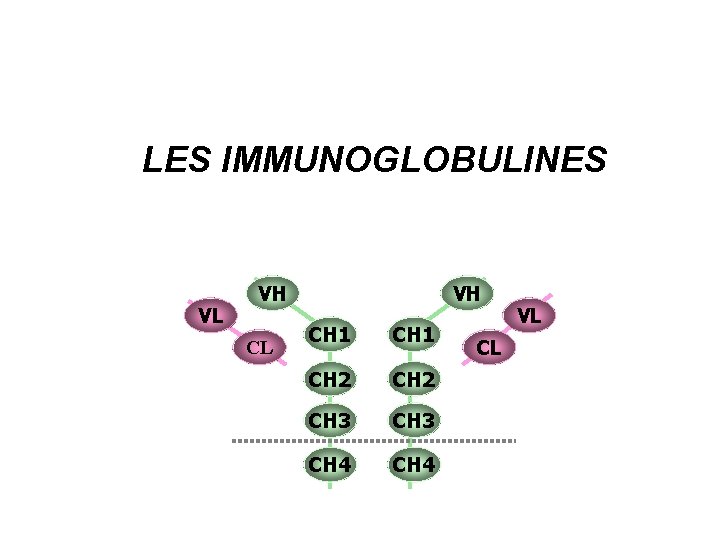
II. STRUCTURE GENERALE DES IMMUNOGLOBULINES Toutes les Ig sont bâties sur un modèle de base commun composé de 4 chaînes polypeptidiques : 2 chaînes légères dites L (Light) 2 chaînes lourdes dites H (Heavy) 2 types de chaînes légères: Kappa (k) Lambda (L) 5 types de chaînes lourdes : Gamma ( ) pour les Ig. G Alpha ( ) pour les Ig. A Mu ( ) pour les Ig. M Delta ( ) pour les Ig. D Epsilon( ) pour les Ig. E
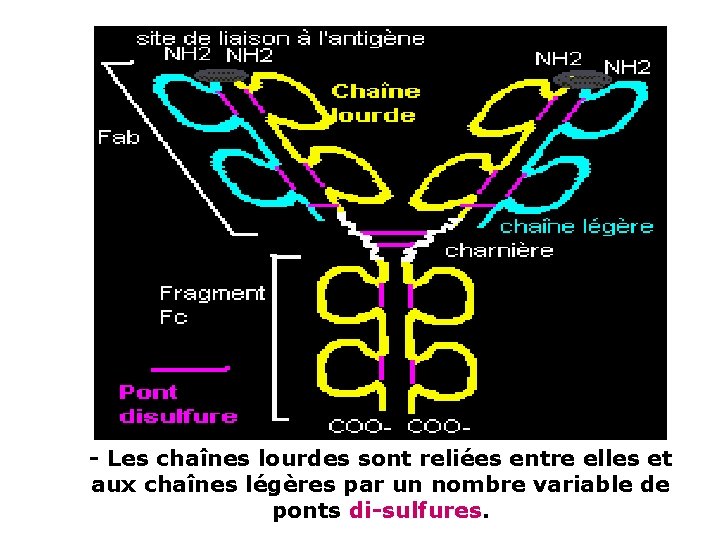
- Les chaînes lourdes sont reliées entre elles et aux chaînes légères par un nombre variable de ponts di-sulfures.

II. 1. Structure des chaînes lourdes Chaque chaîne lourde comporte deux zones caractéristiques - La région constante (CH) ü Située du coté - COOH terminal ü Composée de 330 des 440 acides aminés de la chaîne polypeptidique ü Présente une zone flexible (charnière) responsable de la forme caractéristique en Y de la molécule d’Ac. ü Participe aux fonctions effectrices de la molécule

II. 1. Structure des chaînes lourdes - La région variable (VH) ü Située du côté - NH 2 terminal ü Composée de 117 acides aminés (de 1 à 117). ü Comporte trois zones hyper- variables au niveau desquelles la séquence des acides aminés varie d'une immunoglobuline à l'autre. ü Participe à la reconnaissance de l'Ag.
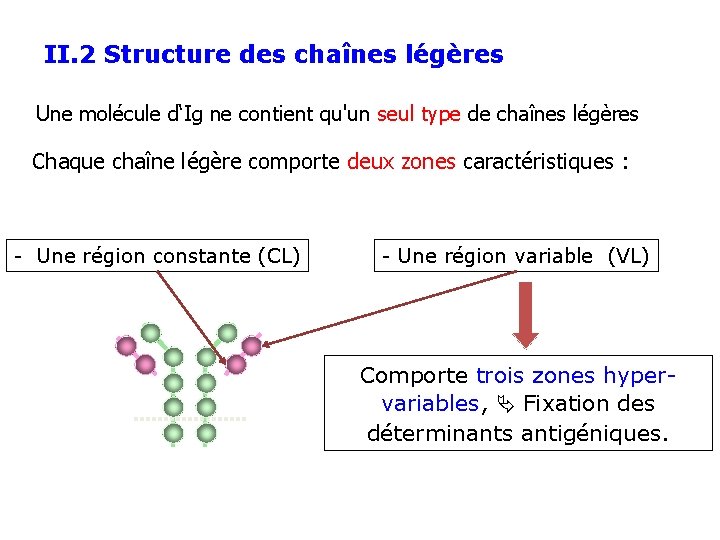
II. 2 Structure des chaînes légères Une molécule d‘Ig ne contient qu'un seul type de chaînes légères Chaque chaîne légère comporte deux zones caractéristiques : - Une région constante (CL) - Une région variable (VL) Comporte trois zones hypervariables, Fixation des déterminants antigéniques.
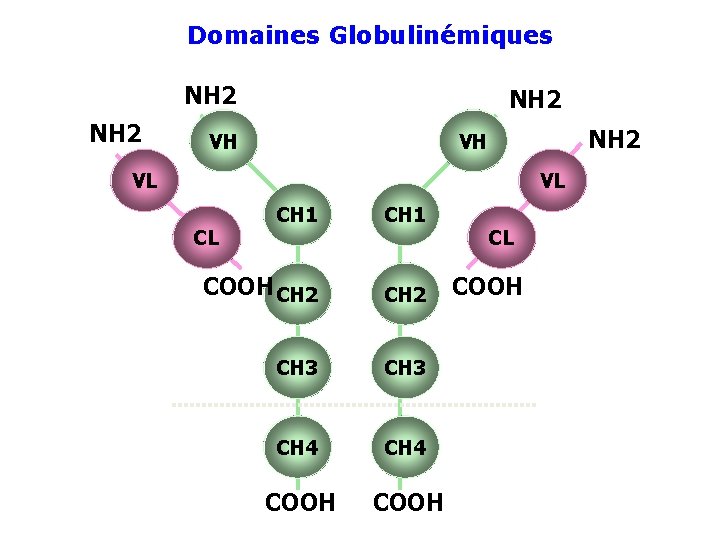
Domaines Globulinémiques NH 2 VH VL VL CH 1 COOH CH 2 CH 3 CH 4 COOH CL CL COOH
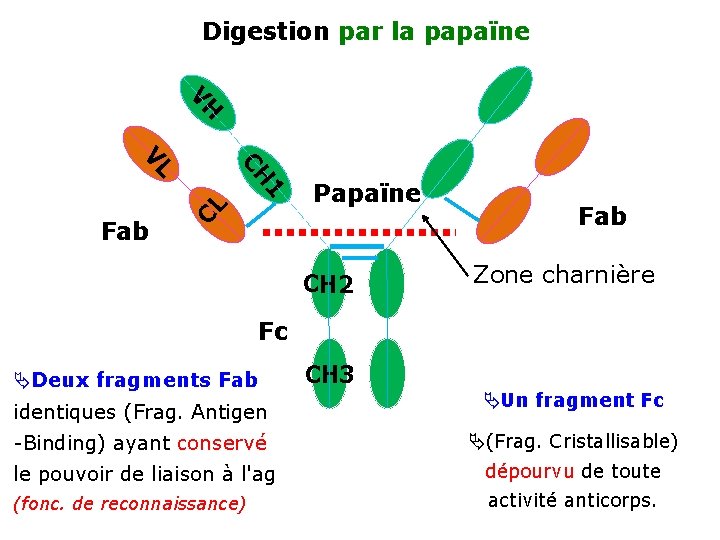
Digestion par la papaïne VH CH VL CL 1 Fab Papaïne CH 2 Fab Zone charnière Fc Deux fragments Fab identiques (Frag. Antigen CH 3 Un fragment Fc -Binding) ayant conservé (Frag. Cristallisable) le pouvoir de liaison à l'ag dépourvu de toute (fonc. de reconnaissance) activité anticorps.
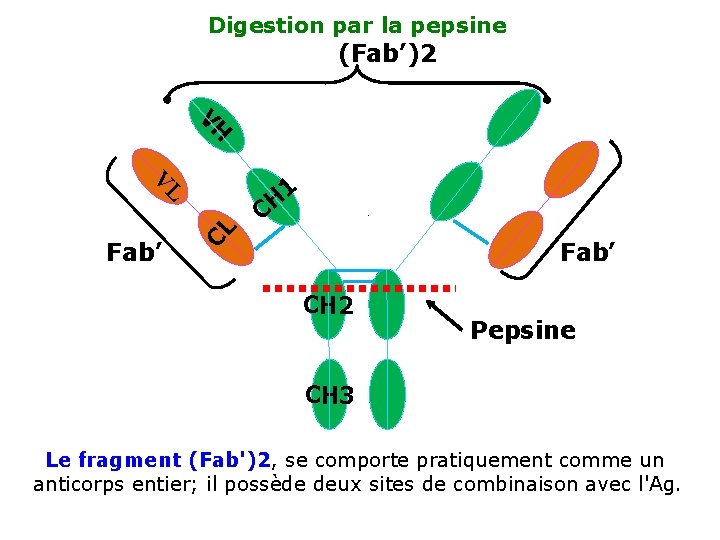
Digestion par la pepsine (Fab’)2 VH V 1 Fab’ CL L CH Fab’ CH 2 Pepsine CH 3 Le fragment (Fab')2, se comporte pratiquement comme un anticorps entier; il possède deux sites de combinaison avec l'Ag.




III. 1. Les immunoglobulines G (Ig G) Les Ig G représentent 70 à 80% de toutes les Ig sériques. La concentration sérique normale : 8 g/l ≤ Ig. G ≤ 16 g/l La fraction la plus importante de toutes les immunoglobulines sur le plan quantitatif. 4 sous classes d'Ig. G identifiées par des différences antigéniques Ig. G 1 Ig. G 2 Ig. G 3 Ig. G 4 1 2 3 4 Chacune de ces sous-classes constitue un isotype
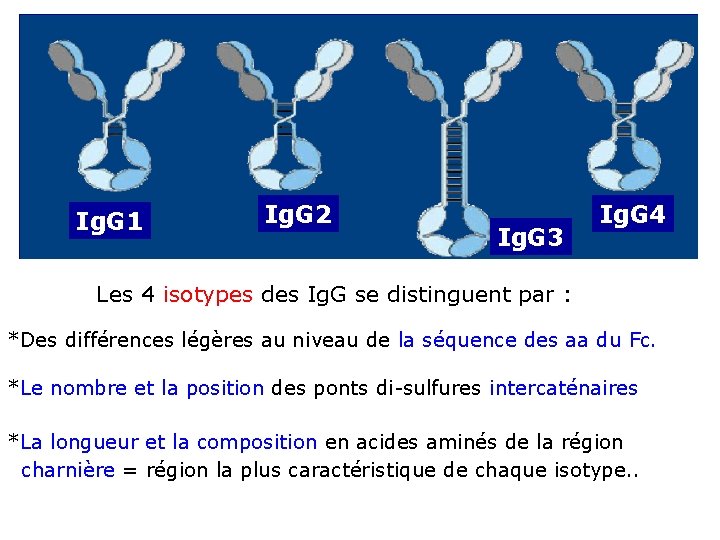
Ig. G 1 Ig. G 2 Ig. G 3 Ig. G 4 Les 4 isotypes des Ig. G se distinguent par : *Des différences légères au niveau de la séquence des aa du Fc. *Le nombre et la position des ponts di-sulfures intercaténaires *La longueur et la composition en acides aminés de la région charnière = région la plus caractéristique de chaque isotype. .

Propriétés des Ig. G * Présentes dans les liquides organiques surtout les liquides extra- vasculaires. * Ont un faible pouvoir agglutinant et ont pour principale fonction anticorps la neutralisation des virus et des toxines bactériennes. * Possèdent un pouvoir opsonisant ( phagocytose des bactéries et des virus ). * Sont les dernières immunoglobulines à apparaître après une immunisation (par rapport aux Ig. M ).

* Seules Ig. G possèdent la capacité de traverser le placenta et de regagner la circulation fœtale. Elles protègent donc le fœtus et constituent la première ligne de défense du nouveau-né. * Les Ig. G sont cytophiles : propriété de se fixer à certaines cell. Présence de Rc cellulaires pour le fragment Fc des Ig. G sur les monocytes, les macrophages, et les granulocytes. * Les Ig G activent le complément Clc: Le fragment Fc des Ig. G est à l'origine de fonctions effectrices : Transfert placentaire, Cytophilie, Fixation du complément. HSI
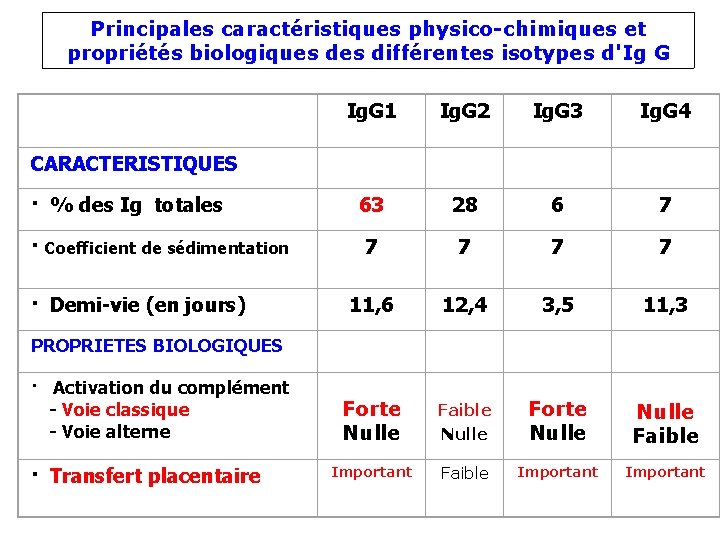
Principales caractéristiques physico-chimiques et propriétés biologiques différentes isotypes d'Ig G Ig. G 1 Ig. G 2 Ig. G 3 Ig. G 4 63 28 6 7 7 7 11, 6 12, 4 3, 5 11, 3 Forte Nulle Faible Nulle Forte Nulle Faible Important CARACTERISTIQUES · % des Ig totales · Coefficient de sédimentation · Demi-vie (en jours) PROPRIETES BIOLOGIQUES · Activation du complément - Voie classique - Voie alterne · Transfert placentaire

III. 2. Les immunoglobulines M (Ig M) * Les Ig M = 10% des Ig totales. * La concentration sérique normale : 0, 5 ≤ Ig. M ≤ 2 g/l * Les Ig M = pentamères, 5 sous- unités réunies par une chaîne polypeptidique, la chaîne J ("joining chain" ou chaîne de jonction), et par un pont di-sulfure. * Les Ig M = grande avidité pour l’Ag car 10 frgts Fab dans chaque pentamère * Les Ig. M sont les premières à apparaître dans la réponse primaire à l'infection. interviennent efficacement dans les infections bactériennes, et virales. * Les Ig M ne peuvent pas traverser le placenta, car masse moléculaire élevée. * Les Ig M fixent très efficacement le complément.
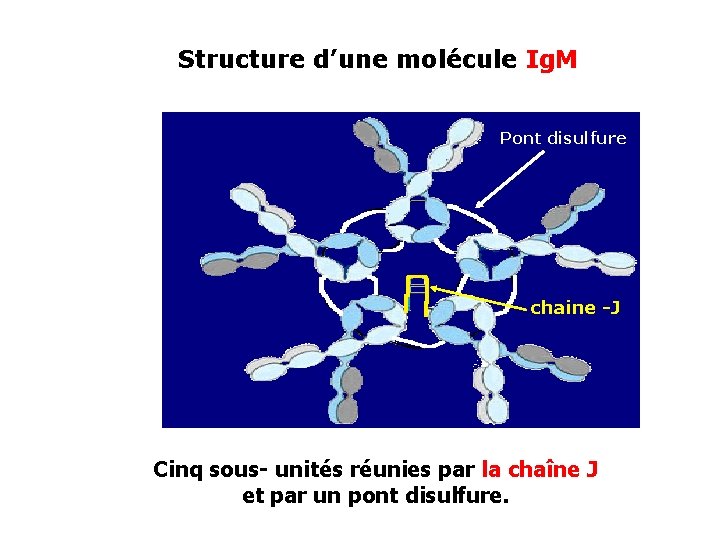
Structure d’une molécule Ig. M Pont disulfure chaine -J Cinq sous- unités réunies par la chaîne J et par un pont disulfure.
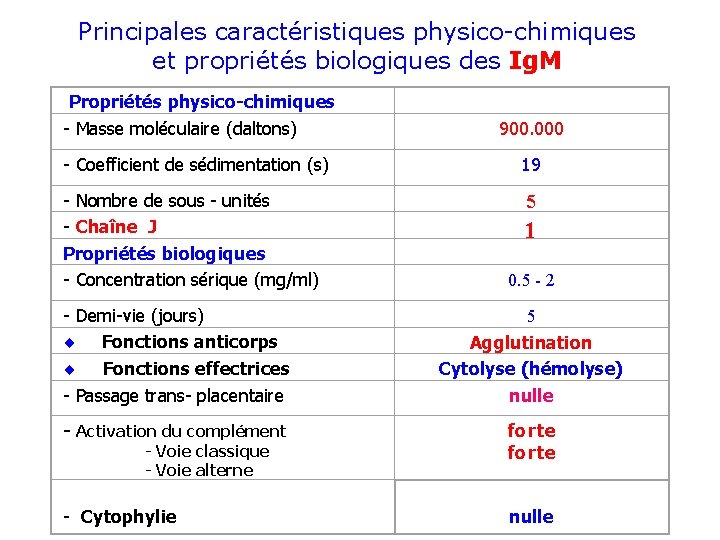
Principales caractéristiques physico-chimiques et propriétés biologiques des Ig. M Propriétés physico-chimiques - Masse moléculaire (daltons) 900. 000 - Coefficient de sédimentation (s) 19 - Nombre de sous - unités - Chaîne J Propriétés biologiques - Concentration sérique (mg/ml) 5 - Demi-vie (jours) ¨ Fonctions anticorps ¨ Fonctions effectrices - Passage trans- placentaire 1 0. 5 - 2 5 Agglutination Cytolyse (hémolyse) nulle - Activation du complément forte - Cytophylie nulle - Voie classique - Voie alterne
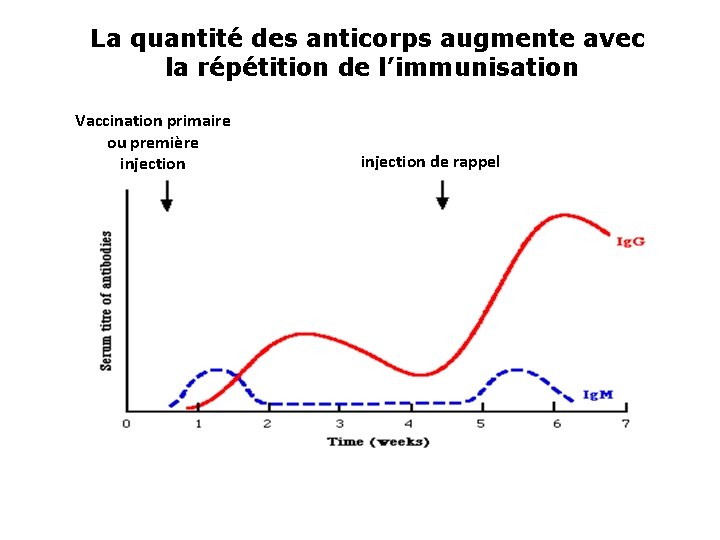
La quantité des anticorps augmente avec la répétition de l’immunisation Vaccination primaire ou première injection de rappel
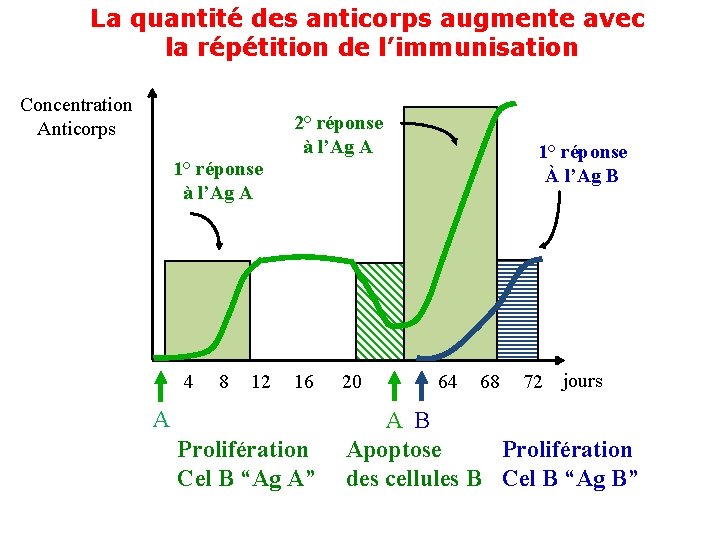
La quantité des anticorps augmente avec la répétition de l’immunisation Concentration Anticorps 1° réponse à l’Ag A 4 8 12 2° réponse à l’Ag A 16 A Prolifération Cel B “Ag A” 20 1° réponse À l’Ag B 64 68 72 jours A B Prolifération Apoptose des cellules B Cel B “Ag B”

Séquence dans la sécrétion des Ig. M et des Ig. G • largement utilisée dans le diagnostic des maladies infectieuses Ig. M+ Ig. G- infection (récente) aiguë Ig. M+ Ig. G+ infection subaiguë Ig. M- Ig. G+ infection ancienne Ig. M- Ig. G- pas d’infection

III. 3. Les Immunoglobulines A (Ig A) Ig. A Sériques * Les Ig. A = 12% des Ig sériques 10% de la totalité des Ig. A * Concentration sérique moyenne : 1, 4 ≤ Ig. A ≤ 4 g/l. Ig. A Sécrétoires *Apparaissent sélectivement dans les sécrétions séro muqueuses Salive Larmes Séc. pulmonaires Fluide nasal Séc. génito-urinaires Sueur Séc. gastro-intestinale
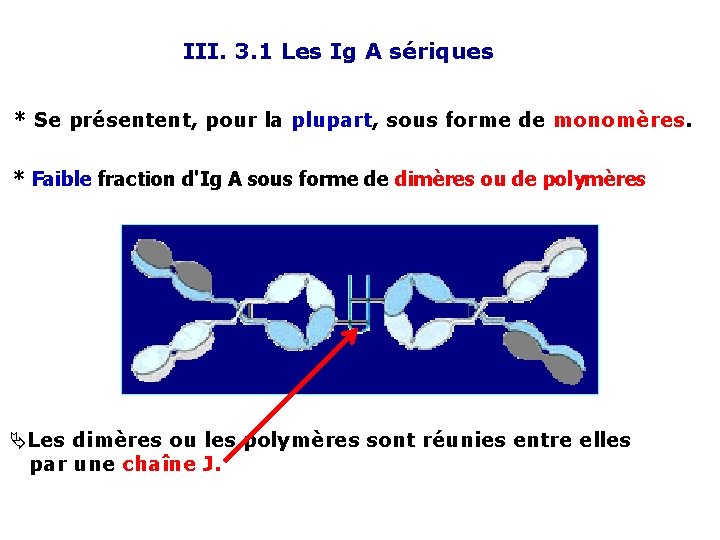
III. 3. 1 Les Ig A sériques * Se présentent, pour la plupart, sous forme de monomères. * Faible fraction d'Ig A sous forme de dimères ou de polymères Les dimères ou les polymères sont réunies entre elles par une chaîne J.
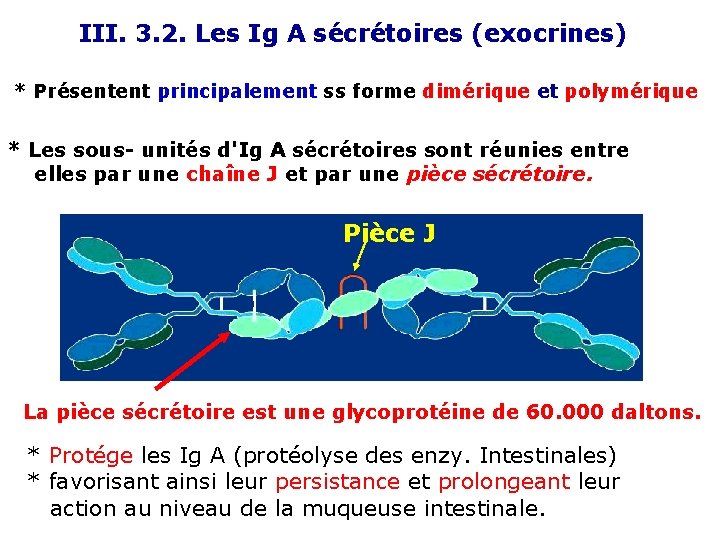
III. 3. 2. Les Ig A sécrétoires (exocrines) * Présentent principalement ss forme dimérique et polymérique * Les sous- unités d'Ig A sécrétoires sont réunies entre elles par une chaîne J et par une pièce sécrétoire. Pièce J La pièce sécrétoire est une glycoprotéine de 60. 000 daltons. * Protége les Ig A (protéolyse des enzy. Intestinales) * favorisant ainsi leur persistance et prolongeant leur action au niveau de la muqueuse intestinale.

2 sous classes d'Ig. A identifiées par des différences antigéniques : Ig. A 1 Ig. A 2 1 2 Chacune de ces sous-classes constitue un isotype III. 4. Les Immunoglobulines D (Ig D) Les Ig. D = dans le sérum en faible concentration (0, 2%-1% des Ig totales) La quasi totalité des Ig. D est présente à la surface des lymphocytes B Immatures avec des Ig M.

III. 5. Les Immunoglobulines E (Ig. E) A l'état de traces dans le sérum humain normal (0, 004% des Ig totales) Possèdent des récepteurs (haute et faible affinité) à la surface des basophiles et des mastocytes = RFc Fixation des Ig. E sur leurs récepteurs • Pontage par l’antigène • Dégranulation • Libération de médiateurs chimiques (Histamine, Leucotriènes, Prostaglandine…)
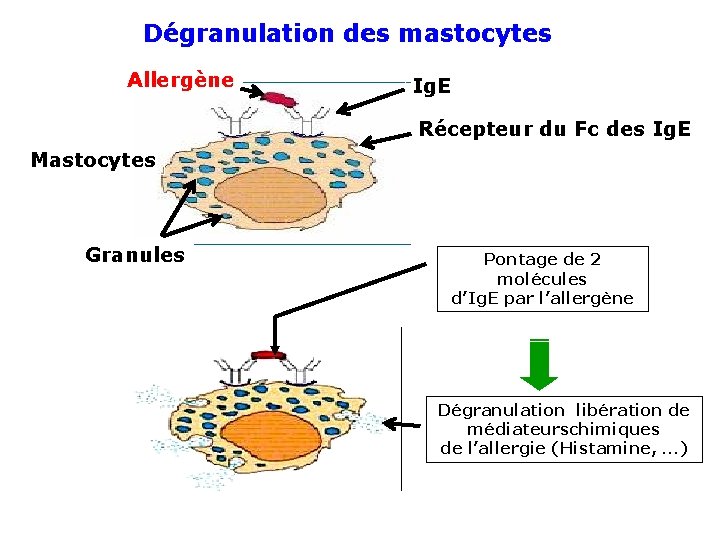
Dégranulation des mastocytes Allergène Ig. E Récepteur du Fc des Ig. E Mastocytes Granules Pontage de 2 molécules d’Ig. E par l’allergène Dégranulation libération de médiateurschimiques de l’allergie (Histamine, …)

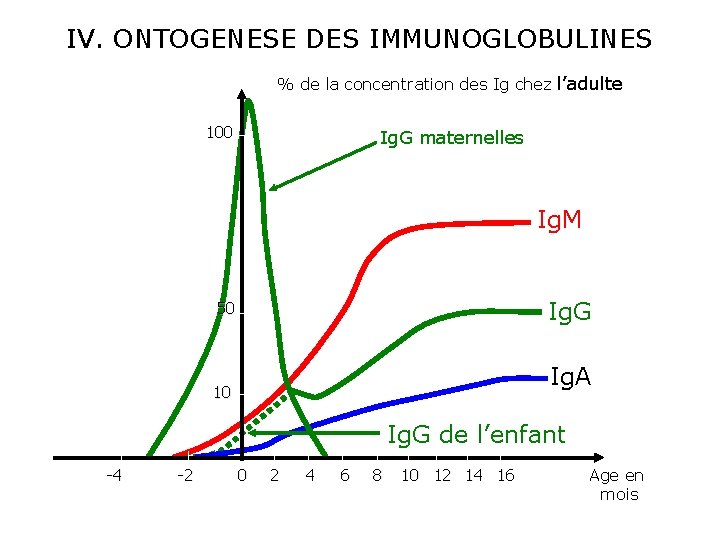
IV. ONTOGENESE DES IMMUNOGLOBULINES % de la concentration des Ig chez l’adulte 100 Ig. G maternelles Ig. M Ig. G 50 Ig. A 10 Ig. G de l’enfant -4 -2 0 2 4 6 8 10 12 14 16 Age en mois

Les Ig. G maternelles franchissent facilement le placenta. Passage modeste pendant les 2 premiers trimestres de la vie fœtale. Augmentation importante de la perméabilité placentaire pour les Ig. G maternelles vers la 20éme semaine. Intérêt pratique - Diagnostic précoce de certaines maladies : toxoplasmose, syphilis congénitale…

V. DIVERSITE DES IMMUNOGLOBULINES ISOTYPES, ALLOTYPES ET IDIOTYPES Ig = structure fondamentale mais * variations d'une molécule d’Ig à l'autre * variations au sein d'une même classe d’Ig * différences entre les Ig de groupes d'individus appartenant à la même espèce.
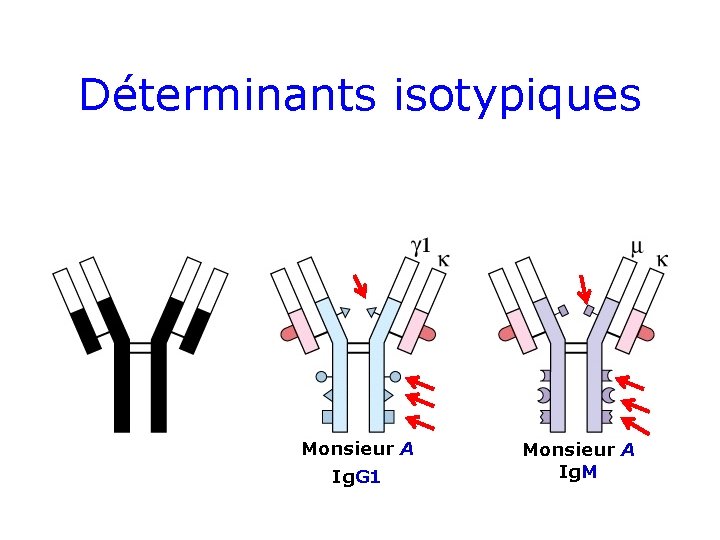
Déterminants isotypiques Monsieur A Ig. G 1 Monsieur A Ig. M
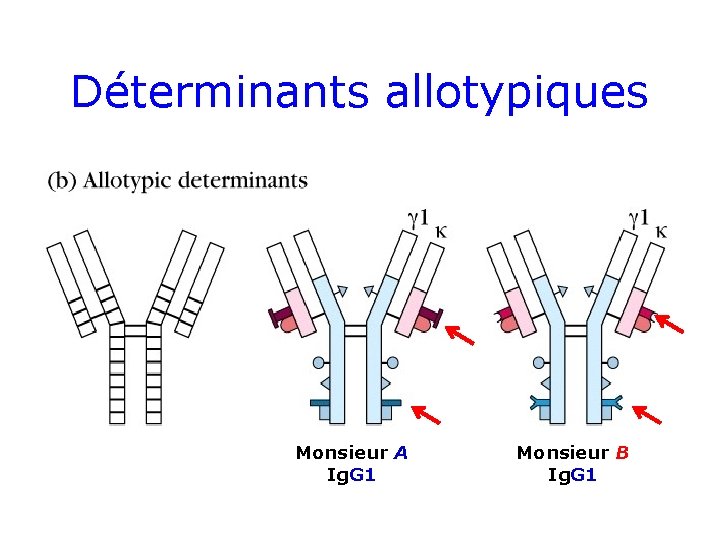
Déterminants allotypiques Monsieur A Ig. G 1 Monsieur B Ig. G 1
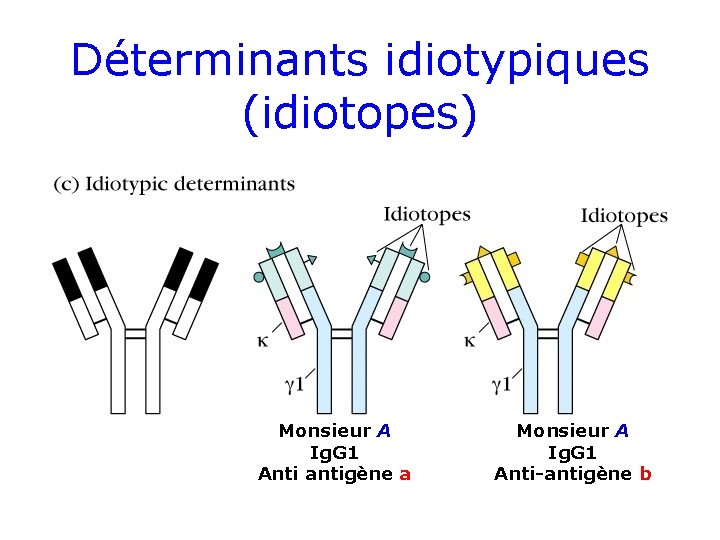
Déterminants idiotypiques (idiotopes) Monsieur A Ig. G 1 Anti antigène a Monsieur A Ig. G 1 Anti-antigène b

VII. LES ANTICORPS MONOCLONAUX Les Anticorps monoclonaux sont des Ig produites par un seul clone lymphocytaire possédant ainsi les mêmes spécificités antigéniques, isotypiques, allotypiques et idiotypiques. Applications : Recherche fondamentale Recherche appliquée et Médecine (diagnostic, traitement…. ) Acs monoclonaux Acs polyclonaux

La pièce « J » existe dans les classes d’immunoglobulines suivantes : A. B. C. D. E. les immunoglobulines G les immunoglobulines M les immunoglobulines A sériques dimériques les immunoglobulines A sécrétoires dimériques les immunoglobulines E Le fragment Fc des immunoglobulines : A. B. C. D. E. permet la fixation des Ig. E sur les mastocytes permet la fixation des Ig. G sur les macrophages est composé des parties constantes et variables des chaînes lourdes et légères permet le passage transplacentaire des immunoglobulines G permet à la molécule d’anticorps de neutraliser certains virus
- Slides: 46