Les hydrocarbures Plan du chapitre Les familles dhydrocarbures

Les hydrocarbures Plan du chapitre : • • Les familles d’hydrocarbures Les alcanes Les alcènes Les alcynes Version 3 - 28/02/2016 1
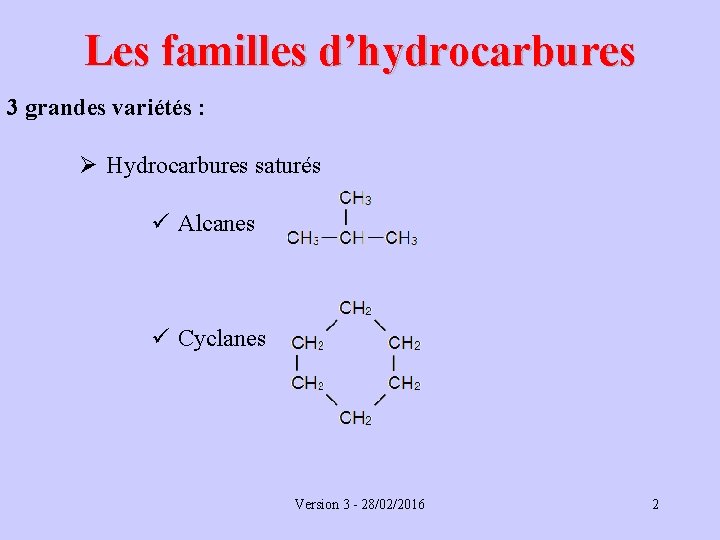
Les familles d’hydrocarbures 3 grandes variétés : Ø Hydrocarbures saturés ü Alcanes ü Cyclanes Version 3 - 28/02/2016 2
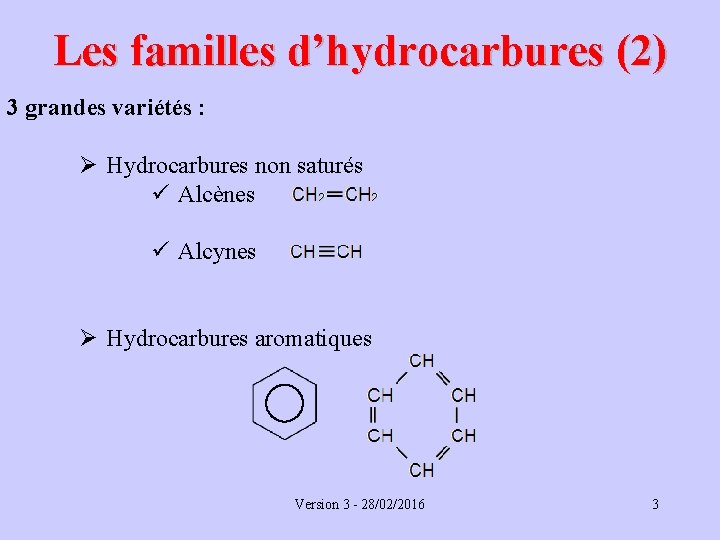
Les familles d’hydrocarbures (2) 3 grandes variétés : Ø Hydrocarbures non saturés ü Alcènes ü Alcynes Ø Hydrocarbures aromatiques Version 3 - 28/02/2016 3

Plan du chapitre : • • Les familles d’hydrocarbures Les alcanes Les alcènes Les alcynes Version 3 - 28/02/2016 4
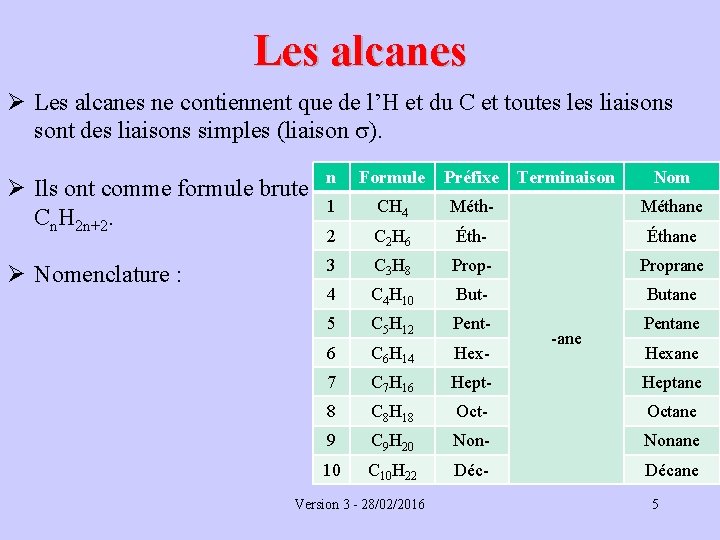
Les alcanes Ø Les alcanes ne contiennent que de l’H et du C et toutes liaisons sont des liaisons simples (liaison s). Ø Ils ont comme formule brute Cn. H 2 n+2. n Formule Préfixe 1 CH 4 Méth- Méthane 2 C 2 H 6 Éth- Éthane Ø Nomenclature : 3 C 3 H 8 Prop- Proprane 4 C 4 H 10 But- Butane 5 C 5 H 12 Pent- Pentane 6 C 6 H 14 Hex- 7 C 7 H 16 Hept- Heptane 8 C 8 H 18 Oct- Octane 9 C 9 H 20 Non- Nonane 10 C 10 H 22 Déc- Décane Version 3 - 28/02/2016 Terminaison -ane Nom Hexane 5

Nomenclature des alcanes ramifiés 1. Repérer la chaîne principale, c’est à dire la plus longue 2. Compter les atomes de carbone 3. Déterminer la racine du nom, tirée (généralement) du nombre grec correspondant au nombre d’atomes de carbone. 4. Rajouter le suffixe “–ane”. Version 3 - 28/02/2016 6

Nomenclature des alcanes ramifiés 5. Précéder ce nom de la description (emplacement, longueur, saturation) de la ramification : ü La position de la ramification est obtenue en numérotant les atomes de la chaîne principale, dans le sens fournissant à la ramification le plus petit chiffre possible ü La longueur de la ramification est décrite par les racines habituelles ü Une ramification saturée est décrite par le suffixe –yl au lieu du –ane habituel. 6. Les restes alkyles sont indiqués par ordre alphabétique. 7. Lorsqu’une même ramification est présente plusieurs fois, le montrer par le multiplicateur « di » , « tri » , « tétra » , « penta » , « hexa » , etc. Version 3 - 28/02/2016 7

Exemples de nomenclature des alcanes ramifiés 3 -méthylhexane 4 -éthyl-2, 5 -diméthylheptane Version 3 - 28/02/2016 8
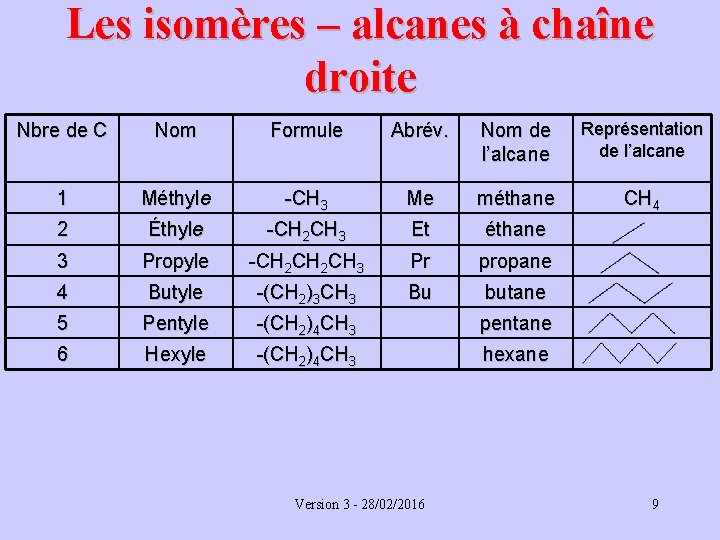
Les isomères – alcanes à chaîne droite Nbre de C Nom Formule Abrév. Nom de l’alcane Représentation de l’alcane 1 Méthyle -CH 3 Me méthane CH 4 2 Éthyle -CH 2 CH 3 Et éthane 3 Propyle -CH 2 CH 3 Pr propane 4 Butyle -(CH 2)3 CH 3 Bu butane 5 Pentyle -(CH 2)4 CH 3 pentane 6 Hexyle -(CH 2)4 CH 3 hexane Version 3 - 28/02/2016 9

Les isomères – nomenclature Version 3 - 28/02/2016 10

Les isomères – nomenclature Ø Noms triviaux vs noms systématiques : ü isopropyle vs 1 -méthyle, ü isobutyle vs 2 -méthylpropyle, ü sec-butyle vs 1 -méthylpropyle, ü tert-butyle vs 1, 1 -diméthyle et ü néopentyle vs 2, 2 -diméthylpropyle Version 3 - 28/02/2016 11

Exercice de nomenclature 2, 7 -diméthyl 5 -(1 -méthylpropyl)-nonane Version 3 - 28/02/2016 12
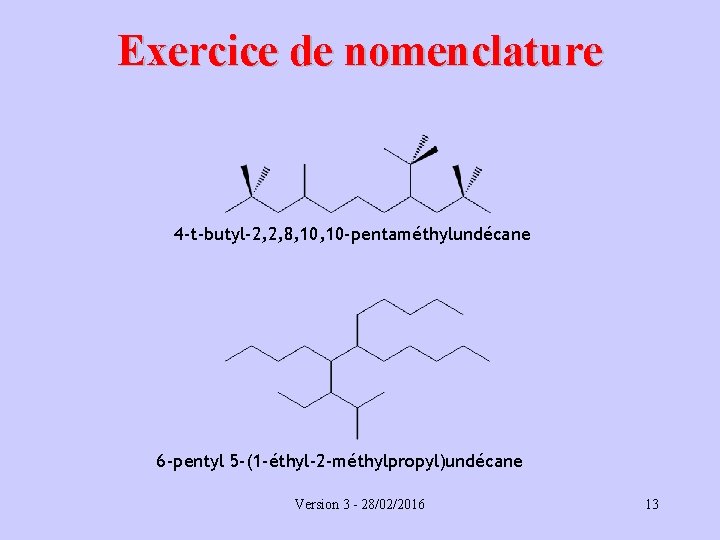
Exercice de nomenclature 4 -t-butyl-2, 2, 8, 10 -pentaméthylundécane 6 -pentyl 5 -(1 -éthyl-2 -méthylpropyl)undécane Version 3 - 28/02/2016 13
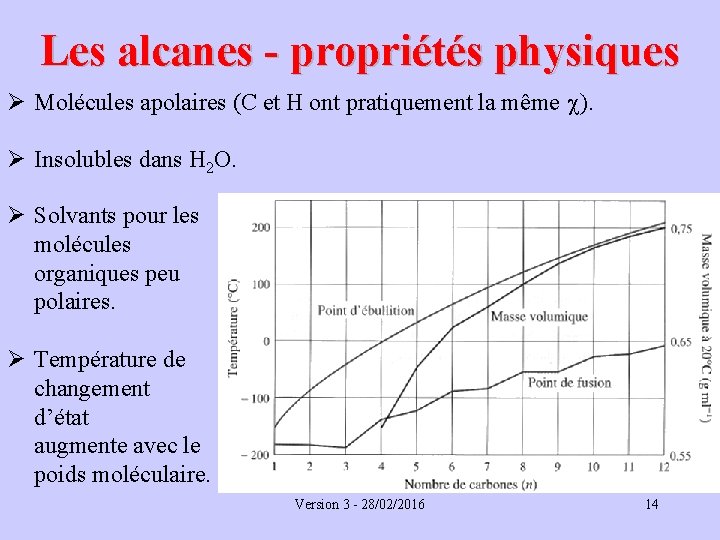
Les alcanes - propriétés physiques Ø Molécules apolaires (C et H ont pratiquement la même c). Ø Insolubles dans H 2 O. Ø Solvants pour les molécules organiques peu polaires. Ø Température de changement d’état augmente avec le poids moléculaire. Version 3 - 28/02/2016 14

Propriétés physiques des alcanes Ø Point d’ébullition : ü T où un liquide devient un gaz ü T où la p de vapeur = p ambiante ü T où les forces retenant les molécules du liquide « ensemble » sont brisées Ø Donc, T ébull. est fonction forces entre les molécules : ü forces T ébull. , ü forces T ébull. Ø Quelles sont ces forces? Version 3 - 28/02/2016 15

Propriétés chimiques des alcanes Ø Les alcanes sont peu réactionnels car : ü les liaisons C-C et C-H sont très stables ü les liaisons C-H. sont peu polarisées ü les liaisons sont peu polarisables ü il n'existe pas de doublet libre pour d'éventuelles réactions Ø Les seules réactions possibles seront donc des réactions de substitution, de dégradation ou de combustion. Ø Pour rappeler leur inertie chimique, les alcanes ont été appelés "paraffines" Version 3 - 28/02/2016 16

Propriétés chimiques des alcanes Ø Réaction de substitution Ø Réaction de dégradation R – CH 2 – R’ → R – CH = CH 2 + CH 3 – R’ Ø Réaction de combustion : (donne toujours comme produits de réaction, du CO 2 et H 2 O) C 5 H 12 + 8 O 2 → 5 CO 2 + 6 H 2 O Version 3 - 28/02/2016 17
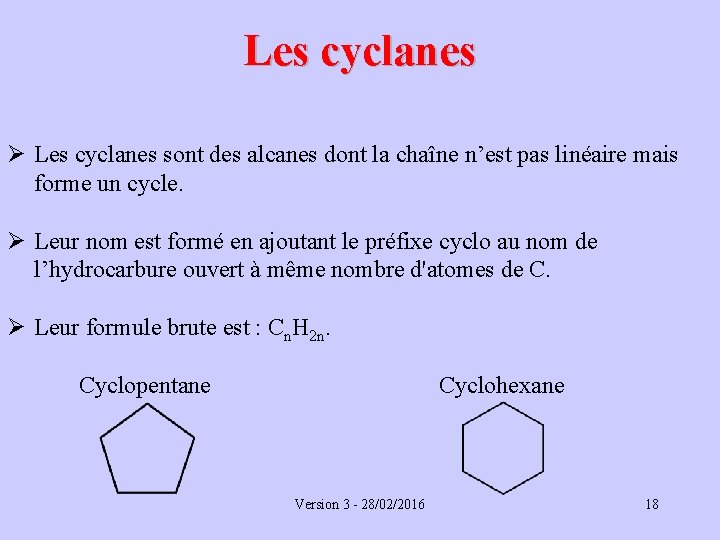
Les cyclanes Ø Les cyclanes sont des alcanes dont la chaîne n’est pas linéaire mais forme un cycle. Ø Leur nom est formé en ajoutant le préfixe cyclo au nom de l’hydrocarbure ouvert à même nombre d'atomes de C. Ø Leur formule brute est : Cn. H 2 n. Cyclopentane Cyclohexane Version 3 - 28/02/2016 18

Les cyclanes Ø A cause des angles naturels de liaison, les cycles plus stables sont des cycles à 5, 6 ou 7 C. Ø Les cyclanes (à partir de C 5) ont des propriétés voisines de celles des alcanes correspondants. Ø Un grand nombre de composés naturels dont les terpènes possèdent un ou plusieurs de ces cycles dans leur structure. Ø Les terpènes sont une classe d’hydrocarbures, produits par de nombreuses plantes, en particulier les conifères. Ce sont des composants majeurs de la résine et de l’essence de térébenthine produite à partir de résine. Version 3 - 28/02/2016 19

Les alcènes Ø Les alcènes sont des hydrocarbures porteurs d'une ou plusieurs doubles liaisons C=C. Ø Formule brute : Cn. H 2 n (pour 1 seule liaison C=C). Ø Les alcènes sont aussi appelés "oléfine'' (générateur d'huile) pour rappeler qu'en présence de nombreux réactifs, ils donnent des substances huileuses. Version 3 - 28/02/2016 20

Les alcènes – nomenclature Ø La chaîne la plus longue portant la double liaison reçoit le même préfixe que celui de l’hydrocarbure saturé correspondant. Ø Ce préfixe est affecté du suffixe -ène au lieu de -ane. Ø Propène CH 2 = CH – CH 3 Ø Butène-1 CH 2 = CH – CH 2 – CH 3 Butène-2 CH 3 - CH = CH 2 – CH 3 Ø Ethylène CH 2 = CH 2 Styrène Version 3 - 28/02/2016 21

Les alcènes – nomenclature Ø Si un alcène possède plusieurs doubles liaisons, on fait précéder la terminaison -ène par le préfixe di, tri, tétra. . . correspondant à leur nombre. Ø Butadiène-1, 3 CH 2 = CH – CH = CH 2 Version 3 - 28/02/2016 22

Les alcènes – propriétés physiques Ø Les propriétés physiques des alcènes sont très proches de celles des alcanes correspondants (un peu plus solubles dans l’eau). Version 3 - 28/02/2016 23

Les alcènes – propriétés chimiques Ø Les alcènes présentent une réactivité marquée au niveau de la double liaison C=C. C'est un centre d’insaturation, on aura donc des réactions d’addition (H 2, H 2 O, Cl 2, HCl) et des réactions de polymérisation. Ø Réactions d’addition : Version 3 - 28/02/2016 24

Les alcènes – propriétés chimiques Ø Réactions de polymérisation : Ethylène Polyéthylène Chlorure de vinyle Polychlorure de vinyle (PVC) Version 3 - 28/02/2016 25

Les alcènes – propriétés chimiques Ø Réactions de polymérisation : Styrène Polystyrène Ø Lorsque les polymères ont des poids moléculaires (P. M. ) très grands, on obtient des matières plastiques très stables et chimiquement inertes. Ø Lorsque les P. M. sont plus faibles, ce sont des liquides plus ou moins visqueux utilisés comme lubrifiants. Version 3 - 28/02/2016 26

Les alcènes – propriétés chimiques Ø Lorsque l’on polymérise ensemble plusieurs monomères différents, on obtient des copolymères (copolymérisation) Version 3 - 28/02/2016 27

Les alcynes Ø Les alcynes sont des hydrocarbures possédant au moins une liaison triple C ≡ C. Ø Le plus simple est l'acétylène H – C ≡ C – H Ø Étant donné les nombreuses possibilités d’addition sur ce genre de molécules, l’acétylène va être le point de départ de nombreuses synthèses organiques. Version 3 - 28/02/2016 28

Les hydrocarbures aromatiques Ø Ces hydrocarbures cycliques ont été appelés "aromatiques'' à cause de leur odeur. Ø Le benzène (C 6 H 6) est le produit de base des composés aromatiques. Version 3 - 28/02/2016 29

Les hydrocarbures aromatiques Ø Le benzène est représenté avec trois doubles liaisons conjuguées. Or il ne présente aucune des propriétés des hydrocarbures à doubles liaisons. Ø Tous les C et les H sont dans un même plan et les électrons qui restent forment ce que l'on appelle le « nuage électronique » au dessus et en dessous de ce plan. Ø Ce système donne au benzène une structure plus stable que si il y avait vraiment des doubles liaisons. Version 3 - 28/02/2016 30

Propriétés des hydrocarbures aromatiques Ø Masse volumique 0, 9 gr/m³, Ø Tvaporisation = 80 °C, Ø Tsolidification = 5, 4 °C. Ø C 6 H 6 est insoluble dans l’eau. Ø C 6 H 6 est soluble dans l'alcool et dans l'éther. Version 3 - 28/02/2016 31

Propriétés des hydrocarbures aromatiques Ø Le benzène dissout un grand nombre de substances : iode, soufre, caoutchouc, corps gras, essences, résines. . . Ø Le benzène est très toxique, on emploiera de préférence des dérivés moins dangereux. Version 3 - 28/02/2016 32

Dérivés du benzène Ø Toluène ou méthylbenzène Ø Xylène ou diméthylbenzène (il existe 3 isomères) Orthoxylène diméthylbenzène-1, 2 Metaxylène diméthylbenzène-1, 3 Version 3 - 28/02/2016 Paraxylène diméthylbenzène-1, 4 33

Les dérivés halogénés Ø Ce sont des dérivés des hydrocarbures dans lesquels des atomes de H sont remplacés par des atomes de Cl, Br, I, F. Ø Nomenclature : Ø Monochlorométhane CH 3 Cl (anesthésique local, gaz réfrigérant) Ø Dichlotométhane : CH 2 Cl 2 (solvant – ici chlorure de méthylène) Version 3 - 28/02/2016 34

Les dérivés halogénés Ø Trichlorométhane : CHCl 3 (chloroforme : anesthésique) Ø Tétrachlorométhane : CCl 4 (tétrachlorure de carbone : dissolvant, détachant) Ø Tétrafluoréthylène Version 3 - 28/02/2016 35

Les dérivés halogénés Ø On peut aussi associer le terme halogénure au nom du radical carboné correspondant : Ø Chlorure de propyle : CH 3 – CH 2 – Cl Ø Chlorure de vinyle : Version 3 - 28/02/2016 36
- Slides: 36