Les Gaz Les proprits et les rgularits Les































- Slides: 37

Les Gaz

Les propriétés et les régularités Les gaz remplissent toujours leur contenant. Ils n’ont ni de forme ni de volume propres. b) Les gaz sont très compressibles. c) Les gaz se diffusent, c’est-à-dire qu’ils se déplacent spontanément pour occuper tout l’espace disponible. d) Les températures ont une influence sur le volume et sur la pression d’un gaz. a)

Les propriétés et les régularités • Lorsqu’on chauffe un gaz, son volume et sa pression augmentent; lorsqu’on lui applique une pression, son volume diminue.

Définition d’un gaz • Un gaz se définit comme une substance qui occupe tout l’espace de son contenant et en adopte la forme, se diffuse rapidement et se mélange facilement aux autres gaz.

La pression: • La pression est la force qui agit sur une unité de surface. • L’unité du SI est le Pascal (Pa). • On utilise aussi d’autres unités.

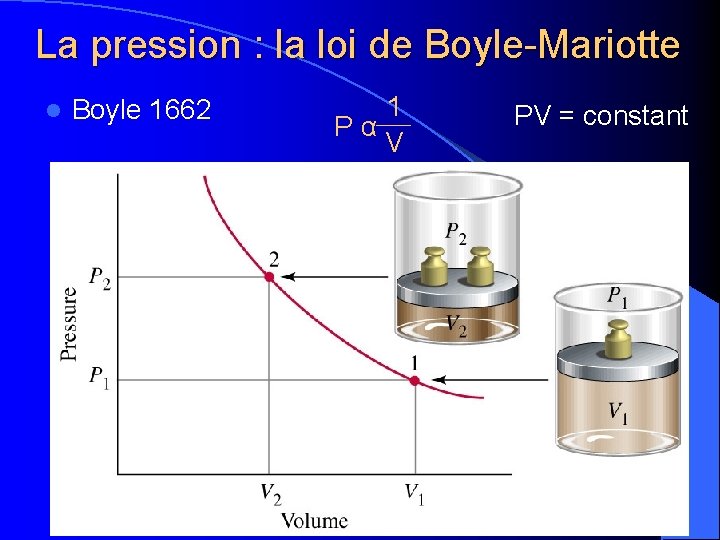
La pression: la loi de Boyle-Mariotte • D’après la loi de Boyle-Mariotte, le volume (V) d’un gaz diminue proportionnellement à l’augmentation de la pression (P) qu’on exerce sur ce gaz, à condition que d’autres variables, comme la température et la quantité de gaz demeurent constantes.

La pression : la loi de Boyle-Mariotte l Boyle 1662 1 P α V PV = constant

La pression: la loi de Boyle-Mariotte • On peut exprimer ce rapport de façon plus pratique en comparant deux ensembles de mesures de la pression et du volume pour le même échantillon de gaz. P 1 V 1 = P 2 V 2 (avant et après) • Cette équation se vérifie lorsque la température et la quantité de gaz demeurent constantes. •

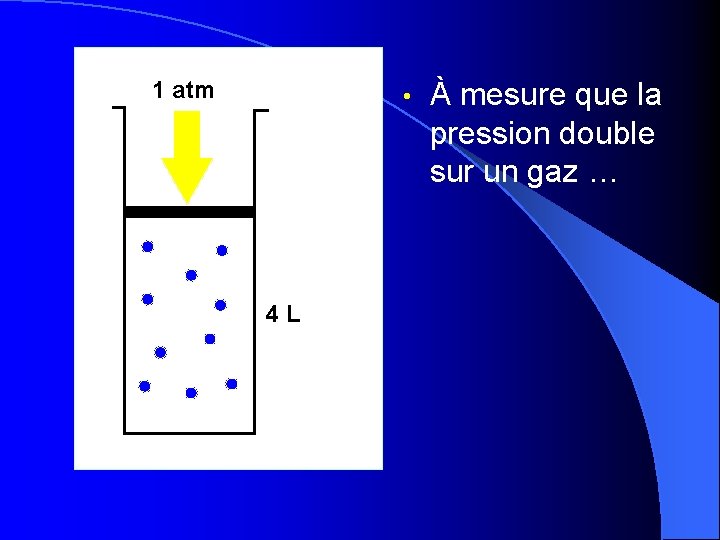
1 atm • 4 L À mesure que la pression double sur un gaz …

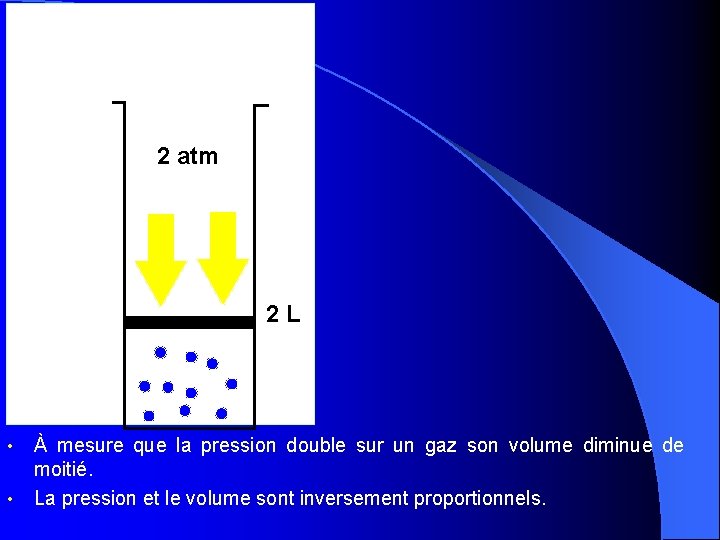
2 atm 2 L • • À mesure que la pression double sur un gaz son volume diminue de moitié. La pression et le volume sont inversement proportionnels.

Exercices a) Un échantillon de gaz 1, 53 L est soumis à une pression de 5, 61 k. Pa. Si on augmente la pression à 15 k. Pa, à température constante, quel est le nouveau volume de ce gaz?

Exercices b) On recueille un gaz dans un contenant de 242 cm 3 et on mesure sa pression qui est de 87, 6 k. Pa. Déterminer le volume de ce gaz à une nouvelle pression de 100 k. Pa. (On suppose que la température ne varie pas. )

La température: la loi de Charles • Selon la théorie cinétique moléculaire, la température est proportionnelle à l'énergie cinétique (c-a-d, énergie de mouvement) moyenne des particules d’une substance. • Plus la température est élevée, plus le nombre de particules ayant une énergie cinétique augmente à la moyenne.

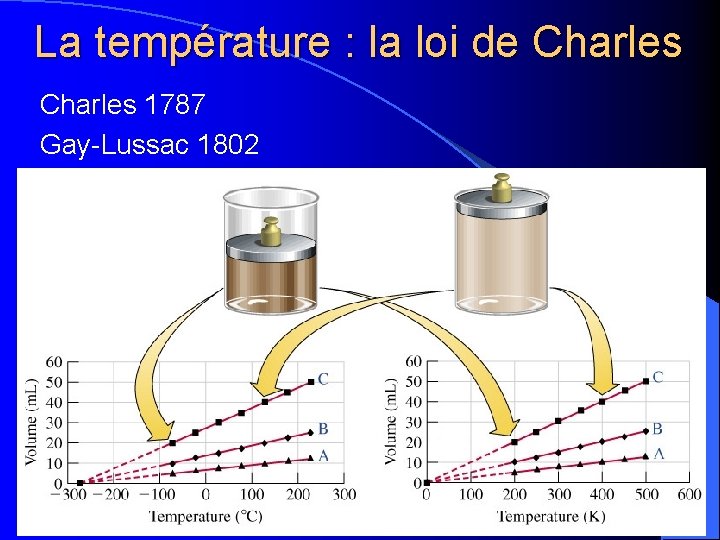
La température : la loi de Charles 1787 Gay-Lussac 1802

La température: la loi de Charles • Quand on analyse la relation entre le volume d’un gaz et sa température en kelvin, on constate qu’il s’agit d’un rapport direct. • D’après la loi de Charles, l’augmentation du volume (V) est proportionnelle à l’augmentation de la température (T).

La température: la loi de Charles Lorsqu’un échantillon de gaz subit une variation de température, le rapport prend la forme suivante: • V 1 = V 2 (loi de Charles) T 1 T 2 • Cette équation se vérifie lorsque la pression et la quantité de gaz restent constantes. •

La température: la loi de Gay-Lussac • Quand on analyse la relation entre la pression d’un gaz et sa température en kelvin, on constate qu’il s’agit également d’un rapport direct. • D’après la loi de Gay-Lussac, l’augmentation de la pression (P) est proportionnelle à l’augmentation de la température (T).

La température: la loi de Gay-Lussac Lorsqu’un échantillon de gaz subit une variation de température, le rapport prend la forme suivante: • P 1 = P 2 (loi de Gay-Lussac) T 1 T 2 • Cette équation se vérifie lorsque le volume et la quantité de gaz restent constantes. •

STP l Les propriétés des gaz dépendent des conditions. l Définition des conditions standards de température et de pression (STP). P = 1 atm = 760 mm Hg T = 0°C = 273. 15 K

La température: la loi de Charles Le kelvin (symbole K, du nom de Lord Kelvin) est l'unité SI de température thermodynamique l degrés Celsius en kelvins : K = °C + 273, 15 l kelvins en degrés Celsius : °C = K - 273, 15 • 0°C = 273 K 0°K = - 273 °C

Exercices a) On recueille un gaz ayant un volume de 225 cm 3 à 58 o. C. Déterminer le volume qu’occupera cet échantillon de gaz à 0 o. C. (On suppose que la pression est constante. ) b) Une masse de dioxygène de 2 dm 3 est à 25 o. C. Si on triple le volume qu’advient-il de la température? (On suppose que la pression est constante. )

La loi générale des gaz Lorsqu’on combine la loi de Charles et celle de Boyle-Mariotte, on obtient la loi générale des gaz, qui définit les rapports entre le volume, la température, et la pression de n’importe quelle quantité donnée de gaz. • D’après cette loi, le produit de la pression et du volume d’un échantillon de gaz est proportionnel à sa température absolue. •

La loi générale des gaz Cette équation ne se vérifie que si la quantité de gaz demeure constante. • P 1 V 1 = P 2 V 2 (loi générale des gaz) T 1 T 2 •

La loi des gaz parfaits • Les lois sur les gaz que nous avons étudiées jusqu’ici ne s’appliquent qu’aux gaz parfaits. • Un gaz parfait est un gaz hypothétique qui obéit à toutes lois des gaz dans toutes les conditions, c’est-à-dire qu’il ne se condense pas pour devenir liquide lorsqu’on le refroidit, et que les graphiques représentant ses variations de volume ou de pression en fonction de la température sont des lignes droites.

La loi des gaz parfaits • Théoriquement, un gaz se compose de particules de taille nulle qui ne s’attirent pas les unes les autres. • Une seule équation suffira donc pour décrire les interrelations de la pression, de la température, du volume et de la quantité de matière - (Les quatre variables qui définissent un système gazeux).

La loi des gaz parfaits • À température constante. P 1 x V 1 = P 2 x V 2 T 1 Loi de Boyle-Mariotte T 2

La loi des gaz parfaits • À pression constante. P x 1 V 1 T 1 = P 2 x V 2 T 2 Loi de Charles

La loi des gaz parfaits • À volume constant. P x 1 P 1 T 1 = P 2 x P 2 T 2 Loi de Gay-Lussac

La loi des gaz parfaits • • n. RT V = P PV = n. RT Cette dernière équation constitue la loi des gaz parfaits et la constante R porte le nom de constante universelle des gaz. P = Pression (k. Pa) V = Volume (L) n = nombre de mol (mol) T = Température (K) R= 8, 314 (k. Pa L) / (mol K)

La loi des gaz parfaits On peut déterminer la valeur de R en remplaçant les termes appropriés de la loi des gaz parfaits par les conditions TPN (ou TAPN) pour une mole de gaz parfait. • R = PV n. T • R = 101, 3 k. Pa x 22, 414 L 1, 00 mol x 273 K • R = 8, 31 k. Pa x L mol x K •

La loi des gaz parfaits P = n. RT V • V = n. RT P • n = PV RT • T = PV n. R •

Hypothèse d’Avogadro l La loi d’Avogadro établit la relation mathématique entre le volume de gaz V et le nombre de moles du gaz présent n. n 1 = n 2 (loi d’Avogadro) V 1 V 2 l Le volume augmente proportionnellement avec le nombre de moles de gaz.

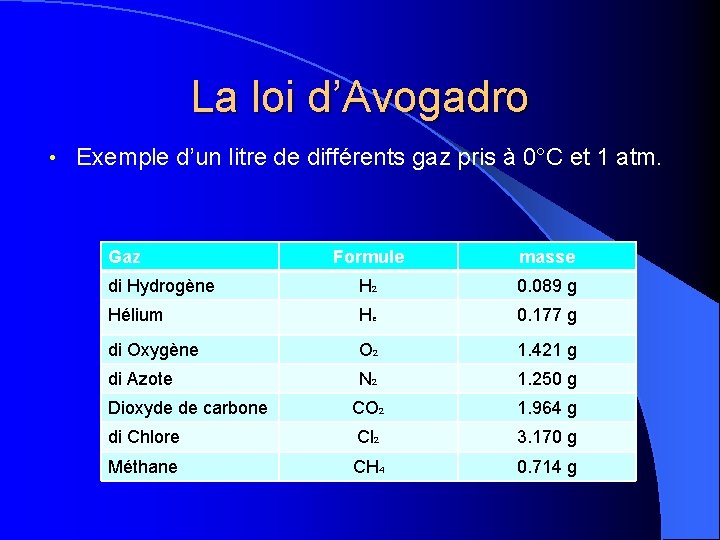
La loi d’Avogadro • Exemple d’un litre de différents gaz pris à 0°C et 1 atm. Gaz Formule masse di Hydrogène H 2 0. 089 g Hélium He 0. 177 g di Oxygène O 2 1. 421 g di Azote N 2 1. 250 g Dioxyde de carbone CO 2 1. 964 g di Chlore Cl 2 3. 170 g Méthane CH 4 0. 714 g

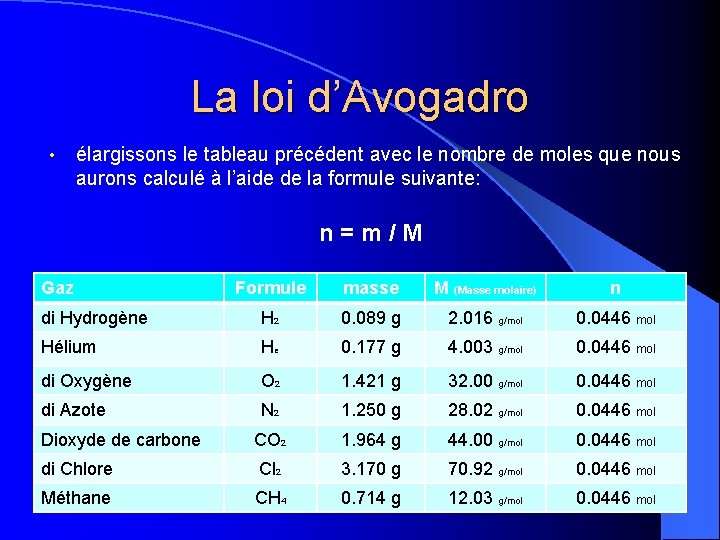
La loi d’Avogadro • élargissons le tableau précédent avec le nombre de moles que nous aurons calculé à l’aide de la formule suivante: n=m/M Gaz Formule masse M (Masse molaire) n di Hydrogène H 2 0. 089 g 2. 016 g/mol 0. 0446 mol Hélium He 0. 177 g 4. 003 g/mol 0. 0446 mol di Oxygène O 2 1. 421 g 32. 00 g/mol 0. 0446 mol di Azote N 2 1. 250 g 28. 02 g/mol 0. 0446 mol Dioxyde de carbone CO 2 1. 964 g 44. 00 g/mol 0. 0446 mol di Chlore Cl 2 3. 170 g 70. 92 g/mol 0. 0446 mol Méthane CH 4 0. 714 g 12. 03 g/mol 0. 0446 mol

La loi d’Avogadro • Cela veut dire que des mêmes volumes de différents gaz, pris dans les mêmes conditions de température et de pression, renferment le même nombre de moles. • En sachant qu’un mole est composé de 6. 022 x 10²³ molécules, également le même nombre de molécules.

La loi d’Avogadro • Conclusion: Si 0. 0446 mol de n’importe quel gaz occupe un volume de 1 L, alors 1 mol de n’importe quel gaz occupe un volume de 1 / 0. 0446 = 22. 4 L • Une mole de n’importe que gaz, pris dans les conditions normales de température et de pression (0°C et 1 atm) occupe un volume de 22. 4 L

Volume des gaz à TPN • Température et Pression Normales (TPN) • Température standard: 0 o. C ou 273 K • Pression standard: 760 mm de Hg= 1 atm= 101, 3 k. Pa • Volume d’une mole de gaz: 22, 4 L • Température Ambiante et Pression Normale (TAPN) • Température: 25 o. C ou 298 K • Pression: 100 k. Pa • Volume d’une mole: 24, 5 L