Les formules chimiques Avant de dbuter voici quelques

Les formules chimiques

Avant de débuter, voici quelques pré-requis!

La formule chimique, les électrons de valence et le nombre d’oxydation. • Le nombre d’électrons de valence déterminent quel sera le nombre d’oxydation d’un atome. · Les éléments du groupe I ont un électron sur leur couche périphérique. Pour qu’il deviennent stable (non réactifs) ces atomes doivent perdre cette électron. Si ces éléments perde 1 électron ils obtiennent automatiquement la charge de +1 (ou nombre d’oxydation de +1).
Les électrons de valence et les ions
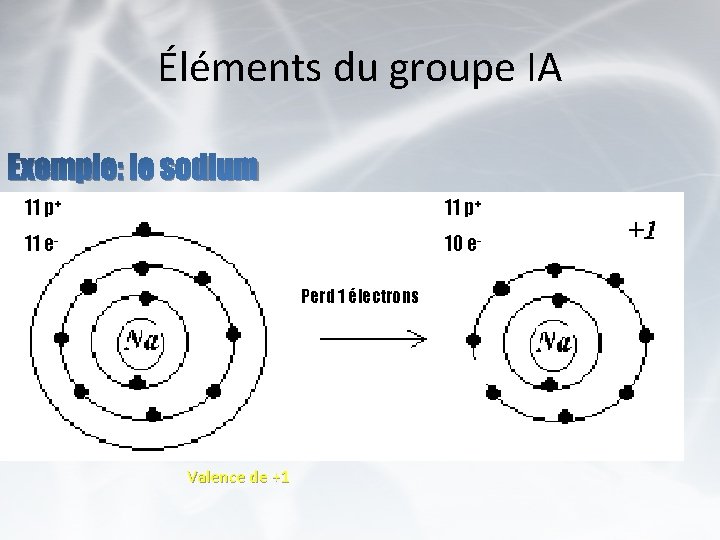
Éléments du groupe IA Exemple: le sodium 11 p+ 11 e- 10 e. Perd 1 électrons Valence de +1
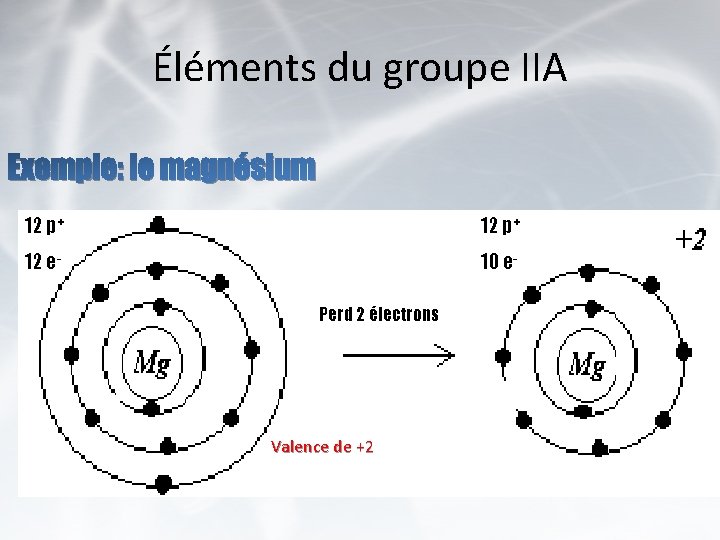
Éléments du groupe IIA Exemple: le magnésium 12 p+ 12 e- 10 e. Perd 2 électrons Valence de +2
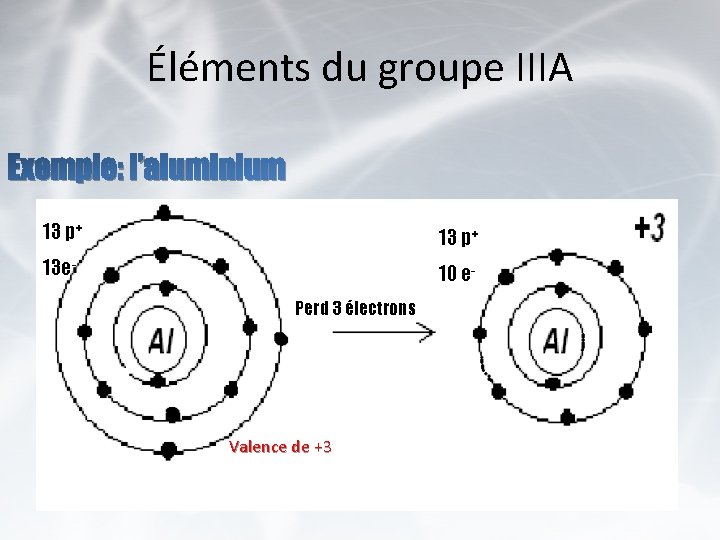
Éléments du groupe IIIA Exemple: l’aluminium 13 p+ 13 e- 10 e. Perd 3 électrons Valence de +3
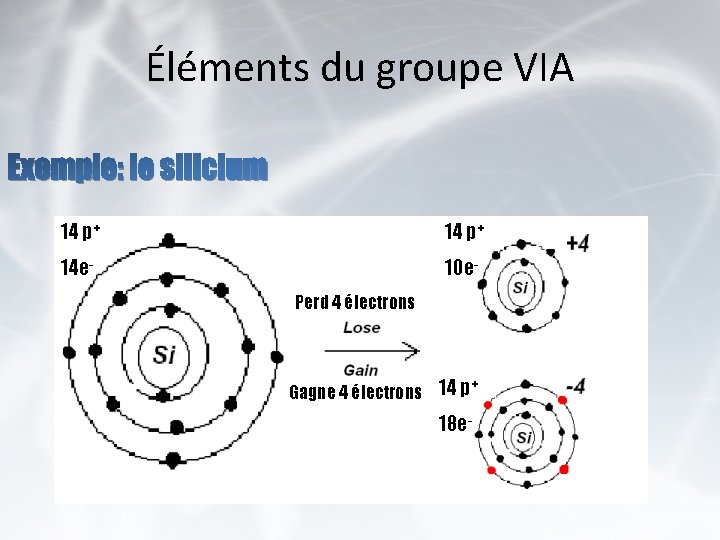
Éléments du groupe VIA Exemple: le silicium 14 p+ 14 e- 10 e. Perd 4 électrons + Gagne 4 électrons 14 p 18 e-
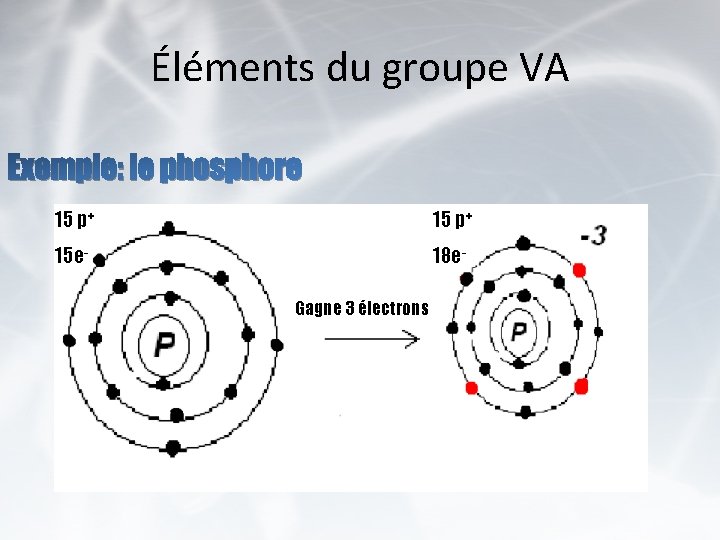
Éléments du groupe VA Exemple: le phosphore 15 p+ 15 e- 18 e. Gagne 3 électrons
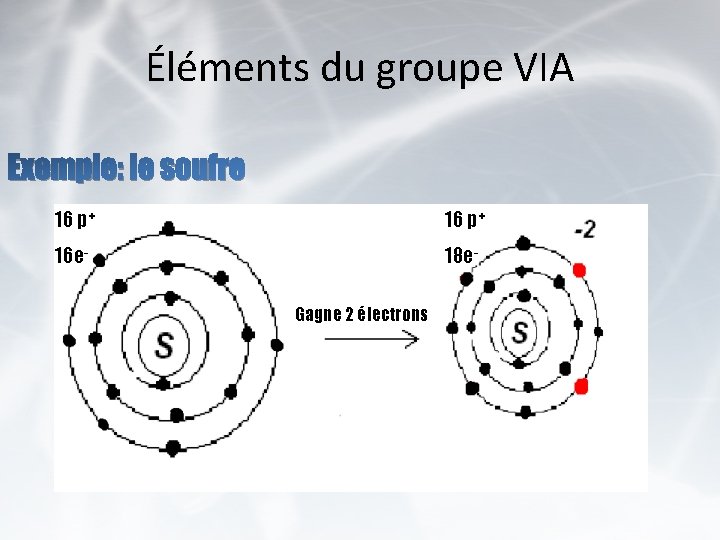
Éléments du groupe VIA Exemple: le soufre 16 p+ 16 e- 18 e. Gagne 2 électrons
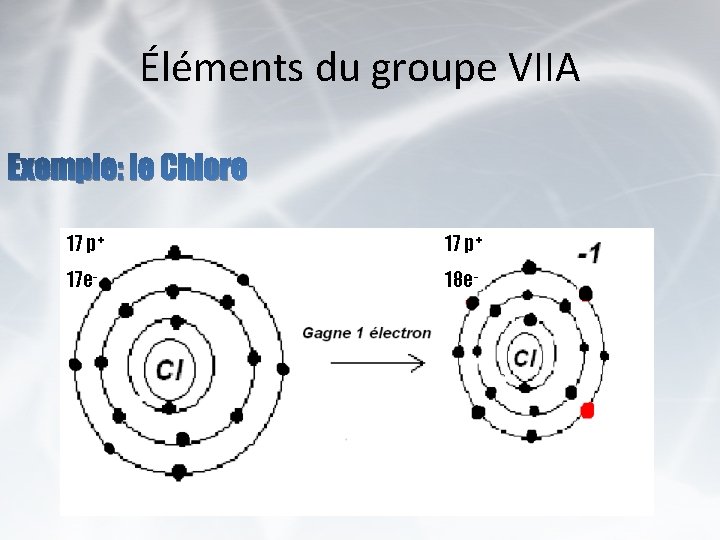
Éléments du groupe VIIA Exemple: le Chlore 17 p+ 17 e- 18 e-
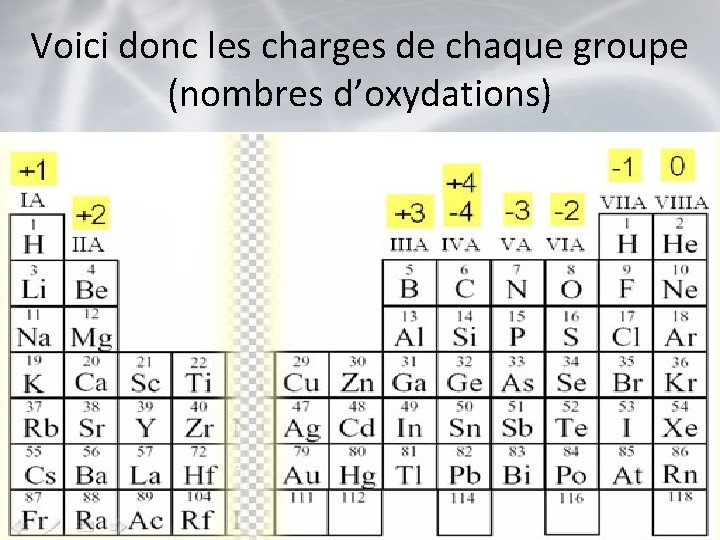
Voici donc les charges de chaque groupe (nombres d’oxydations)

Les éléments du groupe VIIIA Nommé: gaz rare ou gaz noble ont leur dernière couche électronique de pleine. Donc il ne réagirons pratiquement pas.


Ions Polyatomiques Certains éléments se combinent en petit groupe mais restent chargés. Ce sont les ions polyatomiques. Ils agissent comme les atomes simples et peuvent se combiner pour former des composés.

Un ion polyatomique • un ion composé de deux ou plusieurs atomes non-métalliques différents, unis par des liaisons covalentes. • La terminaison d’un anion polyatomique standard est souvent « ate » Exemple: – NH 4+ (ion ammonium), SO 42 - (ion sulfate).

Un ion polyatomique
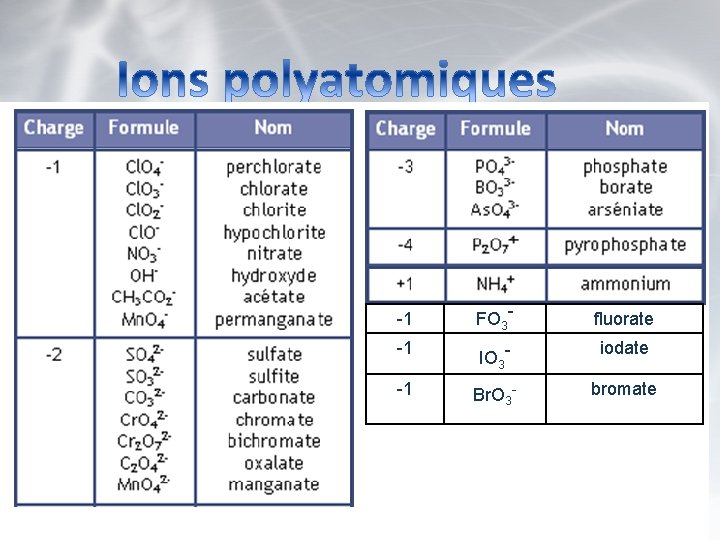
-1 FO 3 - fluorate -1 IO 3 - iodate -1 Br. O 3 - bromate

Bon! Maintenant ont peux débuter la formule chimique

FORMULES CHIMIQUES • Formule moléculaire • Définition : Une formule indiquant le nombre réel d’atomes de chaque élément dans une molécule.

Formule moléculaire Ex : C 6 H 12 O 6 (glucose) La formule pourrait être simplifiée à CH 2 O, mais dans une formule moléculaire on veut le nombre réel d’atomes

FORMULES CHIMIQUES ET NOMENCLATURE • Formule empirique Définition : Une formule chimique exprimant le rapport le plus simple entre les atomes dans un composés.
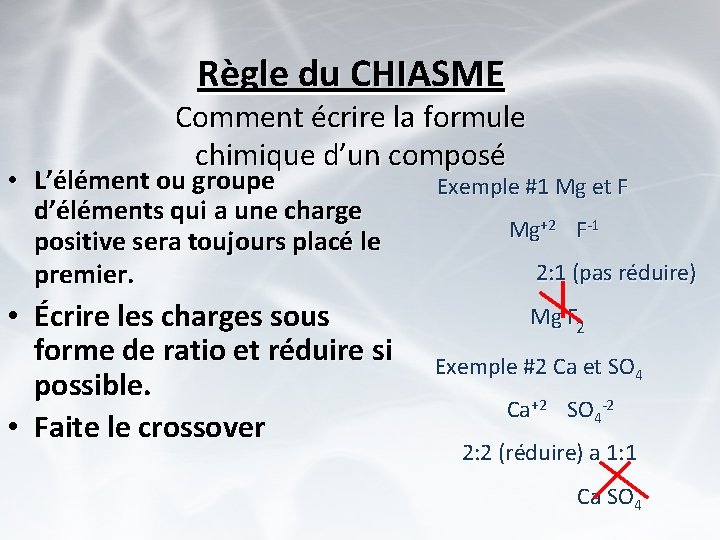
Règle du CHIASME Comment écrire la formule chimique d’un composé • L’élément ou groupe d’éléments qui a une charge positive sera toujours placé le premier. • Écrire les charges sous forme de ratio et réduire si possible. • Faite le crossover Exemple #1 Mg et F Mg+2 F-1 2: 1 (pas réduire) Mg F 2 Exemple #2 Ca et SO 4 Ca+2 SO 4 -2 2: 2 (réduire) a 1: 1 Ca SO 4

Exemple #3 Al et OH Exemple #4 Na et O Al+3 OH-1 Na+1 O-2 3: 1 (non réductible) 1: 2 (non réductible) Al(OH)3 Na 2 O Exemple #5 NH Exemple #6 Ca et Cl. O 3 Note que si dois placer un indice devant un 4 et PO 4 NH 4+1 PO 4 -3 Ca+2 CO 3 -2 groupe d’atome tu dois placer ce groupe 1: 3 (non réductible) 2: 2 (réduire a 1: 1) d’atome entre parenthèse!!! (NH 4)3 PO 4 Ca. CO 3 Quelles sont les formules résultants des associations suivantes. a) Mg + Cl b) B + PO 4 c) H + SO 4

Écris la formule chimique de chaque composé formé lorsque tu réunis les atomes ou groupes d’atomes suivants : a) Chlorate et Lithium f) Potassium et Sélénium b) Ammonium et Phosphate g) Strontium et Azote c) Calcium et Fluor h) Béryllium et Oxygène d) Hydroxyde et Sulfate i) Hydrogène et Carbonate e) Magnésium et Sulfure j) Sodium et Nitrate

Feuille de formules chimiques

La nomenclature e de 11 année

I. nomenclature des oxydes métalliques: Formule Général : MO(métal et oxygène). · Nomenclature: oxyde de M (M doit être remplacé par le nom du métal). – Si le métal a plus qu’une charge il faut l’inclure dans le nom du composé. · Exemple : Na 2 O = Oxyde de sodium Mg. O = Oxyde de magnésium Al 2 O 3 = Oxyde d’aluminium Cu 2 O = Oxyde de cuivre (I)
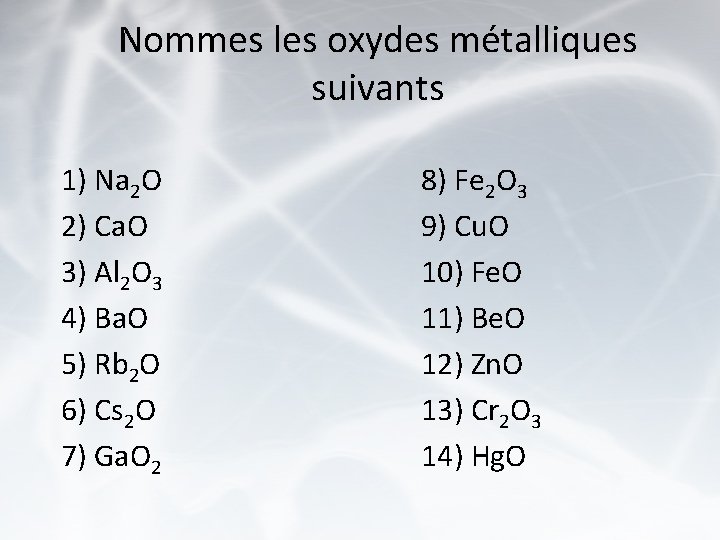
Nommes les oxydes métalliques suivants 1) Na 2 O 2) Ca. O 3) Al 2 O 3 4) Ba. O 5) Rb 2 O 6) Cs 2 O 7) Ga. O 2 8) Fe 2 O 3 9) Cu. O 10) Fe. O 11) Be. O 12) Zn. O 13) Cr 2 O 3 14) Hg. O

II. nomenclature des oxydes nonmétalliques: · Formule générale: N-MO (non-métal et oxygène). · Nomenclature: oxyde de N-M (N-M doit être remplacé par le nom du non-métal). Le non-métal et l’oxygène devraient porter un préfixe représentant combien de chacun il y a. un – mono six – hexa sept – hepta deux – di huit – octo trois – tri neuf – nano quatre – tetra dix - deca cinq – penta

Exemple d’oxydes non-métalliques: CO 2 = dioxyde de carbone N 2 O 5 = pentoxyde de diazote P 4 O 10 = decaoxyde de tetraphosphore

Nommes les oxydes non-métalliques suivants 1) P 2 O 5 2) SO 3) As 4 O 10 4) B 2 O 3 5) Si. O 2 6) H 2 O 7) CO 8) SO 2 9) H 2 O 2 10) Se. O 2

IV. nomenclature des acides binaires gazeux : • Formule générale : HX(g) – Nomenclature: X-ure d’hydrogène (le nom du nonmétal avec la terminaison ure + d’hydrogène). • Exemple : HBr(g) = bromure d’hydrogène H 2 S = sulfure d’hydrogène

IV. nomenclature des acides binaires en présence d’eau: • Formule générale : HX(aq) – Nomenclature: acide Hydro-X-ique (acide Hydro-nom du non-métal + -ique). • Exemple : HBr(aq) = acide bromhydrique H 2 S(aq) = acide sulfhydrique

Nommes les acides suivants: 1) HCl 2) HBr(aq) 3) H 2 S 4) HF(aq) 5) H 2 Se 6) H 3 P 7) H 2 Te(aq) 8) HCl(aq) 9) HBr 10) H 2 S

Nomenclature des acides ternaire Formule générale: HXO Nomenclature: nom de l’ion polyatomique(XO)+ Hydrogène. Exemple : HCl. O 3: chlorate d'hydrogène H 2 SO 4: sulfate d'hydrogène

Nomenclature des acides ternaire Formule générale: HXO(aq) Nomenclature: acide + nom de l’ion polyatomique(XO)-ique. Exemple : H 2 CO 3(aq): acide carbonique H 2 SO 4(aq): acide sulfurique HNO 3(aq): acide nitrique

Exercices de Nomenclature Nommes les composées suivants: • • a. H 2 SO 4 i. HCO 3 b. H 3 PO 4(aq) j. H 2 SO 4(aq) c. HIO 3 k. HNO 3(aq) d. HCl. O 3 l. CH 3 COOH e. CH 3 COOH(aq) m. H 3 PO 4 f. HBr. O 3 n. HCl. O 3(aq) g. HCO 3(aq) o. HIO 3 h. HIO 3(aq) p. HNO 3

III. nomenclatures des hydroxydes: · Formule générale: MOH · Nomenclature: Hydroxyde de M (M est le métal). · Exemple : Li. OH : hydroxyde de lithium KOH : hydroxyde de potassium

Nommes les hydroxydes suivants: 1) Mg(OH)2 2) Na. OH 3) Cr(OH)3 4) Be(OH)2 5) Cs. OH 6) Al(OH)3 7) Ni(OH)2 8) Fe(OH)3 9) Zn(OH)2 10) Li. OH

V. nomenclature des sels: Formule générale: MX (ou M est le métal et X le nonmétal). · Nomenclature : X-ure de Métal Exemple : Na. Cl = chlorure de sodium Rb 2 S = sulfure de rubidium Ca. H 2 = hydrure de calcium
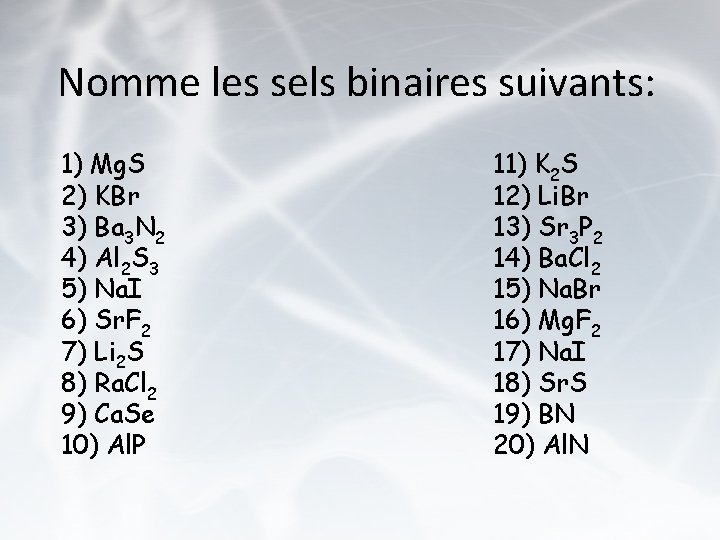
Nomme les sels binaires suivants: 1) Mg. S 2) KBr 3) Ba 3 N 2 4) Al 2 S 3 5) Na. I 6) Sr. F 2 7) Li 2 S 8) Ra. Cl 2 9) Ca. Se 10) Al. P 11) K 2 S 12) Li. Br 13) Sr 3 P 2 14) Ba. Cl 2 15) Na. Br 16) Mg. F 2 17) Na. I 18) Sr. S 19) BN 20) Al. N

Exercices de Nomenclature Nommes les composées suivants: • • • a. Na. Cl b. Sc(OH)3 c. Cs. F d. Al. I 3 e. HI(aq) f. Mg(OH)2 g. H 2 Se h. HI i. K 2 O

Nomenclature des sels ternaire Formule générale: MXO Nomenclature: nom de l’ion polyatomique(XO)+ M. Exemple : KCl. O 3 = chlorate de potassium Mg. SO 4 = sulfate de magnésium Ca. NO 3 = nitrate de calcium

Nommes les sels tertiaires suivants: 1) Na 2 SO 4 2) Na. Cl. O 3 3) Zn(NO 3)2 4) Cs 3 PO 4 5) Be(Cl. O 3)2 6) Fe 2(SO 4)3 7) Ba. CO 3 8) Ti. PO 4 9) K 2 CO 3 10) Al 2(SO 4)3

• • • Révision de Nomenclature générale Nommes les composées suivants: a. Na. Cl b. Sc(OH)3 c. Cs. F d. Al. I 3 e. HI(aq) f. CO g. K 2 CO 3 h. HI i. K 2 O j. Si. F 4 k. H 2 Se l. H 2 Te(aq) m. NH 4 OH n. Ba 3(PO 4)2 o. (NH 4)2 S p. Na 2 SO 4 q. Ca(Cl. O 3)2 r. N 2 O 5

Les Hydrures • M + H • hydrure de M * Ici, H prend une charge de -1 car l’hydrogène est plus électronégatif. Exemples : Li. H hydrure de lithium Na. H Ca. H 2 Fe. H 2 hydrure de strontium hydrure de chrome (II) hydrure de nickel (III) hydrure de sodium hydrure de calcium hydrure de fer (II) Sr. H 2 Cr. H 2 Ni. H 3

e La nomenclature 12 (Noms donnés aux différents composées)

Les peroxydes • XO + O (1 oxygène de plus que normalement) • peroxyde de X Exemples : Na 2 O 2 peroxyde de sodium Ba. O 2 peroxyde de barium H 2 O 2 peroxyde d’hydrogène peroxyde d’aluminium impossible peroxyde de lithium Li 2 O 2 *Seulement les éléments de la famille des alcalins et des alcalino-terreux peuvent former des peroxydes.

RAPPEL: Les ions polyatomiques les plus importants q. NH 41+ - ammonium q. CH 3 COO 1 - - acétate q. OH 1 - - hydroxyde q. NO 31 - - nitrate q. Cl. O 31 - - chlorate q. SO 4 2 - - sulfate q. CO 32 - - carbonate q. PO 43 - - phosphate q. Br. O 31 - - bromate q. IO 31 - - iodate


• Un anion qui se termine par le suffixe ite renferme un atome d’oxygène de moins que celui qui se termine par ate ; les deux ions portent la même charge. ion chlorate Cl. O 3 - ion chlorite Cl. O 2 -

• Un anion de même charge qui porte un atome d’oxygène de moins que celui qui se termine en ite prend alors le préfixe hypo en plus. – ion chlorite, Cl. O 2 - – ion hypochlorite, Cl. O-

• Un anion de même charge qui porte un atome d’oxygène de plus que celui qui se termine en ate prend alors le préfixe per en plus. – ion chlorate, Cl. O 3 - – ion perchlorate, Cl. O 4 -

Résumons • 1 oxygène de plus ate de X = Per- X – • XSO 5 - persulfate de X • Acide de référence (-ate) = X – ate de X • XSO 4 - sulfate de X • 1 oxygène de moins X • XSO - sulfite de X = X – ite de
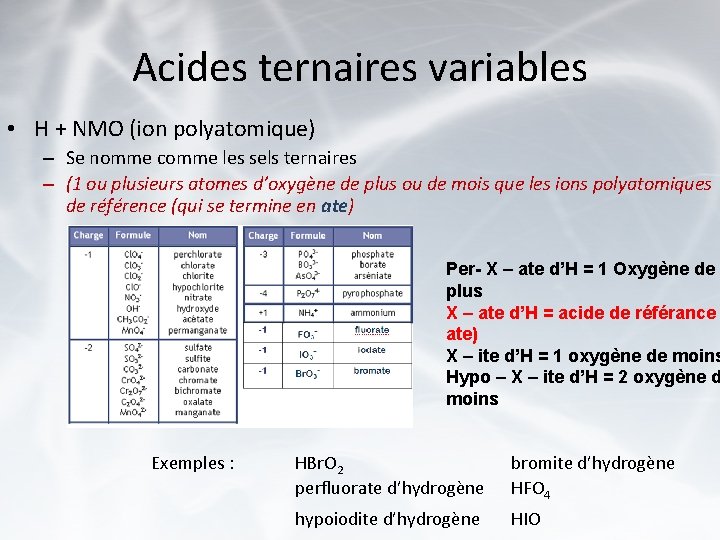
Acides ternaires variables • H + NMO (ion polyatomique) – Se nomme comme les sels ternaires – (1 ou plusieurs atomes d’oxygène de plus ou de mois que les ions polyatomiques de référence (qui se termine en ate) Per- X – ate d’H = 1 Oxygène de plus X – ate d’H = acide de référance ate) X – ite d’H = 1 oxygène de moins Hypo – X – ite d’H = 2 oxygène d moins Exemples : HBr. O 2 perfluorate d’hydrogène bromite d’hydrogène HFO 4 hypoiodite d’hydrogène HIO

Hydracides ternaires variables • H + NMO (ion polyatomique) (aq) – (1 ou plusieurs atomes d’oxygène de plus ou de mois que les ions polyatomiques de référence (qui se termine en ate) Acide Per- X – ique = 1 Oxygène plus Acide X – ique = acide de référa (-ate) Acide X – eux = 1 oxygène de moins Acide Hypo – X – eux = 2 oxygè de moins Exemples : H 2 SO 4 HBr. O 2 acide perfluorique acide sulfurique acide bromeux HFO 4 acide hyponitreux H 2 PO 2

Acides ternaires variables 2 Oxygène de moins (que l’acide de référence) HNO (aq) acide hyponitreux 1 Oxygène de moins (que l’acide de référence) HNO 2(aq) acide nitreux Acide de référence HNO 3(aq) acide nitrique 1 Oxygène de plus (que l’acide de référence) HNO 4(aq) acide pernitrique

Acides ternaires variables 2 Oxygène de moins (que l’acide de référence) H 2 SO 2(aq) hyposulfureux acide 1 Oxygène de moins (que l’acide de référence) H 2 SO 3(aq) acide sulfureux Acide de référence H 2 SO 4(aq) acide sulfurique 1 Oxygène de plus (que l’acide de référence) H 2 SO 5(aq) acide persulfurique

À ton tour! 2 Oxygène de moins (que l’acide de référence) H 3 PO 2(aq) acide hypophosphoreux 1 Oxygène de moins (que l’acide de référence) H 3 PO 3(aq) acide phosphoreux Acide de référence H 3 PO 4(aq) acide phosphorique 1 Oxygène de plus (que l’acide de référence) H 3 PO 5(aq) acide perphosphorique

Sels ternaires variables • M + NMO (ion polyatomique) – (1 ou plusieurs atomes d’oxygène de plus ou de mois que les ions polyatomiques de référence (qui se termine en ate) Per- X – ate de M = 1 Oxygène de plus X – ate de M = acide de référance ate) X – ite de M = 1 oxygène de moin Hypo – X – ite de M= 2 oxygène d moins Exemples : Cu. CO Zn. SO 5 fluorite de strontium periodate de manganèse IV hypocarbonite de cuivre persulfate de zinc Sr(FO 2)2 Mn(IO 4)4

Sels ternaires variables 2 Oxygène de moins (que le sel de référence) Na 2 SO 2 hyposulfite de sodium 1 Oxygène de moins (que le sel de référence) Na 2 SO 3 sulfite de sodium Sel de référence Na 2 SO 4 sulfate de sodium 1 Oxygène de plus (que le sel de référence) Na 2 SO 5 persulfate de sodium
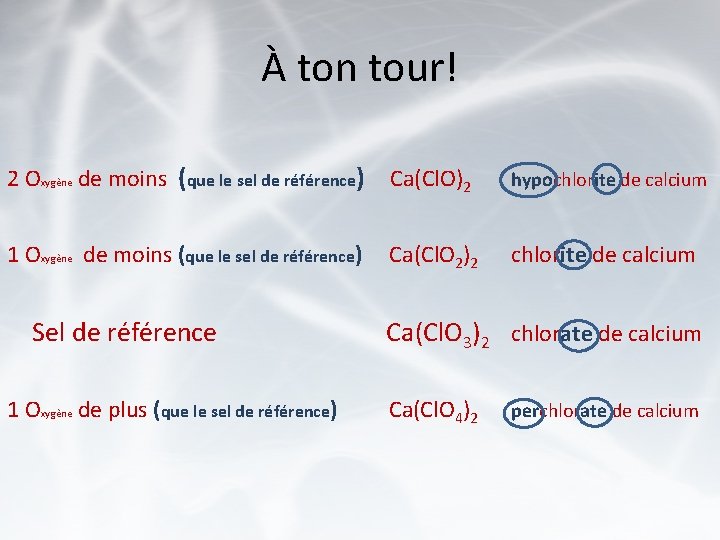
À ton tour! 2 Oxygène de moins (que le sel de référence) Ca(Cl. O)2 hypochlorite de calcium 1 Oxygène de moins (que le sel de référence) Ca(Cl. O 2)2 chlorite de calcium Sel de référence Ca(Cl. O 3)2 chlorate de calcium 1 Oxygène de plus (que le sel de référence) Ca(Cl. O 4)2 perchlorate de calcium

Les composées moléculaires binaires • NM 1 + NM 2 • Préfixe NM 2 + ure de préfixe NM 1 Exemples : BF 3 trifluorure de bore Si. S 2 disulfure de silicium mononitrure de phosphore PN trisulfure de diphosphore P 2 S 3

Les amalgames • alliage de mercure • Hg-M • amalgame de M Exemples : Hg-Na amalgame de sodium Hg-Al amalgame d’aluminium amalgame de francium Hg-Fr amalgame de calcium Hg-Ca

• Ions polyatomiques contenant un ou plusieurs atomes d’hydrogène; – On mentionne sa présence avec la particule hydrogéno. – On utilise également les préfixes de type mono ou di. • ion phosphate, • ion hydrogénophosphate, • ion dihydrogénophosphate, PO 43 - HPO 42 - H 2 PO 4 -

Nomenclature des sels acides Formule générale: MH-ion poly ou MH-NM • Nomenclature : – préfixe-hydrogéno nom de X + -ure + nom de M -ite -ate ure ate ite On se base sur le type de sel (binaire, ternaire ou ternaire variable) Exemple: – Na 2 HPO 4 : hydrogénophosphate de sodium – Na. H 2 PO 3 : dihydrogénophosphite de sodium – KHS: monohydrogénosulfure de potassium

Nomenclature des sels acides Na. H 2 PO 2 dihydrogénohypophosphite de sodium Mg. HPO 3 monohydrogénophosphite de magnésium KHS monohydrogénosulfure de potassium Ca(HCO 3)2 monohydrogénocarbonate de calcium Co(HSO 5)3 monohydrogénopersulfate de cobalt III
- Slides: 68