Les dosages I Objectif dun dosage Un dosage

Les dosages

I) Objectif d’un dosage Un dosage (ou titrage) permet de déterminer la concentration molaire inconnue d’une espèce chimique

II) Principe du dosage On fait réagir une espèce chimique de concentration inconnue avec une espèce antagoniste de concentration connue c’est à dire : n un oxydant avec un réducteur ou inversement. n un acide avec une base ou inversement; La réaction de dosage doit être rapide , totale et spécifique.

Aspect expérimental : n n n On prélève, à l’aide d’une pipette jaugée , un volume V de la solution de concentration inconnue : C’est la prise d’essai ( que l’on verse dans un becher ou un erlenmeyer ) A l’aide d’uneburette graduée , on ajoute ensuite petit à petit une solution de concentration connue. On s’intéresse toujours uniquement aux réactifs ( Les produits n’apportent aucune information utile)
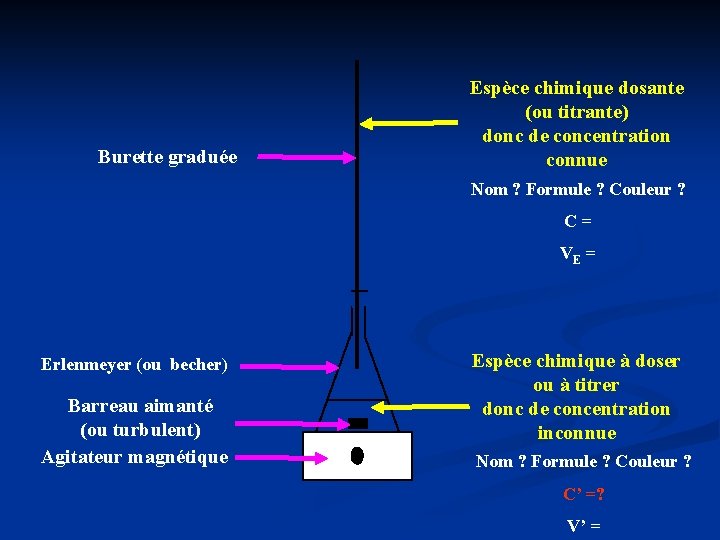
Burette graduée Espèce chimique dosante (ou titrante) donc de concentration connue Nom ? Formule ? Couleur ? C= VE = Erlenmeyer (ou becher) Barreau aimanté (ou turbulent) Agitateur magnétique Espèce chimique à doser ou à titrer donc de concentration inconnue Nom ? Formule ? Couleur ? C’ =? V’ =

III) Précision du dosage ATTENTION : naux bulles d’air dans la burette nau mauvais ajustement des niveaux naux erreurs de parallaxe lors de la lecture ( en général à 0. 1 m. L près !!!) nau changement de couleur (à la goutte près !!!)

IV) Exploitation du dosage et repérage de l’équivalence Définition de l’ équivalence n n Le changement de réactif limitant définit l’équivalence. L’équivalence est atteinte lorsque l’on a réalisé un mélange stoechiométrique des deux réactifs.

1) Pour un dosage colorimétrique : n L’équivalence est repérée par un changement de couleur persistant.

2) Pour un dosage conductimétrique : n n Lors d’un dosage conductimétrique, on G mesure la conductance de la (en m. S) solution au fur et à mesure de l’addition de l’un des deux réactifs. La courbe G=f (Vréactif versé) est formée de deux segments de droites dont l’intersection permet de repérer l’équivalence E. VE Volume versé V (en m. L)

V) Détermination de la concentration inconnue : Etudier les quantités de matières présentes à l’équivalence permet TOUJOURS de trouver la concentration molaire de l’espèce chimique étudiée. totalement disparus L’avancement maximal (xmax ou x. E) de la réaction est identique pour les deux réactifs. A l’équivalence, les 2 réactifs ont n n : Dans le tableau d’avancement qui correspond à la réaction de dosage, à l’équivalence, on indique dans l’état final, la quantité de matière des deux réactifs est nulle.

- Slides: 11